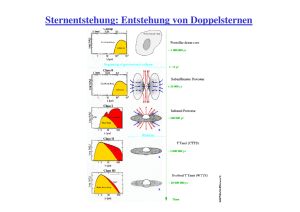
1 1H-NMR-Spektroskopie in metallorganischen Komplexen 1.1
Werbung

1 1.1 1H-NMR-Spektroskopie in metallorganischen Komplexen Allgemeines Chemische Verschiebungen Beispiele für einfache Komplexe 1.2 1.3 Chiralität in Metallkomplexen Dynamische Prozesse 1.4 Heteronukleare Kopplungen ⇒ Allgemeines Heterokerne: Definition, Eigenschaften 2 13C-NMR-Spektroskopie 1.4 Heteronukleare Kopplungen (Erweiterung von 1H-NMR auf Heterokerne) Kerne mit Drehimpuls P (auch Kernspin; gequantelt) I = Kernspinquantenzahl (aus Protonen- plus Neutronenzahl) 0; 1/2, 1, 3/2 etc. Kerne mit Kernspin I = 1/2 Homo- und/oder heteropolare skalare Spin-Spin-Wechselwirkungen 1H-NMR-Spektren 1H-31P-Kopplung 1H-M-Kopplung in CpM-Hydriden 31P-NMR-Spektren Kopplung mit 31P und anderen Kernen Kerne mit Kernspin I >1/2 Informationen aus NMR-Spektren (Zusammenfassung und Vorschau) Parameter Ursache Information Chemische Verschiebung Unterschiedliche chemische Struktur, dynamische Umgebung Prozesse Homo- und/oder Konnektivität im Molekül heteronukleare skalare Spin- Zahl der Kopplungspartner Bindungen) Spin-Wechselwirkungen dynamische Prozesse Relaxationszeiten Dipol-Dipol-, Spin-Rotations- räumliche Struktur, T1 (longitudinal) und skalare Dynamik, Beweglichkeit von T2 (transversal) Wechselwirkungen Gruppen im Molekül, (X) Kopplungskonstanten nJ(AX) (n = Zahl der TQ (Quadrupolinduziert) elektronische Struktur Definition und Eigenschaften von Heterokernen „Heterokerne“: Alle Kerne außer 1H! Wichtige Unterscheidung: Kerne mit Kernspin I = ½ 13C, 19F, 31P etc. (Verhalten wie 1H) Kerne mit Kernspin I > ½ Meistens Metallkerne Gruppe 13: 11B (3/2), 27Al (5/2), 69Ga (3/2) Eigenschaften von Kernen mit Kernspin >1/2 Nachteile Breite NMR-Signale (Kernquadrupol) Geringe Empfindlichkeit Geringe Häufigkeit Sonstige messtechnische Probleme Vorteile Direktinformationen über die Struktur Metall-Ligand-Bindung (z.B. Kopplungen) Ligandeneffekte Metall-Metall-Bindung NMR-Eigenschaften wichtiger Heterokerne (B. Wrackmeyer, Chemie uns. Zeit 28 (1994) 309) Begriffe zur Tabelle „Metallkerne“ Quadrupolmoment Q (nur Kerne I > ½) Ursache: Unsymmetrische Ladungsverteilung Effekt: Verbreiterung der Signale Gyromagnetisches Verhältnis γ Bestimmt die Nachweisempfindlichkeit eines Kernes Großes γ: Empfindlicher Kern Kleines γ: Unempfindlicher Kern Messfrequenz Ξ Magnetische Flussdichte B0 = 2.35 T Informationsmaterial für NMR- und Massenspektroskopie Beispiel für 1H-31P-Kopplung [3J(H-P)] in CpFe(CO)(CH3CO)PPh3 3J(H-P) = 1.24 Hz H 3J Ph3P Fe O C CO CH3 Die heteronukleare Kopplung in deuterierten Lösungsmitteln am Beispiel 1H-2H DMSO-d6 (99% D-Gehalt) CD3 O S CD2H DMSO-d5 M = 2nI + 1 n = Zahl äquivalenter Nachbarn I = Kernspin 2D: I=1 n=2⇒M=5 1H-NMR-Spektrum von Cp2WH2 (400 MHz, CDCl3) Synthese, Struktur Spektrenanalyse von Cp2WH2 Multiplizität M (Zahl der Signale) M = 2nI + 1 n = Zahl äquivalenter Nachbarn I = Kernspin Informationen aus J. Emsley, The Elements, Clarendon Press Isotop 183W ist NMR-aktiv I=½ Natürliche Häufigkeit 14.3 % 1H-NMR-Spektrum von Cp2MoH2 (400 MHz, C6D6) Keine 95Mo-Satelliten! 1H-NMR-Spektrum von Cp2MoH2 (400 MHz, CDCl3) Folie! 2 13C-NMR-Spektroskopie Empfindlichkeit 13C: Natürliche Häufigkeit 13C: 1.6 % von 1H 1.1 % Wesentliche Merkmale: • Scharfe Singuletts (Breitband-1H-entkoppelt): Spektrum „nullter Ordnung“ • Großer Signalbereich (bis 400 ppm) • Kopplungen mit Zentralmetall möglich 13C-Satelliten am Beispiel CHCl3 Hauptsignal bei δ = 7.24 ppm 1.1 % Kopplung 1H-13C zu Dublett J(C,H) = 209 Hz; Int. = 0.55 % vom Hauptsignal 1H-NMR von CHCl3; 13C-Satelliten 15mal verstärkt (nach Fribolin S. 32) Beispiele und Anwendung δ-Werte für metallkoordinierte C-Atome Cr(CO)6 Mo(CO)6 W(CO)6 212 202 192 W(CH3)6 84 δ(Alkyl) 10-20 ppm (C5H5)2Fe 68 δ(C6H6) (CO)5Cr=CPh2 399 ⇒ Studium „beweglicher“ CO-Brücken „Organische“ Vergleichswerte 120 ppm δ(Ph3C+) 212 ppm CO-Austausch in (C5H5)2MoW(CO)4 Synthese 13CO-Anreicherung 13C-NMR (Variable Temperatur) Halbverbrückende („semibridging“) CO-Liganden [Strukturanalyse nach R. H. Crabtree, M. Lavin Inorg. Chem. 25 (1988) 805] O O C M O C C M M M symmetrische Brücke M M bent Unterscheide: σ- oder π-Brücken linear semibridging Merkmale: M-C-Abstände Winkel an C zwischen 120 und 180° IR-Absorptionen zwischen terminal und Brücke Die Substanzklasse [CpM(CO)2]2 (M = Cr, Mo, W) O C Cp Mo O C CO Mo Lokal: 3 IR-Banden (Cs) OC C O C O Toluol, 115 °C 18 e- pro Mo Cp ν(CO): 1960, 1940, 1900 cm-1 - 2CO Formal (aber nicht korrekt): Cp Mo OC O C C Mo O CO Cp 18 e- pro Mo mit Mo-MoDreifachbindung 2 IR-Banden ν(CO): 1890, 1830 cm-1 Lineare Brücke Kristallstruktur von [CpMo(CO)2]2 (M. D. Curtis 1978) Mo1−C2 (−C2‘) = 2.56 Å (a) Mo2−C2 (−C2’) = 2.13 Å (b) Winkel (Mo−Mo−C) = 66° Winkel (Mo−C−O) = 176° Delokalisiertes π-Bindungssystem