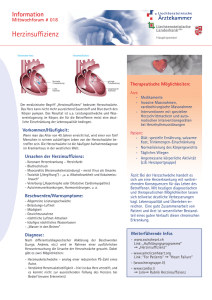
Therapie der Herzinsuffizienz
Werbung

Diplomarbeit Therapie der Herzinsuffizienz- einst und jetzt eingereicht von Alexandra Renka zur Erlangung des akademischen Grades Doktorin der gesamten Heilkunde (Dr. med. univ.) an der Medizinischen Universität Graz ausgeführt am Institut für Experimentelle und Klinische Pharmakologie unter der Anleitung von Univ. Prof. i.R. Mag. pharm. Dr. Eckhard Beubler Graz, 17.Juli 2015 I. Eidesstattliche Erklärung Ich erkläre ehrenwörtlich, dass ich die vorliegende Arbeit selbstständig und ohne fremde Hilfe verfasst habe, andere als die angegebenen Quellen nicht verwendet habe und die den benutzten Quellen wörtlich oder inhaltlich entnommenen Stellen als solche kenntlich gemacht habe. Graz, am 17.Juli 2015 Alexandra Renka eh 2 II. Danksagung Mein besonderer Dank geht an Univ.-Prof. i.R. Mag. pharm. Dr. Eckhard Beubler für seine kompetente und herzliche Betreuung. 3 III. Zusammenfassung Die Herzinsuffizienz zählt in der heutigen Zeit zu den häufigsten Erkrankungen der inneren Medizin. (1) Oft wird sie als „unentdecktes Volksleiden“ angesehen, da ihre Symptome wie z.B. die Atemnot bei physischer Anstrengung als Alterserscheinung bei Betroffenen falsch interpretiert werden. Schon in Zeiten vor Christi Geburt beschrieb man den Symptomenkomplex der Herzinsuffizienz und suchte nach Antworten in der Anatomie und Physiologie des Herzens , um Erkenntnisse über dieses Leiden zu gewinnen. Der erste Therapieansatz gelang mit der Einführung des Aderlasses. Dieser fand zu jener Zeit bei nahezu allen kardialen Erkrankungen Anwendung. Im 16. Jahrhundert beschrieb Leonhardt Fuchs erstmals die Herzdroge Digitalis und läutete damit die medikamentöse Behandlung ein. Durch die fortwährende Forschung und Durchführung von Studien konnten in den 1980-Jahren Inotropika und Vasodilatatoren sowie in den 1990er-Jahren ACE-Hemmer und Betablocker als zusätzliche Medikamente für die Behandlung der Herzinsuffizienz gewonnen werden. Darauf folgten maßgebliche Fortschritte in der Medizintechnik. Linksherzunterstützungssysteme und Resynchronisationssysteme wurden entwickelt und revolutionierten den Markt und somit die Kardiologie. Trotz der Etablierung neuer Therapiestrategien mit vielversprechenden Prognosen ist die Lebenserwartung von Herzinsuffizienzpatienten/-patientinnen dennoch eingeschränkt. Viel Hoffnung wird in die Stammzelltherapie gesetzt, die aktuell schon aussichtsreiche Ergebnisse erzielt. Bis man diese Ergebnisse umsetzten kann, werden noch Jahre bis Jahrzehnte vergehen. Die Therapie der Herzinsuffizienz befindet sich im stetigen Wandel. Deshalb werden im Rahmen dieser Literaturrecherche die Meilensteine und Misserfolge in der Herzinsuffizienztherapie kritisch gegenübergestellt und aktuelle Forschungsgebiete beschrieben. 4 IV. Abstract Heart failure is one of the most common diseases in internal medicine nowadays. It is often called an „undiscovered public disease“, because symptoms such as dyspnea under physical exertion are misinterpreted as signs of ageing. Even in times before Christ, people described the complex of symptoms and searched for answers in the anatomy and physiology of the heart to gain more knowledge. The first therapeutic approach was achieved by the introduction of bloodletting, at that time, was applied for almost all cardiac diseases. In the 16th century, Leonhardt Fuchs first described the heart drug Digitalis and marked the beginning of drug treatment. By continuing research and conducting studies, ACE inhibitors and beta blockers could be gained as additional medication for the treatment of heart failure in the 1980s, inotropes as well as vasodilators in the 1990s. This was followed by significant progress in medical technology. Left ventricular assist devices and resynchronizations systems were developed, and revolutionized the market and consequently cardiology. Despite establishing new therapeutic strategies with promising forecasts, life expectancy of heart failure patients is still limited. Experts have high hopes in stem cell research, which is currently already achieved promising results. However, years or even decades will pass before these results can be implemented. The approaches of heart failure treatment are constantly changing. Therefore, it is important and useful to compare milestones and unsuccessful methods in heart failure therapy critically within a literature review and describe current research. 5 V. Inhaltsverzeichnis I. EIDESSTATTLICHE ERKLÄRUNG .......................................................................................... 2 II. DANKSAGUNG .......................................................................................................................... 3 III. ZUSAMMENFASSUNG ............................................................................................................. 4 IV. ABSTRACT ................................................................................................................................ 5 V. INHALTSVERZEICHNIS ............................................................................................................ 6 VI. GLOSSAR UND ABKÜRZUNGEN ............................................................................................ 9 VII. TABELLENVERZEICHNIS ...................................................................................................... 11 1 DEFINITION ............................................................................................................................. 12 2 EINTEILUNG ............................................................................................................................ 13 3 2.1 LOW-OUTPUT-FAILURE VS HIGH OUTPUT FAILURE .................................................................. 13 2.2 LINKS- VS RECHTSHERZINSUFFIZIENZ ................................................................................... 14 2.3 SYSTOLISCHE VS DIASTOLISCHE HERZINSUFFIZIENZ .............................................................. 15 KLASSIFIKATION .................................................................................................................... 16 3.1 NEW YORK HEART ASSOCIATION ......................................................................................... 16 NYHA I 16 NYHA II 16 NYHA III 16 NYHA IV 16 3.2 AMERICAN HEART ASSOCIATION .......................................................................................... 17 Stadium A 17 Stadium B 17 Stadium C 17 Stadium D 17 4 EPIDEMIOLOGIE ..................................................................................................................... 18 5 GENDER ASPEKT ................................................................................................................... 19 6 ÄTIOLOGIE .............................................................................................................................. 21 7 6.1 SCHÄDIGUNG DES ARBEITSMYOKARDS: ................................................................................ 21 6.2 ERREGUNGSLEITUNGS- UND ERREGUNGSBILDUNGSSTÖRUNGEN ........................................... 21 6.3 BEEINTRÄCHTIGUNG DER VENTRIKELFÜLLUNG: ..................................................................... 21 6.4 AKUTE DRUCK- ODER VOLUMENBELASTUNG: ........................................................................ 22 6.5 CHRONISCHE DRUCK- UND VOLUMENBELASTUNG: ................................................................ 22 PATHOPHYSIOLOGIE ............................................................................................................ 24 6 7.1 FRÜHSTADIEN DER HERZINSUFFIZIENZ ................................................................................. 24 7.2 INTRAVASALE VOLUMENEXPANSION MIT HILFE DES FRANK-STARLING-MECHANISMUS ............. 24 7.3 MOBILISIERUNG DER MYOKARDIALEN KONTRAKTIONSRESERVE .............................................. 25 7.4 MYOKARDIALE HYPERTROPHIE............................................................................................. 25 7.5 SEKUNDÄRE KOMPENSATIONSMECHANISMEN IM SPÄTSTADIUM ............................................. 25 7.6 VERSAGEN DER PRIMÄREN UND SEKUNDÄREN KOMPENSATIONSMECHANISMEN ...................... 26 8 GESCHICHTE DER BEHANDLUNG VON HERZINSUFFIZIENZ .......................................... 27 8.1 DIE ANWENDUNG VON DIGITALIS ALS HEILMITTEL-EIN RÜCKBLICK.......................................... 29 8.2 GESCHICHTE DER ACE-INHIBITOREN ................................................................................... 31 8.3 GESCHICHTE DER DIURETIKA ............................................................................................... 32 8.3.1 Purine ................................................................................................................... 32 8.3.2 Quecksilberverbindungen .................................................................................... 32 8.3.3 Rein synthetisch gewonnene Diuretika ................................................................ 33 8.3.4 Thiaziddiuretika .................................................................................................... 34 8.3.5 Furosemid ............................................................................................................ 34 8.3.6 Kaliumsparende Diuretika .................................................................................... 34 8.3.7 Spironolacton ....................................................................................................... 34 8.3.8 Cycloamidine ........................................................................................................ 35 8.4 BETABLOCKER .................................................................................................................... 35 9 STUDIEN BEI HERZINSUFFIZIENZ PATIENTEN .................................................................. 36 10 AKTUELLE MEDIKAMENTÖSE THERAPIE DER HERZINSUFFIZIENZ .............................. 41 10.1 10.1.1 Blockade des Renin-Angiotensin-Aldosteron-Systems ....................................... 41 10.1.2 Mineralokortikoidrezeptorantagonisten ................................................................ 42 10.1.3 Ivabradin............................................................................................................... 42 10.1.4 Digitalis ................................................................................................................. 43 10.1.5 Diuretika ............................................................................................................... 43 10.2 11 SYSTOLISCHE HERZINSUFFIZIENZ......................................................................................... 41 DIASTOLISCHE HERZINSUFFIZIENZ........................................................................................ 46 CHIRURGIE DER HERZINSUFFIZIENZ.................................................................................. 47 11.1 ORGANERHALTENDE EINGRIFFE ........................................................................................... 47 11.1.1 Mitralinsuffizienz-Therapie ................................................................................... 47 11.1.2 Revaskularisation der Koronargefäße ................................................................. 48 11.2 HERZERSATZTHERAPIE ........................................................................................................ 49 11.2.1 Die Kunstherzen ................................................................................................... 49 11.2.1.1 Extrakorporale Membranoxigenierung (ECMO) ................................................................ 49 11.2.1.2 Extrakorporale ventrikuläre Assistenzsysteme .................................................................. 49 11.2.1.3 Intrakorporale ventrikuläre Assistenzsysteme .................................................................. 50 11.2.2 Komplettes Kunstherz .......................................................................................... 51 7 11.3 HERZTRANSPLANTATION ...................................................................................................... 52 11.3.1 Indikation und Vorbereitung ................................................................................. 52 11.3.2 Technik ................................................................................................................. 53 11.3.2.1 Orthotope Herztransplantation .......................................................................................... 53 11.3.2.2 Heterotope Herztransplantation......................................................................................... 53 12 ZUKUNFTSASPEKTE ............................................................................................................. 54 12.1 STAMMZELLEN .................................................................................................................... 54 12.1.1 Stammzelltherapie bei Herzinsuffizienz ............................................................... 54 13 MATERIAL UND METHODEN ................................................................................................. 56 14 DISKUSSION ........................................................................................................................... 57 15 LITERATURVERZEICHNIS ..................................................................................................... 58 8 VI. Glossar und Abkürzungen ACE Angiotensin-Converting-Enzyme ADH antidiuretisches Hormon ANF atrialer natriuretischer Faktor ARB Angiotensin-Rezeptor-Blocker BPF bradykininpotenzierender Faktor CRT Cardiac Resynchronization Therapy CRT-D Cardiac Resynchronization Therapy Defibrillator ECMO Extracorporale Membrane Oxygenation EF Ejektionsfraktion EGFP Enhanced green fluorescent protein FACS Fluorescent Activated Cell Sorting HF Heart Failure HI Herzinsuffizienz HTX Herztransplantation ICD Implantable Cardioverter Defibrillator If-Kanal Ionenblocker-Kanal LVAD Left Ventricular Assist Device LV-Dilatation Left Ventricular-Dilatation LVEF Left Ventricular Ejection Fraction MACS Magnetic Activated Cell Sorting MRA Mineralkortikoidantagonist n-3 PUFAc n-3 Polyunsaturated fatty acid NYHA New York Heart Association pro Mio. EW pro Millionen Einwohner RAAS Renin Angiotensin Aldosteron System 9 SCNT Somatic Cell Nuclear Transfer ß-Blocker Beta-Blocker VADs Ventricular Assist Devices 10 VII. Tabellenverzeichnis Tabelle 1.................................................................................................12 Tabelle 2.................................................................................................23 Tabelle 3.................................................................................................28 Tabelle 4.................................................................................................44 Tabelle 5.................................................................................................45 Tabelle 6.................................................................................................52 11 1 Definition In den letzten Jahrzehnten hat sich die Definition der Herzinsuffizienz stetig verändert. Verantwortlich für diesen Wandel waren allen voran Veränderungen in wissenschaftlichen Paradigmen und neue pathophysiologische und pathobiochemische Erkenntnisse. (2) Eine Auflistung einiger Definitionen findet sich in der nachstehenden Tabelle 1. 1933 “Unfähigkeit des Herzens adäquat zu entleeren.“ 1950 „Zustand des Herzens, bei dem es nicht in der Lage ist, eine adäquate bedarfsgerechte Perfusion trotz normaler Füllungsdrücke herzustellen.“ 1980 „Pathophysiologischer Zustand, bei dem die Myokardfunktion abnormal ist und nicht in der Lage ist, die periphere Bedürfnisse metabolisierender Gewebe sicherzustellen.“ 1987 „Ein Syndrom bei dem das Herz chronisch unfähig ist, einen adäquat hohen Blutdruck ohne äußere Unterstützungsmaßnahmen herzustellen.“ 1988 „Ein Syndrom der kardialen Dysfunktion , das mit Arrhythmierate und einer verkürzten Lebensdauer assoziiert ist.“ 1995 „Die Unfähigkeit des Herzens, Blut und daher Sauerstoff in einem Maße, das den Bedürfnissen gerecht wird, zu den Organen zu transportieren (pathophysiologisch). Klinisch bedeutet Herzinsuffizienz, das dem Symptomkomplex der Luftnot und schnellen Ermüdbarkeit eine kardiale Erkrankung als Ursache zugrunde liegt.“ Tabelle 1 nach (2) Eine aktuelle Definition der ESC beschreibt die Herzinsuffizienz als die Unfähigkeit des Herzens, aufgrund abnormer kardialer Strukturen und Funktionen, periphere Gewebe mit Sauerstoff zu versorgen. Klinisch ist die Herzinsuffizienz als Syndrom mit typischen Symptomen definiert: unter Anderem durch Atemnot, Leistungsschwäche, Müdigkeit, Knöchelödeme und Zeichen, die aus einer abnormen kardialen Struktur resultieren. (3) 12 2 Einteilung Die Herzinsuffizienz kann nach vielen verschiedenen Gesichtspunkten eingeteilt werden: 2.1 Low-output-failure vs High output failure Low-output-failure: Das Herz hat keine ausreichende Auswurfleistung oder kann diese nur durch einen erhöhten Füllungsdruck erreichen: wie z.B. bei intrinsischer Herzmuskelerkrankungen (Kardiomyopathie, Myokarditis, Chagas-Krankheit, Koronare Herzkrankheit) chronischer übermäßiger Nachlast (Aortenstenose, Hypertonie) chronischer übermäßiger Vorlast (Mitralinsuffizienz) negativer inotroper Medikamente (Antiarrhythmische Medikamente) eingeschränktem Füllungsvolumen (konstriktive Perikarditis oder Tamponade, restriktive Kardiomyopathie) ausgeprägter Bradykadie (Beta-Blocker, kompletter Herzblock) High-output-failure: Das Herz ist nicht in der Lage die Auswurfleistung auf ein normales oder erhöhtes Niveau zu halten, wie es bei einer Anämie, einer Hyperthyreose, einem Morbus Paget oder einer AV-Malformation notwendig wäre. Zuerst überwiegen die Symptome einer Rechtsherzinsuffizienz, später die der Linksherzinsuffizienz. Es ist schwer festzustellen, ob ein Patient/eine Patientin mit hoher Auswurfsleitung eine Herzinsuffizienz entwickelt hat. Der einzige Anhaltspunkt für die Entwicklung einer kongestiven Herzinsuffizienz bei diesen Patienten/Patientinnen ist eine verkürzte Durchblutungszeit. (4) 13 2.2 Links- vs Rechtsherzinsuffizienz Linksherzinsuffizienz: einer primären Die linksventrikuläre Funktion kann entweder aufgrund ventrikulären Dysfunktion oder aufgrund eines starken Ventrikeldruckes, hervorgerufen durch einen arteriellen Hypertonus, beeinträchtigt werden. In beiden Fällen führt eine unzureichende linksventrikuläre Pumpfunktion zum einem erhöhten Druckaufbau im linken Vorhof. Der Rückstau wird auf die Lungenvenen und -kapillaren übertragen und führt zu einer Lungenstauung. In frühen Stadien kann die Lungenstauung durch Rasselgeräusche diagnostiziert werden, die bei einer Auskultation der Brust vorliegen. Falls die Lungenstauung fortschreitet, kann ein Lungenödem, mit einer Symptomatik bestehend aus Husten und Dyspnoe, auftreten. Da die Lungenstauung im Liegen ausgeprägter ist als im Sitzen, ist folglich auch die Atemnot im Liegen stärker: dies ist auch unter dem Begriff Orthopnoe bekannt. Ein verminderter linksventrikulärer Auswurf führt zum anderen zur Beeinträchtigung der Gewebedurchblutung, die zur Gewebehypoxie und zu Folgeerscheinungen führt. (5) Rechtsherzinsuffizienz: Eine primäre ventrikuläre Dysfunktion ist manchmal Auslöser einer Beeinträchtigung der rechtsventrikulären Funktion. Häufiger ist sie sekundär, infolge einer Überlast, die von einer Mitralstenose oder einer parenchymalen Lungenerkrankung ausgeht, wie Lungenemphysem oder Fibrose. Eine Rechtsherzinsuffizienz, die auf Lungenerkrankungen zurückzuführen ist, wird als Cor pulmonale bezeichnet. Wie auch im Fall einer Linksherzinsuffizienz, führt die Rechtsherzinsuffizienz zu einem Rückstau im rechten Vorhof und in den Venen. Eine venöse Stauung führt zu einem erhöhten Jugularvenendruck, Beinödemen, Aszites und zu einer Blutansammlung in der Leber, die eine Lebervergrößerung verursacht. (5) 14 2.3 Systolische vs diastolische Herzinsuffizienz Die systolische und diastolische Herzinsuffizienz sind Krankheitsbilder, die sowohl einfach und zugleich schwer zu definieren sind. Die systolische und diastolische Herzinsuffizienz wird wie folgt leicht definiert: Die systolische Herzinsuffizienz wird durch Beeinträchtigung des Auswurfs verursacht, während die diastolische Herzinsuffizienz auftritt, wenn die Füllung beeinträchtigt ist. Allerdings sind diese Definitionen nicht gültig, da ein Ventrikel der einen verminderten Auswurf vorweist, normalerweise auch nicht normal gefüllt werden kann und umgekehrt. Aus diesem Grund vertraut man bei der Unterscheidung auf die ventrikuläre Architektur: der Ventrikel ist bei Patienten/Patientinnen mit systolischer Herzinsuffizienz dilatiert, während das Herzkammervolumen bei diastolischer Herzinsuffizienz normal, leicht reduziert oder etwas erhöht sein kann. Der Wert der Ejektionsfraktion wird in der Regel verwendet, um zwischen der systolischen und diastolischen Herzinsuffizienz zu unterscheiden. Sie wird aus dem Verhältnis von Schlagvolumen und enddiastolischen Volumen gebildet. Da die Absolutwerte sowohl für das Schlagvolumen als auch für das EDV klinisch schwer zu messen sind, ist die EF der entscheidendste Parameter für diese Unterscheidung geworden. Der Ratio kann unter der Verwendung nicht invasiver Methoden, allen voran der Echokardiografie, bestimmt werden. (6) 15 3 Klassifikation 3.1 New York Heart Association Die NYHA-Klassifikation teilt die Symptomatik der chronischen Herzinsuffizienz in unterschiedliche Grade ein: NYHA I: Herzerkrankung ohne körperliche Limitation: Alltägliche körperliche Belastungen verursachen keine inadäquate Erschöpfung, Rhythmusstörungen, Luftnot oder Angina pectoris. NYHA II: Patienten/Patientinnen mit Herzerkrankungen und leichter Einschränkung der körperlichen Leistungsfähigkeit: keine Beschwerden in Ruhe; alltägliche körperliche Belastung verursacht Erschöpfung, Rhythmusstörungen oder Angina pectoris. NYHA III: Patienten/Patientinnen mit Herzerkrankung und höhergradiger Einschränkung der körperlichen Leistungsfähigkeit: Keine Beschwerden in Ruhe; geringe körperliche Belastung verursacht Erschöpfung, Rhythmusstörungen, Luftnot oder Angina Pectoris. NYHA IV: Patient/Patientin mit Herzerkrankung: Beschwerden bei allen körperlichen Aktivitäten und oft in Ruhe. (7) 16 3.2 American Heart Association Da sich die Herzinsuffizienz Symptomatik stetig verschlechtert, aber auch durch eine passende Behandlung eine Besserung erreicht werden kann, hat die American Heart Association eine zusätzliche Klassifikation eingeführt, die eine stabilere Einteilung des Syndroms vorsieht. Diese Einteilung basiert auf dem kardiovaskulären Kontinuum und beschreibt den Weg der terminalen ohne strukturelle Herzinsuffizienz. Stadium A: Hohes Risiko für eine Herzinsuffizienz Herzerkrankung oder Symptome Stadium B: Strukturelle Herzerkrankung ohne Auftreten von Symptomen einer Herzinsuffizienz Stadium C: Strukturelle Herzerkrankungen mit vorliegenden oder ehemals vorgelegenen Symptomen einer Herzinsuffizienz Stadium D: Therapierefraktäre Herzinsuffizienz, die spezielle Interventionen erfordert. (7) 17 4 Epidemiologie Die Prävalenz der Herzinsuffizienz in Europa wird mit 2-3% angegeben. Bei 70bis 80-Jährigen beträgt sie 10-20%. (8) Innerhalb der Framingham-Studie konnten erste umfassende Informationen zur Inzidenz veröffentlicht werden. Die Studie umfasste 5209 Männer und Frauen, die jährlich bezüglich der Entstehung einer Herzinsuffizienz beobachtet wurden. Nach einem Beobachtungsintervall von 32 Jahren konnte bei 485 Männer und Frauen eine klinisch erkennbare Herzinsuffizienz festgestellt werden. (9) 18 5 Gender Aspekt Männer und Frauen besitzen signifikante Unterschiede in der Herzinsuffizienz im Bereich der Risikofaktoren und der Sterblichkeit. Die Gründe für diese Unterschiede sind multifaktoriell. So spiegeln sie zum Teil ein unvollständiges Verständnis der Geschlechtsunterschiede in der Ätiologie der Herz-KreislaufErkrankungen wider, zum Anderen verweigern sie die Berücksichtigung von Geschlechtsunterschieden in präklinischen Studien einschließlich zukunftsorientierter Diagnostik- und Behandlungsmethoden. (10) Die leitenden Risikofaktoren für die Entstehung der Herzinsuffizienz sind Diabetes und arterieller Hypertonus. Die Herzinsuffizienz verläuft generell bei Frauen sanfter und zeichnet sich durch eine gut funktionierende systolische Ventrikelfunktion aus. Oftmals wird eine diastolische Funktionsstörung beobachtet. Als Ursache vermutet man, dass sich das myokardiale Remodelling im fortgeschrittenen Alter, aufgrund mechanischer Beanspruchung bei beiden Geschlechtern, verschieden abspielt. Das Herz besitzt Östrogenrezeptoren. Anhand von Tiermodellen konnte festgestellt werden, dass Östrogenrezeptoren das Fortschreiten der Herzmuskelhypertrophie Herzinsuffizienz modulieren. Eine und die Reihe der Entwicklung dafür der notwendigen Stoffwechselvorgänge sind heute erforscht und beinhalten z.B. die Herstellung von Stickstoffmonoxid und die Phosphorylierung intrazellulärer Kinasen. (11) 19 Im hohen Alter kann man bei Herzinsuffizienz und Hypertrophie einen Anstieg der Östrogenrezeptoren im Herzmuskel beobachten. Die Befolgung der Leitlinien zur Beurteilung und Behandlung der Herzinsuffizienz wird bei Männern strenger durchgeführt als bei Frauen. Statistisch gesehen bilden Frauen in klinischen Studien die Minderheit. Auch in sämtlichen früheren Überlebensstudien wurde auf eine geschlechtsspezifische Darstellung verzichtet. Bei einer Anzahl von Studien der Angiotensin-Converting-Inhibitoren, konnte bei der Auswertung der Endpunkte keine statistische Aussagekraft für Frauen ausfindig gemacht werden. Jedoch gibt es Metaanalysen, die einen gänzlich positiven Effekt dieser Subtanzgruppe bei Frauen festgestellt haben. Auch für ß-Blocker konnte die Wirkung auf Frauen bei Metaanalysen bewiesen werden. In groß angelegten Studien mit hoher Frauenbeteiligung konnten Angiotensinrezeptorblocker in der Therapie der Herzinsuffizienz überzeugen. Eine Erklärung für die geringere Mortalitätsrate bei Frauen bietet möglicherweise die Digitalis Medikation, da die Effekte von Digitalis im starken Ausmaß blutdruckabhängig sind. (11) 20 6 Ätiologie Die Herzinsuffizienz ist ein pathophysiologischer Komplex, der mit einer Dysfunktion des Herzens einhergeht und eine gemeinsame Endstrecke für viele kardiovaskuläre Erkrankungen bildet. (12) Zu den Ursachen zählen die nachfolgenden Funktionsbeeinträchtigungen: 6.1 Schädigung des Arbeitsmyokards: Eine akute Herzinsuffizienz Sauerstoffversorgung kann durch (Myokardischämie) eine oder spontan durch die verringerte komplette Unterbrechung der Sauerstoffzufuhr eines Herzmuskelareals, infolge eines Herzinfarkts, entstehen. Vereinzelt ist als Ursache eine Myokarditis zu beobachten. Eine chronische Herzinsuffizienz entsteht stattdessen bei einer langsam fortschreitenden koronaren Herzkrankheit oder infolge kleiner Infarkte die zur Überforderung der noch intakten Myokardfasern führen. (13) Kardiomyopathien sorgen für eine beeinträchtigte Kontraktilität des Herzmuskels und führen somit auch zu einer verringerten Pumpleistung. Zu den weiteren Ursachen einer chronischen Herzinsuffizienz zählen Allgemeinerkrankungen, wie Beri-Beri, Amyloidose. Weiters auch die Glykogenspeicherkrankheit und toxische Myokardschädigungen, die durch Alkoholabusus, Arsen und Quecksilber verursacht wurden. (13) 6.2 Erregungsleitungs- und Erregungsbildungsstörungen Das Herz kann bei unkontrollierter Kammerkontraktion (z.B. Kammerflimmern, AV-Block III. Grades), sowie bei zu niedriger Herzfrequenz nicht adäquat pumpen. (13) 6.3 Beeinträchtigung der Ventrikelfüllung: Ausgeprägte Tachykardien, Herzbeuteltamponaden, Trikuspidal- bzw. Mitralklappenstenosen, konstriktive oder restriktive Kardiomyopathien führen zu einer unvollständigen Kammerfüllung und folglich zu einer herabgesetzten Auswurfleistung. (13) 21 6.4 Akute Druck- oder Volumenbelastung: Tritt eine Papillarmuskelruptur im Rahmen einer akuten Mitralinsuffizienz auf, kommt es zu einer akuten Volumenbelastung des linken Ventrikels. Beide Ventrikel sind involviert, wenn eine Perforation des interventrikulären Septums stattfand. Auslöser für eine akute Druckbelastung des rechten Ventrikels ist z.B. eine massive Lungenembolie. Leidet der Patient/die Patientin an einer hypertensiven Krise, führt dies zu einer Druckbelastung des linken Ventrikels. Akute Druck- und Volumenbelastungen des Herzens können Grund einer Herzinsuffizienz sein. Erhöht sich das Volumen, vergrößert sich auch die Herzkammer und kann bei gleichbleibender Länge der Sarkomere ein größeres Schlagvolumen pumpen. Aus Sicht des Frank-Starling Mechanismus verstärkt sich parallel die Kontraktionskraft der Myokardfaser. (14) Ebenfalls verstärkt sich die Wandspannung mit der Vergrößerung des Wanddurchmessers und der daraus folgenden Abnahme des Wanddurchmessers. Dies kann mithilfe des La-Place Gesetzes erläutert werden: (14) σ Wandspannung; P Ventrikelinnendruck; r Radius des Hohlraums (Kugelmodell); d Ventrikelwanddicke (2) 6.5 Chronische Druck- und Volumenbelastung: Entwickelt sich eine Aortenklappeninsuffizienz, kommt es zu einer chronischen Volumenbelastung des linken Ventrikels. Der rechte Ventrikel ist bei einem defekten Vorhofseptum betroffen. Lastet auf beiden Ventrikel eine chronische Volumenerhöhung, kann eine große arterio-venöse Fistel vorliegen. Die chronische Volumenbelastung führt zur Ausbildung einer exzentrischen Hypertrophie. (14) Besteht eine Pulmonalklappenstenose bzw. eine pulmonale Hypertonie, kommt es zu einer chronischen Druckbelastung der rechten Kammer. Liegt eine arterielle Hypertonie oder eine Aortenklappenstenose vor, herrscht vorerst nur eine chronische Druckbelastung der linken Kammer. Die chronische Volumenbelastung führt zu der Ausbildung einer konzentrischen Hypertrophie. (14) Die unten dargestellte Tabelle 2 zeigt nochmals alle Ätiologien: 22 Erniedrigte Ejektionsfraktion (<40%) Koronare Herzkrankheit Myokardinfarkta Myokardischämiea Chronische Drucküberlastung Bluthochdrucka Obstruktive Klappenerkrankunga Chronische Volumenüberlastung Klappenerkrankung mit Regurgation Intrakardialer (Links-Rechts) Shunt Extrakardialer Shunt Erhaltene Ejektionsfraktion (>40-50%) Pathologische Hypertrophie Primär (hypertrophe Kardiomyopathien) Sekundär (Bluthochdruck) Alter Nicht ischämische dilatative Kardiomyopathie Familiäre/genetische Störungen Infiltrative Störungena Toxischer/drogeninduzierter Schaden Metabolische Störunga Viral Chagas-Krankheit Störungen von Herzfrequenz und Rhythmus Chronische Bradyarrhythmien Chronische Tachyarrhythmien Restriktive Kardiomyopathie Infiltrative Störungen (Amyloidose, Sarkoidose) Speicherkrankheiten (Hämochromatose) Fibrose Endomyokardiale Störungen Exzessive Blutflussanforderungen Systemische AV-Shunts Chronische Anämie Pulmonale Herzkrankheit Cor pulmonale Pulmonale Klappendysfunktionen Zustände mit hohem Auswurf Metabolische Störungen Hyperthyreose Ernährungsstörungen (Beriberi) Tabelle 2 nach (50) a Merke: Zeigt Bedingungen an, die auch zu einer Herzinsuffizienz bei erhaltener Injektionsfraktion führen können. 23 7 Pathophysiologie 7.1 Frühstadien der Herzinsuffizienz In den Frühstadien der Herzinsuffizienz stehen „primäre Kompensationsmechanismen“ im Vordergrund um das Herzzeitvolumen trotz Behinderungen zu erhalten. Erst in späteren Stadien kommt es zur Angleichung des Organismus an das verringerte Herzzeitvolumen durch „sekundäre Kompensationsmechanismen“. Die nachfolgenden primären Kompensationsmechanismen spielen in den Frühphasen eine wichtige Rolle. (15) 7.2 Intravasale Volumenexpansion mit Hilfe des Frank-StarlingMechanismus Frank-Starling-Mechanismus 1895 konnte Otto Frank anhand von Beobachtungen beweisen, dass die Spannungsentwicklung des Myokards von seiner Vordehnung abhängig ist. Wird ein bestimmter Bereich erzielt, führt ein Zuwachs des Muskels zu einer Erhöhung der aufgebauten Muskelspannung. Nachfolgend, im 20.Jahrhundert, hat der englische Physiologe Starling durch zusätzliche Studien erkannt, dass die gezeigten Gesetzmäßigkeiten nicht nur für Frösche sondern auch für Warmblüter gelten. (15) Auf zellulärer Ebene, kommt es zu einer Änderung der Aktin-Myosin-Überlappung und zu einer dehnungsabhängigen Steigerung der Empfindlichkeit des kontrakilen Apparats für Ca2+. (16) Ist das Herz gesund, kann durch diesen Mechanismus das Schlagvolumen durch erhöhte diastolische Füllung intensiviert werden. Leidet der Patient/die Patientin aber an einer Herzinsuffizienz, bedarf es einem stärkeren Füllungsdruck um das optimale Schlagvolumen zu erreichen. Das optimale Schlagvolumen ist niedriger angesetzt, im Vergleich zu einem gesunden Herzen mit tiefliegendem Füllungsdruck. (15) 24 7.3 Mobilisierung der myokardialen Kontraktionsreserve Die Steigerung der Kontraktilität des Herzmuskels kann sowohl neuronal als auch humoral erfolgen. Ziel ist eine Erhöhung der Schlagvolumia und somit eine Verschiebung der Frank-Starling Kurve. Der neuronale Weg wird durch postganglionäre Halsganglien, Neuronen in erster des Linie Sympathikus dem Ganglion beschrieben, stellatum, die mit von den peripheren sympathischen Nerven und Spinalnerven zum Herzen führen. Vor Ort wird positiv inotrop wirkendes Noradrenalin ausgeschüttet, welches an die Myozyten abgegeben wird. Humoral wird die Kontraktilität durch die Ausschüttung der Neurotransmitter Adrenalin und Noradrenalin gelenkt. Der vasokonstriktorische Effekt von Noradrenalin überwiegt, da Adrenalin sowohl alpha als auch beta vermittelt zu einer Kontraktilitätssteigerung und peripherenen Vasokonstriktion führt. (15) 7.4 Myokardiale Hypertrophie Das Herz antwortet auf zunehmende Arbeit mit der Ausbildung einer myokardialen Hypertrophie. Im Anschluss an die Neonatalzeit verbleiben Herzmuskelzellen in einem irreversiblen postmitotischen Stadium. Die Hypertrophie der Muskelmasse kann deshalb nur durch Vermehrung der Sarkomere zustande kommen. (17) Durch die Zunahme kommt es zu einem beträchtlichen Anstieg der myokardialen Masse. Betreffend der ventrikulären Geometrie, kann zwischen einer Hypertrophie mit Dilatation des Ventrikels und mäßiger Wanddickenzunahme und einer Hypertrophie mit relativer Verringerung des Ventrikels und anschaulicher Wanddickenzunahme differenziert werden. (15) 7.5 Sekundäre Kompensationsmechanismen im Spätstadium Um das herabgesetzte Herzzeitvolumen zu kompensieren, wird kurzzeitig die Blutversorgung nicht primär lebenswichtiger Organsysteme wie Niere, MagenDarm-Trakt, Haut und Skelettmuskulatur durch Verengung der zugehörigen Blutgefäße vermindert. Kompensationsmechanismus Diesen nennt man entscheidenden Zentralisation. sekundären Sie dient der Aufrechterhaltung einer ausreichenden Perfusion lebenserhaltender Organe, wie Herz, Gehirn und Lunge. (15) 25 Das autonome Nervensystem steuert die periphere Vasokonstriktion durch Ausschüttung von Neurotransmittern. Diese steigern die Kontraktionskraft des Herzmuskels, vor Allem aber auch den peripheren arteriellen Gefäßwiderstand. Zeitgleich bewirkt das Renin-Angiotensin-Aldosteronsystem (RAAS) eine Retention von Wasser und Natrium und aktiviert das sympathische Nervensystem. Bei einer Herzinsuffizienz im Anfangsstadium nehmen Barorezeptoren schon eine minimale Abnahme des Herzzeitvolumens in Ruhe wahr. Die Noradrenalin Ausschüttung wird dementsprechend unterbrochen. Zeitgleich wird der gefäßdilatierende und diuretische Effekt des Atrialen Natriuretischen Faktors genutzt. ANF wird dazu von der Muskulatur der Herzvorderkammer ausgeschüttet, wirkt antagonistisch zu Noradrenalin und hemmt somit den ungezügelten Anstieg des peripheren Widerstandes. (15) 7.6 Versagen der primären und sekundären Kompensationsmechanismen Im Spätstadium kommt es schlussendlich zum Versagen der Kreislaufreflexe. Die kontinuierliche Überstimulation senkt die Empfindlichkeit der atrialen Dehnungsfaktoren. Das Ergebnis ist eine unkontrollierte ADH-Sekretion mit Rückhalt von Wasser und Ausbildung einer Hyponatriämie sowie eine verstärkte periphere Vasokonstriktion. Auch eine Kompensation der Effekte durch ANF ist nicht mehr möglich. Ist die Herzinsuffizienz stark fortgeschritten, kommt es zusätzlich zu einer beeinträchtigten Nierenperfusion und somit zur weiteren Stimulation des Renin-Angiotensin-Systems. Ein Circulus vitiosus ist entstanden, da die unkontrollierte Steigerung des peripheren Widerstands zu einer Erhöhung der Nachlast führt, die wiederum eine Abnahme des Schlagvolumens mit sich bringt. (15) Im finalen Stadium erreicht der Noradrenalinspiegel im Plasma sein Maximum. Bleibt der Noradrenalinwert länger erhöht, kommt es zu einem Rückgang der ß1Rezeptordichte im Myokard. ß1-Rezeptoren schützen generell den Herzmuskel. (15) 26 8 Geschichte der Behandlung von Herzinsuffizienz Schon um 1550 vor Chr. wurde nicht nur das Wort „Herz“ das erste Mal erwähnt, sondern auch eine Beschreibung der Herzinsuffizienz:„ zu müde, um zu sprechen“ formuliert. Im 18.Jahrhundert und in den darauffolgenden 2 Jahrhunderten stand die rheumatische Herzerkrankung als führende Ursache der Herzinsuffizienz im Mittelpunkt. In dieser Zeit studierte man die geometrische Umgestaltung des Herzens (Remodelling), insbesondere bei Patienten/Patientinnen mit Klappenvitien. (18) Durch die Errungenschaften im Bereich der Mikroskopie und Histologie im 19. Jahrhundert gelang es zusätzliche pathogenetische Differenzierungen der Ursachen zu finden. Rudolph Virchow grenzte die interstitielle von der parenchymatösen Entzündung ab und stellte fest, dass der von ihm bewiesene Entzündungsprozess eine grundlegende Ursache der Herzdilatation ist. Einen wichtigen Beitrag für das Verständnis der Entstehung der Herzinsuffizienz leistete 1892 William Osler. In seinem Werk „The priciples and practice of medicine“ wird die Entwicklung der Herzhypertrophie in Anbetracht der Ursachen in 3 Stadien geteilt: Entwicklungsphase Kompensationsphase Phase der Dekompensation Weitere Meilensteine bis zum 19.Jahrhundert sind nachfolgend in Tabelle 3 aufgelistet. (18) 27 Name Hippokrates Daten 467-377 v.Chr. Celsus, A. 25 v.Chr.-50 n.Chr. Galen, C. 130-ca.200 n.Chr. Aretaeus von um 150 n. Kappadozien Chr. Avicenna, I.S. 980-1037 Servetus, M. Capivaccius, H Carolus Piso 1553 verstarb 1589 1563-1633 Harvey, W. 1587-1657 Rivière, L. 1589-1655 Malpighi, M. 1628-1694 Lower, R. 1631-1691 Lancisi, G.M. 1654-1720 de Sénac, J.B. 1693-1770 Morgagni, G.B. 1682-1771 Withering, W. 1741-1799 1755-1821 Corvisart, J.N. Verdienst Detaillierte Beschreibung der Symptome der Herzinsuffizienz, Differenzierung von Ödemen Beschreibung der akuten Herzinsuffizienz im hämorrhagischen Schock Beschreibung der Funktion des Herzens im Sinne von Diastole und Systole Beschreibung der Rechtsherzinsuffizienz bei Cor pulmonale Diastolische Dysfunktion des Herzens bei Perikarderguss Beschreibung des Lungenkreislaufs Verminderung des Pulses beim kardiogenen Schock und bei der Synkope Symptome der paroxysmalen nächtlichen Dyspnoe Entdeckung des Blutkreislaufs „Exercitatio anatomica de motu cordis et sanguinis in animalibus“ (1628), Schwäche des Pulses als Zeichen der Herzinsuffizienz In „Opera omnia“: Beschreibung der klinischen Zeichen der Herzinsuffizienz und Zuordnung zum Pumpversagen des Herzens Entdecker der Kapillaren, beschrieb die Transsudation von Flüssigkeit ins Interstitium als ein Charakteristikum der Herzinsuffizienz Verminderte kardiale Kontraktilität bei Herzinsuffizienz in „Tractus de Corde“ (1669), Konzept der fettigen Degeneration des Herzens Beschreibt in seinem Buch „de subitaneis mortibus“(1702) den Mechanismus, durch welchen das Pumpversagen des Herzens eine Dyspnoe verursacht. Unterscheidung zwischen Dilatation („dilatatione“) und Hypertrophie („augmento molis“) Unterscheidung zwischen Herzdilatation und Atrophie in „Traité de la Structure du Coeur, de son Action et ses Maladies“ (1749) Beschreibt in seinem Werk „de sedibus et causus morborum“ (1761), dass eine mechanische Überlastung des Herzens eine Hypertrophie bedingt und erkennt deren kompensatorische, adaptive Natur Entdeckung der Wirkung der Herzglykoside „An Account of the Foxglove“ (1785) Einteilung des Umbaus des Herzens zum einen als aktives Aneurysma (Hypertrophie), zum anderen als passives Aneurysma (Dilatation) bei Aortenstenose bzw. Insuffizienz. Zwei prinzipielle 28 Möglichkeiten, an Herzinsuffizienz zu sterben Bertin, R.J.H. F.I. Kreysing 1767-1828 Hope, J. 1801-1841 langsam fortschreitendes Pumpversagen plötzlicher Herztod Unterscheidung zwischen konzentrischer und exzentrischer Hypertrophie Therapie mit Digitalis bei Wassersucht und Herzvergrößerung Therapie des Rückwärtsversagen des Herzens (1831) 1770-1839 Tabelle 3 nach (18) 1902 konnte das Vorwärtsversagen durch die Arbeit von James Mackenzie beschrieben nach und erklärt werden. Liljestrand bewies 1938, den Errungenschaften von Frank und Starling im Jahre 1895 und 1918, dass nicht nur das enddiastolische Volumen die Steuerung der Herzleistung beeinflusst. Diese Beobachtung und weitere in Studien gewonnene Erkenntnisse, verhalfen der Forschung zu einer vermehrt biochemisch orientierten Suche. Dies führte zur Aufklärung der Proteine und ihrer Wechselwirkungen. Molekularbiologische Verfahren, die Erforschung der genetischen Steuerung des myokardialen Zelllwachstums und die Entstehung der Herzhypertrophie konnten die Proteinstruktur entschlüsseln. (18) 8.1 Die Anwendung von Digitalis als Heilmittel-ein Rückblick Die Verwendung Digitalis-ähnlicher Substanzen ist seit Hunderten von Jahren in der Volksmedizin bekannt. (19) Die Glykosiddroge mit der ältesten Geschichte ist die schwarze Nieswurz (Helleborus niger). In der griechischen Mythologie wird erzählt, dass Melampus, ein Ziegenhirte und Seher, die rasenden Töchter Proteus mit dieser Pflanze heilen konnte. Deshalb erhielt auch die Pflanze den griechischen Namen Melampodion. Seit dem Altertum fungierte es als Purgans und wurde hoch geschätzt. Das Purgieren, also das Abführen verdorbener Säfte, war Hauptbestandteil der Behandlung geistiger Erkrankungen. Paracelsus beschrieb die Wirkung der Niesenwurz folgendermaßen: „Es leert den Brunnen aus und die Bäche, die da von ihm fließen und die Wassersucht machen; also, das was da wächst, das wird hinweggenommen (…) so viel, dass es denen, die es nicht gesehen haben, nit gläublich ist, gleich als hätte Moses mit einer Rute in die Leber geschlagen, und liefe für und für nichts heraus als Wasser, (was vielleicht nicht 29 anders sein wird, denn daß Gott ebenso eine Rute schägt, wie Moses).“ Hier wird von der diuretischen Wirkung der Herzglykoside, speziell der Nieswurz gesprochen, die lange vor der Wirkung auf das Herz bekannt war. (20) Die Meerzwiebel (Urginea maritima), welche als Bestandteil das Digitaloid Scillaridin beinhaltet, wurde von Ägyptern und Syrern, später von den Römern in der „Herztherapie“ als Diuretikum eingesetzt. In Afrika nutzten die Naturvölker das Wissen über die toxische Wirkung des Hundsgiftgewächses (Strophantus kombé) für die Herstellung von Giftpfeilen. (19) Offenbar nicht bekannt war im Altertum hingegen der Gift- und Heileffekt des Fingerhuts (Digitalis Purpurea). Hauptsächlich in den Blättern weist diese Pflanze neben Digitoxin noch die Substanzen Gitaloxin, Glucogitaloxin und Gitoxin auf. Ihr Einsatz, verbunden mit mystischen Bräuchen, wurde erstmals im 5.Jahrhundert in Irland erwähnt, wo sie als „fairies` herb“ zur Genesung verzauberter Kinder, oftmals mit tödlichem Ende, eingesetzt wurde. Der Fingerhut galt als Zeichen für Schönheit und Magie, aber auch für List und Zauberei. Der englische Name „foxglove“ ist auf eine Sage zurückzuführen. Auch in alten deutschen Schriften wurde wiederholt der Begriff „Fuchskraut“ verwendet. 1250 wurde die Pflanze durch walisische Ärzte zu den Arzneimittelpflanzen gezählt. Im Arzneibuch „Meddygon Myddvai“, verfasst von Rhiwallon, Leibarzt eines walisischen Prinzen, wurde die Verwendung von Digitalis Purpurea niedergeschrieben“. Darin ging er näher auf den äußerlichen Gebrauch von Fingerhutblättern, sowie die innerliche Anwendung gegen Kopfschmerzen ein. Digitalis Purpurea fand ferner Anwendung bei der Förderung des Auswurfs bei Bronchitis, als Brechmittel und bei der Behandlung der Schwindsucht. Weitere Anwendungsgebiete waren unter anderem die Verwendung als „Wundpulver“. (19) Leonhart Fuchs, ein Botaniker, verdanken wir die erste wissenschaftliche Beschreibung von Digitalis Purpurea im Jahre 1542. Der Name „Fingerhut“ erschien erstmals in seinem verfassten Kräuterbuch. Der Name wurde wegen der Blütenform gewählt, die an den, von Schneidern verwendeten Fingerhut erinnert. (19) Der letzte bedeutende Fund auf dem Sektor der Glykosidpflanzen fiel auf das Jahr 1785. William Withering, ein Schotte, erwähnte erstmals die diuretische 30 Eigenschaft der Fingerhutblätter. (20) 1775 soll seine Neugierde geweckt worden sein, als er Bekanntschaft mit einer Patientin mit fortgeschrittener Herzinsuffizienz machte, deren Verfassung sich nach Monaten eindrucksvoll verbessert hatte. Diese drastische Besserung, schrieb sie einem wirkungsvollen Elixier, einem Kräutertee zu, den ihr eine Kräuterfrau zuvor verabreicht hatte. In den darauffolgenden 3 Jahren führte Withering Tests an 163 seiner ödematösen Herzpatienten/-patientinnen durch, um die Wirksamkeit von Digitalis-Aufgüssen bei Ödemen, verursacht durch eine Herzinsuffizienz, zu beweisen. Aufgrund der Beobachtungen konnte Withering unter anderem darauf schließen, dass das Pflanzengift im Körper gespeichert wird, da sich die Wirkung der Substanz bei längerer Gabe verstärkte. Withering legte damit den Grundstein einer medizinisch fundierten Digitalisbehandlung. (19) Da das Risiko, die therapeutische Grenze zu übertreten groß war, setzte sich die Digitalisgabe bei Herzinsuffizienz erst allmählich durch, bis sie schließlich in der täglichen Praxis breite Zustimmung fand. Erst 100 Jahre nach Withering konnte man die Entschlüsselung der Chemie der nutzbringenden Digitalispräparate erreichen. Mittels Reinigungsverfahren konnten erste Substanzen gewonnen werden: die „Digitaline“. 1864 isolierte Nativelle eine Mixtur aus 3 Glykosiden, eines davon wurde später Digitoxin genannt. (21) 8.2 Geschichte der ACE-Inhibitoren Das Angiotensin-converting Enzym (ACE) ist ein Glykoprotein und hat ein Molekulargewicht von 150000. ACE bewirkt die Abspaltung von 2 Aminosäuren und wandelt somit Angiotensin I in Angiotensin II um. (18) 1965 entdeckte Ferreira, dass das Gift der Grubenotter Bothrops Jararaca eine Potenzierung von Bradykinin bewirken konnte. Nach Extrahieren einer Fraktion des Schlangengifts 1970, durchgeführt von Ferreira, wurde es „bradykininpotenzierender Faktor“ (BPF) genannt. (22) 1971 entdeckte Ondetti Teprotid, den ersten Hemmstoff des ACE, im Gift der Schlange Bothrops jararaca. 1977 wurde Captopril, als erster oral wirksamer ACE-Inhibitor, hergestellt. Der erste langanhaltende ACE-Inhibitor war Enalapril. (18) 31 8.3 Geschichte der Diuretika Die Entdeckungsgeschichte der Diuretika basiert vorwiegend auf Zufällen. Aus chemisch verschieden aufgebauten Substanzen, den Quecksilberverbindungen, den Sulfonamiden und den Purinen, deren diuretische Wirkung einstweilen als Nebenwirkung galt, konnte die Forschung eine Arzneimittelgruppe hervorbringen, die bis heute eingesetzt wird. 8.3.1 Purine Im 19. Jahrhundert wurden die Grundsubstanzen der Purine aus Tee, Kakao und Kaffee extrahiert. 1820 gelang es Runge Coffein aus Kaffeebohnen zu gewinnen. Woskresensky isolierte Theobromin 1841 aus Kakaobohnen. 1861 wurde die Substanz Coffein chemisch gleichgesetzt. (23) 1888 konnte Albrecht Kossel das erste Mal geringe Mengen an Theophyllin gewinnen. Der Name „Theophyllin“ leitet sich ursprünglich von Teeblatt ab, aus dem es isoliert wurde. Kurze Zeit später konnte es synthetisch hergestellt werden. Anfangs als Diuretikum eingesetzt, etablierte Samson Raphael Hirsch 1922 Theophyllin in der Asthmatherapie. (21) Der Pharmakologe Woldemar von Schroeder konnte 1887 die diuretischen Eigenschaften von Coffein mit Hilfe von Tierversuchen beweisen. Als Ursache wurde eine Wirkung auf die Nierensekretion vermutet. Durch die Aufklärung der Strukturformel der Purine und die erstmaligen Vollsynthesen waren Pharmakonzerne in der Lage Präparate herzustellen. Eines dieser Präparate, Theophyllin, konnte parenteral verabreicht werden und wurde zum vorherrschenden Diuretikum bis in die 1950er Jahre. Später kam es nur mehr in der Asthmatherapie zum Einsatz. (23) 8.3.2 Quecksilberverbindungen Autoren/Autorinnen des Altertums prägten die Bedeutung des Quecksilbers in der Medizin und ebneten diesem Metall durch aufgestellte Theorien den Weg zu einer Schlüsselstellung in der Geschichte der Medizin und den Naturwissenschaften. Quecksilber gewann zusätzlich durch die Alchemie an Beachtung. Schon in der Zeit vor Christi Geburt wusste man um den Nutzen als Arzneimittel und die Toxizität Bescheid. Als die Syphilis im 16. Jahrhundert in Europa wütete, war 32 Quecksilber Mittel der Wahl und wurde zur äußerlichen Anwendung in unterschiedlichen Darreichungsformen eingesetzt. Paracelsus applizierte Quecksilber bei Syphilis erstmals peroral und wiedersprach damit der Galen’schen Doktrin. Somit revolutionierte Paracelsus die therapeutische Anwendung von Quecksilber und entdeckte als erster ein wirksames Mittel gegen die Wassersucht. Die diuretische Wirkung dieses Arzneimittels konnte jedoch erst Ende des 19. und Anfang des 20. Jahrhunderts wissenschaftlich belegt werden. Zur gleichen Zeit konnte sich Kalomel, also Quecksilber-I-chlorid, in England durchsetzen. Diese Popularität verdankte es den Veröffentlichungen des Mediziners Richard Brights in den Jahren 1827 und 1838. Verwandte Substanzen, wie z.B. Sublimat, Hydrargyrum jodatum flavum oder Hydrargyrum amidatum bichloratum fanden ebenfalls Anwendung in der Wassersucht-Behandlung. Durch die Vielzahl an erhältlichen Quecksilberverbindungen verloren die Purine an Bedeutung. (23) 8.3.3 Rein synthetisch gewonnene Diuretika Die ersten Diuretika, die Quecksilber ersetzten und sich als nützlich bei der Herzinsuffizienzbehandlung erwiesen, wurden Carboanhydrasehemmer genannt. Die Entwicklung dieser Substanzen in der Mitte der 1940er Jahre geht auf die Entdeckung des antibakteriellen Agens Sulfanilamid zurück. Es hemmt das Enzym Carboanhydrase im Nierengewebe und stört die Ansäuerung des Harns. Dieser Tatsache folgte die Beobachtung, dass, wenn Sulfanilamid Herzpatienten/patientinnen verabreicht wurde, sie große Mengen an Natrium und Kalium mit dem Urin ausschieden. Neuere Derivate der Carboanhydrasehemmer bildeten eine weit verbreitete Therapie in den 1950er Jahren. Aber diese Klasse von Diuretika hatte gravierende Nachteile, insbesondere die Ausbildung der metabolischen Azidose. Aus diesem Grund hofften Wissenschaftler/Wissenschaftlerinnen einen Wirkstoff zu entwickeln, der die Resorption von Natrium- und Chloridionen in der Niere hemmen und die Urinproduktion, ohne den körpereigenen Elektrolythaushalt zu stören, steigern sollte. (24) 33 8.3.4 Thiaziddiuretika In den 1950er Jahren entwickelten Forscher und Forscherinnen bei Merck eine oral wirksame Substanz, die sie Chlorothiazid nannten und läuteten damit den Beginn einer neuen Ära der Diuretika ein. In den späten 1950er Jahren wurden Thiaziddiuretika organischen Quecksilberverbindungen und oralen Diuretika, wie z.B. Carboanhydrasehemmern vorgezogen. Der zunehmende Einsatz von Thiaziddiuretika hatte messbare Auswirkungen auf die Sterberaten bei Herzkreislauferkrankungen. (24) 8.3.5 Furosemid In der Folge versuchten Forscher/Forscherinnen die Wirkung schon entdeckter Diuretika weiter zu verbessern. Bei der Suche nach wirkungsvolleren Thiaziden im Jahre 1959 sind sie zufällig auf den Wirkstoff Furosemid gestoßen, der einen vollkommen anderen Wirkungsmechanismus besaß. Die Überraschung war groß, als sich herausstellte, dass der Wirkstoff nicht wie erwartet am frühdistalen Tubulus, sondern an der Henle-Schleife wirkt. Dies war der Beginn der Schleifendiuretika. (23) 8.3.6 Kaliumsparende Diuretika Durch die Entdeckung der sogenannten kaliumretinierenden Diuretika konnte ein weiteres Problem, der Kaliumverlust, behoben werden. Zu dieser Gruppe zählen die cyclischen Amidin-Derivate Triamteren und Amilorid als Natriumkanalblocker im spätdistalen Tubulus und Sammelrohr und Spironolacton als AldosteronAntagonist. (23) 8.3.7 Spironolacton Beobachtungen zeigten, Aldosteronerhöhung, keine dass bei begleitenden Schwangerschaften, Ödeme auftraten. trotz einer Physiologisch gesehen, ist dieser Befund auf die Hemmung von Aldosteron durch das Sexualhormon Progesteron zurückzuführen. Da Progesteron nicht als Diuretikum eingesetzt werden konnte, forschte man nach einem Steroid-Derivat, das Aldosteron an den renalen Rezeptoren verdrängen und ersetzten konnte. (23) 34 8.3.8 Cycloamidine Die Cycloamidine Amilorid und Triamteren bieten eine andere Möglichkeit zu Spironolacton als kaliumsparendes Diuretikum. Triamteren sollte zunächst als Folsäureantagonist fungieren. Jedoch stellte sich heraus, dass es für diese Funktion zu schwach wirksam war. Bei Screening- Untersuchungen konnte Triamteren mit seiner diuretischen Wirkung überzeugen. (23) 8.4 Betablocker Die Geschichte der Betablocker begann im Jahr 1907. Dale postulierte seine Theorie der adrenergen Rezeptoren. 1948 bewies Ahlquist das Vorhandensein von α- und ß-Rezeptoren, indem er nachweisen konnte, dass Katecholamine in verschiedenen Wirkstärken unterschiedliche physiologische Reaktionen auslösen. Slater und Powel beschrieben 1958 zum ersten Mal Dichlorisoproterenol. Es hemmt, die auf Adrenalin zurückzuführende Bronchial- bzw. Uterusrelaxation und Vasodilatation. Black hielt die mutmaßliche klinische Bedeutung der Betablocker bei Herz-Kreislauf-Erkrankungen fest und konnte 1962 Pronethanol entdecken. Später bekam er für seine Verdienste den Nobelpreis.1965 fand Propranolol, als erster klinisch verwendeter nichtselektiver Betablocker, Anwendung. (25) 35 9 Studien bei Herzinsuffizienz Patienten Ausgehend von den Errungenschaften in der Erforschung der Medizin, unter anderem der pathophysiologischen Funktion neurohumoraler Faktoren, der Bedeutung von Vor- und Nachlast, der Nachweis geometrischer und struktureller Veränderungen des Herzens (Remodelling), sind in den letzten 30 Jahren eine Vielzahl an kontrollierten großangelegten Studien bei Patienten/Patientinnen mit chronischer Herzinsuffizienz veröffentlicht worden.(18) Bis in die 1970er Jahre waren die Behandlungsmöglichkeiten für die Herzinsuffizienz bis auf Digitalis und Diuretika begrenzt. Zwar erzielten sie eine Wirkung auf die Symptomatik, es konnte aber kein Rückgang der Mortalität verzeichnet werden und die Kombination war zusätzlich unzureichend für Patienten/Patientinnen mit fortgeschrittenen Symptomen. Die Suche nach wirksameren Alternativen führte zu Strategien, die die Hämodynamik steuern. Zahlreiche physiologische Studien zeigten eine Abhängigkeit der Ventrikelfunktion vom Gefäßwiderstand und Medikamente, die den systemischen Gefäßwiderstand verringern und somit die Herzfunktion verbessern konnten. Eine Zulassungsstudie von Franciosa et al. zeigte, dass Natriumnitroprussid bei Patienten/Patientinnen mit Herzinsuffizienz durch die medikamentöse Einstellung des akuten Herzinfarktes linksventrikuläre Füllungsdrücke senken und zu einem moderaten Anstieg der Herzleistung verhelfen kann. Eine nachfolgende Studie erzielte herausragende Ergebnisse bei Patienten/Patientinnen mit refraktärer Herzinsuffizienz, in welcher Nitroprussid den systemischen Gefäßwiderstand um 50% reduzierte, die Herzleistung um 56% erhöhte und den linksventrikulären Füllungsdruck um 47% verringerte. Diese hämodynamischen Vorteile von Nitroprussid führten zu Studien mit oralen Agenzien, eingeschlossen Hydralazin, Isosorbiddinitrat, Prazosin, Phentolamin und Minoxidil. Obwohl diese Medikamente alle Einfluss auf die Hämodynamik besitzen, war keins davon so wirkungsvoll wie Nitroprussid. 1977 untersuchte Massie et al. die Kombination aus 2 oral verabreichbaren Stoffen, Hydralazin und Isosorbiddinitrat bei Herzinsuffizienzpatienten/- patientinnen der Klasse III-IV. Sie vermuteten, dass die kombinierte Gabe bei der 36 Reduzierung der Vorlast und Nachlast bessere Erfolge erzielen würde als die individuelle separate Verabreichung. Sie belegten, dass die Kombination den linksventrikulären Füllungsdruck um 36% verringert, den Herzindex um 58% erhöht und den systemischen Gesamtwiderstand um 34% senkt. Später verglich Pierpont et al. Hydralazin/Isosorbiddinitrat mit Nitroprussid und belegte, dass die 2 Behandlungsmöglichkeiten ähnliche Wirkungen beim Herzindex und dem WedgeDruck erzielen. Unter Berücksichtigung der hämodynamischen Vorteile der Kombination von Hydralazin und Isosorbiddinitrat wurde in der ersten großen, randomisierten, placebo-kontrollierten Studie, die Vasodilator-Heart Failure Trial (V-HeFT), die Auswirkungen auf die Mortalität erforscht. (26) Bei dieser Studie konnte zum ersten Mal festgehalten werden, dass es bei der Herzinsuffizienz realisierbar ist, Mortalitätsstudien durchzuführen und eine passende Behandlung die Lebenserwartung von Patienten/Patientinnen erhöhen kann. Zusätzlich konnte die Studie zeigen, dass eine Behandlung mit Hydralazin und Isosorbid Dinitrat im Vergleich zu einem Palcebo oder Prazosin, die Mortatlität wesentlich senkt. (18) 1987 konnte in der Consensus-Studie und 1991 in der SOLVD-Treament Studie nachgewiesen werden, dass ACE-Hemmer mit Enalapril die Gesamtmortalität um 16-40% verringern. 1991 wurde zusätztlich die 2. V-HeFT Studie publiziert. Sie hat bestätigt, dass Enalapril einen besseren Benefit hat, als die Kombination aus Hydralazin und Isosorbid Dinitrat. Die SOLVD-Prevention Studie aus dem Jahr 1992 war eine randomisierte, Placebo-kontrollierte, Doppelblindstudie. Insgesamt wurden 4228 Patienten/Patientinnen betreut. (27) Im darauffolgenden Jahr zeigte die SOLVDPrevention Studie, dass Enalapril nicht nur die Hospitalisierungsrate der Herzinsuffizienzpatienten/-patientinnen sondern auch der asymptomatischen Patienten/Patientinnen zu senken vermag. (28) Diese Studien wurden zu Meilensteinen und läuteten die Ära der ACE-Hemmer ein, die das Herzstück der Herzinsuffizienz Behandlung für 25 Jahre darstellte. Die Valsartan Heart Failure Studie 2001 war eine randomisierte, Placebo- kontrollierte, Doppelblindstudie im parallel-Design. (29) Sie stellte das neue Behandlungskonzept der Herzinsuffizienz mit Angiotensin-Rezeptor-Blocker vor. 37 (27) Angiotensin-Rezeptor-Blocker verhindern die Andockung von Angiotensin II an den AT1-Rezeptor. Folglich kommt es vermehrt zur Bindung an den AT2Rezeptor. Dies hat eine antihypertrophe, vasodilatierende und eine antiproliferative Wirkung. (30) Da die Behandlung aber nicht besser als die Behandlung mit ACE-Hemmern ist, werden ARBs nur bei Patienten/Patientinnen eingesetzt, die keine ACE-Hemmer aufgrund von Husten und dem Auftreten von Angioödemen einnehmen dürfen. (28) Der Einsatz der Betablocker Therapie, heute ein Eckpfeiler der Herzinsuffizienz Behandlung, war einst umstritten, da man Sorge trug, ob Patienten/Patientinnen mit verminderter Ejektionsfraktion entweder nicht davon profitieren oder inakzeptable Nebenwirkungen von der adrenergen Blockade erhalten. Jedoch gab es Hinweise, dass sich 3 Betablocker, Bisoprolol, Carvedilol und RetardMetoprolol positiv auf die Mortalität auswirken. (28) Betablocker hemmen generell die Bindung von Katecholaminen an ß-Rezeptoren. (31) Zwei Studien über den Alpha- und Beta- Blocker Carvedilol (U.S. Carvedilol Heart Failure Studie 1996 und COPERNICUS 2001a) zeigten, dass Carvedilol zu einer wesentlichen Verringerung der Mortalität führt und einen wesentlichen Beitrag zum Verständnis der adrenergen Aktivierung in der Pathophysiologie der Herzinsuffizienz leistet. Diese beiden Studien unterstreichen den neuartigen Ansatz in der Therapie. Ein weiterer Paradigmenwechsel in der Herzinsuffizienz Therapie wurde durch die publizierte RALES Studie 1999 ermöglicht. Durch die Anwendung von Spironolacton, einem Forscher/Forscherinnen Mineralkortikoid-Rezeptor einen Rückgang der Antagonist, Mortalität bei konnten 30% der Patienten/Patientinnen beobachten, die bereits ACE-Hemmer und Diuretika einnahmen. Die EMPHASIS-Studie aus dem Jahr 2011, in der Forscher und Forscherinnen die Auswirkungen des Mineralkortikoid-Rezeptor-Antagonisten Eplerenon bei Patienten/Patientinnen mit systolischer Herzinsuffizienz und milden Symptomen studierten, bestätigte nicht nur sondern erweiterte auch die Forschungserfolge. Gemeinsam konnten diese Studien das Behandlungsinstrumentarium der Herzinsuffizienz um eine wichtige Wirkstoffklasse erweitern. Nicht alle Studien erwiesen sich als erfolgreich. Wirkstoffe mit positiv inotropen Effekten, wie der Phosphodiesterase-Hemmer Milrinon, dienen als treffendes Beispiel. (28) In der PROMISE Studie, welche 1088 Patienten/Patientinnen mit 38 schwerer chronischer Herzinsuffizienz umfasste, stellte sich heraus, dass im Vergleich zu Placebo, oral verabreichtes Milrinon die Gesamtmortalität um 28% und die kardiovaskuläre Mortalität um 34% erhöhte. (32) Neuartige inotrope Wirkstoffe enttäuschten im Allgemeinen. Eine ältere Klasse an inotropen Substanzen, die Herzglykoside, konnte ebenfalls nicht überzeugen. Seit den Beobachtungen William Witherings vor 230 Jahren, niedergeschrieben in seinen bahnbrechenden Aufzeichnungen: „An Account of the Foxglove, and Some of Its Medical Uses: With Practical Remarks on Dropsy, and other Diseases“, waren Digitalis Glykoside eine Hauptstütze der Herzinsuffizienztherapie. Allerdings zeigte eine Studie (Digitalis Investigation Group, DIG, 1997) eindeutig, dass Digoxin keinen positiven Effekt auf die Mortalität der Herzinsuffizienz hat, obwohl es die generellen Krankenhauseinweisungen und speziell die Krankenhauseinweisungen aufgrund von Herzinsuffizienz um 28% senken konnte. Trotz ihrer langen Anwendung in der Geschichte, zählen Herzglykoside nicht mehr zur First-Line-Therapie, obgleich sie zur Milderung von Symptomen und zur Prävention der Krankenhauseinweisung aufgrund von Herzinsuffizienz eingesetzt werden können. (28) Nesiritid, ein rekombinantes B-Typ natriuretisches Peptid mit gefäßerweiternden Eigenschaften, wurde 2001 für den Einsatz bei Patienten /Patientinnen mit akutem Herzversagen zugelassen. Als Grundlage dienten Studien, die eine Reduktion des pulmonal-kapillären Verschlussdruckes und die Verbesserung der Dyspnoe nach 3h belegen. In der Studie ASCEND-HF im Jahre 2011 hat Nesiritid die Todesrate als auch die Rehospitalisationsrate weder erhöht noch verringert. (33) Der beobachtete Effekt von Nesiritid, die Atemnot zu verringern, war in dieser Studie gering und nicht signifikant. (33) Somit erwies sich der oft angewendete biologische Wirkstoff als unwirksam. (28) Die Einführung von Herz-unterstützenden Systemen stellt vielleicht den fundamentalsten Paradigmenwechsel dar. Bis zum Jahr 2001 nicht publiziert, häufen sich nun Studien, die sich mit Herz-unterstützenden Systemen auseinandersetzen. Die unterschiedlichen Herz-unterstützenden unterstützungssystem aufgelisteten (LVAD) in der Studien befassten Systemen: REMATCH Das Studie sich mit 3 Linksherz(2001b), der implantierbare Kardioverter-Defibrillator (ICD) in der SCD-HeFT Studie (2005a) 39 und die kardiale Resynchronisationstherapie in der COMPANION (2004), CAREHF (2005b), MADIT-CRT (2009) und RAFT Studie (2010). Bei allen 3 Unterstützungsmaßnahmen konnte ein Rückgang der Mortalität festgestellt werden. LVADs können zur Überbrückung der Wartezeit auf ein Herztransplantat oder als „destination- Therapie“ eingesetzt werden. ICDs können alleine oder in Kombination mit CRT (CRT-D) verwendet werden. Eine erst kürzlich veröffentlichte Studie, die PARADIGM-HF Studie, aus dem Jahr 2014, beschrieb einen neuen Ansatz in der Herzinsuffizienz-Therapie. (28) Die Entwicklung von LCZ696, einer Kombination aus dem Neprilysin-Hemmer Sacubitril und dem Angiotensin-Rezeptor Hemmer Valsartan. Die Studie zeigte, dass LCZ698 im Vergleich zu Enalapril das Risiko der kardiovaskulären Mortalität und die Hospitalisationsrate von Herzinsuffizienzpatienten/-patientinnen senken kann. Neprilysin ist eine neutrale Endopeptidase, die mehrere endogene vasoaktive Peptide abbaut. Die Hemmung von Neprilysin erhöht die Spiegel dieser Substanzen und verhindert die neurohumorale Aktivierung, die zur Vasokonstriktion, einer Natriumretention und zum maladaptiven Remodelling beiträgt. (34) Die Zeitachse zeigt einen stetigen Fortschritt in der Herzinsuffizienz Behandlung, beschleunigt durch mehrere Paradigmenwechsel. Zu Anfang, repräsentierten 2 Wirkstoffe, Digoxin und Diuretika, ohne Auswirkungen auf die Mortalität zu haben, die First-Line Behandlung der Herzinsuffizienz. Zu den letzten Errungenschaften zählen ACE-Hemmer, Betablocker, Aldosteron Antagonisten, kardiale Unterstützungssysteme und Angiotensin-Rezeptor-Neprilysin Inhibitoren, welche streng evidenz-basiert einen Rückgang der Mortalität bewirkten. Dennoch, bleibt die Mortalitätsrate bei Patienten/Patientinnen mit Herzinsuffizienz in der Interventionsgruppe der PARADIGM-HF Studie bei etwa 20% über 2 Jahre gesehen. Dies hebt deutlich hervor, dass ein Ende der Erforschung der Herzinsuffizienz Behandlung noch nicht in Reichweite ist. (28) 40 10 Aktuelle medikamentöse Therapie der Herzinsuffizienz 10.1 Systolische Herzinsuffizienz Das Ziel der medikamentösen Behandlung einer chronischen Herzinsuffizienz ist eine Linderung der Symptome zu erreichen, ein Fortschreiten der Krankheit zu unterbinden und die Sterblichkeit zu verringern. (35) 10.1.1 Blockade des Renin-Angiotensin-Aldosteron-Systems Der Einsatz von ACE-Hemmern führt zu mehreren nützlichen Wirkungen, wie einer Verminderung der Flüssigkeitsretention und einer Blutdrucksenkung, ausgelöst durch eine periphere Vasodilatation. Des Weiteren haben ACE-Hemmer einen positiven Einfluss auf das fortschreitende myokardiale Remodelling. Vergleicht man ACE-Hemmer mit einem Placebo, kann man beobachten, dass ACE-Hemmer in der Lage sind, die Hospitalisierungsrate und Sterblichkeit bei ischämischer und nicht-ischämischer Herzinsuffizienz zu senken und die Lebensqualität samt körperlicher Belastbarkeit zu erhöhen. Folglich empfiehlt man Patienten/Patientinnen mit einer symptomatischen systolischen Herzinsuffizienz ACE-Hemmer in Verbindung mit Beta-Blockern als First-Line Behandlung. Die neuste Leitlinie rät angesichts der Studienlage die Anwendung von Ramipril, Enalapril, Captopril und Lisinopril. Diese sollten mit hoher Zieldosis verabreicht werden. Für die Wirksamkeit niedriger Dosierungen liegen bislang keine Studien vor. Auch Patienten/Patientinnen mit asymptomatisch reduzierter systolischer Ventrikelfunktion profitieren von der Einnahme von ACE-Hemmern. (36) Die Indikation zur Verabreichung von AT1-Rezeptor-Antagonisten bei chronisch systolischer Herzinsuffizienz besteht als „Second-Line“-Medikament bei einer Unverträglichkeit von ACE-Hemmern. Betreffend die Mortalität fand sich kein aussagekräftiger Unterschied zwischen ACE-Hemmer und AT1-Rezeptor- Antagonisten. Die zusätzliche Gabe eines AT1-Rezeptor-Antagonisten zu einem Beta-Blocker und ACE-Hemmer bei systolischer Herzinsuffizienz hatte keinen Einfluss auf die Gesamtsterblichkeit. Die zuvor beschriebene Kombination sollte wegen der mehrfach auftretenden Nebenwirkungen und der Verschlechterung der Nierenfunktion nicht verordnet werden. (35) 41 10.1.2 Mineralokortikoidrezeptorantagonisten In der neuesten Leitlinie gab es eine Ergänzung der Empfehlungen betreffend der Verabreichung von MRA. Aufgrund der errungenen Fakten in der RALES Studie, wurden in den letzten Leitlinien, ausschließlich Patienten/Patientinnen mit Symptomen einer fortgeschrittenen Herzinsuffizienz (NYHA IV) die Einnahme von Mineralokortikoid-rezeptorantagonisten EMPHASIS-HF Studie belegte, empfohlen. dass auch Die bei 2011 veröffentlichte geringradiger, stabiler Herzinsuffizienz (NYHA II) eine Therapie mit MRA Eplerenon von Vorteil sein kann. Innerhalb der Studie konnte ein Rückgang der Krankenhausaufenthalte, der kardiovaskulären Todesfälle, wie auch der Gesamtmortalität verzeichnet werden. Die Wirkung der MRA wurde in der EMPHASIS-HF Studie durch einen Vergleich mit einer beinahe ausschließlichen Behandlung mit ACE-Hemmern (93%) und Betablockern (87%) bestimmt. Basierend auf diesen Erkenntnissen wurde in der Leitlinie festgelegt, dass Patienten/Patientinnen, die trotz laufender Therapie mit Betablockern und ACE-Hemmern dennoch an einer symptomatischen Herzinsuffizienz mit verminderter EF (≤ 35%) leiden, mit einem MRA therapiert werden. Eine durchgeführte Post-hoc-Analyse konnte zusätzlich beweisen, dass Eplerenon die Inzidenzrate von Vorhofflimmern maßgebend verringert. (37) 10.1.3 Ivabradin Ivabradin führt zu einer Blockade des If-Kanals und dient der spontanen Depolarisation des Membranpotentials der Schrittmacherzellen im Sinusknoten. Hauptaufgabe ist die Regulation der Herzfrequenz. Je stärker die Herzfrequenz ansteigt, desto ausgeprägter ist die hemmende und somit herzfrequenzreduzierende Wirkung. Durchschnittlich kann man eine Verringerung der Herzfrequenz von etwa 10 Schlägen/min erzielen. Die myokardiale Kontraktilität als auch die Erregungsweiterleitung werden nicht beeinflusst. Der negativ chronotrope Effekt führt zu einer Verringerung des Sauerstoffverbrauchs des Herzmuskels und zur vermehrten Koronarperfusion in der Diastole. Da ßAdrenozeptor-Antagonisten nicht immer verabreicht werden können, kann Ivabradin zur Behandlung der chronischen koronaren Herzkrankheit verwendet werden. (38) In der SHIFT-Studie wurde Ivabradin für den Einsatz bei Patienten/Patientinnen 42 mit chronischer Linksherzinsuffizienz untersucht. Dabei hat sich gezeigt, dass Patienten/Patientinnen, die trotz Standardbehandlung eine EF ≤35% aufweisen, von Ivabradin profitieren. In der neuesten Leitlinie scheint Ivabradin als IIa- Empfehlung auf. Es wird symptomatischen Patienten/Patientinnen verschrieben, deren Herzfrequenz sich durch Betablocker nicht unter 70/min regulieren lässt. Patienten/Patientinnen, die eine Unverträglichkeit gegenüber Betablockern besitzen, stellt diese Substanz eine nützliche Alternative dar. (36) 10.1.4 Digitalis Ivabradin zeigt keinen Effekt bei Vorhofflimmern. In diesem Fall setzt man zur Frequenzkontrolle Digitalispräparate ein. Studien, die Digitalisglykoside testeten, fanden größtenteils ohne die parallele Gabe von Betablockern statt. Sie wiesen einen Rückgang der Krankenhauseinweisungen und eine verbesserte Symptomatik nach, jedoch keine Auswirkungen auf die Gesamtsterblichkeit. Da Digitalispräparate Nebenwirkungen aufweisen, werden sie nur zur Arrhythmie Behandlung eingesetzt, wenn die Behandlung mit Betablockern ausgeschöpft ist. (36) 10.1.5 Diuretika Da Diuretika die Symptomatik der Atemnot und der Ödembildung lindern, werden sie trotz unbewiesener Senkung von Krankenhauseinweisungen und Mortalität in der Herzinsuffizienz-Therapie eingesetzt. Sie werden genutzt um die Euvolämie des Patienten/der Patienten/Patientinnen Patientin mit einzuleiten und fortgeschrittener aufrechtzuerhalten. Herzinsuffizienz Bei und/oder Niereninsuffizienz ist eine kombinierte Diuretikagabe notwendig. (39) 43 In den nachfolgenden modifizierten Tabellen laut ESC sind die aktuellen Leitlinien zur Behandlung der symptomatischen, systolischen Herzinsuffizienz zusammengefasst: Pharmakotherapie bei allen Patienten/Patientinnen systolischer Herzinsuffizienz (NYHA-Klasse II-IV) Empfehlungen mit symptomatischer, Empf.-grad Evidenzgrad Ein ACE-Hemmer wird - zusätzlich zum Betablocker bei allen Patienten/Patientinnen mit EF ≤ 40% I empfohlen, um das Risiko für HF-Hospitalisierung und vorzeitigen Tod zu senken. A Ein Betablocker wird – zusätzlich zum ACE-Hemmer (oder ARB, falls der ACE-Hemmer nicht toleriert wird) - bei Patienten/Patientinnen mit EF ≤ 40% empfohlen, I um das Risiko für HF-Hospitalisierung und vorzeitigen Tod zu senken. A Ein MRA wird empfohlen bei allen Patienten/Patientinnen mit persistierenden Symptomen (NYHA-Klasse II-IV) und einer EF ≤ 35% trotz Therapie mit ACE-Hemmer (oder ARB, falls I ACE-Hemmer nicht toleriert werden) und einem Betablocker, um das Risiko für HF-Hospitalisierung und vorzeitigen Tod zu senken. A Tabelle 4 nach (39) 44 Empfehlungen anderer Behandlungsverfahren mit weniger eindeutigem Nutzen bei Patienten mit symptomatischer systolischer Herzinsuffizienz (NYHA-Klasse II-IV) sind in Tabelle 5 ersichtlich: Empfehlungen Empf.-grad Evidenzgrad Empfohlen zur Senkung der HF-Hospitalisierungsrate und der Mortalität bei Patienten/Patientinnen mit einer EF ≤ 40% die wegen Husten keine ACE-Hemmer vertragen (die Patienten/Patientinnen sollten auch einen Betablocker und einen MRA erhalten). I A Empfohlen zur Senkung der HF-Hospitalisierungsrate bei Patienten/Patientinnen mit einer EF ≤ 40% und mit – trotz Therapie mit einem ACE-Hemmer und einem Betablocker – persistierenden Symptomen (NYHA-Klasse II-IV), die MRA nicht a vertragen. I A Sollte in Erwägung gezogen werden zur Senkung der HFHospitalisierungsrate bei Patienten/Patientinnen mit Sinusrhythmus, einer Ejektionsfraktion ≤ 35% und einer Herzfrequenz ≥ 70/min und persistierenden Symptomen (NYHAKlasse II-IV) trotz Behandlung mit einer adäquaten BetablockerDosis (oder max. tolerierte Dosis unterhalb der empfohlenen Dosis), einem ACE-Hemmer (oder ARB) und einem MRA (oder b ARB). IIa B Kann in Erwägung gezogen werden zur Senkung der HFHospitalisierungsrate bei Patienten/Patientinnen mit Sinusrhythmus, einer EF ≤ 35% und einer Herzfrequenz ≥ 70/min, die Betablocker nicht vertragen. Die Patienten/Patientinnen sollten außerdem einen ACE-Hemmer b (oder ARB) und einen MRA (oder ARB) erhalten. IIb C Kann in Erwägung gezogen werden zur Senkung der HFHospitalisierungsrate bei Patienten/Patientinnen mit Sinusrhythmus und EF ≤ 45%, die keinen Betablocker tolerieren (Ivabradin stellt eine Alternative bei diesen b Patienten/Patientinnen mit Herzfrequenz ≥ 70/min dar). Die Patienten/Patientinnen sollten außerdem einen ACE-Hemmer (oder ARB) und einen MRA (oder ARB) erhalten. IIb B Kann in Erwägung gezogen werden zur Senkung der HFHospitalisierungsrate bei Patienten/Patientinnen mit EF ≤ 45% und persistierenden Symptomen (NYHA-Klasse II-IV) trotz einer Behandlung mit einem Betablocker, einem ACE-Hemmer (oder ARB) und einem MRA (oder ARB) IIb B IIb B ARB Ivabradin Digitalis (Digoxin) H-ISDN Kann als Alternative zu einem ACE-Hemmer oder ARB in Erwägung gezogen werden, falls beide nicht toleriert werden, um 45 das Risiko für HF-Hospitalisierung und vorzeitigen Tod bei Patienten/Patientinnen mit EF ≤ 45% und LV-Dilatation (oder EF ≤ 35%) zu senken. Die Patienten/Patientinnen sollten auch einen Betablocker und einen MRA erhalten. Empfehlungen Empf.grad Evidenzgrad Kann in Erwägung gezogen werden zur Senkung der HFHospitalisierungsrate und der Mortalität bei Patienten/Patientinnen mit EF ≤ 45%, LV-Dilatation (oder EF ≤ 35%) und persistierenden Symptomen (NYHA-Klasse II-IV) trotz Behandlung mit Betablocker, ACE-Hemmer (oder ARB) und MRA (oder ARB) IIb B Ein n-3 PUFAc-Präparat kann bei Patienten/Patientinnen, die mit einem ACE-Hemmer (oder ARB), einem Betablocker und einem MRA (oder ARB) behandelt werden, zur Senkung der Gesamtmortalität und der kardiovaskulären Hospitalisierungsrate in Erwägung gezogen werden. IIb B Tabelle 5 nach (39) a In der CHARM-Added-Studie senkte Candesartan auch die kardiovaskuläre Mortalität b Die EMA (European Medicines Agency) hat Ivabradin für Patienten und Patientinnen mit einer Herzfrequenz von ≥ 75/min zugelassen. c Präparat, das in der GISSI-HF-Studie untersucht wurde; die GISSI-HF-Studie hatte kein EF-Limit. 10.2 Diastolische Herzinsuffizienz Bislang war es nicht möglich für jegliche medikamentöse Behandlung eine Verbesserung der Mortalität/Morbidität bei Patienten/Patientinnen mit diastolischer Herzinsuffizienz zu erzielen. Leidet der Patient/die Patientin an Luftnot und Stauung kommen Diuretika, wie bei einer symptomatisch systolischen Herzinsuffizienz, zum Einsatz. (39) 46 11 Chirurgie der Herzinsuffizienz Die chirurgische Behandlung der HI wird in die Herzersatz- und organerhaltende Therapie unterteilt. Besonders die organerhaltenden Maßnahmen in den letzten Jahren bieten durch Mitralklappen-und Aneurysma-Eingriffe sowie HochrisikoBypass-Operationen neue Möglichkeiten. (40) 11.1 Organerhaltende Eingriffe 11.1.1 Mitralinsuffizienz-Therapie Die terminale Herzinsuffizienz ist oft mit einer Mitralinsuffizienz verbunden. Die Überlebensrate wird durch die fortschreitende Ventrikeldilatation und durch das Erscheinen der MI auf 6 bis 24 Monate verkürzt. Eine Wiederherstellung der Mitralklappe kann nicht nur die Mitralkompetenz rekonstruieren, sondern zusätzlich auch die Ventrikelfunktion steigern. Die Bewahrung der Beständigkeit von Klappensegel, Sehnenfäden und subvalvulärem Apparat ist notwendig für die Bewahrung der Klappengeometrie und für die Rekonstruktion der Klappenkompetenz. Deshalb steht die Wiederherstellung der Klappe an oberster Stelle. Der entscheidende Diameter ist der Durchmesser des Klappenannulus. So entstand der Plan des „relative undersized valvular repair“, welcher das Ziel verfolgt, mit Hilfe einer Überkorrektur des dilatierten Klappenannulus eine Koaptation der Segel zu ermöglichen. Durch den Eingriff ist die Klappenkompetenz wiederhergestellt. Zum Schluß erfolgt der Rückgang der Ventrikelgröße. Laut internationalen Studien ist die operative Sterblichkeit bei Patienten/Patientinnen mit LVEF <25% um 5-10% gesteigert. Prolongierter Intensivaufenthalt und additionale Kreislaufunterstützung sind oft Teil der Behandlung. Die durchschnittliche Überlebensrate nach dem Korrektureingriff beträgt 80% nach dem 1. Jahr und 60% nach dem 5. Jahr. (40) 47 11.1.2 Revaskularisation der Koronargefäße Schon vor mehr als 20 Jahren war bekannt, dass Patienten/Patientinnen mit sehr eingeschränkter LVEF von einer Revaskularisation profitieren können und sich damit die Lebenserwartung um bis zu 25% steigern lässt. Leider musste man anfangs dafür eine hohe perioperative Sterblichkeit in Kauf nehmen. Durch die zunehmende Routine mit Patienten/Patientinnen und den Techniken, konnte man eine Sterblichkeit von unter 5% bei Patienten/Patientinnen mit einer LVEF von <30% erzielen. Das geschädigte Herz wird wieder durchblutet und noch zu rettende Zellen mobilisiert, die die Herzleistung verstärken. Grundlegend für den operativen Eingriff sind eine genaue Planung der Operation und eine, im optimalen Fall, vollständige Revaskularisation. Ein vorrausschauender Plan mit Abwägung der Möglichkeiten und Grenzen von Anastomosen sollte entworfen werden. Sind kleinere Gefäße betroffen und benötigt man weitere Techniken zur Revaskularisation wie z.B. die Endarteriektomie kann der Eingriff von Nachteil sein. Ein „off-pump“ Eingriff, ohne Verwendung einer Herz-Lungen-Maschine, wird kontrovers diskutiert. Trotz allem steht das Leben des Patienten/der Patientin die Steigerung der Lebensqualität, oder zumindest das Aufrechterhalten des Status vor dem Eingriff, an erster Stelle der chirurgischen Maßnahmen. Patienten/Patientinnen, die an einer ischämischen Kardiomyopathie leiden und Auswurffraktionen <25% besitzen, profitieren auch von der Koronarchirurgie betreffend Lebenserhaltung und funktionellem Zustand. Die Erfahrungen mit Hochrisiko-Revaskularisationen bei Patienten/Patientinnen mit Herzinsuffizienz nehmen stetig zu und ermöglichen Fortschritte in Operationsplanung und Myokardschutz. In Mortalitätsverringerung, Zukunft sogar erwartet bei man weitere Patienten/Patientinnen mit Risiko- und verminderten Auswurffraktionen (<10%). (40) 48 11.2 Herzersatztherapie 11.2.1 Die Kunstherzen Die Einteilung erfolgt in pulsatile und nicht-pulsatile, sowie in intra- und extrakorporale Assistenzsysteme. (41) 11.2.1.1 Extrakorporale Membranoxigenierung (ECMO) Die extrakorporale Membranoxigenierung bietet die Möglichkeit das Herz auf eine einfache Art zu unterstützen und ähnelt einer Herz-Lungen-Maschine. Der Zugang für die Kanüle wird entweder direkt am Herzen gewählt oder erfolgt über die Leiste. Das Blut wird mit Hilfe einer Zentrifugalpumpe transportiert. Wird kein zwischengeschalteter Oxygenator verwendet, kann man es als temporäres linksventrikuläres Unterstützungssystem nutzen. (41) 11.2.1.2 Extrakorporale ventrikuläre Assistenzsysteme Ist eine längerfristige Unterstützung geplant, als „bridge to transplant“ oder „bridge to recovery“, verwendet man extrakorporale pulsatile Systeme. Diese werden pneumatisch gesteuert und sind in unterschiedlichen Größen erhältlich und somit auch für pädiatrische Patienten/Patientinnen von Nutzen. Die Kanülierung erfolgt im linken, wenn notwendig auch im rechten Ventrikel. Mit Hilfe von Prothesen an der Aorta oder an der Pulmonalarterie wird eine Verbindung mit dem großen bzw. kleinen Kreislauf hergestellt. Die pulsatilen rechts-, links-, oder biventrikulären extrakorporalen Assistenzsysteme sind heutzutage klein und bieten den Patienten/Patientinnen die Möglichkeit mobil zu sein und ambulant betreut zu werden. (41) 49 11.2.1.3 Intrakorporale ventrikuläre Assistenzsysteme Da sich die Wartezeiten für ein Spenderherz stetig verlängern und auch vermehrt bleibende Herzunterstützungen Herzinsuffizienz eingesetzt bei werden, Patienten/Patientinnen stand in den mit letzten terminaler Jahren die Weiterentwicklung implantierbarer intrakorporaler Systeme im Vordergrund. Pulsatile Systeme, mechanisch oder pneumatisch betrieben, wurden von den nicht pulsatilen Systemen, mit Axialpumpen oder Zentrifugalpumpen, ersetzt. Die anfänglichen Systeme waren mit verschiedenen Komplikationen verbunden. Da sie größer waren, konnten sie nur außerhalb des Thorax eingesetzt werden. Da die nichtpulsatilen tierexperimentellen Systeme bei kurzen Langzeitstudien den Überbrückungsphasen pulsatilen Systemen und in in nichts nachstanden, wurden sie der 1. Generation der pulsatilen VADs vorgezogen. Die Verwendung einer simpleren Mechanik, z.B. das Entfernen der Klappen und der zusätzliche Einsatz von Oberflächenbeschichtungen bewog einen Rückgang der Thrombembolien. Durch diese Anpassungen konnte das Einsatzgebiet vergrößert werden. Der Anwendungsbereich umfasst somit „bridge to transplant“ und „destination therapy“. Die Überbrückungsphase kann kritischen Patienten/Patientinnen zu der Möglichkeit verhelfen, den Kreislauf zu festigen, nachfolgende Organschäden zu vermeiden oder schon entstandene Funktionsbeeinträchtigungen zu korrigieren. Notfalloperationen können reduziert werden, Transplantationen finden elektiv und unter besseren Ausgangssituationen statt. Patienten/Patientinnen, die sich auf der Warteliste befinden, können durch dieses Überbrückungssystem überleben. Es konnte kein Unterschied zwischen einer zu Beginn durchgeführten Transplantation und einer nach langer Wartezeit durchgeführten Transplantation festgestellt werden. Da die fortgeschrittene Herzinsuffizienz oft mit einem Unterstützungssystem und nicht mit einem gesamten Ersatz der Herzfunktion therapiert wird, werden auch kleinere Geräte entworfen, die 3-4 Liter fördern und das Herz entlasten, bei gleichzeitiger Stabilisierung des Kreislaufes. Die Größe der Implantate unterscheidet sich kaum von einem Schrittmacher. Durch die minimal-invasive Technik ist keine Sternotomie sondern nur eine kleine Thorakotomie ohne HLM notwendig. Zur Energieversorgung und Steuerung wird das Kabel nach außen verlegt. Derzeit wird an einem komplett implantierbaren und transkutan aufladbaren System 50 geforscht. Dies würde die Akzeptanz erhöhen und die betroffenen Patienten/Patientinnen ungebundener und mobiler machen. Auch ein geringerer Durchmesser des Kabels schützt nicht vor Komplikationen, wie z.B. Verschleiß oder Infektionen an der Übertrittsstelle zur Haut. Schlussfolgernd kann gesagt werden, dass der Trend zu einem kleinen, zur Gänze implantierbaren Unterstützungsgerät geht. Kann dies umgesetzt werden, wird es zu einem ähnlichen Meilenstein, wie die Markteinführung der transvenösen Defibrillatoren vor rund 20 Jahren. (41) 11.2.2 Komplettes Kunstherz Der gesamte Herzersatz („total artificial heart“), die Entfernung des eigenen Herzens und der Einsatz eines totalen biventrikulären Ersatzsystems, nimmt im Gegensatz zu den Assistenzsystemen eine weniger wichtige Stellung ein. Auch wenn die Steuerungs- und Kompressoreinheit mit der Zeit an Größe abgenommen hat, ist die Technik und Implantation noch immer mit viel Aufwand verbunden und wird nur in Einzelfällen in bestimmten Spezialzentren angeboten. (41) 51 11.3 Herztransplantation 11.3.1 Indikation und Vorbereitung Viele Entscheidungen rund um die Herztransplantation werden individuell nach Patienten/Patientinnen und Herzzentrum beschlossen, obwohl diesbezüglich Leitlinien vorhanden sind. In erster Linie sollten alle Behandlungsmöglichkeiten der Herzinsuffizienz in Betracht gezogen werden. Dazu zählt die adjuvante medikamentöse Behandlung, sowie herzchirurgische Eingriffe bei Herzvitien, Hochrisiko-Bypass-Operationen bei einer ischämischen Kardiomyopathie und der Einsatz von Defibrillatoren und biventrikulären Schrittmachern um die Wartezeit zu überbrücken. Die zusätzliche Bestimmung hämodynamischer Parameter ist vor dem Eingriff notwendig und wird im Rahmen einer Rechtsherzuntersuchung vorgenommen. Neben den hämodynamischen Werten spielen unter Anderem Alter, Compliance und psychosoziale Eingliederung eine wichtige Rolle. Zu den Kontraindikationen zählen: eine Alkoholerkrankung, Diabetes mellitus (mit Folgeschäden), Nikotinabusus, sowie komplizierte psychiatrische Erkrankungen. Sind alle nötigen Parameter erhoben, wird der Herzempfänger auf die Warteliste bei Eurotransplant in Leiden gesetzt und einem Auditverfahren zugewiesen. (41) Die Tabelle 6 zeigt die Entwicklung des Transplantations- und Spendergeschehens für Herzen in Österreich im Zeitraum von 2004-2013 Transplant. ges. 2004 2005 2006 2007 2008 2009 2010 2011 2012 2013 Herz 62 55 51 57 59 72 69 50 59 62 pro Mio. EW 7,6 6,7 6,2 6,9 7,1 8,6 8,3 6,0 7,0 7,3 Tabelle 6 modifiziert nach (49) 52 11.3.2 Technik 11.3.2.1 Der Orthotope Herztransplantation weltweit anerkannte Goldstandard in der terminalen Herzinsuffizienzbehandlung ist die orthotope Herztransplantation (HTX). Die Hauptindikation mit 54% ist die dilatative Kardiomyopathie, gefolgt von der ischämischen Kardiomyopathie mit 37%. Shumway und Lower beschrieben 1960 erstmals den Verlauf der HTX bei einem Tierexperiment. (39) Bei dieser Technik, mit Anschluss an die Herz-Lungen-Maschine, wird annähernd das gesamte Empfängerherz entfernt. Die verbleibenden Anteile von Pulmonalgefäß, Aorta und die rechte und linke Vorhofmanschette, werden mit dem Spenderherz anastomosiert. (38) Bei der bikaval-bipulmonalen Technik werden zusätzlich zur Arteria pulmonalis und Aorta, die linke und rechte Pulmonalvenenmanschette samt unterer und oberer Hohlvene anastomosiert. Die bikavale Vorgehensweise hat den Vorteil, dass man einfacher eine Größenangleichung der Vorhöfe erzielen kann, wenn eine merkliche Differenz zwischen Empfänger- und Spenderherz vorliegt. Fortgeschrittene Trikuspidal- und Mitralklappeninsuffizienzen nach Herztransplantation sind durch diese Technik rückläufig. Darüber hinaus stabilisiert sich auch nach dem Eingriff der Sinusrhythmus. Zu den Nachteilen gehören Verdrehungen, Stenosen der oberen und unteren Hohlvene und Knickbildungen. Kommt es zu Einflussstauungen, muss es chirurgisch oder interventionell via Stent behoben werden. (42) 11.3.2.2 Heterotope Herztransplantation Bei der sporadisch eingesetzten heterotopen HTX wird das Spenderherz an einem anderen Ort, wenn möglich auch im „Huckepack-Verfahren“ an die großen Gefäßstämme angebunden. Das beeinträchtigte Herz verbleibt bei dieser Form der HTX im Körper des Patienten/der Patientin. Das Transplantat fungiert hier ausschließlich als eine unterstützende Maßnahme. Die Indikation für eine heterotope HTX ist ein erheblich erhöhter pulmonalarteriolärer Widerstand beim Empfänger/bei der Empfängerin. Wegen der verringerten Ventrikelkontraktion des verbliebenen Empfängerherzens erhöht sich das Risiko der Thrombenbildung. Infolgedessen ist eine dauerhafte Antikoagulanzientherapie erforderlich. (43) 53 12 Zukunftsaspekte 12.1 Stammzellen In der gegenwärtigen Literatur werden humane Stammzellen als unerschöpfliche Quelle gehandelt, die aus adultem, fötalem als auch aus embryonalem Gewebe gewonnen werden. Im Vergleich zu Zellen des adulten Patienten/der adulten Patientin lassen sich Stammzellen nach Belieben vervielfältigen und stehen deshalb für therapeutische Zwecke in ausreichendem Maße zur Verfügung. Das Risiko einer Abstoßungsreaktion aus immunologischer Perspektive ist nicht vorhanden, wenn die Stammzellen dem eigenen Körper oder der eigenen Nabelschnur entnommen werden. Nutzt man allerdings Stammzellen einer anderen Person, treten die Gesetzmäßigkeiten der Gewebeverträglichkeit in Kraft. Stammzellen entwickeln sich aus frühembryonalen Stadien eines menschlichen Keims, können aber auch aus dem Nabelschnurblut oder aus dem Gewebe eines Erwachsenen gewonnen werden. Da die Zellen verschiedene Entwicklungspotenzen aufweisen, wird von pluri-, bzw. totipotenten Zellen gesprochen. Die eigentliche medizinische Eignung der Stammzellen besteht darin, dass sie durch Hormone und Wachstumsfaktoren experimentell zu unterschiedlichsten Gewebezelltypen heranreifen können. (44) 12.1.1 Stammzelltherapie bei Herzinsuffizienz Zehn Jahre kardiale Stammzelltherapie - ein Resümee Die intrakoronare und intramyokardiale Stammzelltherapie zielt auf die Reparatur des Herzmuskels, um als kausale Therapie das ventrikuläre Remodelling zu verhindern und dessen Gesamtleistung zu verbessern. Die 3 Hauptindikationen sind akuter Herzinfarkt, chronisch-ischämische Herzinsuffizienz und dilatative Kardiomyopathie. Seit dem ersten Einsatz von Knochenmark-Stammzellen 2001 bei Menschen nach einem Myokardinfarkt, haben viele Studien dessen klinische Tauglichkeit gezeigt: die Knochenmark-Stammzell-Therapie kann bei üblichen Herzkatheter-Eingriffen, aber auch einfach bei herzchirurgischen Interventionen durchgeführt werden. Die NYHA Einstufung der Patienten wie auch die physikalische Belastbarkeit verbesserte sich. Die Stammzelltherapie stellt auch einen entscheidenden Ansatz 54 in der fortgeschrittenen Herzinsuffizienz dar. Einige Studien zeigen auch positive Auswirkungen auf die chronische dilatative Kardiomyopathie. Die klinische Anwendung der autologen Knochenmark-Stammzell-Therapie impliziert keine ethischen Probleme, wenn unmodifizierte primäre Knochenmark-Stammzellen ausgewählt werden. stammzellbedingten Die Verwendung Nebenwirkungen, dieser führt insbesondere zu keinen keinen starken Herzrhythmus- störungen und Entzündungen. Verschiedene Mechanismen der Stammzellwirkung im menschlichen Herzen werden diskutiert, beispielsweise die Zelltransdifferenzierung, die Zellfusion, die Aktivierung intrinsischer kardialer Stammzellen und zytokinvermittelter Effekte. Neue Techniken erlauben eine patientennahe Zellpräparation, beispielsweise während einer kardialen Intervention oder im Operationssaal. Da sich dadurch die Vorbereitungszeit verkürzt und die Logistik des Zelltransportes vereinfacht wird, kann eine Kostenersparnis des Gesamtverfahrens erzielt werden. Zukünftige Studien sind wünschenswert um weitere Erkenntnisse in Bezug auf den Wirkmechanismus der Stammzellen zu gewinnen und das aktuelle Einsatzgebiet der intrakoronaren und intramyokardialen Stammzelltherapie durch größere und vermutlich multizentrische Studien zu erweitern. (45) 55 13 Material und Methoden Für die vorliegende Arbeit wurde als Methode die Literaturrecherche gewählt. Größtenteils wurden dafür Fachbücher und medizinische Artikel herangezogen. Da sich die Therapie der Herzinsuffizienz im Laufe der Zeit, aufgrund mehrerer Paradigmenwechsel stetig angepasst hat, wurde anhand von Überlieferungen aus alten Schriften, Langzeitstudien und aktuellen Erkenntnissen die Entwicklung verschiedener Therapieansätze Literaturquellen dazu wurden reflektiert und zusammengefasst. Die aus der wissenschaftlichen Datenbank Pubmed, medizinischen Fachzeitschriften sowie Fachbüchern entnommen. 56 14 Diskussion Trotz vieler Errungenschaften in der Medizin gilt die Herzinsuffizienz heute noch als unheilbares Syndrom. Nun stellt sich die Frage: Sind wir auf dem richtigen Weg dieses Syndrom zu heilen? Verfolgt man die Zeitachse kann man mehrere Paradigmenwechsel in der Therapie der Herzinsuffizienz beobachten. Wurde z. B. Digitalis früher noch als First-Line Medikament bei Herzinsuffizienz gehandelt, wird es in den aktuellen Leitlinien nur noch zur Behandlung einer Arrhythmie eingesetzt, falls die Therapie mit Betablockern ausgeschöpft ist. (36) ACE-Hemmer, die bis heute noch einen wichtigen Eckpfeiler in der Herzinsuffizienztherapie darstellen, lösten die Kombination aus Hydralazin und Isosorbid Dinitrat ab. Innerhalb einer Studie konnte festgestellt werden, dass vor 1990 60-70% der Patienten/Patientinnen innerhalb von 5 Jahren nach Diagnosestellung an einer systolischen Herzinsuffizienz verstarben. Im Vergleich dazu konnte 13 Jahre später durch eine wirksame Behandlung eine Verringerung der Sterblichkeit von 20-30% erreicht werden. Somit beträgt die Sterblichkeit trotz Behandlung noch immer 40-50%. (46) Nun stellt sich die Frage ob man den Schwerpunkt nicht vermehrt auf die Diagnose und Prävention der möglichen Ursachen der Herzinsuffizienz legen sollte. Fast jeder 4. Patient/jede 4. Patientin leidet unter einer arteriellen Hypertonie, aber nur jeder 2. weiß von seiner Erkrankung und nur ungefähr 1/3 befinden sich in Behandlung. (47). Eine Studie, die sich mit einer anderen möglichen Ursache der Herzinsuffizienz, dem Diabetes mellitus beschäftigte, zeigte ähnliche Ergebnisse. Ungefähr 40% der Bevölkerung haben eine gestörte Glukosetoleranz oder leiden an Diabetes mellitus. Bei der Hälfte der Betroffenen ist Diabetes nicht diagnostiziert und wird deshalb auch nicht therapiert. (48) Die vorliegenden Zahlen bestärken die Annahme, dass die Erkennung der Ursachen einer Herzinsuffizienz und deren Behandlung von enormer Bedeutung sind, solange diese noch immer zu den unheilbaren Erkrankungen gerechnet wird. 57 15 Literaturverzeichnis 1. Rauch B. Kardiologische Rehabilitation. Georg Thieme Verlag; 2007. 2. Böhm M, Bäumer AT. Herzinsuffizienz. Stuttgart: Thieme; 2000. p.28. 3. McMurray JJV, Adamopoulos S, Anker SD, Auricchio A, Böhm M, Dickstein K. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. Eur Heart J 2012 Jul;33(14)1787–847. 4. Alagappan R. Manual of practical medicine. 5th ed. New Delhi: Jaypee Bros. Medical Publishers; 2014. p.290. 5. Bijlani RL, Manjunatha S. Understanding medical physiology: a textbook for medical students. 4th ed. New Delhi: Jaypee Bros. Medical Publishers; 2011. p.191. 6. Katz, AM. Physiology of the heart. 5th ed. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins Health; 2011. p.514. 7. Siegenthaler W, Amann-Vesti BR. Klinische Pathophysiologie: 239 Tabellen. 9., völlig neu bearb. Aufl. Stuttgart: Thieme; 2006. pp. 598-600. 8. Greten H, Rinninger F, Greten T. Innere Medizin. Georg Thieme Verlag; 2010. p.99. 9. Erdmann E. Klinische Kardiologie: Krankheiten des Herzens, des Kreislaufs und der herznahen Gefäße. Heidelberg: Springer-Verlag; 2013. p.542. 10. Greiten LE, Holditch SJ, Arunachalam SP, Miller VM 2014. Should There Be Sex-Specific Criteria for the Diagnosis and Treatment of Heart Failure? Journal of Cardiovascular Translational Research 2014;7(2):139–55. 11. Regitz-Zagrosek V, Lehmkuhl E. Heart Failure and its Treatment in Women: Role of Hypertension, Diabetes, and Estrogen. Herz Kardiovaskuläre Erkrankungen 2005 Aug;30(5) 356–67. 12. McPhee SJ, Hammer GD. Pathophysiology of disease: an introduction to clinical medicine. McGraw- Hill Education; 2014. p.266. 13. Mutschler E, Schaible HG, Vaupel P. Anatomie, Physiologie, Pathophysiologie des Menschen: 140 Tabellen. 6., völlig überarb. und erw. Aufl. Stuttgart: Wiss. Verl.-Ges.; 2007. p. 227. 14. Buddecke E, Fischer M. Pathophysiologie, Pathobiochemie, klinische Chemie: für Studierende der Medizin und Ärzte. Berlin: de Gruyter; 1992. p.324. 15. Baenkler HW, Clement U, Fritze D. Innere Medizin: 299 Synopsen. Sonderausg. Stuttgart: Thieme; 2001. pp.99-102. 16. Schmidt RF, Lang F, Thews G. Physiologie Des Menschen: Mit Pathophysiologie. Berlin Heidelberg: Springer; 2007. p. 583. 17. Benzer H, Burchardi H, Larsen R, Suter PM. Lehrbuch der Anästhesiologie 58 und Intensivmedizin: Band 2: Intensivmedizin. Springer-Verlag; 2013. p. 457. 18. Lüderitz, B. & Arnold, G. 75 Jahre: Deutsche Gesellschaft für KardiologieHerz- und Kreislaufforschung. Berlin: Springer-Verlag; 2011. p.308-10, 317, 202. 19. Ritz E, Schoner W. Von Digitalis purpurea zur Krötenhaut. DMW - Deutsche Medizinische Wochenschrift 2008 Dec;133(51/52)2690–4. 20. Stille G 2013. Krankheit und Arznei: Die Geschichte der Medikamente. Springer-Verlag;2013. p.93-4, 96-7. 21. Gosch M, Dovjak P. Digitalis und Theophyllin: Alt und entbehrlich? Zeitschrift für Gerontologie und Geriatrie 2013 Jun 20;46(5):479-88. 22. Dominiak P, Bönner G. ACE-Hemmer in Klinik und Praxis. Berlin: SpringerVerlag; 2013. p.57. 23. Rau S. Die Geschichte der Diuretika: Vom Coffein zum Furosemid. Pharmazie in unserer Zeit 2006 Jul;35(4)286–92. 24. Hollinger MA. Introduction to Pharmacology. 3rd ed. Boca Raton: CRC Press; 2007. p.250. 25. Dominiak P, Hjalmarson A, Kendall MJ, Kübler W, Olsson G. Betablocker: Im Mittelpunkt der Forschung. Berlin: Springer-Verlag; 2013. p.1. 26. Cole RT, Kalogeropolous AP, Georgiopoulou VV, Gheorghiade M, Quyyumi A, Yancy C, Butler. Hydralazine and Isosorbide Dinitrate in Heart Failure: Historical Perspective, Mechanisms, and Future Directions. Circulation 2011 May 31;123(21):2414-22. 27. The SOLVD Investigators. Effect of Enalapril on Mortality and the Development of Heart Failure in Asymptomatic Patients with Reduced Left Ventricular Ejection Fractions. N Engl J Med 1992 Sep 3;327(10)685–91. 28. Sacks AC, Jarcho JA, Curfman GD. Paradigm Shifts in Heart-Failure Therapy - A Timeline. N Engl J Med 2014 Sep 11;371(11)989–91. 29. Cohn JN, Tognoni G. A Randomized Trial of the Angiotensin-Receptor Blocker Valsartan in Chronic Heart Failure. N Engl J Med 2001 Dec 6;345(23):1667-75. 30. Gerok W. Die Innere Medizin: Referenzwerk für den Facharzt. Schattauer Verlag; 2007. p.144. 31. Böhm M, Borst UE, Schmieder RE, Wehling M. Therapiehandbuch Carvedilol. Georg Thieme Verlag; 2001. p.1. 32. Kato M, Sanada S, Kitakaze M. Should We Use Outpatient Dobutamine or Milrinone? Circulation: Heart Failure 2009 Jul;2(4):377–8. 33. O’Connor CM, Starling RC, Hernandez AF, Dickstein K, Hasselblad V, Heizer GM.Effect of Nesiritide in Patients with Acute Decompensated Heart Failure. N Engl J Med 2011 Jul 7;365(1)32–43. 34. McMurray JJV, Packer M, Desai AS, Gong J, Lefkowitz MP, Rizkala AR, Rouleau JL et al. Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure N Engl J Med 2014 371(11):993–1004. 59 35. Steinacher R, Rottlaender D, Hoppe UC 2012. Diagnostik und Therapie der Herzinsuffizienz. Herz 2012 Jul 29;37(5)543–54. 36. Hofmann U, Ertl G. Medikamentöse Herzinsuffizienztherapie. CardioVasc 2012 Sep 28;12(4):40-5. 37. Pöss J, Link A, Böhm M. Akute und chronische Herzinsuffizienz im Spiegel der neuen ESC-Leitlinie. Herz 2013 Oct 23;38(8)812–20. 38. Freissmuth M, Böhm S. Pharmakologie und Toxikologie: Von den molekularen Grundlagen zur Pharmakotherapie. Heidelberg: SpringerVerlag; 2012. p.386-7. 39. ESC Pocket Guidelines. Herzinsuffizienz. Leitlinien für die Diagnose und Behandlung der akuten und chronischen Herzinsuffizienz. Available at: http://leitlinien.dgk.org/files/2013_PocketLeitlinien_Herzinsuffizienz_Update_2012_Internet.pdf. Accessed July 14, 2015. 40. Weber H, Herrmann-Lingen C. Herzinsuffizienz: vom Symptom zum Therapie-Erfolg. Wien: Springer; 2008. p.144-7 41. Moosdorf R. Kunstherz 28;37(8)869–74. 42. Puehler T, Ensminger S, Schulz U, Fuchs U, Tigges-Limmer K, Börgermann J. Herz- und Herz-Lungen-Transplantation: Indikationen, Chancen, Risiken. Herz 2014 Jan 24;39(1)66–73. 43. Roche Lexikon Medizin. München: Urban & Fischer Verlag; 2003. p. 822. 44. Minuth WW, Strehl R, Schumacher K. Zukunftstechnologie Tissue Engineering: Von der Zellbiologie zum künstlichen Gewebe. John Wiley & Sons; 2012. 45. Strauer B-E, Steinhoff G. 10 Years of Intracoronary and Intramyocardial Bone Marrow Stem Cell Therapy of the HeartFrom the Methodological Origin to Clinical Practice. J Am Coll Cardiol. 2011 Sep 6;58(11):1095–104. 46. Jhund PS, Macintyre K, Simpson CR, Lewsey JD, Stewart S, Redpath A, et al. Long-term trends in first hospitalization for heart failure and subsequent survival between 1986 and 2003: a population study of 5.1 million people. Circulation. 2009 Feb 3;119(4):515–23. 47. Palisch H. Volkskrankheit 2013;65(3):30-4. 48. Rathmann W, Haastert B, Icks A, Löwel H, Meisinger C, Holle R , et. al. High prevalence of undiagnosed diabetes mellitus in Southern Germany: target populations for efficient screening. The KORA survey 2000. Diabetologia. 2003 Feb;46(2):182-9. 49. Gesundheit Österreich GmbH. Geschäftsbereich ÖBIG. Entwicklung des Transplantations- und Spendergeschehens in Österreich. Available at: http://www.goeg.at/cxdata/media/download/tx_statistik_2004_2013.pdf. Accessed July 16, 2015. 50. Dietel M, Suttorp N, Zeitz M. Harrisons. Innere Medizin. Berlin: ABW Wissenschaftsverlag; 2008. p.1778. und Herztransplantation. Bluthochdruck. Das Herz 2012 Oct Pflegemagazin. 60