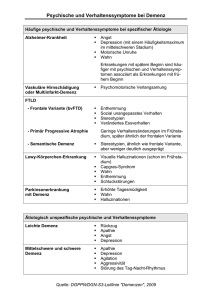
Neuropsychologische DD AD und FTD
Werbung

Neuropsychologische Aspekte der Demenzdiagnostik PD Dr. phil. Helmut Hildebrandt Universität Oldenburg Klinikum Bremen-Ost Demenzen nach DSM IV • Definiert durch erheblichen kognitiven Abbau, d.h. durch eine funktionelle, psychologische Leistungsveränderung, nicht primär durch Ätiologie; • Abbau kann aufgrund einer akuten oder schleichenden Schädigung erfolgen, muss aber unabgängig von einer akuten, aber vorübergehenden Störung des bestehen (DD Delir); • Er muss verschiedene psychologische Leistungen gleichzeitig betreffen (DD Amnesie oder organisch bedingte Persönlichkeitsstörung); • Er muss erheblich sein (DD leichte kognitive Störung oder organisches Psychosyndrom); • Er muss führend gegenüber affektiven Veränderungen sein (DD Psychose). Klassifikation der Demenzen • Ätiologisch im Sinne des ICDs • Syndromspezifisch * Alzheimer Demenz * atypische Alzheimer Demenz * vaskuläre Demenz * fronto-temporale Demenz * Lewy-Körperchen Demenz • Amnestisches Syndrom bzw. MCI Epidemiologie Reischies et al., 1997 Messung des Schweregrads einer Demenz Differenzialdiagnose demenzieller Prozesse DD Demenz und Pseudodemenz (Depression) Cut-off Score Sensitivität WMS-R Calabrese et al., 1999 Spezitivität Differenzialdiagnose zwischen verschiedenen Formen der degenerativ bedingten Demenz (AD, FTD, LKD) mit neuropsychologischen Mittel Alzheimer-Demenz (DSM-IV, Saß et al., 1996) A. Entwicklung multipler kognitiver Defizite, die sich zeigen in sowohl (1) einer Gedächtnisbeeinträchtigung als auch (2) mindestens einer der folgenden kognitiven Störungen: Aphasie, Apraxie, Agnosie, Störungen der Exekutivfunktionen. B. Die kognitiven Defizite aus den Kriterien A1 und A2 verursachen jeweils in bedeutsamer Weise Beeinträchtigungen in sozialen oder beruflichen Funktionsbereichen und stellen eine deutliche Verschlechterung gegenüber einem früheren Leistungsniveau dar. C. Der Verlauf ist durch einen schleichenden Beginn und fortgesetzten kognitiven Abbau charakterisiert. D. Die kognitiven Einbußen in Kriterium A1 und A2 sind nicht zurückzuführen auf: (1) andere Erkrankungen des Zentralnervensystems, die fortschreitende Defizite in Gedächtnis und Kognition verursachen (z.B. zerebrovaskuläre Erkrankungen, Parkinsonsche Erkrankung, Huntingtonsche Erkrankung, subdurale Hämatome, Normaldruckhydrocephalus, Hirntumor), (2) Systemische Erkrankungen, die eine Demenz verursachen können (z.B. Hypothyreose, Vitamin-B12-Mangel, Hyperkalzämie, Neurolues, HIV-Infektion), (3) Substanzinduzierte Erkrankungen. E. Die Defizite treten nicht ausschließlich im Verlauf eines Delirs auf. F. Die Störung kann nicht durch eine Psychose (z.B. Major Depression, Schizophrenie) erklärt werden. Frontotemporale Demenz: Klinischdiagnostische KonsensusKriterien Neuropsychologische Kennzeichen der AD • Ausgangspunkt im limbischen System speziell im erweiterten hippokampalen System • In späterer Phase dann Übergreifen auf sekundäre Assoziationsareale • Nicht immer komplett symmetrisch, jedenfalls nicht in der frühen Phase Blick auf den Thalamus PET-Aktivierung Hippocampus bei leichter und schwerer AD bei Gedächtnisaufgabe in Relation zu Ruhebedingung Desgranges et al., Brain, 2002 Laakso et al., 2000, Biological Psychiatry Structural MRI Gedächtnisleistung und hippokampale Atrophie bei AD Mild cognitive impairment • Viele Patienten, die sich als kognitiv schleichend beeinträchtigt erleben, erfüllen nicht die Kriterien einer Demenz • Trotzdem lassen sich bei diesen Personen u.U. Veränderungen in der kognitiven Leistungsfähigkeit nachweisen • Die DD des MCIs ist deshalb von besonderer Bedeutung, weil die Konversionsrate zur Demenz hoch ist und Personen mit MCI evt. besser zu behandeln sind als AD Patienten Frühdiagnose 1. Der Hausarzt sollte Hinweise auf geistige Leistungseinschränkungen, insbesondere Gedächtnisstörungen, Wesens- und Verhaltensänderungen unter dem Verdacht des Vorliegens einer Demenz nachgehen. Ziel der Frühdiagnose ist der Nachweis oder Ausschluss einer organischen Erkrankung. Hierbei kommt der Fremdanamnese besondere Bedeutung zu. 2. Beobachtungen, die einen kognitiven Abbau berichten, sollten ernst genommen werden und eine fachärztliche Untersuchung einschließlich Prüfung kognitiver Funktionen und bei Verdachtsmomenten weitere Diagnostik (einschließlich kognitiver Screeningverfahren und ggf. apparativer und Laboruntersuchungen) nach sich ziehen. 3. Im Verdachtsfall sollten kognitive Screeningverfahren eingesetzt werden. Sie sollten jedoch nur von erfahrenen Untersuchern angewendet werden. Besonders sensitiv, wenn auch etwas zeitaufwendiger als z.B. der MMS (30 min.) erscheint der CERAD. 4. Personen mit kognitiver Beeinträchtigung („minimal cognitive impairment“), die nicht die Kriterien einer Demenz erfüllen, haben ein erhöhtes Risiko, in den folgenden Jahren eine Demenzerkrankung zu entwickeln. Diagnostik einschließlich cerebraler Bildgebung zum Ausschluss eines symptomatischen Geschehens sowie Kontrolluntersuchungen einschließlich Wiederholung des kognitiven Screening werden empfohlen. Sensitivität und Spezifizität von neuropsychologischen Tests zur Trennung von MCI und gesunden Personen. n = 140 C. A. DE JAGER,1 E. HOGERVORST, M. COMBRINCK, M. M. BUDGE: Psychological Medicine, 2003, 33, 1039–1050. Memory & MCI: Verbal: 17/29 Räumlich: 16/29 Beides: 10 Progression in einzelnen Funktionsbereichen Matthew et al., Brain (2003) n = 55 Asymmetrie von Testergebnissen in der präklinischen AD Diagnostik Jacobson et al., Neuropsychology, 2002 Konversionsrate von MCI zu AD nach Beeinträchtigung N= 929, modified Classification = nach objektiver Leistungsfähigkeit A. BUSSE,1 J. BISCHKOPF, S. G. RIEDEL-HELLER AND M. C. ANGERMEYER: Subclassifications for mild cognitive impairment. Psychological Medicine, 2003, 33, 1029–1038. Lewy Körperchen Demenz: Klinische DD zur AD Neuropsychologische DD AD und DLB Calderon et al., 2001 Subtests aus der VOSP Calderon et al., 2001 Calderon et al., 2001 Figur-Hintergrund (aus der BORB) Unterscheidung ist sensitiv für DLB (speziell bei Produktivsymptomatik) Zusammenfassung AD/DLB • AD in jedem Fall Gedächtnisstörung führend (aber untypische AD!) • DLB in jedem Fall visuoperzeptive Störungen führend (nicht unbedingt Lesen) • DLB durch schwankende Aufmerksamkeit gekennzeichnet und visuelle Halluzinationen • AD in frühem Stadium wenig „produktive Symptomatik“ Klinische DD der FTD: Verhaltensauffälligkeiten und Störungen der Sprachproduktion bzw. Sprachrezeption Spezifische Formen der FTD • Primäre progressive Aphasie: Störung der Flüssigkeit der Sprache bei erhaltener Sprechfähigkeit; Schwierigkeiten in der Grammatik (Verben und Funktionswörter), Wortfindungsstörungen. Sprachverständnis über längere Zeit in Ordnung, wird aber später einbezogen. Spätform: Mutismus • Semantische Demenz: Flüssige Sprache bei inhaltsleerer Aussage. Verlust des Wissens um Wortbedeutungen, nicht der Wörter. Sprache Neuropsychologische DD AD und FTD Gedächtnis Nur per Autopsie gesicherte Fälle von entweder AD oder FTD Neurology, 2002 Zusammenfassung FTD/AD • AD wieder Gedächtnisstörung führend • FTD dagegen Sprachstörung führend (Flüssigkeitsmarker, Comprehension) • FTD mit exekutiven Funktionsdefiziten (wie DLB), aber keine visuo-perzeptiven. • Konversionsrate MCI ohne Gedächtnisstörung in andere Formen der Demenz weitgehend unbekannt Möglichkeiten psychologischer Therapie • In den frühen Phasen und bei leichter kognitiver Störung ist eine funktionelle Therapie wirksam. • Frühes Überlernen extrem wichtiger persönlicher Information und des Umgangs mit externen Hilfen ein Ansatz der Therapie. • Bei schwereren Formen ist eine Konzentration auf biographische Information und Angstreduktion ein sinnvoller Ansatz (Romeo Selbsterhaltungstraining). • Angehörigenberatung Kritik psychologischer Therapie • Sinnlos, weil progressiver Prozess aber: dann ist medikamentöse Therapie auch sinnlos, denn neurobiologisch wenig Unterschied • Belastend, weil Patienten auf ihre Defizite gestoßen werden aber: Krankengymnastik bei Parkinson? aber: Beleg dieser Aussage würde nur unsachgemäßes Vorgehen der Psychologen beweisen Patienten wollen Behandlung 2001 N = 11, mild to moderate stage of AD (mean MMS: 23), mean age: 79, splitted in two groups: 7 training, 4 control. Stimulation training & physical fitness vs. Physical fitness training alone. Smaller (none) MMS decrease in the training group significant Quayhagen & Quayhagen, 2001: Stimulationstraining by caregivers, one hour a day, 5 days a week, for 12 weeks. 7 weeks memory training, 3 weeks problem solving, 2 weeks fluency and communication significant Quayhagen & Quayhagen, 2001: Stimulationtraining by caregivers, one hour a day, 5 days a week, for 8 weeks. Mixed intervention schedule No improvement in memory performance Kognitive Therapie und Alzheimer Prävention n = 25, 9 Monate Zeitraum, ca. 50 Stunden Therapie Ishizaki et al., 2002 Positiver Effekt nachweisbar auch für Affektzustand! That‘s it! Leitlinien medikamentöse Therapie 1. Cholinesterasehemmer sind bei Patienten mit leichter bis mittelschwerer AD wirksam. Ihre Wirksamkeit ist jedoch individuell verschieden, daher sind Erfolgskontrollen erforderlich. 2. Positive Ergebnisse liegen für Donepezil, Rivastigmin und Galantamin und Memantine vor. 3. Vor Verordnung soll eine Baseline von kognitiven, globalen und Verhaltenssowie ADL-Funktionen erstellt werden. Compliance ist sicherzustellen. Eine Kontrolluntersuchung soll nach 2-4 Monaten erfolgen, danach in 6monatigen Abständen. 4. Bei DLB können sich kognitive Funktionen, Verhalten und Halluzinationen unter ChE-Hemmern bessern. 5. Zur Wirksamkeit von Amantadin bei AD liegen einzelne positive Ergebnisse vor. Die Studienlage für Gingko biloba ist derzeit nicht eindeutig. 6. Zur Wirksamkeit von Pirazetam, Nicergolin, Hydergin liegen für Kollektive dementer Patienten ohne differentialdiagnostische Zuordnung positive Ergebnisse vor. Eine Aussage zur Wirksamkeit bei AD und DLB ist nicht möglich. Atypische AD • Atrophie parieto-okzipital; • Funktionelle Einbußen schleichend für die Funktionen, die dort lokalisiert sind, d.h. primär Sehstörungen; • Dyslexie (Zeilenverlust, Oberflächendyslexie) • Agnosie (incl. Simultanagnosie, eher apperzeptive denn assoziative Agnosie) • Im späteren Verlauf dann komplettes Balint Syndrom 1998 Fallzahl Demenz/MCI 2003 25 20 15 Demenz MCI 10 5 0 Tagesmedizin PP/amb.&stat. Gesamt 61 (von ca. 130 Anforderungen TM & PP/ambulant/stationär) Reischies et al., 1997 Tests für die Demenzdiagnostik Klinischer Eindruck: schwere oder leichte Demenz • Schwere Demenz: CERAD-NP, Sprachverstehen, Sehen, Rechtschreibung, Rechnen, Lesen • Leichte Demenz: CERAD-NP ohne Gedächtnisteil, stattdessen CVLT, Rey Figur, Sprachverstehen, Sehen (VOSP und Poppelreuther), Rechtschreibung, Rechnen, Lesen, u.U. RBMT und Fahrtauglichkeit • MCI: CVLT, (WMS-R), Rey Figur, MT, Sprachverstehen, TAP Arbeitsgedächtnis, TAP Reaktionswechsel, TAP Inkompatibilität, BORB