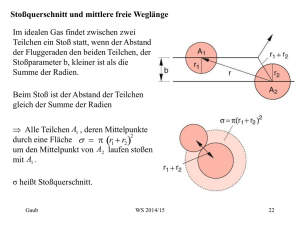
7.1
Werbung

Newton‘s Mechanics Stellar Orbits Gravity Galilei Leibniz Gaub WS 2014/15 1 Statistical Mechanics Steam Engine Chemical Reactions A + B AB Gaub Mayer Joule Helmholtz Clausius Kelvin Boltzmann Gibbs WS 2014/15 2 Molekular-Dynamik Rechnungen Nobelpreis 2013!!! Gaub WS 2014/15 3 MD Simulations Water http://www.youtube.com/watch?v=x8Atqz 5YvzQ http://www.youtube.com/watch?v=B3cXuisH8PI Gaub WS 2014/15 http://www.youtube.com/watch?v=xcMS Hy3CqXA 4 §7 Gase Kinetische Energie der Teilchen größer als die potentielle Energie der gegenseitigen Anziehung Teilchen bewegen sich frei mit beliebig großem Abstand makroskopische Betrachtung Boyle-Mariotte‘sches Gesetz: bei konstanter Temperatur gilt V dV const. 2 p dp p Def: Kompressibilität p V = const. 1 V 1 V p p const . m p m V => für konstante Temperatur ist p ~ ρ Gaub WS 2014/15 T=const. 5 Makroskopische Betrachtung Möglichkeit zur Messung des Druckes: Quecksilbermanometer Im Gleichgewicht gilt: g h p p0 Bei Zimmertemperatur ist der Dampfdruck von Quecksilber vernachlässigbar. Normaldruck: 1 torr 1 mmHg Gaub 1 atm 101325Pa N p 1 2 1Pa m 1 atm 133,33 Pa 760 WS 2014/15 6 Luftdruck und barometrische Höhenformel Herleitung der barometrischen Höhenformel Abnahme des auf der Fläche A lastenden Gewichts mit der Höhe: dFG g dm g h dV g h A dh dp g h dh mit p h p0 0 const. p dp g h p0 ph dh ph 0 ln h g p0 p0 dp 0 g p' h p dh ' 0 p 0 0 mit po= 1013hPa und 0= 1.24 kg/m3 ' 0 ph p0 e ph 1013 hPa e g h 8,33 km 0 p0 h Luftdruck und barometrische Höhenformel ph p0 e g 0 p0 h ph p0 g h Wie in Flüssigkeiten tritt in Gasen Auftrieb auf. Schweben entspricht Schwimmen in Luft! Für einen Ballon mit Masse M und Volumen V gilt: Gaub WS 2014/15 M g V Luft g 8 §7.3 Kinetische Gastheorie Das ideale Gas Gas aus starren Kugeln (Atome oder Moleküle) mit r0 Stöße der Teilchen untereinander und mit der Gefäßwand erfüllen Energie- und Impulssatz Wechselwirkung nur bei Berührung Wechselwirkungspotential V: 0 V r für r 2r0 für r 2r0 (Hardcore-Potential) Gaub WS 2014/15 9 Das ideale Gas Vorraussetzung: Atomradius << mittlerer Atomabstand Behandlung der Atome/Moleküle als Massenpunkte Druck p des Gases wird über Impulsübertrag auf die Gefäßwand verstanden: F d mv A dt A Treffen im Zeitintervall dt N dt Moleküle mit der Geschwindigkeit v senkrecht auf die Fläche A, dann ist der pro Sekunde übertragene Impuls 2 N m v. p Gaub p 2 Nm v A WS 2014/15 10 Grundgleichung der kinetischen Gastheorie Nur Betrachtung der Translation, keine Rotation oder Schwingung! Anzahl Z der in der Zeit Δt auf das Wandstück A treffenden Moleküle: Z nx v x A t wobei n x die Dichte der Moleküle ist, die sich mit der Geschwindigkeit v x in x-Richtung bewegen. Jedes Molekül überträgt den Impuls px 2 m vx F Z p x v 2 Zm x t t F p 2 m nx v2x A Gaub WS 2014/15 11 Grundgleichung der kinetischen Gastheorie Bewegung in y- und z-Richtung bleibt beim Stoß unbeeinflußt. Da der Druck eine isotrope Größe ist, gilt: v 2 x 1 N N v v x 2 x dv x v 2 y v 2 z 1 2 v 3 Im Mittel fliegen gleich viele Moleküle in +x- wie in –x-Richtung p p V Gaub 1 1 2 n 2 m v2x m n v2 n E kin 2 3 3 2 N Ekin 3 WS 2014/15 12 Mittlere kinetische Energie und absolute Temperatur Experimentell ergibt sich für konstantes N, dass p V nur von T abhängt. E kin 1 m v2 2 hängt nur von T ab. Es gibt eine Temperaturskala, für die gilt: E kin ~ T Definition der absoluten Temperatur T: 1 3 2 mv kT 2 2 mit der Bolzmann-Konstante pV N k T k 1,380541023 J K allgemeine Gasgleichung Gaub WS 2014/15 13 Mittlere kinetische Energie und absolute Temperatur Jedes Teilchen kann sich in x-, y- und z-Richtung bewegen. 3 Freiheitsgrade der Translation Die mittlere kinetische Energie eines Teilchens bei der Temperatur T ergibt sich zu: E kin 1 k T pro Freiheitsgrad 2 Reale Moleküle können Energie auch in Rotation und Schwingung aufnehmen mehr Freiheitsgrade Gleichverteilungssatz: (allgemeine Herleitung in T4) In einem Gas verteilt sich die Energie stets gleich auf alle Freiheitsgrade. Bei f Freiheitsgrade hat jedes Teilchen im Mittel die Energie E kin f Gaub 1 kT 2 WS 2014/15 14 Verteilungsfunktion Allgemeine Herleitung des Drucks erfordert mathematische Definition der Verteilung der Geschwindigkeit auf die Moleküle. Verteilungsfunktion f(v) Für die Geschwindigkeitskomponente in x-Richtung muss gelten: f v x dvx N v x dvx N mit N N v dv x x Die Anzahl der Teilchen im Intervall v x ; v x dv x ist dann: Nvx dvx N f vx dvx f v x 1 dvx N Nv dv x x 1 Bem: f v d v 1 0 Die Anzahl der Teilchen mit v u ist: x N v x u N f v dv x u x 15 Von allen Seiten des Halbraums prallen Moleküle auf die Wand Auf ein Flächenelement dA prallen während des Zeitintervalls Δt im Mittel dZ Moleküle im Geschwindigkeitsfenster v+dv aus dem Raumwinkelbereich dΩ, der um den Winkel ϑ gegen die Flächennormale geneigt ist dZ n f v dv v t dA cos d r d r sin d r 2 d 4 d sin d Die Impulsänderung eines Teilchens ist : p 2 m v cos Impulsübertrag durch dZ Teilchen im Zeitintervall Δt ist dann dZ p t p p total dA t Gaub 2 nm 4 2 2 v f v dv cos 2 2 sin d d 0 0 v0 v2 2π/3 p 1 n m v2 3 16 Maxwell-Boltzmannsche Geschwindigkeitsverteilung Aus der barometrischen Höhenformel ergibt sich durch Erweitern mit dem Volumen V einer Gasmenge der Masse M = mN =V und der Teilchenzahldichte n=N/V 0 e 0 g h p0 0 e M gh N kT nh n0e Modell: Moleküle starten auf der Erdoberfläche mit der Geschwindigkeit vz senkrecht nach oben und erreichen die Höhe h: mgh kT n0 e E pot kT m 2 vz m g h 2 => Die Anzahl der Moleküle, über die Höhe h hinausfliegen, ist gleich der Zahl, die von z = 0 aus mit Geschwindigkeiten vz>u starten. Nvz u z 0 Nvz 0 z h 17 Maxwell-Boltzmannsche Geschwindigkeitsverteilung Allgemein gilt für die Anzahl N(vz) der Moleküle mit der Geschwindigkeit vz die pro Zeit ∆t durch ein FlächenN z stück ∆A fliegen (Flussdichte): N vz nvz vz Az t Aus der Annahme einer isothermen Atmosphäre folgt, dass die Geschwindigkeitsverteilungsfunktion unabhängig von der Höhe ist. Nvz 0 z h nh Nicht die mittlere Geschwindigkeit, wohl aber die Flussdichte nimmt mit der Höhe ab: N vz 0 z 0 n0 v f v dv z z z vz 0 v f v dv z vz 0 z z Nvz 0 z h nh nh C(T ) Nvz u 0 C(T ) n0 vz f vz dvz Nvz 0 0 Nvz 0 0 n0 vz u 2 m gh m u kT 2 kT Es gilt aber auch: nh n0 e n0 e Const (T) m u2 2 kT 18 v z f v z dvz C1T e Nvz u 0 u Maxwell-Boltzmannsche Geschwindigkeitsverteilung Differentiation nach u liefert: u f u mu kT C1T e m u2 2 kT m u2 m 2 kT mit: C2 C1 T f u C2 e kT m C2 weil f u du 1 und 2 k T m u2 m 2 kT Symmetrische f u e Gaussverteilung 2 k T Ist die mittlere kinetische Energie sehr groß gegen die Differenz der potentiellen innerhalb eines abgeschlossenen Volumens V, ist keine Richtung ausgezeichnet. 3 2 e x2 dx m 2m kv T f v 2 k T e 2 19 Maxwell-Boltzmannsche Geschwindigkeitsverteilung Geschwindigkeitsvektoren mit der Länge v+dv enden in einer infinitesimalen Kugelschale mit dem Betrag der Geschwindigkeit als Radius. Ingegration über 2 alle Richtungen liefert den Faktor: 4 v dv 3 2 Zahl der Moleküle pro Volumeneinheit mit einer Geschwindigkeit im Betrag zwischen v undv+dv Mittlere Geschwindigkeit m 2 2 nv dv n 4 v e 2 k T 3 2 m v v f v dv 4 2 k T 0 Mittlere Geschwindigkeitsquadrat 3 kT fkT 2 2 v v f v dv m m 0 Wahrscheinlichste Geschwindigkeit dn 0 vw dv vw 2 kT m m v2 v 3 e m v2 2 kT dv 8 kT m 0 kT 2 vw dv Maxwell-Boltzmannsche Geschwindigkeitsverteilung nv dv n 4v v 3 w 2 e m v2 2 kT n dv 4 v 2 3 w v e v2 v w2 dv Die Geschwindigkeitsverteilung hat eine ausgeprägte Temperaturabhängigkeit vw 2 kT m WS 2014/15 21