aminosäuren und proteine - Physiologische Chemie Tiermedizin
Werbung

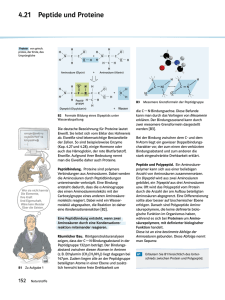
© Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München AMINOSÄUREN UND PROTEINE Beispiele für Stoffinhalte aus der Chemie als Grundlage für das Verständnis dieses Teiles: Prinzipien der chemischen Bindung, isoelektrischer Punkt, pH-Stabilität durch Pufferung, Chemie des Ammoniaks (und der Amine), funktionelle Gruppen und deren Reaktivität (z. B. Aktivierung von Biomolekülen für Synthesen und Säureamidbindung). Schlüsselwörter: Struktur: Einteilung und Strukturformeln der 21 proteinogenen Aminosäuren (inkl. Definition des isoelektrischen Punktes); biomedizinische Bedeutung ihrer funktionellen Gruppen in Proteinen (z. B. Hydroxylgruppen als Akzeptor für Substitutionen). Stoffwechsel: Prinzipien des Aminosäurestoffwechsels: Transaminierung, Decarboxylierung mit Bildung biogener Amine (u. a. Catecholamine/Histamin), oxidative Desaminierung; Einteilung in glukogene/ketogene Aminosäuren und Abbauwege der proteinogenen Aminosäuren; pathobiochemische Aspekte (insbesondere Ahornsirupkrankheit, Albinismus, Alkaptonurie, Homocystinurie, Phenylketonurie (hier Bedeutung des Tetrahydrobiopterin) sowie Nachweis von Folsäuremangel), Ammoniakbildung und -entgiftung (Glutamin-Synthese, Glutamatdehydrogenasereaktion, Synthesen von Carbamoylphosphat, Harnstoffzyklus). Peptide und Proteine: Peptidbindung (Chemie und Bedeutung für die Sekundärstruktur von Proteinen, ihre Bildung in der Proteinbiosynthese mit Berücksichtigung der Aminosäureaktivierung und Übertragung auf tRNA); Isopeptidbildung; biologisch wichtige Peptide (Glutathion, Endorphine); Sequenzierung von Proteinen, ko- und posttranslationale Modifikationen von Proteinen: Anheftung von Ubiquitin, N-Glykosylierung (Haupttypen der N-Glykane (Abb. 1 im Anhang)*, Dolicholpyrophosphat, Prozessierung der übertragenen Glykankette im ER und im Golgiapparat, Funktion von N-Glykanketten im endoplasmatischen Retikulum in der Qualitätskontrolle), OGlykosylierungen, Hydroxylierung (Prolin/Lysin in Kollagenbiosynthese und Tripelhelixbildung, Mechanismus unter Berücksichtigung von Vitamin C und O2, Skorbut – Vergleich zur Hydroxylierung von Phenylalanin), Phosphorylierung, Sulfatierung (inkl. Nutzung von PAPS als Substrat), Methylierung und Acetylierung von Aminosäuren, am Beispiel der Histone (Bedeutung für die Genregulation). © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Literatur: relevante Abschnitte der empfohlenen Lehrbücher in der jeweils aktuellsten Auflage: LEHNINGER/NELSON/COX „Biochemie“; STRYER „Biochemie“; * Abbildung 3 aus Kapitel 6 („The Sugar Code“, Hrsg. H.-J. Gabius; frei auf Webseite des Buches und als Anhang hier verfügbar). Bestimmung des Gesamtproteingehalts Vorbemerkung: H2 N O C N H O C Serumproben bestehen aus einem komplexen Gemisch von ca. 200 (Glyko)proteinen. Der quantitative Nachweis des NH2 Abbildung 1: Biuret Proteingehalts erfolgt häufig anhand von Farbreaktionen funktioneller Gruppen der Proteine mit farbstoffbildenden Reagenzien. Die Intensität des Farbstoffs korreliert direkt mit der Konzentration der reagierenden Gruppen und kann in einem Spektralphotometer gemessen werden. Eine auch in der Labordiagnostik verwendete Proteinbestimmungsmethode ist der Biuret-Assay, dessen O C C O Bezeichnung auf eine Farbreaktion mit gelöstem H N N H Biuret (Carbamoylharnstoff, Abb. 1) und Kupfersulfat in alkalischem, wässrigem Milieu zurückzuführen ist. Es entsteht ein rotvioletter Farbkomplex zwischen H C R O C H N H C R Cu2+ R C H C O N H R C H 2+ den Cu -Ionen und je zwei Biuretmolekülen. Die Reaktion ist typisch für Verbindungen mit mindestens zwei CO-NH-Gruppen (Peptidbindungen) und kann daher für den kolorimetrischen Nachweis von Abbildung 2: Der farbige Protein-Cu2+-Komplex, der bei der Biuret-Reaktion entsteht. Peptiden und Proteinen verwendet werden (siehe Abb. 2). Aufgabe: In einer Serumprobe ist der Gesamtproteingehalt zu bestimmen und in g/100 ml anzugeben. 2 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Prinzip: Proteine bilden in alkalischer Lösung mit Kupferionen einen blauvioletten Farbkomplex. Die Intensität der Farbe ist der Proteinkonzentration proportional und wird im Photometer bei 546 nm bestimmt. Durchführung: Folgende Versuchsansätze werden benötigt: Küvette mit Standardlösung Küvette mit Probenlösung Biuret-Lösung 1,0 ml 1,0 ml Plasmaprobe - 0,02 ml Standardlösung (6 g BSA* in 100 ml) 0,02 ml - * BSA = bovines Serumalbumin Nach 30 min werden die Extinktionswerte am Photometer abgelesen. Als Leerwert dient eine mit Biuret-Reagenz gefüllte Vergleichsküvette. Auswertung: Der Gesamtproteingehalt der Serumprobe wird mithilfe der angegebenen Konzentration der Standardlösung, sowie der gemessenen Extinktionswerte von Proben- und Standardlösung berechnet. Auftrennung von Serumproteinen mittels CAF-Elektrophorese Vorbemerkung: Unter dem Vorgang Elektrophorese versteht man die Wanderung geladener Teilchen in einem elektrischen Feld. Auf diesem Phänomen basiert eine leistungsfähige Methode zur Trennung von Proteinen und anderen Makromolekülen (u. a. DNA, RNA). Unterschiedliche Ladungen und Größe der Teilchen bewirken eine unterschiedliche elektrophoretische Beweglichkeit. Ein Substanzgemisch wird dabei in einzelne Zonen aufgetrennt. Elektrophoretische Trennungen führt man in unterschiedlichen Medien durch. Dabei gibt es folgende Möglichkeiten: 3 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München a. In Lösung: in offenen Kapillaren oder dünnen Pufferschichten (trägerfreie Elektrophorese) werden die Probenkomponenten hauptsächlich aufgrund der Ladungsunterschiede getrennt. Da bei der Elektrophorese Joulesche Wärme entsteht, können thermische Strömungen (Konvektion) die Trennung stören. b. In stabilisierenden (antikonvektiven) Matrices: antikonvektive Membranen (z. B. aus Celluloseacetat) oder Gele (z. B. aus Agarose oder Polyacrylamid) wirken Verbreiterungen von Zonen, die durch Konvektion verursacht werden, entgegen. Die Wanderungsgeschwindigkeiten der Teilchen werden in diesen porösen Matrices je nach Größe unterschiedlich verzögert (retardiert), so dass sie von der Größe und der Ladung abhängig sind. Zudem werden Auflösung und Trennschärfe verbessert. Die Fraktionierung von Serumproteinen für diagnostische Zwecke wird mithilfe von Celluloseacetatfolien (CAF) erreicht. Dieses Trägermaterial wird aus Cellulose in einer Reaktion (Veresterung) mit Essigsäure gewonnen. Es liegen ca. zwei acetylierte Hydroxylgruppen pro Glucosemolekül vor (s. Abb. 3). Aufgrund dieser chemischen Modifikation ist eine Adsorption der Serumproteine an das Trägermaterial nahezu ausgeschlossen. Wichtig ist zudem die Verwendung einer alkalischen Pufferlösung (pH 8,6)! Unter diesen Bedingungen „deprotonieren“ funktionelle Gruppen der Proteine, so dass diese negative Nettoladungen erhalten und in Richtung Anode wandern. Im allgemeinen ist die Wanderungsgeschwindigkeit um so schneller, je geringer die Molmasse und je größer die negative Ladung eines Proteins ist. Erleichtert wird dieser Effekt noch dadurch, dass eine große Anzahl der Serumproteine bereits negativ geladen ist. Albumin weist unter diesen Bedingungen die größte Zahl negativer Ladungen auf und wandert am weitesten in Richtung Anode. Globuline, die weniger negative Ladungen besitzen, wandern langsamer zur Anode, während γ-Globuline nicht bzw. sogar in Richtung der Kathode wandern. Nach abgeschlossener Elektrophorese färben sich die aufgetrennten Proteinfraktionen je nach ihrem Anteil an der Gesamtmenge der vorhandenen Serumproteine in einer Ponceau-S-Lösung mehr oder weniger intensiv rot. Im Elektropherogramm, der graphischen Aufzeichnung des Trennmusters, sind neben der Präalbumin- und der Albuminfraktion, drei Fraktionen der Globuline zu erkennen. Diese werden mit α, β und γ bezeichnet und können je nach Tierspezies auch in zwei Subfraktionen vorliegen. Veränderungen im Elektrophoreseprofil der Serumproteine liefern dem Kliniker wichtige diagnostische Hinweise (siehe Zusatzinformationen: CAF-Elektrophorese und Dysproteinämien). 4 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München O CH3 H O H H O HO H O O HO O H H O CH3 O H O H H3C H O CH3 H O O n Abbildung 3: Die chemische Formel zeigt einen Ausschnitt des Celluloseacetatmoleküls mit zwei acetylierten Hydroxylgruppen pro Glukosemolekül. Abbildung 4: Aufbau einer CAF-Elektrophoresekammer Aufgabe: Die Serumproteine werden durch CAF-Elektrophorese in Fraktionen (siehe oben) aufgetrennt und anhand mitgeführter Standardproteine identifiziert. Durchführung: Die am Platz aufgestellte Elektrophorese-Kammer (BIOTEC-FISCHER, vgl. Abb. 4) mit einer Pufferlösung (pH 8,6) gleichmäßig füllen. Den Trennsteg zwischen den Kammerhälften trocken wischen! Achten Sie darauf, die Celluloseacetatfolie (micro solid, BIOTEC-FISCHER) zwischen den Perforationen nicht mit den Fingern zu berühren! Folie in Pufferlösung mind. 2 min vorpuffern, anschließend mit einer Perforation auf den beweglichen Steg der BFA-Folienbrücke legen. Ziehen Sie mit der Pinzette die Folie vorsichtig soweit, bis die andere Perforation auf den starren Steg aufgelegt werden 5 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München kann. Stellen Sie die Folienbrücke in die Kammer, und zwar so, dass die Folienenden Kontakt zum Puffer haben. Von jeder Lösung (Standardsubstanzen und Serumproben) werden 20 µl in die Vertiefungen des BFA-Auftragesystems gegeben und der BFAApplikator wird in die entsprechende Führungsnut der Serumpalette gesetzt, um das Serum aufzunehmen. Den Applikator direkt in die mittlere Schiene der BFA-Folienbrücke einsetzen und nach ca. 5 Sekunden wieder entfernen. Kontrollieren Sie, ob die Brücke richtig in der Kammer sitzt. Die Auftragstelle muß kathodenseitig liegen. Anschließend den Deckel der Kammer fest verschließen und die Elektrophorese durch Einschalten des Spannungsgeräts in Gang setzen. Nach etwa 40 Minuten Laufzeit bei 200 V die Folie entnehmen und in der Färbewanne etwa 10 min anfärben (Färbelösung: 0,2 g Ponceau S in 100 ml Essigsäure 10%, v/v). Die Beseitigung überschüssiger Färbelösung erfolgt beim Entfärben in verdünnter Essigsäure (3% v/v). Auswertung: Die erhaltenen Trennmuster sind anschließend zu interpretieren und die Ergebnisse im Protokollheft festzuhalten. Bestimmung der Molmasse einzelner Proteinen nach Auftrennung in SDS-Polyacrylamidgelen Vorbemerkung: Natriumdodecylsulfat (sodium dodecyl sulfate, SDS) ist ein anionisches Detergens und überdeckt die Eigenladung der Proteine so effektiv, dass Micellen mit konstanter negativer Ladung pro Masseneinheit entstehen (ca. 1,4 g SDS pro g Protein). Dieses Prinzip wird zur Bestimmung des Molekulargewichts von Proteinen genutzt. Bei der Probenvorbereitung werden die Proben mit einem Überschuß an SDS auf 95 °C erhitzt. Dies hat zur Folge, dass die Tertiär- und Sekundärstrukturen der Proteine durch Aufspaltung der Wasserstoffbrücken und durch die Streckung der Moleküle aufgelöst werden. Disulfidbrücken zwischen Cysteinen werden durch Zugabe einer reduzierend wirkenden Thiolverbindung, wie z. B. β-Mercaptoethanol oder Dithiothreitol (DTT), gespalten. Als Trägermedium wird das chemisch inerte Polyacrylamid verwendet, das in einer Kopolymerisationsreaktion (siehe Abb. 5) aus Acrylamid und dem quervernetzenden Reagenz, N,N´Methylenbisacrylamid (Bis) hergestellt wird. Der Vernetzungsgrad C in der Gelmatrix wird 6 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München bei der Routineanwendung konstant bei ca. 3% gehalten. In diesem Fall werden die Porendurchmesser durch die steigende Totalacrylamidkonzentration T kleiner. Ein Gel mit 5% T hat einen Porendurchmesser von ca. 5,3 nm, eines mit 20% T von ca. 3,3 nm. Die negative Ladung des SDS „maskiert“ die ursprüngliche Ladung des Proteins, so dass zwei Proteine gleicher Masse, die identische Mengen an SDS-Molekülen gebunden haben, im elektrischen Feld gleichweit wandern. Im Polyacrylamidgel werden die Proteine dann nach ihrer Größe aufgetrennt. Die Wanderungsgeschwindigkeit von Proteinen mit kleiner Masse wird nicht so stark verzögert wie die von Proteinen mit großer Masse: deswegen legen sie eine größere Wegstrecke zurück. Wegen der hohen Auflösung, die mit der diskontinuierlichen Elektrophorese erreicht werden kann, wird standardmäßig (auch im experimentellen Teil der Übung!) für Proteintrennungen ein von U.K. Laemmli eingeführtes SDS-haltiges, diskontinuierliches Tris-HCl/Tris-Glycinpuffersystem eingesetzt. Die Gelmatrix besteht dabei aus einem kurzen weitporigen Sammelgel und einem daran anschließenden längerem engporigen Trenngel. Durch die im Sammelgel erzielte Konzentrierung der zu trennenden Proteine in einer scharfen Bande wird im Trenngel eine optimale Zonenbildung erreicht (siehe Zusatzinformationen: DiskElektrophorese). CH2 CH CH2 CH2 CH CH2 CH CH2 CH CH2 CH C O C O C O C O C O N H2 H 2C N H2 NH C O NH 2 CH2 N H2 N H2 CH2 CH NH C O H 2 C CH NH (N H4 )2S 2O 8 2NH 4+ 2SO 4 TEM ED NH C O C O C H 2 CH [CH 2 CH] x CH 2 CH CH 2 CH CH 2 CH CH2 CH C O C O C O C O C O NH 2 NH NH N H2 N H2 H 2C C H CH 2 CH 2 NH NH C CH 2 CH C H2 C H H 2N C O C O O CH 2 CH CH 2 CH CH2 CH CH2 CH CH2 CH C O C O C O C O NH 2 N H2 N H2 N H2 Abbildung 5: Struktur eines Polyacrylamidgels. Durch chemische Copolymerisation von Acrylamidmonomeren mit dem Quervernetzer N,N´-Methylenbisacrylamid erhält man ein durchsichtiges Gel. Als Initiator dient das Persulfat-Anionradikal, das aus Ammoniumperoxodisulfat entsteht, als Katalysator Tetramethylethylendiamin (TEMED). 7 der Reaktion N,N,N´-N´- © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Prinzip: Bei der Elektrophorese im Polyacrylamidgel mit 0,1% SDS erhält man über bestimmte Bereiche eine lineare Beziehung zwischen dem Logarithmus der Molmasse und den Wanderungsstrecken der SDS-Polypeptid-Micellen. Mithilfe von Standardproteinen bekannter Molmasse lassen sich die Molmassen der zu analysierenden Proteine ermitteln. Bei Gelen mit konstanten T-Werten erstreckt sich die Linearität über einen begrenzten Bereich, der vom Größenverhältnis Molmasse zu Porendurchmesser bestimmt ist. Exakt ermitteln lassen sich jedoch nur die Molmassen von Untereinheiten (Monomere), die durch Spaltung von Disulfidbrücken entstanden sind. Durchführung (Demonstrationsversuch): Zunächst wird das Elektrophoresesystem Protean II der Fa. BioRad (München) erklärt. Ebenso liegt ein gefärbtes SDS-Gel mit aufgetrennten Standardproteinen bekannter Molmassen sowie mit Proteinen, deren Molmassen zu berechnen sind, bereits vor. Um das Gel in der vorliegenden Form zu erhalten wurden folgende Schritte durchgeführt: Die Proben bzw. eine Mischung der Standardproteine wurden mit dem gleichen Volumen an Probenpuffer (62,5 mM Tris-HCl, pH 6,8; 10% (w/v) Glycerol; 2% (w/v) SDS; 50 mM β-Mercaptoethanol; 0,001% (w/v) Bromphenolblau) gemischt und 5 min bei 95 °C erhitzt. Anschließend wurden mit einer Mikroliterspritze die Proben in die Geltaschen eines Sammelgels (4% g/v Bis-Acrylamid; 125 mM Tris-HCl, pH 6,8; 0,1% SDS; 0,01% Ammoniumperoxodisulfat; 0,05%-0,1% TEMED), das nach ca. 1,5 cm Laufstrecke in ein Trenngel (12% Acrylamid;375 mM Tris-HCl, pH 8,8; 0,1% SDS; 0,01% Ammoniumperoxodisulfat; 0,05%-0,1% TEMED) übergeht, pipettiert. Der Laufpuffer (20 mM Tris; 192 mM Glycin; 0,05% SDS) wurde in die Gelkammer gefüllt, diese an ein Spannungsgerät angeschlossen und die Elektrophese bei 200 Volt konstanter Spannung durchgeführt die mit Bromphenolblau gefärbten Proben den unteren Gelrand erreichten. Danach erfolgte ca. 15 min die Färbung in Coomassie-Lösung (0,25% (w/v) Coomassie-Brilliant-Blau-R250; 45% (v/v) Ethanol; 10% (v/v) Essigsäure). Nach 2-3 Stunden Lagerung des Gels in der Entfärbelösung (45% (v/v) Ethanol; 10% (v/v) Essigsäure) heben sich die deutlich blau gefärbten Proteintrennbanden vom leicht bläulich gefärbten Hintergrund ab. 8 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Auswertung: Um die Molmassen der aufgetrennten, unbekannten Proteine zu ermitteln, werden die Laufstrecken der Standardproteine mit ihren bekannten Molmassen in cm gemessen und diese Werte in einem Koordinatensystem auf der Abzisse (x-Achse) aufgetragen. Demgegenüber werden die bekannte molaren Massen der Standardproteine logarithmisch (Zehnerlogarithmus) transformiert und die erhaltenen Werte in Bezug zur Laufstrecke auf der Ordinate (y-Achse) eingetragen. Mithilfe der eingezeichneten Geraden (bitte durch möglichst viele Messpunkte führen!) und den Laufstrecken der Probenproteine in cm werden die entsprechenden logarithmisch transformierten Werte der molaren Massen ermittelt. Anschließendes Delogarithmieren ergibt die molaren Massen in Da. Ammoniak- und Harnstoffbestimmung in einer Serumprobe Vorbemerkung: Harnstoff wird in der Leber aus Ammonium-Ionen (im Dissoziationsgleichgewicht mit Ammoniak), die aus dem physiologischen Aminosäuren- und Proteinstoffwechsel sowie aus dem Proteinabbau im Darm stammen, erzeugt. Zweck der Harnstoffbildung ist die Fixierung des giftigen Ammoniaks in einem ungiftigen Produkt, das über die Nieren ausgeschieden wird. Eine gestörte Leberfunktion kann zu einem Anstieg des Ammoniakgehalts im Serum führen in dessen Folge eine hepatische Enzephalopathie mit komatösen Zuständen entstehen kann. Prinzip: Im Experiment, wird Harnstoff mithilfe des Enzyms Urease zu Ammoniak und Kohlendioxid gespalten: O H2N C NH 2 + H 2O Urease 2NH3 + CO2 (Gl.1) Ammoniak und α-Ketoglutarat werden wiederum von das Enzym Glutamat-Dehydrogenase (GLDH) und unter Verbrauch von reduziertem Nicotinamidadenindinukleotid (NADH) zu L-Glutamat umgesetzt: 9 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München !-Ketoglutarat + NADH + NH 4+ GLDH L-Glutamat + NAD+ + H2 O (Gl. 2) In einer Serumprobe wird der Harnstoffgehalt bestimmt. Um eine Fehlerquelle bei der Bestimmung von Harnstoff auszuschließen, wird zunächst die in der Serumprobe bereits vorhandene Konzentration an Ammoniak (diese steigt nach Blutabnahme an, vor allem durch Abbauprozesse und Hämolyse) gemessen. Dazu wird die Ammoniakbestimmung ohne Zugabe des Enzyms Urease durchgeführt. Es läuft somit lediglich die in der Gleichung 2 (Gl. 2) angegebene Reaktion ab. Die während der Reaktion verbrauchte NADH-Menge ist der Ammoniakmenge äquivalent. NADH ist Messgröße und aufgrund seiner Absorption bei 365 nm photometrisch zu bestimmen. Durchführung: Die Lösungen entsprechend dem unten angegebenen Schema in Küvetten pipettieren und die Extinktionswerte am Photometer ablesen: 10 © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Harnstoffbestimmung Ammoniakbestimmung Reagenzienleerwertb) Probenwertb) Reagenzienleerwertb) Probenwertb) Reaktionsgemischa) 1,0 ml 1,0 ml 1,0 ml 1,0 ml Serum - 0,05 ml - 0,05 ml dest. Wasser 0,5 ml 0,45 ml 0,51 ml 0,46 ml UreaseLösung 0,01 ml 0,01 ml - - mischen, nach ca. 5 min bei 20-25 °C Extinktionswerte der Lösungen messen (E1), Reaktion starten durch Zugabe von GLDH-Lösung 0,01 ml 0,01 ml 0,01 ml 0,01 ml mischen, nach ca. 20 min bei 20-25 °C Extinktionswerte der Lösungen messen (E2). Falls die Reaktion nach 20 min nicht zum Stillstand gekommen ist, die Extinktionswerte im Zeitintervall von 2 min messen, bis eine konstante Abnahme pro Zeitintervall erreicht ist. a) b) u. a. Triethanolaminpuffer (pH 8,0), α-Ketoglutarat, NADH; sowohl für Proben- als auch Reagenzienleerwerte die Extinktionsdifferenzen (E1-E2) berechnen. Die Differenz der Leerwerte (ΔEL ) von der Differenz der Proben (ΔEP) abziehen. Aus der Harnstoffprobe erhält man: ΔEHarnstoff + Ammoniak (aus Harnstoffprobe) und ΔEAmmoniak (aus Ammoniakprobe). Die Differenz dieser Werte ergibt: ΔEHarnstoff. Berechnung: Nach der allgemeinen Berechnungsformel für die Bestimmung der Konzentration gilt: c= V •M• "E #•d• v V, Testvolumen in ml; v, Probenvolumen in ml; M, Molmasse (g/mol) von Harnstoff bzw. Ammoniak; d, Schichtdicke in cm; ε, molarer Extinktionskoeffizient von NADH bei einer ! Wellenlänge von 365 nm = 3427 l • mol-1 • cm -1 Daraus ergibt sich für die Berechnung des Gehalts an Ammoniak (1) und des Gehalts an Harnstoff (2): ! c= 1,52 • 60,06 • "E Harnstoff 3427 •1• 0,05 • 2 mol • cm • ml • g = 0,266 • "E Harnstoff g /l (2) l • cm • ml • mol c= 1,52 •17,03 mol • cm • ml • g • "E Ammoniak = 0,151• "E Ammoniak g /l (1) 3427 •1• 0,05 l • cm • ml • mol 11 ! © Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München Anhang (siehe Schlüsselwörter): Abbildung 1: Illustration of principal oligosaccharide structures occurring during the biosynthesis of N-glycans. The A, B and C branches are indicated in the LLO precursor and high mannose-type Nglycan; 3′ and 6′ indicate the respective antenna of the N-glycan. 12