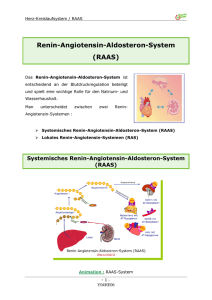
Gesamtpräsentation zum Öffnen/Download
Werbung

Hypertonie Aktuelles zur Therapie Mag.med.vet. Heinz Steinmaßl Medical & Regulatory Affairs Director Solvay Pharma e-mail: [email protected] Definition und Einteilung des Blutdrucks (mmHg) WHO/ISH-Richtlinien: systolisch diastolisch Optimal Normal Hochnormal < 120 < 130 130-139 < 80 < 85 85-89 Hypertonie: milde (Grad 1) - Grenzwerthypertonie mittelschwere (Grad 2) schwere (Grad 3) isoliert systolische (ISH) - Grenzwert-ISH 140-159 140-149 160-179 180 140 140-149 90-99 90-94 100-109 110 < 90 < 90 J Hypertens 17 (1999) Dezember 2003 2 Status Österreich Strenge Grenzwerte (seit 1997) für die Selbstmessung Hypertonie über 135 mmHg systolisch und über 85 mmHg diastolisch Werte als Ergebnis von mindestens 30 (Selbst-) Messungen Wenn mehr als 1/4 der Einzelwerte (= 7) über den Grenzwerten liegen Hypertonie Dezember 2003 3 Prävalenz der Hypertonie Abhängigkeit von Alter und Geschlecht 50 Häufigkeit (%) 40 30 Männer Frauen 20 10 0 25-34 35-44 45-54 55-64 65-74 Alter (Jahre) MONICA Project Augsburg, 1993 Dezember 2003 4 Prävalenz und Behandlung Hypertonie in Österreich Hypertoniker in Österreich Hypertoniker, denen regelmäßig ihre Erkrankung behandelte bekannt ist Hypertoniker suffizient behandelte Hypertoniker 200.000 1,5 Millionen 750.000 500.000 Schmeiser-Rieder et al., 1995 Dezember 2003 5 HOT-Studie: Optimaler Blutdruck HOT = Hypertension Optimal Treatment Kardiovaskuläre Risikoreduktion (%) 0 -5 -10 105 100 95 90 85 80 erzielter diastol. Blutdruck (mmHg) - 82.6 mmHg -15 -20 -25 -30 Minimales CV-Risko bei 139/83 mmHg ! Hansson, Lancet 1998 Dezember 2003 6 Bedeutung des systolischen Blutdrucks lange Zeit unterschätzt Relatives Risiko für Tod durch KHK in Abhängigkeit vom Blutdruck 4 systolisch diastolisch 3 2 1 0 1 2 tiefste 10% Syst. <112 Diast. <71 3 4 5 6 125 81 7 8 9 10 höchste 10 % >151 mmHg >98 mmHg Daten von Stamler et al.; Arch.Intern.Med. 1993;153:598-615 Dezember 2003 8 Relatives Risiko für Tod durch Schlaganfall in Abhängigkeit vom Blutdruck 10 8 systolisch diastolisch 6 4 2 0 1 2 tiefste 10% Syst. <112 Diast. <71 3 4 5 6 125 81 7 8 9 10 höchste 10 % >151 mmHg >98 mmHg Daten von Stamler et al.; Arch.Intern.Med. 1993;153:598-615 Dezember 2003 9 Bedeutung der systolischen Wirkung Hypertonie – Subtypenverteilung Subtypenverteilung (%) 100 isolierte systolische Hypertonie systolische-diastolische Hypertonie 80 isolierte diastolische Hypertonie 60 40 20 0 < 40 40-49 50-59 60-69 70-79 80 Alter (Jahre) Franklin et al. Hypertension 2001 Dezember 2003 10 Das Problem des Hypertonikers ab 50 ist die Systole ! 150 140 systolisch 130 130 120 120 110 100 90 diastolisch Frauen 150 mmHg mmHg 140 Männer systolisch 110 100 90 80 80 70 70 60 60 diastolisch Alter (Jahre) Alter (Jahre) Weiße (ohne Hispaniola) Systolischer und diastolischer Blutdruck im Verlauf der Lebensdekaden Modifiziert nach NHANES III, 1991 bis 1994 Dezember 2003 11 Pulsdruck als Risikofaktor Differenz zwischen maximalem systolischem und minimalem diastolischem Blutdruck Frühzeitiger Risikoindikator Ursache z.B. verringerte Gefäßwandelastizität Dezember 2003 12 Pulsdruck als Risikofaktor Risiko einer Herzinsuffizienz bezogen auf den Pulsdruck Tertile 1: Pulsdruck 26-48 mmHg, Tertile 2: 49-60 mmHg, Tertile 3: 61-150 mmHg Framingham Heart Study; Ann.Intern.Med. 2003; 138:10-16 Dezember 2003 13 Eprosartan & Pulsdruck: ETAPA-2 Pulsdruck in mmHg 80 72,5 70 63,4 60,4 58,6 8 Wochen 12 Wochen 60 50 40 30 20 10 0 Baseline 4 Wochen 3.133 Patienten; Ǿ RR 165,9/93,5 mmHg Modifiziert nach A.de la Sierra; Hipertension 2003; 20(2):56-62 Dezember 2003 14 Senkung der Mortalität durch antihypertensive Therapie Mortalitätsrate / 1000 Personen 50 Risiko 40 Risiko - 31% 30 ohne Behandlung mit Behandlung 20 - 60% 10 0 p<0.001 n=77 n=36 kardiovaskuläre Todesfälle n=132 n=105 Todesfälle (gesamt) Daten aus Framingham Heart Study Dezember 2003 Sytkowski et al.,15 1996 Therapieschema bei arterieller Hypertonie Monotherapie Betablocker Diuretikum Zweifachkombinationen Kalziumantagonist* ACE-Hemmer AT1-Blocker z.B. Eprosartan Diuretikum plus Betablocker Kalziumantagonist* ACE-Hemmer AT1-Blocker z.B. Eprosartan oder Kalziumantagonist* plus Betablocker *Untergruppen beachten! Dezember 2003 ACE-Hemmer AT1-Blocker z.B. Eprosartan Nach Deutscher Hochdruckliga 16 Regulation des Blutdrucks (vereinfacht) Humoral: RAAS (Niere und lokal) Neural: Sympathikus Dezember 2003 17 Renin-Angiotensin-Aldosteron-System Angiotensinogen Niere Renin Angiotensin I Sympathikusaktivierung ACE NNR Angiotensin II Aldosteron Na+-Retention Vasokonstriktion Blutdruck Dezember 2003 18 Beeinflussung des RAAS Angiotensinogen Reninhemmer Renin Inaktive Bruchstücke Angiotensin I ACE ACE-Hemmer Bradykinin ACE-Hemmer Angiotensin II AT1-Rezeptorantagonisten + Vasodilatation - Husten Dezember 2003 B2 AT1 AT2 19 ACEI - Nachteile Angiotensin II entsteht auch unabhängig von ACE Chymasen, Cathepsin G, t-PA, Tonin, CAGE = chymostatinsensitive angiotensin generating enzyme Unvollständige Blockade des RAAS Kombination mit A-II-Antagonisten noch kontrovers diskutiert (VALHEFT: vermutlich positiv) Akkumulation von Bradykinin: günstig: Vasodilatation ungünstig: Reizhusten Dezember 2003 20 Alternative AII-Bildung Angiotensinogen Renin t-PA Cathepsin G Tonin Reninhemmer Angiotensin I ACE ACE-Hemmer Chymases Cathepsin G CAGE Angiotensin II AT1-Rezeptorantagonisten AT1 AT2 t-PA = tissue plasminogen activator CAGE = chymostatin-sensitive angiotensin generating enzyme Dezember 2003 21 Angiotensin II - Nachteile Aktivierung von Wachstumsfaktoren für Gefäßmuskelzellen Aktivierung von Makrophagen Einwanderung von Makrophagen Stimulation der Plättchenaggregation Produktion von Superoxid Förderung der Oxidation von LDL-Cholesterin Dezember 2003 22 Angiotensin II-Rezeptorsubtypen Funktion AT1 AT2 Vasokonstriktion kardiale Kontraktilität Aldosteronfreisetzung Antiproliferation Zelldifferenzierung Apoptosis ? Proliferation (Herz, Gefäße) zentrale Osmoregulation Noradrenalinfreisetzung Chung et al., 1996 Dezember 2003 23 AT1-Rezeptorblockade Physiologische Effekte Selektive Blockade der AT1-Rezeptoren Angiotensin-II Hemmung der AldosteronProduktion Hemmung der Gefäßkontraktion Abschwächung der sympathischen Stimulation Abnahme der Stimulation von Wachstumshormonen Hemmung der renalen Natrium- und Wasserretention Dezember 2003 Vermehrte Stimulation der AT2-Rezeptoren Antiproliferative Effekte, u.a. an Herzmuskelzellen Regulierung des Zellwachstums bzw. der Zelldifferenzierung BLUTDRUCKSENKUNG 24 Sympathikus: A-II-Wirkung Periphere Nervenendigung Stimulation Präsynapse NA NA - + NA AT1 NA NA NA Blutgefäß Noradrenalinfreisetzung NA NA A II NA A II NA NA 1 Angiotensin II (Aktiviertes RAAS) A II AT1 Systolischer BD Vasokonstriktion Dezember 2003 25 Sympathikus: A-II-Blockade Periphere Nervenendigung Stimulation NA Präsynapse NA NA - NA NA Noradrenalinfreisetzung NA NA NA + AT1 NA A II NA A II Blutgefäß Angiotensin II (Aktiviertes RAAS) NA 1 AT1 Systolischer BD Vasokonstriktion In therapeutischer Dosierung nur für Eprosartan gezeigt! Dezember 2003 Ohlstein et al., Pharmacol. 1997 26 Angiotensin-II-Antagonisten Am Beispiel von Eprosartan Teveten® Chemische Struktur der “Sartane” nicht-biphenylischer Typ biphenylischer Tetrazol-Typ H N N N N COOH N N COOH S Eprosartan Dezember 2003 N N OH Cl Losartan, Candesartan, Valsartan, Telmisartan 28 Eprosartan vs. Enalapril bei milder bis mittelschwerer Hypertonie diastolisch systolisch 80 -3 -6 -9 -12 -15 -12.9 -11.9 -15.5 -14.7 Responderrate (%) Abnahme Blutdruck im Sitzen (mmHg) 0 p <0.05 82 73 60 40 20 0 -18 Eprosartan (400-600 mg/Tag) Enalapril (5-20 mg/Tag) 532 Patienten mit milder Hypertonie (DBP >95<114 mmHg) 26 Wo. behandelt Argenziano, Curr.Med.Res.Opin., 1999 Dezember 2003 29 Eprosartan vs. Enalapril bei schwerer Hypertonie Mittlere Veränderung am Endpunkt der Studie im Vergleich zum Ausgangswert –5 –5 –10 –15 –20 –16,2 –20,1 p=0,136 –25 Eprosartan Enalapril (n=59) (n=59) Senkung des systolischen Blutdrucks im Sitzen (mmHg) Senkung des diastolischen Blutdrucks im Sitzen (mmHg) 0 –10 –15 –20 –21,2 –25 p=0,025 –30 –29,1 Eprosartan Enalapril (n=59) (n=59) Eprosartan mindestens gleich wirksam wie Enalapril, systolisch signifikant stärker Sega, Blood Pressure, 1999; 8:114-121 Dezember 2003 30 Ein Dosistrick? Eprosartan Tagesdosis 400 mg 600 mg 800 mg 800 mg+HCT % Patienten 25 17 19 39 40 800 mg+HCT 35 30 400 mg 25 20 15 10 5 0 Dezember 2003 800 mg 600 mg % der Patienten in den einzelnen Dosisgruppen Häufige Kritik: „Alle vergleichen versus niedrige Enalaprildosen“ Teveten tendenziell mehr Patienten in niedriger Dosis Enalapril Tagesdosis 10 mg 20 mg 40 mg 40 mg+HCT % Patienten 10 22 31 37 40 35 40 mg 40 mg+HCT 30 25 20 mg 20 15 10 mg 10 5 0 Nach Sega, Blood Pressure, 1999; 8:114-121 31 Reduction in sitting diastolic blood pressure (mmHg) Einmaldosis 0 Eprosartan Eprosartan 1x1 2x1 Placebo (n=78) (n=79) (n=80) –2 –4 –6 –8 p<0.0001 –10 Hedner et al, J Hypertens, 1999 Dezember 2003 32 Unerwünschte Erscheinungen (>2%): Eprosartan vs. Placebo Chest pain Viral infection Injury Diarrhoea Placebo (n=352) Dizziness Eprosartan (n=1202) Sinusitis Coughing Pharyngitis Rhinitis Myalgia Upper resp.tr. infect. Headache 0 1 2 3 4 5 6 7 8 9 10 Patients reporting an adverse experience (%) Gavras and Gavras, Pharmacotherapy, 1999 Dezember 2003 33 Verträglichkeit Gesamthäufigkeit unerwünschter Ereignisse unter Eprosartan mit der unter Placebo vergleichbar. Absetzrate wegen unerwünschter Ereignisse bei Eprosartan 4,1%, bei Placebo 6,5% Ref.: Austria-Codex Fachinformation Dezember 2003 34 Vergleich der A-II-As Pharmakologische Eigenschaften der AT1-Blocker Substanz Eprosartan Losartan/EXP Valsartan Irbesartan Candesartan Telmisartan Nicht in Ö. nein ja (14%) nein nein ja nein kompetitiv komp./ nicht komp. nicht komp. nicht komp. nicht komp. nicht komp. 13 33 25 60-80 42 43 Nahrungseffekt nein minimal bis 40-50% nein nein nein Halbwertszeit (h) 5-9 2/6-9 6-7 11-15 4/9-10 bis zu 24h Proteinbindung (%) 98 98.7/99.8 95 90 99.8 99 Verteilungsvolumen (l) 13 34/12 17 53-93 9.1 500 Interaktion CYP 450 nein ja nein ja ja nein Elimination (hep./renal) 61/37 50/43 70/30 80/20 67/33 98/2 600 50-100 80-160 150-300 8-16 40-80 >80% 57-70% Prodrug (akt. Metab.) Rezeptorhemmung Bioverfügbarkeit (%) Erhaltungsdosis (mg) Trough/peak-Wert Dezember 2003 67% 50-75% 66% 58-74% 36 Vergleich Alle A-II-As sehr ähnlich Geringfügige Unterschiede in chemischer Struktur und pharmakokinetischen Eigenschaften Klinische Relevanz dieser Unterschiede nicht restlos geklärt Dezember 2003 37 Unterschiede (mögliche) Vorteile von Eprosartan Chemische Struktur: Eprosartan einziger nicht biphenylischer A-IIAntagonist Stärkere Affinität zum präsynaptischen AT1Rezeptor? Mögliche Erklärung für pharmakologische Unterschiede Dezember 2003 38 Unterschiede Vorteile von Eprosartan Keine Interaktion mit Cytochrom P 450 Deutlich verringertes Interaktionspotenzial Dezember 2003 39 Unterschiede Vorteile von Eprosartan Hemmung des Sympathikus (Noradrenalin-Outflow) Klasseneffekt, aber Dosisvorteil für Eprosartan Verstärkte Wirkung auf systolischen Blutdruck Schlaganfallprophylaxe ? Dezember 2003 40 Änderung des diastolischen Blutdrucks vs Kontrolle (%) Sympathikus - Substanzvergleich 40 30 20 10 0 -10 -20 -30 -40 -50 Eprosartan (0.3 mg/kg) Losartan (0.3 mg/kg) Valsartan (0.3 mg/kg) Irbesartan (0.3 mg/kg) * i.v.10 min vor Stimulation (Akutwirkung) * p < 0.05 Sympathikus-Stimulation bei 1 Hz (Tiermodell) Ohlstein, 1997 Dezember 2003 41 Bestätigung durch neuen Vergleich 200 Candesartan Verhältnis* 150 100 Valsartan 50 Embusartan Eprosartan 0 Verhältnis* der Sympathikus hemmenden Dosis zur direkten Gefäßwirkung. Redrawn from J. Balt, M-J Mathy, M. Pfaffendorf and P.A. van Zwieten, Journal of Hypertension 2001; 19: 2241 - 2250. Dezember 2003 42 Verträglichkeit der AT-1-Blocker im Vergleich mit anderen Antihypertensiva Verträglichkeit von Antihypertensiva Nebenwirkungshäufigkeit (%) 20 Diuretika β -Blocker und Kalziumantagonisten ACE-Hemmer Angiotensin-II-Antagonisten 10 0 Dosis Ménard et al., 1997 Dezember 2003 44 Angiotensin II-Antagonisten Therapie-Compliance nach 1 Jahr 80 n=6567 n=5842 60 n=5094 n=4994 n=4226 40 20 0 A-II-A Diuretikum Ca-Antagonist ACE-Hemmer ß-Blocker Bloom, 1999 Dezember 2003 45 Vorteile Eprosartan (Teveten®) Keine Biphenylstruktur (= vermutete Ursache für Unterschiede) Duale Wirkung: RAAS + Sympathikus Betonte Senkung systolisch Schlaganfall-Risikofaktor! Keine Interaktion mit Cytochrom-P450 Der preisgünstigste A-II-A Dezember 2003 46 „Alle Weisheit beginnt mit der Erkenntnis der Tatsachen.“ Cicero Dezember 2003 47 Laufende Forschung Eprosartan Rationale: Eprosartan Sympathikus Systolischer Blutdruck Stroke Morbidity/Mortality Dämpfung des Sympathikus und Senkung der Schlaganfallmortalität im Tierversuch gezeigt Klinische Überprüfung am Menschen läuft Dezember 2003 48 Erster Test: Schlaganfallmortalität Spontaneously hypertensive - stroke prone rats Überlebensrate (%) 100 80 60 40 Eprosartan (60 mg/kg/d) Placebo 20 0 0 2 4 6 8 Zeit (Wochen) 10 12 Barone et al., Am.J.Hypertens., 1999 Dezember 2003 49 Laufende Forschung zu Eprosartan MOSES Morbidität und Mortalität nach Schlaganfall Eprosartan vs. Nitrendipin in der Sekundärprophylaxe Deutschland, Österreich (5 österr. Zentren mit 33 Patienten) 1.400 Hypertoniker nach Schlaganfall Essentielle Hypertonie nach cerebraler Ischämie (Apoplex/TIA in den letzten 24 Monaten, Ausschluss: relevante Carotis-Stenose) 2 Jahre Therapie Abschluss 2004 Dezember 2003 50 MOSES – Endpunkte Primärer Endpunkt Beurteilung der Gesamtmortalität und der Gesamtzahl kardiovaskulärer und cerebrovaskulärer Ereignisse Sekundäre Endpunkte Mortalität und Morbidität aufgrund rezidivierender cerebrovaskulärer Ereignisse Funktionelle Leistungsfähigkeit (Barthel-Index, Ranking Scale) Mentale Leistungsfähigkeit (Mini Mental Score) Dezember 2003 51 Laufende Forschung zu Eprosartan Untersuchungen der Sympathikusdämpfung am Patienten: (klinische Überprüfung der präklinischen Daten) Studie in Australien vs. Placebo und vs. Losartan Ergebnisse 2004 Pilotstudie Prof. Magometschnigg: Gefäßwandelastizität – Augmentation Index Publikation Anfang 2004 erwartet Dezember 2003 52 Laufende Forschung zu Eprosartan STARLET Stress am Arbeitsplatz Langzeitstudie mit Eprosartan im Vergleich zur Standardtherapie Deutschland; ca. 2.500 Patienten CV-Morbidität/Mortalität bei stressinduzierter Hypertonie Dauer: 5 Jahre (Ende 2004) Dezember 2003 53 Laufende Forschung zu Eprosartan OSCAR Untersuchung der Wirkung auf Blutdruck und kognitive Funktionen unter Praxisbedingungen Ziel: 100.000 Patienten weltweit Therapiedauer 6 Monate Start Ende 2003 Dezember 2003 54 Möglich Vorteile von Teveten Dual: RAAS + Sympathikus Chemische Struktur Dezember 2003 Systolischer BD Schlaganfall Untersuchungen laufen 55 Vielen Dank für Ihre Aufmerksamkeit