Vorlesung 20.07.00
Werbung

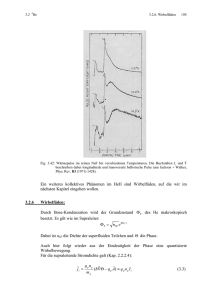
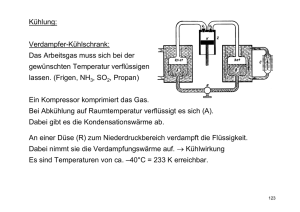
5.1.5 3He/4He Mischungskühlung 214 5.1 Kühltechniken 5.1.3 Joule-Thomson Kühler Fig. 5.13 zeigt das Prinzip des Joule-Thomson-Effekts. Dabei strömt ein Arbeitsgas mit hohem Druck durch einen porösen Stopfen oder eine Drossel und entspannt sich. Fig. 5.13: Joule Thomson Effekt Ändert das Gas dabei seine Temperatur, so spricht man vom Joule-Thomson-Effekt. Wir betrachten die Arbeitsbilanz. Während links ein Volumen V1 im Stopfen verschwindet, entsteht neu auf der rechten Seite das Volumen V2. Da die Drücke p1 und p2 konstant gehalten werden, gilt links: 0 0 W1 = − pdV = − p1 dV = + p1V1 V1 da p = p1 = const. V1 und entsprechend rechts V2 W2 = pdV = p2V2 0 Nach dem 1. Hauptsatz ist zudem: ∆U = ∆Q − ∆W Da keine Wärme zu- oder abgeführt wird, ist ∆Q=0, (adiabatisch), so dass gilt: U 2 − U 1 = W1 − W2 = p1V1 − p2V2 bzw. U 2 + p 2V2 = U 1 + p1V1 D.h. die Enthalpie H ≡ U + pV bleibt beim Durchtritt durch den Stopfen ungeändert. Dies gilt generell für alle Gase. Nehmen wir zunächst an, das Arbeitsgas sei ein ideales Gas, d.h. die Teilchen wechselwirken nicht miteinander. Dann enthält die innere Energie U nur die kinetische Energie der Teilchen, und diese hängt nur von der Temperatur, aber nicht von der Gasdichte bzw. dem Druck ab. Wegen pV=NkT hängt auch das Produkt pV nur von der Temperatur ab, nicht aber vom Druck. Insgesamt ist also auch H nur von T abhängig. Da sich H nicht ändert (s.o.) kann sich also auch T nicht geändert haben. Ideale Gase zeigen also keinen Joule-Thomson-Effekt. Wie verhält sich nun ein reales Gas? Betrachten wir dazu das pT-Diagramm für Stickstoff (Fig. 5.14). In dieses sind die Isenthalpen eingezeichnet. Dies sind die Kurven mit konstanter Enthalpie H, auf denen sich das Gas beim Durchgang durch den Stopfen bewegt. Sie sind für ideale Gase horizontale Geraden, da die Temperatur 5.1 Kühltechniken 5.1.5 3He/4He Mischungskühlung 215 Fig. 5.14: pT-Diagramm für Stickstoff bzw. Helium(aus: Kent) konstant ist. Für ein reales Gas sind sie stark gebogen und durchlaufen ein Maximum. Dieses Verhalten kann mit dem in Fig. 5.15 dargestellten interatomaren Potenzial erklärt werden. Bei hohen Drücken ist der mittlere Abstand der Teilchen klein, so dass sie sich häufig im stark abstoßenden Bereich des Potenzials befinden. Bei Expansion laufen sie also bergab und werden beschleunigt, so dass ihre kinetische Energie und damit die Temperatur zunimmt. Entsprechend steigt die Isenthalpe bei abnehmendem Druck zu höherer Temperatur an. Bei niedrigeren Drücken halten sich die Teilchen dagegen bevorzugt im anziehenden Bereich des Potenzials auf. Dort werden sie bei Expansion verzögert. Also abgekühlt. Entsprechend sinkt die Isenthalpe wieder ab. Das Maximum der Isenthalpe ist die Grenze zwischen Erwärmung und Abkühlung und heißt daher Inversionsdruck. Die Verbindungslinie aller Maxima heißt Inversionskurve. Sie ist in fig. 5.14 gestrichelt eingezeichnet und umfaßt das schraffierte Gebiet, in dem Abkühlung auftritt. Die höchste Temperatur, bei der gerade noch bei p=0 Abkühlung auftritt, heißt Inversionstemperatur. Es dürfen also nicht zu hohe Anfangs-Temperaturen und -Drücke verwendet werden. Für Luft (N2,O2) liegt die Inversionstemperatur höher als die Zimmertemperatur, so dass deren Verflüssigung mit Hilfe des Joule-Thomson-Effekts möglich ist. Dies wird im Linde-Verfahren angewendet, siehe Fig. 5.16. Hier strömt das Gas erst durch einen Gegenstromkühler und dann durch die Drossel, so dass das expandierte kalte Gas das einströmende warme Gas vorkühlen kann. Dabei wird das Gas laufend kälter, bis Flüssigkeit von der Düse tropft. 5.1.5 3He/4He Mischungskühlung 216 5.1 Kühltechniken Fig. 5.15: Interatomares Potenzial im realen Gas Fig. 5.16: Linde-Verfahren zu Verflüssigung von Luft. 5.1.4 Verdampfungskühler Wenn wir die Windrichtung feststellen wollen, können wir einen Finger anfeuchten und hochstrecken. Die angeströmte Seite wird kalt, da hier die Feuchtigkeit verdunstet. Die Abkühlung kommt daher, dass beim Übergang der Teilchen in die Gasphase Arbeit gegen die Bindungskräfte zu den Nachbarn in der Flüssigkeit geleistet werden muß, siehe Fig. 5.17. Fig. 5.17: Prinzip der Verdunstung In Fig. 5.18 ist das entsprechende Potenzial dargestellt. Die Bindungsenergie wirkt als Potenzialschwelle zwischen Flüssigkeit und Gas. Bei endlicher Temperatur haben die Teilchen in der Flüssigkeit eine Boltzmann-Verteilung, in der sich stets auch 5.1.5 3He/4He Mischungskühlung 217 5.1 Kühltechniken Teilchen mit genügend hoher Energie befinden, so dass sie die Schwelle überwinden und verdampfen können. Dabei ändert sich die Exponent der Verteilung nicht. Die verdampften Teilchen haben also die Temperatur der Flüssigkeit. Jedoch gehen der Flüssigkeit ständig die schnellsten Teilchen verloren, so dass sich deren Boltzmannverteilung abkühlt. Dies erklärt die Verdampfungskühlung. Läßt man eine Flüssigkeit unter vermindertem Druck verdampfen (durch Abpumpen), so kühlt sie sich laufend ab. Diese Abkühlung erreicht aber eine Grenze, wenn kBT<<EBindung wird, weil dann nur noch exponentiell wenige Teilchen die Potenzialschwelle überwinden können. Für 4He liegt diese Grenze bei ca. 1K, bei 3 He bei 0,3K. Noch tiefere Temperaturen können durch sog. Mischkühler erreicht werden. Fig. 5.18: Potenzialverlauf in der Flüssigkeit bzw. im Gas 3.1.5 3 He/4He Mischungskühlung: Zunächst betrachten wir nochmals das Phasendiagramm der 3He/4He-Mischungen (Fig. 5.19), das in Kap. 3.4 besprochen wurde. Bei Temperaturen unter 0,87K entmischen sich die Isotope. Bei T≈0 ist die 3He-Phase praktisch zu 100% konzentriet, während die 4He Phase im Gleichgewicht noch 6,4% 3He enthält. Dieses bildet (siehe Kap. 3.4) ein entartetes Fermigas mit sehr niedriger Fermi-Temperatur. Fig. 5.19: Phasendiagramm 5.1 Kühltechniken 5.1.5 3He/4He Mischungskühlung 218 Die Wärmekapazität je Teilchen des Fermigases ist 1 π 2 k BT / TF (s. Kittel). Da die 2 Fermitemperatur TF des 3He im 4He viel niedriger ist als im konzentrierten 3He, ist die Wärmekapazität je Atom entsprechend höher. Treten also 3He-Atome von der konzentrierten in die verdünnte Phase über, so können sie dort sehr viel mehr Wärme aufnehmen. Wird jedoch keine Wärme von außen zugeführt, so kühlen sich die 3HeAtome ab. Dies ist das Kühlprinzip des 3He-4He-Mischungskühlers. Um ständig 3He-Atome vom 3He ins 4He übertreten zu lassen, ist ein kontinuierlicher Kreislauf gemäß Fig. 5.20 nötig. Fig. 5.20: 3He-4He-Entmischungskühler (aus: Mc Clintiock). Von oben strömt flüssiges 3He aus einem 1K Wärmebad durch eine sogenannte Destillationskammer nach unten. In dieser wird es auf 0,7K gekühlt. Das 3He fließt weiter über einen Wärmetauscher in die Mischkammer (mixing chamber). Diese enthält die beiden Phasen: 3He reich (concentrated phase) und 4He-reich (dilute phase). Dazwischen liegt die Phasengrenze. Damit das 3He ständig durch diese hindurchtritt, muß auf der 4He-Seite die 3He-Konzentration unter den Gleichgewichtswert abgesenkt werden. Dies entspricht genau dem „Abpumpen“ des Gases bei der Verdampfungskühlung, siehe 5.1.4. Die „Abpumpen“ des 3He im 4He erfolgt über ein zweites Rohr, das über den Wärmetauscher zur Destillationskammer führt. Diese befindet sich auf 0,7K, so dass das 3He bereits verdampfen kann und durch ein Pumprohr abdestilliert wird, während das 4He bei dieser Temperatur praktisch noch nicht verdampft. Durch die Destillation wird die 3He-Konzentration in der oberen Kammer sehr niedrig gehalten, so dass das 3He im Konzentrationsgradienten kontinuierlich von unten nach oben fließt und so die Lösung von immer neuem 3He im 4He ermöglicht. So ergibt sich eine kontinuierliche Abkühlung bis auf Temperaturen von ca. 10mK. Der Rekord liegt bei ca. 2mK. Für noch tiefere Temperaturen nutzt man die magnetischen Kernmomente. Auf dieses Prinzip wollen wir im nächsten Kapitel eingehen. 5.1 Kühltechniken 5.1.6 5.1.6 Kühlung durch magnetische Zentren 219 Kühlung durch magnetische Zentren: Lokalisierte magnetische Momente im Festkörper können zur Kühlung verwendet werden. Dabei kann es sich entweder um Momente der Elektronenhülle (paramagnetische Salze) oder des Kerns (z.B. Cu-Metall) handeln. Zunächst beschreiben wir den Kühleffekt allgemein. Im äußeren Magnetfeld bildet der Gesamtdrehimpuls J eines magnetischen Zentrums bekanntlich Eigenzustände zu festem Jz mit den Energieabständen: ∆E = γDB Die Niveauabstände sind also durch das Magnetfeld abstimmbar. In kleinen Feldern, entsprechend ∆E<<kT sind alle Niveaus gleichmäßig bevölkert, in großen Feldern mit ∆E>>kT nur das unterste. Damit läßt sich eine Kühlvorrichtung aufbauen, die in Fig. 5.21 schematisch dargestellt ist. Fig. 5.21 Kühlvorrichtung Die Probe befindet sich thermisch isoliert im Vakuum in einem supraleitenden Magneten. Sie ist über einen „Wärmeschalter“ mit einem Wärmebad verbunden. Der Wärmeschalter ist meist ein Al-Draht, der durch eine kleine Magnetspule normalleitend geschaltet wird und dann hohe Wärmeleitfähigkeit besitzt, während er im supraleitenden Zustand bei tiefer Temperatur die Wärme sehr schlecht leitet. Anfangs ist der Wärmeschalter geschlossen. Dann ist die Probe bei der Temperatur T0. Nun wird der SL Magnet hochgefahren, bis ∆E>>kBT0 ist. Dabei entvölkern sich alle höheren Niveaus. Sie geben ihre Energie entweder ans Gitter (Salze) oder an die Leitungselektronen (Metalle) ab. Über den Wärmeschalter fließt die Energie ins Wärmebad. Nach einiger Zeit sind alle magnetischen Zentren im Grundzustand. Dann wird der Wärmeschalter geöffnet, und das Magnetfeld der Probe langsam wieder abgesenkt. Dies kann Stunden bzw. Tage dauern, denn die Zentren müssen stets mit der Probe im Gleichgewicht bleiben, um irreversible Prozesse zu vermeiden. Durch die Absenkung des Magnetfeldes kommt die Probe in den Bereich ∆E≈kBT, so dass die höheren Niveaus langsam wieder bevölkert werden und dabei Energie aufnehmen. Die Energie wird jetzt wieder dem Gitter bzw. den Leitungselektronen entzogen. Dadurch kühlt die Probe ab. Soll bei konstanter Temperatur eine Messung vorgenommen werden, wird das Magnetfeld so lange angehalten. Bei B=0 ist die tiefste Temperatur erreicht. Im Prinzip müßten sich auf diese Weise beliebig tiefe Temperaturen erreiche lassen. Eine Grenze wird aber durch die Wechselwirkung der magnetischen Zentren 5.1 Kühltechniken 5.1.6 Kühlung durch magnetische Zentren 220 untereinander gesetzt. Diese richtet ihrerseits die magnetischen Momente aus und verhindert so, dass sich diese in schwachen Magnetfeldern (entsprechend kleinen Temperaturen) noch nach den äußeren Feldern ausrichten können. Diese Grenze liegt für magnetische Salze (z.B. Cer-magnesium-Nitrat, CMN) bei ca. 10mK. Da dieser Temperaturbereich heutzutage durch Mischkühler leichter erreichbar ist, werden die Salze nicht mehr verwendet. Weit tiefere Temperaturen kann man jedoch durch Verwendung von Kernspins erreichen. Diese haben viel kleinere Momente, so dass sie nur bei sehr tiefen Temperaturen (<10mK) verwendet werden können. Da aber die Wechselwirkung der Kernspins untereinander ebenfalls verschwindend gering ist, können damit Temperaturen bis herab zu ca. 50µK erreicht werden. Dies sind die tiefsten bisher erreichten Gittertemperaturen in Festkörpern. Fig. 5.22 zeigt eine detailliertere Skizze eines 1-stufigen Kernentmagnetisierungskühlers in üblicher Bauform. Fig. 5.22: Einstufige Kernspinentmagnetisierungsmaschine