EINFÜHRUNG IN DIE ISOTOPENGEOCHEMIE
Werbung

E INFÜHRUNG IN DIE I SOTOPENGEOCHEMIE
basierend auf Vorlesungen am
Mineralogisch-Petrographischen Institut
der Universität zu Köln
zwischen 1988 und 1994
überarbeitet und ergänzt ab Winter 1999
HEINZ-GÜNTER STOSCH
Pt S
m
U
Lu
Re
La
Rb
La
K
La
Pb
Os
Ce
Nd
He
Ca
K
Hf
P
Ar b
Pb r Ba
S
He
U
Th
Institut für Mineralogie und Geochemie
Universität Karlsruhe
Manuskript bitte nur zum eigenen Gebrauch verwenden! – Alle Rechte vorenthalten.
Dieses Skript ist bei einer Serie von Vorlesungen im Fach Mineralogie entstanden. Daraus ergibt sich, daß es sich weitgehend mit
der Isotopengeochemie von magmatischen Gesteinen, untergeordnet von Sedimenten und Metamorphiten beschäftigt. Große
Teile der Anwendungen der stabilen Isotope in den Umweltwissenschaften, der Paläobiologie, der Klimatologie werden Sie dagegen hier vergeblich suchen, und ich bitte um Nachsicht für dieses Versäumnis. Ich erhebe weder Anspruch auf Vollständigkeit
noch Aktualität oder Richtigkeit. Meine beschränkte Zeit wird es mir nur hin und wieder gestatten, das Skript zu aktualisieren,
und auch dies nur in jeweils kleinen Bereichen, da diese Art der Isotopengeochemie bei den Karlsruher Studierenden keinen Anklang findet.
Wenn Sie sachliche Fehler oder auch Druckfehler und sprachliche Unzulänglichkeiten feststellen, oder falls Ihnen sonstige
beklagenswerte Zustände aufstoßen, teilen Sie mir dies bitte mit!
Dank an: die aktiveren der Hörer/innen der damaligen Vorlesungen, namentlich D. Bosbach, U. Fleischer und G. Lorenz sowie an
Herrn Kollegen W. Heinrich/Potsdam für Lob, Tadel und Hinweise, welche letztlich den Ausschlag für die Überarbeitung im Winter
1999 gaben. Dank weiterhin an Z. Berner vom IMG/Karlsruhe für diverse Diskussionen. Besonderer Dank gebührt Herrn R.L.
Romer/Potsdam für Hinweise auf Fehler und für seine zahlreichen Verbesserungsvorschläge.
letztmals geändert am 5.1.2004
Inhaltsverzeichnis
Seite
Bücher zur Isotopengeochemie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 1
Einführung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Einleitung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Geschichtliches . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Radioaktives Zerfallsgesetz . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Der Ursprung der Elemente . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9
Massenspektrometrie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23
Isotopenverdünnungsanalyse . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27
Datierungsmethoden – allgemeine Bemerkungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 30
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden) . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 31
Die K–Ar-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 32
Die 40Ar/39Ar-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 37
Das Rb–Sr-Isotopensystem . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 42
Das Rb–Sr-System als Mittel der Altersbestimmung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 43
Das Rb–Sr-System als Tracer . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 49
Die Sr-Isotopenentwicklung der Meteorite und des Erdmantels . . . . . . . . . . . . . . . . . 49
Die Sr-Isotopenentwicklung der Ozeane . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 51
Das Sm–Nd-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 53
Allgemeines . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 53
Sm–Nd – Anwendung zur Datierung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 58
Nd-Isotope als Tracer und die Korrelation zwischen Sr- und Nd-Isotopen . . . . . . . . . . . . . . 61
Modellalter. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 62
Zweikomponentenmischungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 67
Die Massenfraktionierung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 75
Das Lu–Hf-Isotopensystem . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 83
Die Hf-Isotopensignatur des subozeanischen oberen Erdmantels . . . . . . . . . . . . . . . . . . . . 87
Die Hf-Isotopenentwicklung der Erde . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 88
Hinweise von den Hf-Isotopen auf das Ausmaß des globalen Recycling . . . . . . . . . . . . . . . 89
Das La–Ce-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 92
Das K–Ca-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 94
Die Re–Os-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 96
Die U,Th–Pb-Methoden . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 105
Die U–Pb- und Th–Pb-Isochronenmethoden . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 107
Konkordia und Diskordia . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 109
Die Pb–Pb-Methoden („gewöhnliches Blei“ oder „common lead“) . . . . . . . . . . . . . . . . . . 120
Die Fission-Track-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 133
Die Ungleichgewichtsmethoden . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 139
Geschichtliche Anmerkungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 140
Die 210Pb-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 141
Die Ionium-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 143
Die 234U/238U-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 146
Die 230Th/234U- und 234U/238U-Methoden . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 148
238
U–230Th-Ungleichgewichte in Vulkaniten . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 152
I
Inhaltsverzeichnis
Seite
Kosmogene Radionuklide . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 158
Die 14C-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 159
Das 10Be . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 161
Kosmogene Radionuklide in der Kosmochemie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 167
Die Beschleuniger-Massenspektrometrie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 172
Edelgase und abgeklungene Radionuklide . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 173
3He/4He . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 173
Xenon . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 182
Hf-W-Chronometer . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 186
Stabile Isotope • Allgemeines . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 193
Wasserstoff und Sauerstoff. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 204
Sauerstoff und Wasserstoff in Hydro- und Atmosphäre . . . . . . . . . . . . . . . . . . . . . . . . . . . 205
Sauerstoff und Wasserstoff in der Lithosphäre . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 211
Kohlenstoff . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 228
Stickstoff . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 234
Schwefel . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 236
Calcium . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 243
Eisen und andere schwere Elemente . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 245
Literaturzitate . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 250
II
Einführung in die Isotopengeochemie
1.0
Bücher zur Isotopengeochemie
A. Basu & S. Hart [Herausgeber] (1996) Earth Processes – Reading the Isotopic Clock
Geophysical Monograph 95 , American Geophysical Union, Washington,
437 Seiten, 65 US-$
zusammenhanglose Einzelartikel von Fachautoren, von Prozessen in der frühesten
[Zeit der Erde bis hin zur industriellen Pb-Verschmutzung reichend]
D.J. DePaolo: Nd Isotope Geochemistry
Springer-Verlag, Berlin 1988, 187 Seiten, vergriffen
[spezielle Abhandlung eines des Sm–Nd-Isotopensystems]
Dickin, A.P.: Radiogenic Isotope Geology
Cambridge University Press, Cambridge 1997, 490 Seiten, Paperback-Ausgabe ca.
35 £
[für die radiogenen Isotope ähnlich umfassend wie das „klassische“ Buch von Faure, aber im Gegensatz zu jenem stärker auf die Traceranwendungen in Petrologie/
Geochemie und Kosmochemie ausgerichtet]
Faure, G.: Principles of Isotope Geology
2nd Edition, John Wiley & Sons, New York 1986 (608 Seiten), ca. 95 US-$
[umfassende Übersicht über radiogene und stabile Isotope]
Faure, G: Origin of Igneous Rocks: The Isotopic Evidence
Springer Verlag, New York 2001 (512 Seiten), 75 €
[Darstellung der Entstehung von Magmatiten aus dem Blickwinkel der Isotopengeochemie]
Geyh, M.A.: Einführung in die Methoden der physikalischen und chemischen Altersbestimmung
Wissenschaftliche Buchgesellschaft, Darmstadt 1980 (276 Seiten), vergriffen
[ z.T. nur stichwortartige Übersicht]
Heaman, L. & Ludden, J.N. (Herausgeber): Applications of Radiogenic Isotope Systems to Problems in Geology
Mineral. Assoc. Canada, Short Course Handbook 19, 25Can.$
[Spezielle Darstellung verschiedener Aspekte der Isotopengeochemie in Einzeldarstellungen]
Hoefs, J.: Stable Isotope Geochemistry
2nd Edition, Springer-Verlag, Heidelberg 1997 (201 Seiten), 45 €
[umfassende Darstellung der Geochemie stabiler Isotope]
Jäger, E. & Hunziker, J.C. (Herausgeber): Lectures in Isotope Geology
Springer-Verlag, Heidelberg 1979 (329 Seiten), vergriffen
[Übersicht über die Methoden und Probleme der Isotopengeochemie an Hand von
Einzeldarstellungen]
1
Bücher zur Isotopengeochemie
Kyser T.K. (Herausgeber): Short Course in Stable Isotope Geochemistry of low temperature fluids
Mineralogical Association of Canada (Short Course Vol. 13) 1987, (452 Seiten)
[sehr spezielles Werk mit Einzelkapiteln von Fachautoren]
Valley, J.W., Taylor & Cole, D.R. (Herausgeber): Stable Isotope Geochemistry
Reviews in Mineralogy Vol. 43, Mineralogical Society of America 2001 (662 Seiten), 32 US-$
[Geochemie stabiler Isotope in Einzeldarstellungen, von der Petrologie bis zur organischen Geochemie reichend]
Valley, J.W., Taylor, H.P. Jr. & O'Neil, J.R. (Herausgeber): Stable Isotopes in High Temperature Geological Processes
Reviews in Mineralogy Vol. 16, Mineralogical Society of America 1986 (570 Seiten), 24 US-$
[umfassende, aber sehr spezielle Übersicht über die Fraktionierung stabiler Isotope
bei magmatischen und metamorphen Prozessen]
Wagner, G.A. & Van den Haute, P.: Fission-Track Dating
Ferdinand Enke Verlag, Stuttgart, 1992 (285 Seiten), ca. 150DM
[umfassende Darstellung der Spaltspurenmethode]
Wendt, I.: Radiometrische Methoden in der Geochronologie
2. Auflage, Clausthaler Tektonische Hefte 23,
Clausthal-Zellerfeld 1986 (70 Seiten); 24 DM
[nicht sehr befriedigende Abhandlung der Methoden der Altersbestimmung]
2
A. Radiogene Isotopensysteme
2.0
Einführung
2.1
Einleitung
Jeder Atomkern eines chemischen Elementes hat die gleiche Ordnungszahl Z – bedingt
durch die Zahl der Protonen. Verschiedene Kernarten desselben Elementes unterscheiden
sich in der Anzahl der Neutronen N und damit in der Massenzahl A = Z + N. Solche verschiedenen Kerne eines Elementes bezeichnet man als Isotope. Kernarten ohne Beziehung
zu einem Element werden Nuklide genannt, von denen 264 stabil sind. Isobare sind
Nuklide mit identischer Massenzahl und gehören damit also verschiedenen Elementen an.
Unter den Elementen gibt es 20, die nur aus einem einzigen stabilen Isotop zusammengesetzt sind, die sogenannten Reinelemente [Be, F, Na, Al, P, Sc, Mn, Co, As, Y, Nb, Rh, I, Cs,
Pr, Tb, Ho, Tm, Au, Bi]. Alle übrigen stabilen Elemente sind aus mindestens 2 in der Natur
vorkommenden Isotopen aufgebaut, den Rekord hält Sn mit 10 stabilen Isotopen.
In der Isotopengeochemie betrachtet und mißt man natürliche Variationen in der Isotopenzusammensetzung einiger Elemente und versucht, daraus Schlüsse abzuleiten. Die Reinelemente können daher nicht Gegenstand der Untersuchung sein. Isotopenvariationen
können auf zweierlei Weise zustande kommen:
a) durch Fraktionierung bei physikalisch-chemischen oder biochemischen Prozessen.
Große Effekte zeigen dabei vor allem die leichteren und flüchtigen Elemente H, C, N, O, S,
Se, Li, B, Mg, Si und auch Ca, dessen zwei häufigste Isotope mit 40 und 44 einen sehr großen Massenunterschied aufweisen). Wasserstoff z.B. besteht aus den stabilen Isotopen 1H
und 2H (D), Sauerstoff aus 16O, 17O und 18O. Bei der Verdampfung von H2O gehen die leichten Isotope beider Elemente etwas bevorzugt in die Gasphase (Atmosphäre). Bei der Photosynthese nehmen die grünen Pflanzen das leichtest flüchtige der Kohlenstoffisotope, 12C,
bevorzugt aus dem Luft-CO2 auf. Fortschritte in der Meßtechnik führen dazu, daß bei
immer mehr Elementen natürliche Isotopenvariationen gefunden werden, z.B. auch bei Fe.
Beschreibung und Anwendung dieser Effekte ist der Gegenstand der Geochemie stabiler
Isotope.
b) Bei einigen der Elemente, die aus mehr als einem natürlich vorkommenden Isotop
bestehen, unterliegt eines der Isotope dem radioaktiven Zerfall direkt oder über eine Kette
von instabilen Produkten in einen anderen stabilen Kern, bei dem es sich immer um ein
Isotop eines anderen Elementes handelt. In der Nuklearchemie bezeichnet man das radioaktive Ausgangsnuklid meist als Mutternuklid (kurz „Mutter“), das Zerfallsprodukt als
Tochternuklid (kurz „Tochter“). Betroffen von diesem Zerfallsprozeß sind also immer mindestens 2 Elemente. Beim a-Zerfall wird ein He-Kern emittiert; dadurch sinkt die Massenzahl um 4 Einheiten, die Zahl der Protonen um 2. Beim b–-Zerfall zerfällt ein Neutron im
Atomkern in ein Proton, ein Elektron und ein Antineutrino; die Massenzahl ändert sich
dabei nicht, die Ordnungszahl erhöht sich um 1. Beim b+-Zerfall wandelt sich ein Proton
unter Emission eines Positrons und eines Neutrinos in ein Neutron um; es entsteht also ein
Element mit einer um 1 verringerten Ordnungszahl. Beim K-Einfang wird ein Elektron aus
der K-Schale durch den Kern eingefangen; durch seine Reaktion mit einem Proton wird ein
Neutron gebildet, und die Ordnungszahl sinkt um 1. Bei der Spontanspaltung schließlich
zerfällt ein schwerer Kern in zwei ungleich große Bruchstücke unter Emission einiger Neutronen. Da magmatische, metamorphe und selbst sedimentäre Vorgänge immer auch eine
chemische Fraktionierung zur Folge haben, findet man in der Natur eine mehr oder weniger große Variation der Verhältnisse des Tochterelementes zum Mutterelement einer radioaktiven Zerfallskette. Das wiederum führt über geologische Zeiträume zu einer meßbaren
3
Einführung
Variation in der Isotopenzusammensetzung des Tochterelementes. Diese Effekte sind
Untersuchungsgegenstand der Geochemie radiogener Isotope. Isotopenverhältnisse dienen einerseits zur Altersbestimmung, andererseits als Tracer zur Aufklärung petrogenetischer Prozesse.
Isotope
a-aktive Nuklide
b-
158 24.87
157
Tb
15.68 158.92
156 20.47
155 14.73
2.15
154 22.71
52.18
153
152 26.72
0.200
151
47.82 Gd
150 5.62
149
11.24
147
14.97
3.09
143 12.17
Sm
140 88.48
139
27.11
100
Nd
Pr
144.24
157.25
Isobare
Pm
144 23.85
142 11.07
Eu
13.83 151.96
148 5.73
146 17.22
145 11.30
141
7.44
150.35
140.91
99.91
Die Zahlen in den Boxen geben die
prozentuale Häufigkeit des Isotops an
der Zusammensetzung des jeweiligen
Elementes an. Die Zahlen auf der linken
Seite neben den Boxen stellen die
Massenzahlen dar. Die Zahlen unter
den Elementsymbolen geben das
Molekulargewicht des Elements an.
Isotope
b+
¬ 138La ® 138Ce
Massenzahl
138Ba
Ausschnitt aus der
Nuklidkarte
160 21.90
100
159
a
c
b
Isobare
138 71.66 0.089 0.250
Protonenzahl
137 11.32
136 7.81
La
0.193
a b--Zerfall
b b+-Zerfall, K-Einfang
c a-Zerfall
135 6.59 138.91
Ce
134 2.42
140.12
Ba
137.34
ABBILDUNG 1
4
Ausschnitt aus der Nuklidkarte
A. Radiogene Isotopensysteme
2.2
Geschichtliches
Im Jahr 1896 berichtete der Franzose Henri Becquerel* der Akademie der Wissenschaften zu
Paris über seine Versuche mit U-Salzen, von denen er fand, daß sie eine Strahlung aussenden, die Gase beim Durchtritt ionisiert – genauso wie die kurz zuvor entdeckten Röntgenstrahlen. Davon inspiriert, begannen unmittelbar darauf Marie Curie und ihr Ehemann
Pierre† auch andere Elemente und ihre Salze auf mögliche Eigenstrahlung zu untersuchen.
Marie Curies Bemühungen führten zu der Entdeckung, daß auch Th eine durchdringende
Strahlung aussendet. Außerdem beobachtete sie, daß die natürlich vorkommenden Minerale und Erze von U und Th eine noch wesentlich stärkere Strahlung aussenden. Bei der
Aufarbeitung von Pechblenden aus den Vorkommen von Joachimsthal im Erzgebirge
gelang es den Curies, zwei neue stark strahlende Elemente zu isolieren, die sie Radium und
Polonium nannten. Für die Entdeckung der Radioaktivität durften sich die Curies mit Becquerel den Physik-Nobelpreis des Jahres 1903 teilen.
1899 gelang es Ernest Rutherford‡, die radioaktive Strahlung in drei Komponenten aufzuschlüsseln, die er Alpha, Beta und Gamma nannte. Die a-Strahlen ließen sich schon durch
ein Blatt Papier absorbieren, die b-Strahlen durch eine dünne Metallfolie, die g-Komponente dagegen nur durch dicke Platten von Schwermetallen. Später wurde erkannt, daß die
a-Strahlen aus He-Kernen bestehen, die b-Strahlen Elektronen sind und nur die g-Komponente elektromagnetische Strahlung ist, welche die Eigenschaft der Röntgenstrahlen aufweist, fast immer aber wesentlich energiereicher ist. Rutherford war es auch, der mit seinen
berühmten Streuexperimenten von a-Partikeln an Metallfolien Anfang des 20. Jahrhunderts nachwies, daß die Atome einen sehr kleinen positiv geladenen Kern haben und von
einer Hülle von negativ geladenen Elektronen umgeben sind.
2.3
Radioaktives Zerfallsgesetz
Grundlage der Geochemie radiogener Isotope ist das radioaktive Zerfallsgesetz, das 1903
von Frederick Soddy¶ und Rutherford aufgestellt wurde. Die beiden schlugen vor, daß die
Atome eines radioaktiven Kerns spontan unter Aussendung von Strahlung zerfallen. Nach
ihrer Vorstellung ist der Zerfall begleitet von der Aussendung von a- und b-Partikeln, und
die Intensität der Strahlung ist proportional zur Anzahl der vorhandenen radioaktiven
Atome. Das faßten sie mathematisch in die Gleichung:
-dN/dt = lN
[GL 1]
Darin ist N die Zahl der radioaktiven Atome und l die sogenannte Zerfallskonstante, welche die Wahrscheinlichkeit beschreibt, daß ein Atom pro Zeiteinheit zerfällt. Diese Gleichung läßt sich umformen und integrieren zu:
-ò
dN
= l ò dt
N
oder -ln N = lt + C
[GL 2]
[GL 3]
* 1852–1908; Nobelpreis für Physik 1903 (eine Hälfte); die andere Hälfte ging an Pierre und Marie
Curie.
† Pierre Curie (1859–1906), französischer Physiker, und Marie Curie (1867–1934), polnisch–französische Chemikerin und Physikerin; für die Entdeckung von Radium und Polonium erhielt M. Curie
einen zweiten Nobelpreis (in Chemie) im Jahr 1911.
‡ neuseeländisch–englischer Physiker (1871–1937), der „Vater der Kernphysik“, 1908 Nobelpreis für
Chemie. Rutherford entwickelte ein einfaches Atommodell, das später von Niels Bohr wesentlich
verbessert wurde.
¶ englischer Physiker (1877–1956), Nobelpreis für Chemie 1921; Soddy formulierte um 1913 das
Konzept der Isotope und zeigte, daß beim a-Zerfall ein Element mit einer um 2 verminderten Kernladungszahl entsteht.
5
Einführung
Die Integrationskonstante C läßt sich aus der trivialen Bedingung bestimmen, daß zur Zeit
t = 0 eine ursprüngliche Zahl von radioaktiven Atomen No vorgelegen haben muß, d.h.
C = -ln No
[GL 4]
-ln N = lt - ln No
[GL 5]
Dies, in GL 3 eingesetzt, ergibt:
ln N - ln No = -lt
ln(N/No) = -lt
N/No = e-lt
bzw. N = No ´ e-lt
[GL 6]
In dieser Zerfallsgleichung stehen 2 Unbekannte, nämlich No und t. Man kann No jedoch
eliminieren, wenn man die Anzahl der durch den Zerfallsprozeß entstehenden Tochternuklide D berücksichtigt, da
No = N + D
[GL 7]
ist. In GL 6 eingesetzt, ergibt sich damit:
N = (N + D) ´ e-lt
N ´ elt = N + D
D = N ´ (elt - 1)
[GL 8]
Hierin ist N die Anzahl der Atome des radioaktiven Mutternuklids, die nach einer beliebigen Zeit t von einer ursprünglich vorhandenen Anzahl No noch übrig geblieben ist. Das ist
die grundlegende Gleichung, um Altersbestimmungen durchführen zu können, denn –
zumindest prinzipiell – sind sowohl die Zahl der Tochternuklide als auch die Zahl der noch
nicht zerfallenen radioaktiven Mutternuklide bestimmbar. Voraussetzung ist jedoch einerseits, daß sich der Zerfall in einem geschlossenen System vollzieht, d.h. die gesamte Menge
von Mutter- und Tochternuklid bleibt im betrachteten Gestein oder Mineral seit ihrer Bildung eingeschlossen. Die zweite Voraussetzung ist, daß l für jedes radioaktive Nuklid eine
Naturkonstante ist. Nach allem, was man weiß, ist das tatsächlich der Fall. Lediglich die
Zerfallskonstante des K-Einfangs läßt sich in Einzelfällen geringfügig durch extreme
Drücke erhöhen. Das mag nach einer Theorie von M. Dirac auch für die anderen Zerfallsprozesse im Innern von Sternen gelten. Datierungen an Meteoriten mit verschiedenen
Methoden (U–Pb, Sm–Nd, Rb–Sr, Lu–Hf) haben für das Alter unseres Sonnensystems aber
Werte von 4.55 Ga ergeben und legen damit die Konstanz von l nahe.
Anstatt mit der Zerfallskonstanten l rechnet man in der Isotopengeochemie häufig mit der
Halbwertszeit T. Das ist die Zeit, nach welcher von einer ursprünglich vorhandenen Zahl
von radioaktiven Nukliden No genau die Hälfte zerfallen ist, also
N = 1/2 No
1
/2 No = No ´ e-lT
ln(1/2) = -lT
ln 2 =lT
T = ln 2/l
[GL 9]
So sind z.B. über den Verlauf der Erdgeschichte (ca. 4.55 Ga) bis heute rund die Hälfte der
ursprünglich vorhandenen 238U-Atome (Halbwertszeit ca. 1 Erdalter), aber fast 99% der
235
U-Atome (Halbwertszeit ca. 700Ma) zerfallen (siehe Abbildung 2).
6
A. Radiogene Isotopensysteme
Nachdem um die 1900 das Phänomen der Radioaktivität bekannt war, erkannte man auch
rasch die potentielle Bedeutung für die Geologie, insbesondere die Frage nach dem Alter
der Erde. Der bekannteste Physiker Englands im letzten Drittel des 19. Jahrhunderts, William Thomson* – besser bekannt unter seinem späteren Namen Lord Kelvin, berechnete die
Abkühlungsgeschwindigkeit der Erde unter der Voraussetzung, sie sei einmal geschmolzen
gewesen. In einem berühmten Vortrag 1897 setzte Lord Kelvin das Alter der Erde mit zwischen 20 und 40 Ma an – eine Ansicht, die wegen seiner großen Autorität einen erheblichen Einfluß auf das Denken der damaligen Zeit ausübte. Einer Reihe von Geologen war
dabei jedoch unwohl, da aus der Stratigraphie unter Anwendung des aktualistischen Prinzips – Konstanz der Sedimentationsraten durch die geologische Geschichte hindurch – ein
wesentlich höheres Alter seit dem Beginn des Kambriums abgeschätzt worden war.
Mit Entdeckung der natürlichen Radioaktivität erkannten Physiker und Chemiker rasch,
daß der radioaktive Zerfall ein exothermer Prozeß ist. 1904 war es Rutherford klar, daß der
radioaktive Zerfall eine große Rolle für die Wärmeproduktion der Erde spielte und daß
damit die Erde auf eine weit längere Abkühlungsgeschichte zurückblicken könnte als von
Lord Kelvin berechnet. Darüber hinaus erkannte Rutherford auch, daß der radioaktive Zerfall des Urans die Möglichkeit bietet, U-Minerale zu datieren. Er versuchte das, indem er die
Menge an He maß, die in U-Minerale eingeschlossen ist.
1.0
Relative Abnahme der beiden
U-Isotope 238U und 235U über
den Verlauf der Erdgeschichte
0.9
relative Häufigkeit
0.8
238
0.7
U
0.6
0.5
0.4
23
0.3
238U
5
U
235U
ca. 1 Halbwertszeit,
ca. 6.5 Halbwertszeiten
0.2
0.1
0.0
4.55
4.0
3.5
3.0
2.5
2.0
1.5
1.0
0.5
0 [heute]
Zeit [Ga]
ABBILDUNG 2
Der Zerfall der beiden U-Isotope über den Verlauf der Erdgeschichte
Zur selben Zeit (um 1904) fand ein mit Rutherford kooperierender Amerikaner namens
Bertram Borden Boltwood†, daß das U/Ra-Verhältnis in den meisten U-Mineralen konstant
* 1824–1907, vielseitiger Physiker, der sich mit Problemen der Elektrizität, Hydro- und Thermodynamik befaßte. Für seine Verdienste um die Theorie und Praxis der elektrischen Signalübertragung,
die Anwendung bei der Verlegung und Nutzung der transatlantischen Kabel zwischen Europa und
Nordamerika fand, wurde W. Thomson zum Baron Kelvin of Largs geadelt (Kelvin ist der Name eines kleinen Flusses der durch den Campus der Glasgow University fließt, an der Thomson gearbeitet hat). Die absolute Temperaturskala ist nach Lord Kelvin benannt.
† 1870–1927, Professor für Radiochemie an der Yale University (1910–1927). Boltwood entdeckte das
Ionium (230Th) in der Zerfallskette von 238U, hielt es aber für ein neues Element.
7
Einführung
TABELLE 1:
(wichtige) Methoden der Geo- und Kosmochronologie
Isotopensystem
Zerfall
Zerfallsarta
40
K–Ar
K ® 40Ar
[e]
[von Weizsäcker 1937, Aldrich & Nier 1948]
40
Ar–Ar
K ® 40Ar
[Merrihue & Turner 1966]
87
Rb–Sr
Rb ® 87Sr
[b–]
[Hahn & Welling 1938, Hahn et al. 1943]
147
Sm–Nd
Sm ® 143Nd
[a]
[Lugmair 1974]
138
La–Ce
La ® 138Ce
[b–]
[Tanaka & Masuda 1982]
176
Lu–Hf
Lu ® 176Hf
[b–]
Zerfallskonstante
le = 0.581´10–10 a-1
Halbwertszeit
T = 1.25 ´ 109 a
l = 1.42´10-11 a-1
T = 48.8´109 a
l = 6.54´10-12 a-1
T = 106´109 a
lb » 2.58´10-12 a-1
T » 97 109 a
l = 1.865´10-11 a-1
oder 1.93´10-11 a-1
T = 37.2´109 a
oder 35.9´109 a
[Herr et al. 1958, Patchett et al. 1980]
187
Re–Os
Re ® 187Os
[b–]
l = 1.64´10-11 a-1
T = (42.3±1.3)´109 a
[Herr et al. 1961, Luck & Allègre 1983]
40
K–Ca
K ® 40Ca
[b–]
lb =4.962´10-10a-1
T = 1.25´109a
[Ahrens 1950, Marshall & DePaolo 1982]
238
U–Pb
U ® 206Pb
[8a,6b–]
la = 1.5512´10-10a-1
T = 4.468´109a
235
207
–
-10 -1
U ® Pb
[7a,4b ]
la = 9.848´10 a
T = 0.7038´109a
232
Th–Pb
Th ® 208Pb
[6a,4b–]
la = 4.9475´10-11a-1
T = 14.01´109a
207
204
206
204
Pb–Pb
[ Pb/ Pb– Pb/ Pb,
208
Pb/204Pb–206Pb/204Pb]
[Holmes 1946, Houtermans 1946]
Spaltspurennutzt die Störungen aus, die in
lf=8.46´10-17a-1
methode (Fission
Kristallen durch die SpontanTracks)
spaltung von 238U erzeugt werden
[Price & Walker 1962]
230
U-UngleichgeTh – 238U
l230 = 9.217´10-6 a-1
T = 75.2´103a
wichtsmethoden,
anwendbar über die letzten ca. 3´105 a, auch wenn es durch einen Prozeß zur Trennung von 238U
und seinen Folgeprodukten, z.B. 230Th, kam [Picciotto & Wilgain 1954]
kosmogene/erloschene Radionuklide, produziert durch Wechselwirkung (Spallationsprozesse)
der kosmischen Strahlung mit Materie (Atmosphäre der Erde, Oberfläche von Himmelskörpern
ohne nennenswerte Atmosphäre, z.B. Mond) und/oder nur vorhanden im frühen Sonnensystem:
14
14
N + 1n ® 14C + 1H
C [Libby 1946]
l = 1.209´10-4 a-1
T = 5.73´103a
10
-6 -1
Be
l = 0.462´10 a
T = 1.5´106 a
26
26
Al
Al ® 26Mg
[b+]
l = 0.968´10-6 a-1
T = 0.716´106 a
36
-6 -1
Cl
l = 2.25´10 a
T = 0.308´106 a
53
53
Mn
Mn ® 53Cr
[e]
l = 1.87´10-7 a-1
T = 3.7´106 a
92
92
92
-8 -1
Nb
Nb ® Zr
[e]
l = 1.93´10 a
T = 3.6´107 a
107
107
Pd
Pd ® 107Ag
[b–]
l = 1.07´10-7 a-1
T = 6.5´106 a
182
182
182
–
–
-8 -1
Hf
Hf ® W
[b , b ]
l = 7.7´10 a
T = 9´106 a
a. a, b, e = Zerfall durch a- oder b–-, b+-Strahlung bzw. Elektroneneinfang
8
A. Radiogene Isotopensysteme
ist, und er vermutete außerdem, daß Pb das stabile Endprodukt des U-Zerfalls ist. Aus dem
U/Pb-Verhältnis von Uraniniten berechnete er dann deren Alter – in der Rückschau
betrachtet sogar relativ exakt. Seine und Rutherfords Ergebnisse erhöhten das Alter der
Erde gleich auf rund 1/2 Milliarde Jahre. Zur Ehrenrettung von Lord Kelvin muß man aber
ergänzend anführen, daß er auch mit Kenntnis des radioaktiven Zerfalls nicht zu einem
auch nur annähernd richtigen Alter der Erde gekommen wäre, da er zu seiner Zeit keine
Kenntnis vom Mechanismus des Wärmetransports in der Erde haben konnte. Die frühen
Datierungsmethoden, also die U,Th–He-Methode ist zwar zwischenzeitlich als unzulänglich betrachtet worden, weil man glaubte, daß Minerale das entstandene He diffusiv abgäben; inzwischen weiß man aber diese Methode in der „Thermochronometrie“ einzusetzen,
um – ähnlich wie mit der Spaltspurenmethode – die Abkühlungsgeschichte von Plutoniten
und Metamorphiten abzuleiten, denn wenn die Temperaturen genügend niedrig sind, verhalten sich die Minerale auch gegenüber He wie geschlossene Systeme[1]. In der Folgezeit
bis heute sind mehrere weitere Methoden entwickelt worden, die sich von Fall zu Fall einsetzen lassen und z.T. sehr zuverläßlich sind. Die wichtigeren Methoden sind in Tabelle 1
zusammengestellt.
Es gibt noch einige andere Methoden, die in der Geologie oder Archäologie gelegentlich
Anwendung zur Altersbestimmung finden wie Thermolumineszenz, Dendrochronologie
oder Warwenchronologie; sie können jedoch nicht Gegenstand einer Abhandlung über
Isotopengeologie sein. Unmittelbar einsichtig ist sicherlich, daß zum einen das Alter, zum
anderen die Zusammensetzung einer Probe bestimmt, welche der aufgeführten Methoden
prinzipiell geeignet sind, um eine gestellte Aufgabe zu lösen.
2.4
Der Ursprung der Elemente
Die Elemente des Sonnensystems stammen im wesentlichen aus zwei Quellen*:
• der primordialen Nukleosynthese in den ersten Minuten des Universums,
• der Nukleosynthese in Sternen
Das Alter des Universums wird gegenwärtig mit 13.7 Ga angesetzt[2]. Nach dem Standardmodell war die Temperatur nach »3 Minuten nach dem kosmologischen Beginn, dem
Urknall (Big Bang), soweit gefallen, daß Protonen und ein geringer Anteil an Neutronen
vorlagen, so daß oberhalb von 109K Fusionsreaktionen zwischen den einfachsten Kernbausteinen möglich wurden, z.B.
p + p ® D + e+ + n;
p+n®D+g
D + D ® 3He + n
n+D®T+g
n + 3He ® 4He + g
(p = Proton, n = Neutron, e+ = Positron, n = Neutrino, D = Deuterium, T = Tritium). Daneben entstand wahrscheinlich ein Teil des 7Li. Die häufigsten Kerne waren 1H (= p) und 4He.
Da es keine stabilen Nuklide mit den Massenzahlen 5 und 8 gibt, wurden Elemente mit
Massenzahlen >7 durch Reaktion zwischen den beiden häufigsten Nukliden nicht gebildet.
Am Ende der primordialen Nukleosynthese – »103s nach dem Urknall – soll die Materie des
Universums zu etwa 76% aus Wasserstoff und 24% aus Helium und Spuren von Li bestanden haben. Allerdings erscheint die Zusammensetzung des Universums in den letzten Jahren zunehmend seltsam, nämlich nur zu ca. 4% insgesamt aus Materie zusammengesetzt,
die wir kennen. 23% ist der Anteil „dunkler Materie“ (ein noch nicht entdecktes Teilchen)
* Ein lesenswertes populärwissenschaftliches Buch zu diesem Thema unter Betonung des historischen Aspektes ist: M. Chown (2002) Die Suche nach dem Ursprung der Atome, Deutscher Taschenbuch Verlag, München, 315 Seiten, 16 €
9
Einführung
und der große Rest von 73% soll aus „dunkler Energie“ bestehen, deren Wesen unbekannt
ist[2].
Für die Bildung der schwereren Elemente
im Universum (mit Ausnahme von Li, Be
und B) ist die stellare Nukleosynthese verantwortlich. 0.5´106a nach dem Urknall
soll die Temperatur des Universums bereits
auf unter 3000K gefallen sein, und bald
danach begann das „dunkle kosmische
Zeitalter“, das mit Bildung der ersten
Sterne vorüber war[3]. Quasare könnten ca.
1 Ga nach Entstehung des Universums
existiert haben; die ersten Sterne müssen
sich dann schon viel früher gebildet
haben.
Die Lebensdauer von Sternen hängt direkt
von ihrer Masse ab: Je massereicher der
Stern, desto rascher verbraucht er seinen
Vorrat an Brennstoff. Am Ende der Lebensdauer von Sternen oberhalb von etwa
0.8 M( (M( = Masse unserer Sonne) steht
ein Abwerfen der Gase der Hülle; dadurch
gelangen auch schwerere Elemente in den
interstellaren Raum und können als Saatmaterial für zukünftige Sterngenerationen
dienen. Die erste Sterngeneration verfügte
nur über H und He als Ausgangsmaterial;
jüngere Sterne dagegen enthalten zunehmend mehr Anteile an schwereren Elementen bei ihrer Bildung.
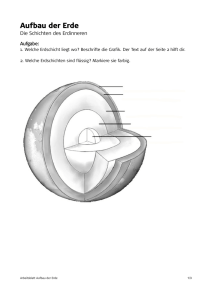
ABBILDUNG 3 Sternbildung im Nebel NGC
1748 in der Großen Magellanschen Wolke. Der
hellste (und heißeste) Stern hat eine Masse von
ca. 45 M ( . Der eher bescheiden aussehende
Stern exakt im Zentrum hat ca. 30 M ( und ist
fast 200000-mal heller als die Sonne. Sein heftiger Sternenwind hat bereits einen erheblichen
Teil des Gase der Umgebung fortgeblasen und
ein „Loch“ von ca. 25 Lichtjahren Durchmesser
geschaffen. Aufnahme des Hubble Space Telescope (http://oposite.stsci.edu/)
Sterne entstehen durch lokale Kontraktion
besonders kalter Bereiche (<10K) von Molekülwolken (Abbildung 3), wobei je nach Größe
der Molekülwolke Hunderte oder gar Tausende von Sternen gebildet werden können. Die
Akkretion eines Sternes von der Größe der Sonne mag dabei relativ rasch vonstatten gehen
(105a[4]). Nach Ende der Akkretion ist ein Stern von 1 M( erheblich größer als die Sonne
und hat eine höhere Leuchtkraft; er kontrahiert nun unter dem Einfluß der Gravitation
langsam weiter. Ein Stern von Sonnengröße durchläuft dann die T Tauri-Phase, bei welcher
durch einen intensiven Sternenwind Gas und Staub aus der Umgebung fortgeblasen werden. Die Energie stammt in dieser Phase noch aus der Akkretion. T Tauri-Sterne sind Li-reicher als unsere Sonne; dies liegt wahrscheinlich daran, daß Li schon ab ca. 2.5´106K durch
thermonukleare Reaktionen abgebaut wird. Wenn durch die Kontraktion die Temperatur
im Kern ca. 10´106K erreicht hat – bei einem Stern von 1 M( nach einigen 107a, werden
die Fusionsreaktionen gezündet, die He aus H aufbauen. Sterne mit Massen von mindestens 0.08 Sonnenmassen erreichen dieses Stadium. Die Fusionsreaktionen werden dabei
durch einen stark temperaturabhängigen quantenmechanischen Tunneleffekt ermöglicht;
ohne diesen Mechanismus würde die Kernverschmelzung erst bei Temperaturen in der
Größenordnung von 10´109K ablaufen. Auf diese Art der Synthese von Helium aus Wasserstoff wurde zuerst von Houtermans* und Atkinson† hingewiesen, nachdem Gamow‡ den aZerfall als Konsequenz des Tunneleffekts gedeutet hatte.
* Friedrich Georg Houtermans (1903–1966), deutscher Physiker; nach dem zweiten Weltkrieg wandte
er sich dem Gebiet der Altersbestimmung zu. Nach ihm ist das Holmes-Houtermans-Modell der
Entwicklung der Pb-Isotopenzusammensetzung der Erde benannt (siehe Seite 120).
10
A. Radiogene Isotopensysteme
Die stets ablaufende Fusionsreaktion (Proton–Proton-Zyklus) lautet
1
H(p,e+n)D(p,g)3He(3He,2p)4He + 26.2 MeV[5] (MeV = Megaelektronenvolt)
Der Stern erreicht mit diesem Wasserstoffbrennen
die sogenannte Hauptreihe im Hertzsprung–Russell-Diagramm † (HR-Diagramm, Abbildung 4). Bei
etwas höheren Temperaturen von mehr als 14´106K
gibt es eine konkurrierende Reaktion, die das
Vorhandensein von 12 C
voraussetzt, welches die
jüngeren Sterne aber
bereits bei ihrer Entstehung aus einer molekular e n Wo l k e e r w o r b e n
haben; dies ist der CNOZyklus – nach den Entdeckern auch Bethe‡–
We i z s ä c k e r ¶ - Z y k l u s
genannt, bei dem C, N und
O als Katalysatoren dienen:
Spektralklasse
O
B
100000
A
F G K
M
e
Rot sen
rie
r
e
Üb
Blaue
Übe rries e n
10000
Leuchtkraft relativ zur Sonne
Der Energiegewinn ergibt
sich dabei (und bei allen
anderen Fusionsreaktionen und in analoger Weise
bei Zerfallsreaktionen)
nach der Einsteinschen
Gleichung E = mc2 aus dem
Massendefekt*.
[GL 10]
1000
Ha
100
10
1
up
tr
Ze
pla ntra
ne lste
t
Ne arisc rne
be he
r
l
e
Rot
ei
Rie
So
n
rad nen
ien 10
00
R
(
sen
10
0R
(
he
È
10
Sonne
R
(
0.1
We
0.01
0.001
0.0
iße
Zw
er
0.0
01
50000 40000
0.1
ge
1R
R
(
(
1R
(
R
(
20000
10000 7000 5000
3000
2000
Oberflächentemperatur [K]
ABBILDUNG 4 Eine Version des HR-Diagramms. Nach dem Stefan-Boltzmann-Strahlungsgesetz ist die Leuchtkraft L proportional
zur Oberfläche (oder dem Quadrat des Radius) und zur vierten
Potenz der Temperatur. Blaue Sterne sind heiß, rote sind kalt. Die
meisten Sterne befinden sich in ihrer Entwicklung auf der Hauptreihe (Wasserstoffbrennen im Kern). Während ihrer T Tauri-Phase
sollte die Sonne heller (weil größer) und vielleicht etwas kühler
gewesen sein als heute; ihre Position wird daher etwas oberhalb
und rechts der heutigen gewesen sein. Wenn der Wasserstoff im
12
C(p,g)13N(e+ n)13C(p,g)14 Kern verbraucht ist, verlassen die Sterne die Hauptreihe wieder
N(p,g)15O(e+ n) 15N(p,a)12C nach rechts oben (massearme Sterne; die Sonne wird zu einem
+ 25.0 MeV
[GL 11]
Roten Riesen) bzw. rechts (massereiche Sterne).
† Robert d‘Escourt Atkinson (1898–1982) englischer Physiker und Astronom, lehrte ab den 1960-er
Jahren an der Indiana University
‡ George Gamow (1904–1968), russisch-amerikanischer Physiker; Gamow gilt auch als Erfinder der
„Big Bang“-Hypothese. Er glaubte zunächst, alle Elemente seien beim Urknall entstanden.
* Beim Proton–Proton-Zyklus bilden sich letztlich aus 4 1H-Atomen insgesamt 1 4He-Atom, 2 Positronen und zwei Neutrinos; außerdem bleiben 2 der 4 Elektronen des Wasserstoffs übrig. Der Massendefekt Dm ergibt sich damit zu Dm = 4´1.0078250 – 4.0026032 – 4´0.0005486 = 0.0265024 Masseneinheiten (die Neutrinos haben keine nennenswerte Ruhemasse) oder 0.0265024´1.6605402´10-27
= 4.40083´10-29 kg. Für die Energiefreisetzung erhält man damit DE = Dm´c2 = 4.40083´10-29 [kg] ´
2997924582 [m2/s2] = 3.95527´10-12 [kg m2 s-2 = J] bzw. 3.95527´10-12 / 1.602177´10-13 = 24.69 MeV.
Dazu kommt noch die Vernichtungsstrahlung von Elektronen und Positronen (1.02 MeV je Elektron–Positron-Paar), also 26.73 MeV. Davon werden ca. 2% durch die Neutrinos davon getragen,
die nicht nennenswert mit Materie wechselwirken und dem System daher verloren gehen; es verbleiben 26.2 MeV.
11
Einführung
Oberhalb von ca. 20´106 K dominiert der CNO-Zyklus. Eine Nebenreaktion im CNOZyklus erzeugt zusätzliches 14N:
15
N(p,g)16O(p,g)17F(e+ n) 17O(p,a)14N
Die Verweildauer eines
Sterns auf der Haupt- TABELLE 2:
reihe des HR-Diagramms ist durch das
Masse
Wasserstoffbrennen im
[Sonne = 1]
Kern bestimmt und
m a c h t d e n w e i t a u s 25
l ä n g s t e n Te i l d e r 15
Lebensdauer des Sterns 3
aus. Diese wiederum
1.5
hängt sehr stark von
der Masse ab (verglei- 1
0.75
che Tabelle 2).
0.50
[GL 12]
Verweildauer von Sternen auf der
Hauptreihe des HR-Diagramms[4]
Oberflächen–
Leuchtkraft
Zeit auf Haupttemperatur [K] [Sonne = 1]
reihe [Ga]
35000
80000
0.003
30000
10000
0.015
11000
60
0.50
7000
5
3
6000
1
10
5000
0.5
15
4000
0.03
200
log L/L
Wenn etwa 95% des Wasserstoffs
3.5
He-Schale wird
im Kern verbrannt sind, kontradünner; Expansion:
hiert der Kern wieder, weil nun der
AGB-Stern
3.4
Strahlungsdruck des Kerns nicht
He-Brennen
22
mehr ausreicht, die GravitationsHauptphase des
in dicker
[5]
He-Brennens
im
18
3.3
kräfte zu kompensieren ; der
Schale
21
Kern 9´106a
17
Stern verläßt die Hauptreihe des
23
H-Brennen in
20
HR-Diagramms (Abbildung 5).
Konktraktion;
He
im
dicker Schale
3.2
Kern geht zur Neige
Wenn etwa 99% des H im Kern ver1.3´106a
Beginn des
brannt sind, erlischt dort die
6
konvektive Hülle wird
16 3a-Prozesses
3.1
Fusion. Der Kern kontrahiert wei13
flacher, rasche Kon5
4
traktion 106a
ter und kühlt wegen der fehlenden
erste Phase des
He-Brennens im
Wärmequelle ab. Parallel dazu
3
3.0
Kern 6´106a
Kontraktionsphase
15
setzt eine Fusion von H nach He in
2.2´106a
Phase der Roten
H-Schale wird
5
einer Schale um den Kern ein.
Riesen 5´10 a
dünner 8´105a
2.9
Kleine Sterne, bei denen die Masse
konvektive Hülle wird
Gesamtdauer des
10
ihres He-Kerns <0.5 M ( ist (die
tiefer: Fusionsprodukte
H-Brennens im Kern
6a
gelangen
an
Oberfläche
65´10
Gesamtmasse <0.8 M(), schrump2.8
1
fen rasch bei zu niedriger Tempera4.3
4.2
4.1
4.0
3.9
3.8
3.7
3.6
tur. Der nächste Schritt der Fusion,
log TOberfläche
das He-Brennen, wird nicht mehr
möglich, und ihre Entwicklung ist ABBILDUNG 5 Entwicklung eines Sterns der Masse 5M ,
(
beendet. Diese H-Schale der größe- nachdem er bei einer Oberflächentemperatur von
ren Sterne wird mit der Zeit dün- 20000K und einer Leuchtkraft von 600L die Hauptreihe
(
ner, der Kern aber durch die Anla- des HR-Diagramms verläßt (Punkt 1); nach [5], leicht
g e r u n g v o n H e d u r c h d a s verändert
Schalenbrennen mächtiger. Als
Folge kontrahiert der Kern rascher und wird wieder heißer. Andererseits brauchen die Pho-
† benannt nach Ejnar Hertzsprung (1873–1967), dänischer Chemiker und Astronom, und Henry
Norris Russell (1877–1957), amerikanischer Astronom an der Princeton University
‡ Hans Albrecht Bethe, deutsch-amerikanischer Physiker, seit 1935 an der Cornell University in Ithaca, geb. 1906, Nobelpreis für Physik 1967; nach der Machtergreifung der Nazis in die USA emigriert.
¶ Carl Friedrich von Weizsäcker, geb. 1912; Bethe und Weizsäcker erarbeiteten die Reaktionen dieses
Zyklus unabhängig voneinander 1937–1939
12
A. Radiogene Isotopensysteme
tonen aus der Fusionsquelle nun keinen so weiten Weg mehr nach außen wie zuvor, so daß
sie die äußere Hülle des Sterns stärker aufheizen, in welcher der Temperaturausgleich konvektiv erfolgt. Die Hülle dehnt sich erheblich aus: der Stern ist zu einem (Roten) Riesen
geworden. Wenn die Sonne dieses Stadium erreicht, wird sie sich bis ungefähr an die Erdumlaufbahn aufblähen.
Infolge der effizienten konvektiven Durchmischung lassen sich Fusionsprodukte aus dem
CNO-Zyklus (14N) in diesem Stadium auch in den Spektren der Sterne erkennen. Die Riesen
sind nicht mehr in der Lage, ihre gesamte äußere Hülle an sich zu binden; Folge ist ein
mehr oder minder starker Massenverlust, typischerweise von 0.1ppm M( pro Jahr. Als
Roter Riese wird die Oberflächentemperatur der Sonne zwar geringer sein als die heutige,
aber infolge der erheblich größeren Oberfläche wird ihre Leuchtkraft weit über der heutigen liegen (vergleiche die berechnete Änderung der Leuchtkraft für einen 5 M(-Stern in
Abbildung 5 auf dem Weg von der Hauptreihe zum Roten Überriesen).
Wenn die Temperatur im He-Kern des Sterns infolge Kontraktion und das Hinzufügen von
Masse aus dem H-Schalenbrennen ca. 0.9´108K erreicht hat, setzt das stark temperaturabhängige He-Brennen der 3a-Reaktion ein:
4
He(a,g)8Be(a,g)12C + 7.3 MeV
[GL 13]
8
Be ist ein extrem instabiler Kern. Erst bei dieser hohen Temperatur wird die Reaktion
ermöglicht; im thermodynamischen Gleichgewicht steht ein einziges Atom 8Be ca. 109
Atomen 4H gegenüber, und die Reaktion von He zu Be ist zudem endotherm (-0.1 MeV).
Eine weitere wichtige Reaktion beim He-Brennen führt zum Sauerstoff:
12
C(a,g)16O + 7.16 MeV
[GL 14]
[6]
Des weiteren werden unter Umständen noch Ne und Mg gebildet :
16
O(a,g)20Ne + 4.73 MeV
20
Ne(a,g)24Mg
[GL 15]
[GL 16]
Als Nebenreaktion, die freie Neutronen liefert, die
zum Aufbau schwererer Isotope und Elemente dienen können, sei genannt:
20
Ne (p,g)
21
Na (e+n)
21
Ne (a,n)
Das im CNO-Zyklus gebildete
abhängig reagieren zu
14
N(a,g)18F(e+ n)18O(a,g)22Ne
24
Mg
[GL 17]
14
N kann temperatur-
[GL 18]
Die letzte Teilreaktion erfordert besonders hohe
Temperaturen und findet daher nicht immer statt.
Aus diesen Reaktionen ist zu erkennen, daß die
Nukleosynthese für die leichten Elemente (H, He, C,
N, O) zu einer Dominanz der Isotope mit geraden
Massenzahlen führt; Isotope von C, N und O treten
beim H-Brennen nur untergeordnet auf.
Beim He-Brennen dehnt sich der Kern des Sterns als
Folge der Wärmeproduktion aus, während die Hülle
kontrahiert; der Stern wird vorübergehend kleiner.
In masseärmeren Sternen setzt das He-Brennen mit
kurzfristigen Instabilitäten schlagartig ein (der sogenannte Helium-Blitz). Wenn das He im Kern verbrannt ist, liegt ein Gemisch aus weitgehend C und
ABBILDUNG 6 Der Rote Überriese Beteigeuze (a-Orionis), ca. 600 Lichtjahre
entfernt, »750-mal größer und 20-mal
schwerer als die Sonne sowie mit
1000-mal höherer Leuchtkraft versehen. Beteigeuze ist ein veritabler
Kandidat für eine „baldige“ (innerhalb
von vielleicht 10 5 a) Supernova. Bild
des Hubble Space Telescope (http://
antwrp.gsfc.nasa.gov/apod/
ap980419.html)
13
Einführung
O vor, zu dessen weiterer Verbrennung erheblich höhere Temperaturen nötig sind, die in
Sternen mit einem C–O-Kern unterhalb ca. 1.4 M( (der Chandrasekhar-Grenze*) nicht
erreicht werden. Nach Verbrauch des He im Kern zündet die 3a-Reaktion in einer Hülle um
den Kern; um diese herum vollzieht sich weiterhin die Verbrennung von H zu He: der Stern
enthält einen zwiebelschalenförmigen Aufbau. Sein Kern kühlt ab und kontrahiert, während sich die Hülle wiederum ausdehnt: der Stern wird größer als je zuvor. Unsere Sonne
mag in diesem Stadium einen Durchmesser erreichen, der bis an die Umlaufbahn des Mars
reicht. Massereiche Sterne (> ca. 8M() sind noch größer; sie werden dann Überriesen
genannt (Abbildung 6). Sterne auf diesem „asymptotischen Riesenast“ (kurz: AGB-Sterne –
asymptotic giant branch stars; Abbildung 5) des HR-Diagramms verlieren noch mehr Masse
ihrer Hülle als im Stadium der Roten Riesen. Das Abstoßen der Hülle erfolgt dabei im
Spätstadium periodisch und katastrophal, z.B. als Folge der He-Blitze beim He-Schalenbrennen. Während eines solchen Ereignisses wirft ein Stern mit einer Masse von weniger
als ca. 8 M( die gesamte noch verbliebene Hülle ab; es bleibt der ausgebrannte C–O-Kern
als heißer Weißer Zwerg zurück, der infolge seiner intensiven UV-Strahlung die Gashülle
zum Leuchten anregt. Diese ausgestoßenen Gashüllen (Abbildung 7) sind als Planetarische
Nebel bekannt, die sich innerhalb von 105 Jahren soweit vom Weißen Zwerg entfernt
haben, daß sie aufhören zu leuchten. Die Gashülle des ehemaligen Sternes reichert damit
das interstellare Medium mit schweren Elementen an, die in einer fernen Zukunft in neue
Sterne eingebaut werden. Der Weiße Zwerg, typischerweise von der Größe der Erde und
einer Dichte um 109kg/m3, kühlt langsam ab, bis er nach vielleicht 1 Ga eine Temperatur
um 5000 K an der Oberfläche erreicht hat.
ABBILDUNG 7 Der Planetarische Ringnebel M57 im Sternbild
Leier, ca. 2000 Lichtjahre entfernt und rund 1 Lichtjahr im
Durchmesser. Der Weiße Zwerg, der die Gase ausgestoßen hat,
ist unmittelbar im Zentrum als Punkt zu sehen. Weiße Zwerge
haben zu Beginn Oberflächentemperturen von 105 K und mehr
(hier ca. 120000K). Der innere Ring des Nebels (blau-violett) besteht aus heißem Wasserstoff; es folgt ionisierter Sauerstoff
(grün). Das äußere Rot ist ionisierter Stickstoff. Die Farben entsprechen ungefähr den tatsächlichen. Nach unserem derzeitigen
Verständnis der Sternentwicklung wird die Sonne in vielleicht 6 –
7 Ga als ein Weißer Zwerg enden, nachdem sie ihre Hülle als planetarischer Nebel abgeworfen hat (http://oposite.stsci.edu/).
In massereichen Sternen geht die Nukleosynthese weiter, und sofern ihre Masse > 5 – 8 M(
ist, enden sie in einer Explosion. Bei einer Kerntemperatur um 0.6´109K setzt das Kohlenstoffbrennen ein[6]; Neutrinos werden für den Energietransport wichtiger als Photonen:
12
C(12C,n)23Mg – 2.63MeV (endotherm)
[GL 19]
12
C(12C,a)20Ne + 4.62MeV
[GL 20]
12
C(12C,p) 2 3Na + 2.24MeV
[GL 21]
9
Die erste dieser Reaktionen verläuft stark temperaturabhängig; bei 0.8´10 K ist die Wahrscheinlichkeit dieser Reaktion nur 0.01%, bei 2´109K aber schon gut 5%; die beiden anderen Reaktionen laufen mit gleicher Wahrscheinlichkeit ab. Es tritt noch eine Vielzahl weiterer Reaktionen mit Protonen, a-Teilchen und Neutronen auf. Insgesamt entstehen beim
C-Brennen signifikante Mengen an 16O, 20Ne, 23Na, 24Mg und 28Si. Ab ca. 1´109K zerfällt
20
Ne durch Photodisintegration:
* S. Chandrasekhar, indisch-amerikanischer Physiker (1910 – 1995), Nobelpreis 1983 für seine Arbeiten über die Sternentwicklung
14
A. Radiogene Isotopensysteme
20
Ne(g,a) 16O
[GL 22]
Die dabei frei werdenden TABELLE 3:
a-Teilchen werden vorwiegend durch noch vorhandenes 20Ne eingefan- Stadium
gen und reagieren damit H-Brennen
zu 24 Mg und dieses mit
einem weiteren a zu 28Si. He-Brennen
Ab ca. 2´10 9 K findet das C-Brennen
Sauerstoffbrennen statt, Ne-Brennen
wobei die beiden wichtig- O-Brennen
sten Reaktionen zu Phosphor und Silizium führen: Si-Brennen
Kernkollaps
16
O + 16O ® 31P + p+ 7.68 Explosion
MeV
[GL 23]
16
O +
Entwicklungsstadien eines
Sternes von 25 Sonnenmassen[4]
Dichte im
Temperatur
im Kern [K]
Kern [kg/m3] Dauer
4´107
5´103
7 Ma
8
5
2´10
7´10
0.5 Ma
8
8
6´10
2´10
600 a
1´109
4´109
1a
9
10
1.5´10
1´10
0.5 a
9
10
2.7´10
3´10
1 Tag
9
12
5.4´10
3´10
<1 s
» 109
variabel
Sekunden
16
O ® 2 8Si + a + 9.59 MeV
[GL 24]
31
Durch weitere Reaktionen bildet sich vor allem aus P das Isotop
erstoffbrennens neben 28Si das häufigste Nuklid ist.
Bei weiter steigender Temperatur setzt
ab ungefähr 2.7´10 9 K das Siliziumbrennen ein. Dabei ist die direkte Verschmelzung von zwei 28 Si-Kernen
wegen der hohen Coulomb-Barriere
(gegenseitige Abstoßung) nicht möglich. Hunderte von Einzelreaktionen
bauen viele Isotope der Elemente bis
hin zu Fe und Ni auf. Hier endet die
Fusion, weil 56 Fe die höchste Bindungsenergie aller Isotope je Nukleon
aufweist; das bedeutet, daß zur Bildung der schwereren Elemente Energie zugeführt werden muß. Zudem
werden unter stabilen Bedingungen
im Kern eines Sternes keine genügend
hohen Temperaturen erreicht, um
schwerere Elemente durch Reaktionen
mit geladenen Teilchen aufzubauen.
Dazu sind freie Neutronen nötig, bei
deren Einfang durch einen Atomkern
keine Coulomb-Barriere überwunden
werden muß.
32
S, das am Ende des Sau-
1H, 4He
4 1H ® 4He
3 4He ® 12C
4 4He ® 16O
X 12C ®
20Ne, 24Mg, 28Si, 32S, 40Ca
4 16O ® 56Fe + 2 4He
56Fe
®
26p+30n
ABBILDUNG 8 Modell des Aufbaus eines masserei-
chen Sternes unmittelbar vor seiner Explosion als Typ
II-Supernova[5]. Nach Ablauf des Si-Brennens im Kern
zerfällt das gebildete 56Fe in Protonen und Neutronen, und der Kern kollabiert zum Neutronenstern
(gestrichelt angedeutet), besonders massereiche
Die Reaktionen vom Kohlenstoffbren- Sterne wahrscheinlich sogar zu einem Schwarzen
nen bis zum Siliziumbrennen vollzie- Loch, aus dem nicht einmal mehr Photonen entweihen sich zunehmend rascher (Tabelle chen können.
3). In der Modellvorstellung sollte jeder neue Schritt der Nukleosynthese einher gehen mit
dem Schalenbrennen des vorhergehenden Schrittes um den Kern herum. Um diese Schale
herum befindet sich eine Schale, in welcher der nächst niedrige Fusionsschritt abläuft und
so fort. Der Stern sollte demnach einen zwiebelschalenförmigen Aufbau zeigen (Abbildung
8). Nach Ablauf des Siliziumbrennens besteht der Kern weitgehend aus 56Fe. Dichte und
Temperatur sind nun so immens hoch geworden, daß die Photonen eine genügend hohe
Energie erreicht haben, um die Fe-Kerne spontan zerlegen:
15
Einführung
56
Fe(g,4n)13 4 He
[GL 25]
4
He(g,4n)2p
[GL 26]
p + b– ® n + n
[GL 27]
Der Kern zerfällt in Sekundenbruchteilen in einen extrem kompakten Neutronenkern von vielleicht 10 km Durchmesser bei einer Dichte von 4´1017 kg/
m3 und einer Masse von 1.4 bis »2 – 3
M(. Damit ist der Kern nun extrem steif
und nicht weiter komprimierbar. Die
innere Hülle des Sterns (weitgehend
wohl Fe) fällt mit sehr hoher Geschwindigkeit nach unten, prallt am Kern ab
und bildet eine nach außen gerichtete
Schockwelle, welche zusammen mit der
Flut von Neutrinos die äußere Hülle des
Sterns fortbläst. Der massereiche Stern ABBILDUNG 9 Der Crab-Nebel in »6500 Lichtjahhat eine Supernova-Explosion vom Typ ren Entfernung, Relikt eines Supernova-Ausbruchs,
II erlitten (Abbildung 9). Das Material der nach chinesischen Quellen im Jahr 1054 sichtum den Kern herum wird sich durch die bar wurde. In seinem Zentrum befindet sich (nicht
Schockwelle und die Neutrinos stark sichtbar) ein Pulsar – ein Neutronenstern (http://
aufheizen. Die Element- und Isotopen- www.usm.uni-muenchen.de/people/gehren/
häufigkeiten werden hier wahrschein- vorlesung/black_dias_II.html).
lich massiv verändert. Nach Berechnungen sollen insbesondere große Mengen an 44Ca, 48Ti, 49Ti, 52Cr, 55Mn und 56Fe gebildet
werden[6]. Zurück bleibt ein extrem kompakter, heißer(106 K an der Oberfläche) und rasch
rotierender (Millisekunden) Neutronenstern von nur wenigen (101 km) Kilometern Durchmesser. Im Millisekundenbereich bis in den unteren Sekundenbereich pulsierende Radioquellen (Pulsare) werden Neutronensternen zugeschrieben.
ABBILDUNG 10 Eta Carinae, ca. 7500 Lichtjahre entfernt, mit ungefähr 120 M ( der
gewichtigste bekannte Stern (im Zentrum
der zentralen Explosionswolke nicht auszumachen) in unserer Galaxis. Die äußere rote
Hülle ist bei einer Explosion entstanden, die
um 1830 sichtbar gewesen ist und Eta Carinae damals zum zweithellsten Stern am
Himmel gemacht hat. Eta Carinae ist rund
4´106 -fach heller als unsere Sonne und hat
bei der großen Masse eine nur geringe Lebenserwartung (wenige Ma). Sterne dieser
Masse sind extrem instabil und können jederzeit in einer „Hypernova“ (eine SuperSupernova) explodieren. Quelle: http://
www.seds.org/
Wenn die Masse des Kerns >2 – 3 M( ist, gibt es keinen Gleichgewichtszustand für die
Materie mehr: der Kern kollabiert zu einem Schwarzen Loch, einer sogenannten Singularität. Selbst Licht kann dann innerhalb des Schwarzschild-Radius*
16
A. Radiogene Isotopensysteme
RSchwarzschild =
2GM
M
» 3 Kern
2
M(
c
[GL 28]
nicht mehr entkommen (G = Gravitationskonstante [6.67´10-11 m 3/(kg ´ s 2)], c = Lichtgeschwindigkeit [3´108 m/s], M = Masse). Damit erhält man für ein Schwarzes Loch der Masse
5 M( (M( = 1.99´1030 kg) einen Schwarzschild-Radius von lediglich ca. 14750m!
p
b{
nur s
s, r
s, r
(n,g)
s, r
p
nur s
s, r
nur s
r
r
r
Protonenzahl Z
s, r
s, r
s, r
s, r
nur s
s, r
r
b{
Neutronenzahl N
ABBILDUNG 11
Die drei für die Bildung der schwereren Elemente in Sternen relevanten Prozesse: Beim s-Prozeß (blaue Pfeile und Linien) fängt ein stabiler Atomkern
ein Neutron ein; es entsteht ein Isotop desselben Elementes mit einer um 1
höheren Massenzahl. Wenn dieses Isotop stabil ist, werden weitere Neutronen eingefangen, solange bis ein instabiles Isotop gebildet wird, dessen b–Halbwertszeit klein ist im Vergleich zur mittleren Zeitdauer für den Einfang
eines weiteren Neutrons. Das Isotop zerfällt dann in ein gleich schweres Isotop des Elementes mit der nächst höheren Ordnungszahl (gestrichelte rote
Linien). Beim r-Prozeß (rote Pfeile und gestrichelte Linien – diese kennzeichnen generell in der Skizze den b–-Zerfall) ist die Zahl der zur Verfügung stehenden Neutronen so groß (die mittleren Einfangszeiten für Neutronen
durch ein Nuklid liegen in der Größenordnung von 10-4s), daß radioaktive
Isotope weitere Neutronen einfangen, bevor die b–-Zerfallsrate überwiegt.
Es entstehen neutronenreiche Nuklide. Erst wenn auf diese Weise Nuklide
mit sehr kurzen Halbwertszeiten entstanden sind (diese Nuklide haben 10 –
20 Neutronen mehr als das schwerste stabilste Isotop des betreffenden Elementes), vollzieht sich der b–-Zerfall rascher als der Einfang eines weiteren
Neutrons. Die Dauer des r-Prozesses wird mit Sekunden angegeben; deshalb muß als Ursache ein explosiver Prozeß angenommen werden, z.B. eine
Supernova. Inzwischen wird auch die Kollision zwischen zwei Neutronensternen eines Doppelsternsystems als Mechanismus diskutiert; dabei bilden
* benannt nach dem deutschen Physiker und Astronomen Karl Schwarzschild (1873–1916), Direktor
des Astrophysikalischen Observatoriums in Potsdam
17
Einführung
sich nach Simulationen Spiralarme um ein massives Zentralobjekt (das zu einem Schwarzen Loch wird?), in denen bei rascher Druckentlastung und extremen Temperaturen eine Vielzahl von Nuklearreaktionen ablaufen könnte.
Insgesamt 32 stabile Nuklide auf der neutronenarmen Seite der Elemente
sind weder dem s- noch dem r-Prozeß zugänglich. Diese Nuklide sind stets
mit nur geringen Häufigkeiten am Aufbau des jeweiligen Elementes beteiligt. Für ihre Bildung wird ein p-Prozeß angenommen (p für Protoneneinfang). Im Innern massereicher Sterne stehen kurz vor oder bei einer
Supernova-Explosion bei Temperaturen von 2 – 3´109K wahrscheinlich genügend Protonen zur Verfügung, um aus den im s-Prozeß (oder r-Prozeß)
gebildeten Nukliden durch (p,g)-Prozesse die neutronenarmen Nuklide zu
erzeugen. Bei diesen extremen Temperaturen sind (g,n)-Prozesse (Photodisintegration) eine Alternative. Umgezeichnet nach [6]; siehe auch [7].
121
Sb, 51
ü
ï
ï
ý
ï
ï
þ
p-Prozeß
112
1.0%
112d
57.4%
114
115
116
nur s
117
s+r
118
s+r
119
s+r
120
s+r
0.65%
0.35%
14.5%
7.7%
24.2%
8.6%
32.6%
Sn, 50
113
115
4.3%
95.7%
111
112
113
Pfad des s-Prozesses
114
In, 49
2.8d
42.6%
122
nur r
27h
4.6%
r-Prozeß
110
Cd, 48
12.5%
62
12.8%
63
24.1%
64
116
28.7%
54h
7.5%
65
66
67
68
40m
5.8%
nur rProzeß
13s
12.2%
124
nur r
ì
í
ï
ï
î
Z
123
69
70
71
72
73
74
N
ABBILDUNG 12
18
Illustration der s-, r- und p-Prozesse am Beispiel des Zinns. Sn ist das Element
mit den meisten stabilen Isotopen (10), bedingt durch eine „magische“ Protonenzahl (hier: 50). Der s-Prozeß verläuft über die stabilen Cd-Isotope, bis
mit dem 115Cd ein Isotop erreicht ist, daß mit einer Halbwertszeit von 54h
durch b–-Zerfall in 115In übergeht. Daraus bildet sich über Neutroneneinfang
116
In, das mit einer Halbwertszeit von 13s in 116Sn zerfällt. Dieses ist durch
das stabile 116Cd von einer Bildung über den r-Prozeß abgeschirmt, also ein
reines „s-Isotop“. Durch erneuten Neutroneneinfang geht 116Sn in die stabilen Isotope 117Sn bis 120Sn über. Diese vier Nuklide können aber genausogut
durch den r-Prozeß entstehen, weil es keine stabilen Isotope leichterer Elemente mit diesen Massenzahlen gibt, so daß deren b–-Zerfall erst bei 117Sn
bis 120Sn endet. Wenn 120Sn ein weiteres Neutron einfängt, entsteht radioaktives 121Sn, das mit einer Halbwertszeit von 27h in stabiles 121Sb zerfällt.
Die stabilen Isotope 122Sn und 124Sn können deswegen nicht (oder nicht in
beträchtlicher Menge) durch den s-Prozeß entstehen, sondern sind reine rProzeß-Nuklide. Für die stabilen Isotope 112Sn, 114Sn und 115Sn gibt es keine
Bildungsmöglichkeiten durch s- oder r-Prozeß. Sie sind daher p-Prozeß-Nuklide, was auch durch die geringe Häufigkeit nahegelegt wird. 115Sn könnte
z.B. entstehen, wenn durch ein hoch energetisches Photon ein Neutron aus
116
Sn entfernt wird. 114Sn könnte durch Protonenbeschuß von 113In (ebenfalls ein p-Nuklid) erzeugt werden. Verändert nach [6] bzw. [11].
90
A = 208
A = 195
Z = 82
N = 82
+
Po
Pt
Hf
A = 138
2s
Dy
Gd
Nd
Ce
r-Prozeß-Pfad
für T = 109K
den
Sm
Ba
U
Os
Yb
A = 130
Th
Ra
Rn
4s
Th
W
Er
60
Pu
U
Pb
Hg
70
r
eE
ten
Sel
Xe
Te
50
Pd
Ru
Mo
ll
Sr
0.5s
fa
Zr
er
40
Z = 50
Sn
Cd
{ -Z
b
N = 50
Protonenzahl Z
80
Kr
30
N = 184
r-Prozeß-Nuklide
s-Prozeß-Pfad
Fm
Cf
Cm
Spaltung in zwei ungleich große Kerne
100
N = 126
A. Radiogene Isotopensysteme
Zeit für einen Aufbauzyklus ca. 5s
Se
Ge
Z = 28
von Fe
20
40
50
60
70
80
90
100
110
120
130
140
150
160
170
180
190
Neutronenzahl N
ABBILDUNG 13
Die Bildung der Isotope der schweren Elemente durch s- und r-Prozeß. Der
s-Prozeß folgt der blauen Kurve und endet beim 209Bi. Stabile Isotope eines
Elementes mit ungerader Massenzahl haben in der Regel höhere Einfangquerschnitte für Neutronen als solche mit gerader Massenzahl. Erstere werden daher bevorzugt durch weiteren Neutroneneinfang beim s-Prozeß
abgebaut. Daher sind die Isotope eines Elementes mit ungerader Massenzahl in der Natur meist geringer als die Isotope mit gerader Massenzahl (dasselbe gilt auch für die Elemente mit gerader und ungerader Ordnungszahl,
Abbildung 14). Die Existenz eines s-Prozesses ist belegt, seitdem 1952 in
den Spektren von Roten Riesen das Element Tc nachgewiesen wurde[9]. Tc
besitzt keine stabilen isotope. Die beiden längstlebigen Isotope weisen nur
Halbwertszeiten um 4 Ma auf. Tc muß daher tief im Innern der Riesen synthetisiert und konvektiv an ihre Oberfläche transportiert werden. Durch den
r-Prozeß entstehen neutronenreiche radioaktive Nuklide mit kurzen Halbwertszeiten (durch die hellroten Felder ausgewiesen), die 10 bis 20 Neutronen mehr enthalten als stabile Isotope der jeweiligen Elemente. Durch
mehrfache b–-Zerfälle entstehen stabile Isotope von Elementen mit höherer
Ordnungszahl (rote Punkte). Dem r-Prozeß sind auf diese Weise Elemente
bis zur Massenzahl von etwa 270 zugänglich. Bei den „magischen“ Neutronenzahlen 82 und 126 entsteht ein Rückstau, weil solche Nuklide im Vergleich zu den benachbarten stabiler sind und besonders kleine
Neutroneneinfangquerschnitte aufweisen. Ein zunächst entstandenes Sroder Y-Isotop mit 82 Neutronen wird demnach kein weiteres Neutron aufnehmen, sondern b–-Zerfälle in andere Elemente erleiden, bevor weitere
Neutronen eingefangen werden. Nach [6] bzw. [11], verändert.
Die Explosionshülle der Supernova breitet sich mit einigen Dutzend Kilometern pro
Sekunde in den interstellaren Raum aus und reichert diesen mit vielen und auch schweren
Elementen des Periodensystems an. Das hat seine Ursache darin, daß in der Nähe des Neutronenkernes extrem hohe Neutronenflüsse zur Verfügung stehen, die, vom 56Fe der innersten Hülle ausgehend, insbesondere neutronenreiche Isotope der schweren Elemente
19
Einführung
durch den sogenannten r-Prozeß aufbauen können (r für rapid; siehe Abbildungen 11 und
12 zur Erläuterung). Auch die Existenz von Th und U in der Natur läßt sich nur so erklären.
Viele andere Isotope der schweren Elemente entstehen durch den s-Prozeß (s für slow,
Abbildungen 11 + 12) bei geringen Neutronenflüssen über vergleichsweise lange Zeit. Als
Entstehungsumgebung werden die Hüllen massereicher Sterne (>8 M() genannt, die sich
irgendwann zu Supernovae entwickelt haben bzw. entwickeln werden, und die inneren
Hüllen der AGB-Sterne*. Dort werden durch Nebenreaktionen wie
22
Ne(a,n) 2 5Mg
[GL 29]
13
[GL 30]
C(a,n) 1 6O
freie Neutronen gebildet, die von anderen Kernen wieder eingefangen werden können. Vor
allem die erste dieser beiden Reaktionen soll in den massereichen Sternen von entscheidender Bedeutung sein[8].
Der sogenannte p-Prozeß (p für Protoneneinfang und/oder Photodisintegration) schließlich ist für die Entstehung neutronenarmer stabiler Nuklide relevant (Abbildungen 11 und
12). Welche Isotope der schweren Elemente dem s- und welche dem p-Prozeß zugänglich
sind, läßt sich Abbildung 13 entnehmen.
Abbildung 14 zeigt die Häufigkeit der Elemente im Sonnensystem. Auffällig ist die sehr
geringe Häufigkeit der leichten Elemente Li, Be und B. Diese werden bei der stellaren
Nukleosynthese weitgehend ausgeschlossen. Das bei der primordialen Nukleosynthese
entstandene 7Li wird in Sternen sogar bereits ab ca. 3´106 K durch Reaktion mit Protonen
weitgehend zu He abgebaut (Li-Gehalte in T Tauri-Sternen sind höher als in Sternen der
Hauptreihe des HR-Diagramms). Man nimmt an, daß Li, Be und B ihre Existenz zum großen Teil Spallationsreaktionen in molekularen Wolken verdanken. Hochenergetische kosmische Partikelstrahlung (insbesondere Protonen, a-Teilchen) trifft auf die Kerne schwererer Elemente (C, N, O) und zerlegt sie. Li, Be und B entstehen demnach nicht durch den
Aufbau aus leichteren, sondern durch die Zerstörung schwererer Elemente.
* P. Merrill identifizierte 1952 Tc in Spektren von einigen Roten Riesen. Da das längstlebige Isotop,
98
Tc, nur eine Halbwertszeit von 4.2 Ma hat, muß das Tc in den Riesensternen entstanden sein. Das
wurde als Indiz für das Ablaufen des s-Prozesses in solchen Sternen gewertet.
20
A. Radiogene Isotopensysteme
100000000000
beim „Big Bang“ entstanden
10000000000
entsteht in Sternen der Hauptreihe
(z.B. unserer Sonne) durch H-Verbrennung
1000000000
Häufigkeit der Elemente
im Sonnensystem
[relativ zu 106 Atomen Si]
100000000
C
relative Häufigkeit
10000000
1000000
Elemente, die in Roten Riesen
Ne synthetisiert werden
Mg Si
Fe
S
Ar Ca
100000
Cr
10000
K
1000
100
Ti
Co
F
Li
1
Be
Sr
Sc
B
10
entstehen in Molekülwolken
durch Reaktionen mit
kosmischer Strahlung
0.1
Elemente, die in Supernovae und
in AGB-Sternen entstehen
Cu Ge
As
Rb
Zr
Y
Mo
Nb
Sn
PdCd
Ba
La
Pb
Nd
Sm
Dy Yb
Os
Hg
Hf W
Eu
Lu
0.01
Pt
Au
Bi
Re
Ta
Th
U
0.001
H Be N Ne Al S
K Ti Mn Ni Ga Se Rb Zr Tc Pd In Te Cs Ce Pm Gd Ho Yb Ta Os Au Pb
He B O Na Si Cl Ca V Fe Cu Ge Br Sr Nb Ru Ag Sn I Ba Pr Sm Tb Er Lu W Ir Hg Bi
Li C F Mg P Ar Sc Cr Co Zn As Kr Y Mo Rh Cd Sb Xe La Nd Eu Dy Tm Hf Re Pt Tl
ABBILDUNG 14
Th
U
Normierte Häufigkeit der Elemente im Sonnensystem[10]. Der starke Abfall
von Sauerstoff bis Titan spricht stark für den Ursprung dieser Elemente durch
Fusionsprozesse. Besonders häufig unter diesen Elementen sind Nuklide mit
Massenzahlen, die ganze Vielfache von 4 (He!) darstellen (12C, 16O, 24Mg,
28
Si, 32S, 40Ca, 44Ca, 48Ti, 52Cr, 56Fe). Jenseits von Fe oder Ni werden die Elemente durch Neutroneneinfang gebildet. Markant ist die im Vergleich zu
den benachbarten Elementen geringere Häufigkeit der Elemente mit ungerader Ordnungszahl (mit wenigen Ausnahme Nuklide mit ungerader Anzahl
an Protonen und gerader Anzahl an Neutronen); dies ist Ausdruck der höheren Wirkungsquerschnitte für Neutroneneinfang der Elemente mit ungerader Ordnungszahl. Die solare Häufigkeit der Elemente entspricht
näherungsweise (mit Ausnahme von H und He) auch der kosmischen Häufigkeit, wie sie in der Photosphäre vieler Sterne gemessen werden kann. Das
Rohmaterial, aus dem die Sterne entstehen, scheint demnach zumindest in
unserer Galaxis relativ gut durchmischt zu sein.
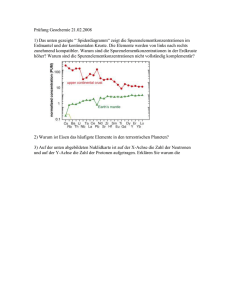
In Abbildung 15 ist ein Vergleich der Häufigkeiten der leichteren Elemente gegeben, wie sie
in Supernovae vom Typ II und vom Typ Ia beobachtet werden*. Diese Modellrechnungen
scheinen zu zeigen, daß eine bessere Übereinstimmung zwischen Supernovae vom Typ II
und der Materie des Sonnensystems besteht als zwischen Typ Ia-Supernovae und dem Sonnensystem, mithin, daß das Material des Sonnensystems in massereichen Sternen synthetisiert worden ist. Einschränkend ist zu sagen, daß die Häufigkeiten der leichten Elemente
niedriger werden, wenn man für die Rechnungen eine kleinere Masse für den Stern
annimmt, der in der Supernova vom Typ II explodiert, als 25 M([5].
21
Einführung
log Häufigkeit relativ zur solaren Häufigkeit
Man wird annehmen dürfen, daß
1
die molekulare Wolke, aus welcher
SN II
das Sonnensystem entstanden ist,
Ne
Al
Fe
Mg
P
den Sternenstaub von mehr als
Cr
O
0
einer Supernova-Explosion enthalC
Si
Ca
ten hat. Der Hinweis auf die ExiSc Ti
S
stenz von radioaktiven Nukliden
Mn
-1
V
mit kurzen Halbwertszeiten (siehe
Kapitel 16.2, Seite 182 und Kapitel
16.3, Seite 186) im frühen Sonnensystem erfordert jedoch, daß der
-2
SN Ia
letzte Supernova-Ausbruch, der
Material in der präsolaren Wolke
deponiert hat, allenfalls einige
-3
107a vor der Bildung der Meteorite
10
20
30
40
50
60
erfolgt sein kann. Das SonnensyMassenzahl
stem ist eventuell nicht an der
Stelle unserer Galaxis geboren ABBILDUNG 15 Vergleich der normierten (auf solare Häuworden, an der es sich heute befin- figkeit und auf 56 Fe) Elementhäufigkeiten zwischen
det, sondern gut 6000 Lichtjahre Supernovae vom Typ Ia und (für 25 M() vom Typ II. Insnäher am Zentrum[14]. Die größere besondere bei den leichten Elementen (gelber Bereich)
Materiedichte dort könnte einen entsprechen die Häufigkeiten der Supernovae II der solagrößeren Anteil an schweren Ster- ren Häufigkeit besser. Daraus hat man geschlossen, daß
nen mit entsprechend geringer Supernovae dieses Typs den Hauptteil der Masse liefern,
Lebensdauer, eine höhere Dichte die in molekularen Wolken das Rohmaterial für neue Steran Sternen je Volumeneinheit und nengenerationen darstellen. Umgezeichnet nach [5].
eine größere Häufigkeit an Supernova erzeugt haben als im Bereich des Spiralarms, an dem sich die Sonne heute befindet.
Chondritische Meteorite enthalten in ihrer feinkörnigen Grundmasse geringe Mengen
(einige 100 ppm) an nicht säurelöslichen Rückständen von nm- bis µm-großen Mineralen
wie SiC, C (Mikrodiamanten und Graphit), Al2O3, Si3N4 und MgAl2O4 (Spinell) mit variablen und z.T. exotischen Isotopenzusammensetzungen. Nachdem der Ursprung dieses
Materials lange zeit enigmatisch war, glaubt man inzwischen, daß sie präsolare Körner darstellen. Auf Grund der Isotopenzusammensetzungen könnten sie sich in Roten Riesen
gebildet haben und mit dem starken Sternenwind dieser Giganten in den interstellaren
Raum verdriftet worden sein. Andere Isotopenzusammensetzungen deuten auf eine Entstehung in Supernovae hin. Leicht lesbare Zusammenfassungen dazu bieten [12] und [13].
* Supernovae vom Typ I unterscheiden sich von denen des Typs II durch das Fehlen von Wasserstofflinien in ihren Spektren. Supernovae vom Typ Ia entstehen vermutlich, wenn in einem engen Doppelsternsystem aus einem Weißen Zwerg (M( ³ 1) und einem massereichen großen Begleiter
Material auf den Weißen Zwerg überströmt oder wenn zwei Weiße Zwerge ineinanderstürzen[15].
Wenn dabei die Chandrasekhar-Masse von ca. 1.4 M( überschritten wird, kommt es zur explosionsartigen Elementsynthese im Weißen Zwerg bis hin zu 56Ni, das über 56Co (Halbwertszeit ca. 77 Tage)
in 56Fe zerfällt; die bei diesem Zerfall freigesetzte g-Strahlung macht Supernovae vom Typ Ia zu den
hellsten aller Supernovae. Im Unterschied dazu entstehen Novae durch denselben Mechanismus,
wenn die Masse des Weißen Zwerges geringer ist und bleibt. Supernovae der Typen Ia und II sind
ungefähr gleich häufig und ereignen sich in unserer Galaxis im Schnitt zusammengenommen zweibis dreimal pro Jahrhundert.
22
A. Radiogene Isotopensysteme
2.5
Massenspektrometrie
Die Entwicklung der Isotopengeochemie zu einem der leistungsfähigsten Bereiche der Geowissenschaften wäre nicht möglich gewesen ohne die Erfindung und Entwicklung geeigneter Meßgeräte, den Massenspektrographen, mit deren Hilfe Isotopenverhältnisse i.a.
wesentlich genauer gemessen werden können als mit den ursprünglich allein zur Verfügung stehenden Zählrohren. Mit den letzteren lassen sich außerdem ja nur Zerfallsprozesse
registrieren, d.h. man hat keinen Zugang zu den stabilen Endprodukten des Zerfalls, also
den Tochternukliden (siehe Zerfallsgleichung).
Die ersten massenspektrographischen Arbeiten wurden von dem englischen Physiker J.J.
Thomson* mit einem von ihm entwickelten „Parabelspektrographen“ in Cambridge durchgeführt. Bei diesem Gerät wird ein Strahl positiv geladener Ionen durch ein elektrisches
und ein diesem parallelen Magnetfeld abgelenkt. Ionen gleicher Masse, aber unterschiedlicher Energie können auf einer Photoplatte entlang einer Parabel nachgewiesen werden.
Damit gelang es Thomson 1910 nachzuweisen, daß Neon aus verschiedenen Atomarten
zusammengesetzt ist, den Isotopen 20Ne und 21Ne. 1918/19 wurde diese Bauart des Massenspektrographen unabhängig voneinander durch F.W. Aston† in Cambridge und A.J. Dempster‡ an der University of Chicago verbessert durch Entwicklung von Fokussierungsverfahren (meist Doppeltfokussierung), die es erlaubten, den Ionenstrahl zu bündeln und höhere
Strahlenintensitäten zu erzielen.
Vakuumpumpe
Elektromagnet
Ionenstrahl
An
aly
Ionenquelle
608
sat
or
Durchführungen für
Beschleunigungsspannung
und Filamentstrom
ABBILDUNG 16
Kollektor
zur digitalen
Signalaufzeichnung
V
prinzipieller Aufbau eines Massenspektrometers
Der heutige Typ des Massenspektrometers (-„meter“ weil die Registrierung des Ionenstroms
nicht mehr durch Belichtung von Photoplatten erfolgt, sondern kontinuierlich durch elektronische Messung) geht zurück auf ein Design des einfachfokussierenden Gerätes, das
A.O. Nier¶ 1940 einführte. Ein solches Massenspektrometer, das schematisch in Abbildung
16 wiedergegeben ist[16], besteht aus drei wesentlichen Teilen, (i) der Ionenquelle, (ii) dem
Analysator mit Trennrohr und Elektromagnet und (iii) dem Kollektor, einem Faradaybecher oder Elektromultiplier.
* Joseph John Thomson (1856–1940), englischer Physiker, Professor in Cambridge, entdeckte 1897
das Elektron, Nobelpreis für Physik 1906
† Francis W. Aston (1877–1945), Schüler von J. J. Thomson, erhielt 1922 für die Konstruktion des
Massenspektrographen den Physik-Nobelpreis. Mit diesem Instrument konnte er in den folgenden
Jahren 212 natürlich vorkommende Isotope identifizieren.
‡ Arthur Jeffrey Dempster (1886–1950), amerikanischer Physiker, Entdecker von 235U
¶ Alfred Otto Nier (1911–1994) amerikanischer Physiker an der University of Minnesota
23
Einführung
Werden feste Proben
analysiert, dann ist die Schema einer Ionenquelle
Eintrittsspalt [0V]
Ionenquelle eine sogenannte Thermionenz-Ablenkung [z.B. 300V]
quelle (siehe Abbildung
y-Ablenkung [z.B. 0-50V]
17[17]), das Massenspektrometer ein ThermioFokussierungslinsen [z.B. 1580V]
nenmassenspektrometer, und das Verfahren
Abschirmblende [z.B. 1580V]
wird als TIMS (thermal
ionization mass spectroZiehblende [z.B. 1750V]
metry) abgekürzt. Dabei
wird die Probe – ein
Ionisierungsbändchen [Re, Ta, W]
chemisch rein aus
e i n e m G e s t e i n o d e r ABBILDUNG 17 Schema des Aufbaus der Ionenquelle eines ThermMineral
i s o l i e r t e s ionenmassenspektrometers
Metallsalz – auf ein
schmales (»1mm breites, »10mm langes »0.02mm dickes) Bändchen aus einem hochschmelzenden Metall (Re, Ta, W) aufgetragen. Die Ionisierung erfolgt beim Austritt des
Metalls (z.B. Sr, Nd, Pb) aus der glühenden Oberfläche des Filamentes. Die positiv geladenen Ionen werden dann in einem Hochspannungsfeld in der Ionenquelle beschleunigt
(typischer Wert: 8kV) und auf einen Eintrittsspalt gegen das Trennrohr hin fokussiert. Im
Trennrohr gelangt der Ionenstrahl in das magnetische Sektorfeld eines Elektromagneten,
dessen Polschuhe so ausgerichtet sind, daß die magnetischen Feldlinien senkrecht zur
Flugrichtung der Ionen stehen (Abbildung 19). Ein solches magnetisches Sektorfeld wirkt
auf Ionen verschiedener Masse und Energie ähnlich wie ein optisches Prisma auf Strahlung
von unterschiedlicher Frequenz. Die Ionen werden auf Kreisbahnen abgelenkt, entsprechend ihrem Verhältnis von Masse m zu Ladung e, mit anderen Worten, die Ablenkung
von der geraden Flugrichtung ist umso größer, je kleiner die Masse oder größer die Ladung
ist (I.a. dampfen aber nur die einwertigen Metallionen vom Filament ab, also z.B. Sr+, Nd+,
Hf+).
Die auf diese Weise den Massen entsprechend separierten Ionenstrahlen fliegen
dann auf getrennten Bahnen weiter zum
Kollektor, meist ein oder mehrere Metallb e c h e rc h e n ( F a r a d a y b e c h e r ) . D a s
Magnetfeld wird so eingeregelt, daß
einer der Ionenstrahlen (der also eine
einzige Masse repräsentiert, z.B. 87 Sr)
einen Schlitz in einer vor dem Faraday
angebrachten Platte durchfliegt und im
Faradaybecher aufgefangen wird, während die übrigen Strahlen (z.B. 84Sr, 86Sr
und 88Sr) auf die geerdete Schlitzplatte
oder bereits vorher auf die Wände des
Trennrohrs prallen und neutralisiert werden. Die durch den Ionenstrom dem
Auffänger zugeführte Ladung wird über
einen hochohmigen Widerstand – typischerweise 10 11 Ohm – abgeleitet. Die
Spannungsdifferenz, die auf diese Weise
an den beiden Enden des Widerstandes
erzeugt wird, wird verstärkt und mit
einem Digitalvoltmeter (DVM) gemessen. Ein typischer Wert für den Ionen24
ABBILDUNG 18 Links ein Einzelfilament, auf das
die zu analysierende Substanz aufgetragen wird.
Rechts ein Dreifachfilament; hier wird die Substanz auf die beiden Seitenfilamente aufgetragen,
von denen sie natürlich auch abgedampft werden.
Das Zentralfilament dient zur Kontrolle der Ionisation [aus P.J. Potts (1992) A Handbook of Silicate
Rock Analysis, Blackie, Glasgow, 622 Seiten.].
A. Radiogene Isotopensysteme
strom, der z.B. bei einer Sr-Analyse für das häufigste Isotop (88Sr) eingestellt wird, ist 1–
2´10-11A, was sich auf dem DVM in 1–2 Volt umsetzt. Im Fall eines Massenspektrometers
mit nur einem Kollektor werden die verschiedenen Ionenstrahlen eines Elementes im
Abstand von einer oder mehreren Sekunden in den Faradaybecher geschickt, indem man
das Magnetfeld des Elektromagneten variiert. Schneller wäre und denselben Effekt hätte es,
anstatt dessen die Beschleunigungsspannung zu verändern. Das führt jedoch zur Defokussierung der Ionenoptik und wird deshalb in der Praxis nicht gemacht.
Bei der derzeitigen Generation der Thermionenmassenspektrometer besteht der
Auffänger aus mehreren (bis
zu neun) einzelnen wenige
fm
mm breiten FaradaybeA''3
Bild
A''1
kur ve
chern, so daß meistens alle A'
A''2
Ionenstrahlen eines Elementes gleichzeitig in separate Becher aufgefangen ABBILDUNG 19 Prismenwirkung eines homogenen magnetiwerden. Da bei einem sol- schen Sektorfeldes; Abbildung eines ionenemittierenden Punkchen Multikollektor natür- tes A' durch ein magnetisches Sektorfeld mit dem Sektorwinkel
lich jeder Becher seinen
f für drei verschiedene Massen bei senkrechtem Eintritt des
eigenen Ableitwiderstand m
Mittelstrahls des Ionenbündels ins Sektorfeld; Ionen verschiedehat und mit einem separaMassen und gleicher Energie gelangen längs der Bildkurve
ten DVM verbunden ist, ner
''
''
''
,
A
s p a r t m a n m i t d i e s e r 1 A2 , A3 zur Fokussierung.
Methode vor allen Dingen
Meßzeit und erreicht, zumindest prinzipiell, auch eine höhere Präzision.
Noch einige Bemerkungen zur Bewegung der Ionen im
Magnetfeld:
Durch die Beschleunigungsspannung V
in der Ionenquelle
nimmt ein Ion der
Masse
m
und
Ladung e die kinetische Energie
E = eV = 1/2 mv2 [GL 31]
auf, wobei v die
Geschwindigkeit des
Ions ist. Beim Eintritt ins Magnetfeld
der Feldstärke B werden diese Ionen auf
Kreisbahnen mit
Radius r abgelenkt,
entsprechend der
Gleichung:
ABBILDUNG 20 Ansicht eines Thermionenmassenspektrometers [Micromass Sector 54 – http://www.micromass.co.uk]. In der Mitte die Ionenquelle, in die bis zu 20 Proben in einen Probenwechsler geladen werden
können. Rechts der Auffänger, der mit bis zu neun Faradaybechern bestückt sein kann.
Bev = mv2/r
oder, nach v aufgelöst:
[GL 32]
v = Ber/m.
Dies, in GL 31 eingesetzt, ergibt:
25
Einführung
eV = 1/2 mB2 e2 r2/m2
V/e = 1/2B2 r2/m
m/e = B2 r2/2V
[GL 33]
Wenn B in Gauß angegeben wird, r in cm, m in Atommassen und e´V die Voltenergie der
Ionen ist, dann erhält man:
m/e = 4.825´10-5 B2 r2/V.
Da der Radius der Ionenbahn durch den Radius des Trennrohres gegeben ist und V bei der
Analyse zweckmäßigerweise nicht verändert wird, bleibt als Variable nur B, um den Ionenstrahl auf der Kreisbahn in den Faradaybecher zu zwingen:
B=
143.95 m ´ V
r
e
[GL 34]
So muß man z.B. B=3960 Gauß einstellen, um den 88Sr+-Strahl bei einer Beschleunigungsspannung von 8000V mit einem „normalen“ Massenspektrometer zu messen (Radius des
Trennrohres r = 12 Zoll = 30.48cm, m = 87.9056, e = 1).
Ein Multikollektormassenspektrometer ist in Abbildung 20 dargestellt. Es gibt daneben
andere Verfahren, die sich zur Trennung von geladenen Teilchen in speziellen Fällen oder
auch allgemein eignen. Dadurch gehören z.B. die Flugzeitspektrometer, die Ionen unterschiedlicher Masse auf Grund ihrer unterschiedlichen Flugzeit entlang einer vorgegebenen
Strecke trennen, oder die Bahnstabilitätsspektrometer, bei denen die Ionen zum Durchlaufen des Spektrometers bestimmten Stabilitätsbedingungen genügen müssen.
Zu den letzteren gehören die
Quadrupolmassenspektrometer, bei
denen die Massentrennung durch
Schwingung der Ionen in einem hochfrequenten elektrischen Quadrupolfeld erfolgt (Abbildung 21). Das Feld
wird durch vier zylindrische parallele
Stabelektroden erzeugt, an dem an je
zwei sich gegenüberliegende Elektroden eine mit einer hochfrequenten
Wechselspannung überlagerte Gleichspannung angelegt wird. Die in das
Feld eingeschlossenen Ionen führen
senkrecht zu ihrer Flugbahn Schwingungen aus. Bei geeignet eingestellten
Werten der Hochfrequenzamplitude ABBILDUNG 21 Prinzip eines Quadrupolmassenfilters
und der Gleichspannung können nur Ionen bestimmter Massenzahl zum Auffänger gelangen, die im Quadrupolfeld stabil schwingen. Ionen anderer Massenzahl schwingen instabil; ihre Schwingungsamplitude wächst rasch an; sie werden von der Flugbahn abgelenkt
und prallen auf die Stabelektroden. Solche Quadrupolspektrometer eignen sich für die
Analyse von Gasen; sie finden Verwendung z.B. in ICP-MS-Geräten und in Knudsenzellenspektrometern.
26
A. Radiogene Isotopensysteme
In den vergangenen Jahren hat sich eine weitere
Revolution vollzogen,
nämlich die Kopplung von
ICP zur Verdampfung und
Ionisierung der Probe mit
einem Magnetsektormassenspektrometer zur Trennung der Isotope und ihre
Registrierung mittels
Multikollektorsystem
(Abbildung 22). Während
sich Quadrupolmassenspektrometer infolge einer
unzureichenden Peakf o r m ( D a s „ D a c h “ d e s ABBILDUNG 22 Beispiel für ein doppeltfokussierendes ICP-MS
Peaks ist über einen klei- [Plasma 54 von VG Elemental – http://www.thermoelemennen Massenbereich nicht tal.com/]. Der ICP-Teil befindet sich rechts, der Auffänger links.
flach) wenig zur präzisen Bestimmung von Isotopenverhältnissen eignen – zumal bei Verwendung eines Plasmas als Ionenquelle – trifft diese Beschränkung auf die kombinierten
Geräte nicht mehr zu, und sie erreichen fast die Präzision von Thermionenmassenspektrometern. Da da Plasma zudem eine um mehrere tausend Grad höhere Temperatur aufweist
als das Metallbändchen einer Thermionenquelle, lassen sich mittels ICP auch Elemente
effektiv ionisieren, bei denen dies bei der klassischen Massenspektrometrie nicht möglich
ist. Dazu gehören z.B. Hf[18],[19] und W[20].
2.6
Isotopenverdünnungsanalyse
Für eine Altersbestimmung muß gemäß GL 8 sowohl die Anzahl der noch vorhandenen
Atome (oder eine ihr proportionale Größe, z.B. die Konzentration in m/g) des radioaktiven
Mutternuklids als auch die der bereits durch den Zerfallsprozeß entstandenen Tochternuklide bekannt sein. Das läßt sich nach dem Verfahren der Isotopenverdünnungsanalyse
machen. Diese Methode beruht auf der Messung der Isotopenzusammensetzung (oder
mindestens eines Isotopenverhältnisses) eines Elements in einer Mischung. Die Mischung
besteht aus der unbekannten Menge des zu bestimmenden Elementes in der Probe, der
eine exakt abgemessene Menge eines sogenannten Spikes zugefügt wurde. Ein solcher
Spike ist eine Lösung, die ein (selten 2) Isotop(e) des zu bestimmenden Elements hoch
angereichert über dessen Häufigkeit im normalen in der Natur vorkommenden Element
enthält. Z.B. besteht Rb aus den beiden Isotopen mit den Massenzahlen 85 und 87, von
denen das letztere in 87Sr zerfällt. Das Verhältnis von 85Rb zu 87Rb im natürlichen Rb
beträgt 2.593. Als Spike für die Rb-Konzentrationsbestimmung nimmt man i.a. eine RbVerbindung, in der 87Rb mit einem Massenseparator (einem Massenspektrometer) hoch
angereichert wurde, so daß das 85Rb/87Rb-Verhältnis des Spikes nahe Null ist.
Die Formel für die Konzentrationsberechnung läßt sich folgendermaßen ableiten. Man
beschränkt die Betrachtung dabei zunächst auf 2 Isotope des zu bestimmenden Elementes
oder genauer, auf ein Isotopenverhältnis. Die Zahl der Atome des einen Isotops der Probe
A
(vor Zugabe des Spikes) soll mit N Probe
bezeichnet werden, die des zweiten Isotops mit
B
A
B
N Probe
die entsprechende Anzahl der Atome beider Isotope im Spike sei N Spike
und N Spike
,
A
B
die in der Mischung (Probe + Spike) sei N Mix
und N Mix
. Für die Zahl der Isotope gelten
dann die einfachen Massenbilanzgleichungen:
A
A
N Mix
= NPrA obe + N Spike
[GL 35]
27
Einführung
B
B
B
= NPr
und N Mix
obe + N Spike
[GL 36]
Dividiert man beide Gleichungen durcheinander, also:
A
A
A
N Probe
+ N Spike
N Mix
=
B
B
B
N Mix
N Probe
+ N Spike
und schreibt im Zähler für
A
æ N Probe
ö
æ NAö
A
B
B
N
N Probe
= N Probe
=
Probe ç
ç B ÷
B÷
è N Probe ø
è N ø Probe
A
æ N Spike
ö
æ NAö
A
B
B
N Spike
= N Spike
=
N
ç B ÷
Spike ç
B÷
è N ø Spike
è N Spike ø
sowie
dann ergibt sich:
æ NAö
=
ç B÷
è N ø Mix
æ NAö
æ NAö
B
B
N Probe
N
+
Spike
ç B÷
ç B÷
è N ø Probe
è N ø Spike
B
B
N Probe
+ N Spike
Mole Rb
In dieser GleiIllustration der Isotopenverdünnungsanalyse
B
c h u n g i s t N Probe
3.0
2.7
die einzige UnbeRb-85
2.6
2.6
kannte, da das IsoRb-87
topenverhältnis
NA/NB für den
Spike bekannt ist
und für die Probe
2.0
1.6
dem konstanten
irdischen oder
solaren Verhältnis
entspricht * . Das
1
entsprechende
1.0
Ve r h ä l t n i s d e r
Mischung läßt
sich leicht mit
dem Massenspek0.1
trometer messen.
Obige Gleichung
0.0
muß also nur
Mischung
Spike
Probe
B
noch nach N Probe
aufgelöst werden: ABBILDUNG 23 Beispiel einer Isotopenverdünnungsanalyse
* In allen Fällen, in denen das betrachtete Element mindestens zwei natürlich vorkommende Isotope
hat, die weder radioaktiv sind noch radioaktiv gebildet werden, sind die hier abgeleiteten Formeln
gültig, weil das Verhältnis NA/NB der Probe so gewählt werden kann, daß es eine Naturkonstante ist.
Ausnahme ist das Pb, bei dem von vier Isotopen drei durch Zerfall aus U und Th entstehen.
28
A. Radiogene Isotopensysteme
æ NAö
æ NAö
æ NAö
æ NAö
B
B
B
B
N
N
N
N Probe
+
=
+
Spike
Probe
Spike
ç B÷
ç B÷
ç B÷
ç B÷
è N ø Mix
è N ø Mix
è N ø Probe
è N ø Spike
B
N Probe
éæ A ö
æ NAö ù
B
ú
êç N ÷
N Spike
êè N B ø Spike çè N B ÷ø Mix ú
û
ë
=
æ NAö
æ NAö
-ç B÷
ç B÷
è N ø Mix è N ø Probe
[GL 37]
Die Anzahl der A-Atome in der Probe ergibt sich anschließend zu:
æ NAö
A
B
N Probe
= N Probe
ç B÷
è N ø Probe
[GL 38]
Beispiel: Der Aufschluß von 50mg eines Phlogopits wird mit 3g einer Rb-Spikelösung versetzt. Das natürliche Rb besteht aus den beiden Isotopen 85Rb und 87Rb in einem Verhältnis
von 2.593. Das 85Rb/87Rb-Verhältnis des Spikes betrage 0.02047, und der Spike enthalte
1.046´10-8m 87Rb pro g Lösung. (NA/NB)Mix sei 1.200. Da die Konzentrationsangabe m/g
über die Avogadrosche Zahl direkt der Zahl der Atome pro g Lösung proportional ist,
begnügen wir uns mit der Berechnung der Konzentrationen C.
B
C Probe
= 3[ g ] ´ 1.046 ´ 10 -8 [ m / g ] ´
und
0.02047 - 1.200
= 2.657 ´ 10 -8 m
1.200 - 2.593
A
CProbe
= 2.657 ´ 10 -8 ´ 2.593 = 6.890 ´ 10 -8 m
87
Rb
85
Rb
(Umrechnung in N: Ergebnis ´ 6.023´1023 Atome)
A
B
CProbe = CProbe
+ CProbe
= 9.547 ´ 10 -8 m Rb.
Ist die Konzentrationsangabe Prozent oder ppm erwünscht, braucht das Ergebnis nur noch
mit dem Atomgewicht des natürlichen Rb multipliziert zu werden:
CProbe = 9.547´10-8 [m] ´ 85.47 [g/m] = 8.160´10-6g Rb
oder
8.160´10-6[g]/50´10-3[g]´106 = 163.2 ppm.
Die Isotopenverdünnungsmethode ist ziemlich tolerant gegenüber der Menge an zugefügtem Spike, solange nur diese Menge einerseits nicht verschwindend gering gegenüber dem
Isotop in der Probe ist und die Menge in der Probe nicht verschwindend gering gegenüber
dem Isotop im zugefügten Spike. Dies erkennt man, wenn man beide Seiten von GL 37
A
durch N Spike
dividiert und den Zähler auf der rechten Seite ausmultipliziert:
éæ B ö
B
æ NAö
N Probe
êç N ÷
1
=
ç
÷
A
êè N A ø Spike è N B ø Mix
NSpike
ë
ù
æ NAö
æ NAö
ú
ç B÷
ç B÷
è N ø Mix è N ø Probe ú
û
[GL 39]
Wenn die Menge an zugefügtem Spike extrem gering ist, geht der Nenner der Gleichung
gegen 0. Ist die Menge zu groß, ist (NA/NB )Spike » (NA/NB )Mix, und der Zähler geht gegen 0.
Wenn aus demselben Probenaufschluß allerdings sowohl Konzentrationen als auch ein
radiogenes Isotopenverhältnis bestimmt werden sollen, dann darf die Spike-Menge nicht
zu groß werden, weil der Spike in der Regel nicht nur aus einem Isotop besteht. Ein 84SrSpike z.B. wird auch 86Sr und 87Sr enthalten, und dessen Beitrag muß exakt korrigiert werden können, um das 87Sr/86Sr-Verhältnis der Probe zu bestimmen.
29
Einführung
2.7
Datierungsmethoden – allgemeine Bemerkungen
Infolge der unterschiedlichen Halbwertszeiten der Mutternuklide in den verschiedenen
Zerfallssystemen ist klar, daß ihrer Anwendung zur Altersbestimmung Grenzen gesetzt
sind. Zusätzliche Einschränkungen werden durch die Art (Chemismus) der zu datierenden
Gesteine oder Minerale auferlegt sowie durch ihre thermische Geschichte. Mit verschiedenen Isotopensystemen können an ein- und demselben Gestein in Extremfällen sogar
unterschiedliche Ereignisse datiert werden. Das ist besonders einleuchtend bei der FissionTrack-Methode (Kapitel 13.0, Seite 133), die stets die jüngsten Alter liefert, weil die Spaltspuren in einem Mineral schon bei niedriger Temperatur durch Ausheilprozesse verschwinden; daher eignet sich die Methode z.B. zur Rekonstruktion der tektonischen Hebungsgeschichte eines Gesteinskomplexes und der Abtragungsgeschwindigkeit an der
Erdoberfläche. Oft genug stellt aber die Dateninterpretation uns Geowissenschaftler vor
Probleme, und es ist zu hinterfragen, ob ein vermeintlich nicht in einen geologischen Rahmen passendes Alter nicht auf ungeeigneter Probenwahl, ungeeigneter Wahl der Datierungsmethode, Störungen des Isotopensystems oder mangelhafte Feldarbeit beruht. Einem
Alter wird sicherlich eine geologische Bedeutung beigemessen, wenn verschiedene Isotopensysteme (z.B. Rb–Sr und Sm–Nd) innerhalb der Fehler identische Werte liefern.
30
A. Radiogene Isotopensysteme
3.0
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
K gehört zu den Hauptelementen der meisten Gesteine, und es ist das siebthäufigste Element der Erdkruste. Zudem hat 40K eine für die radiometrische Datierung günstige Halbwertszeit, die gut 1/4 des Alters der Erde entspricht. Obwohl damit zwei wesentliche Voraussetzungen für eine weite Anwendbarkeit der beiden Methoden erfüllt sind, erlegen die Art
des Zerfalls von 40K und die chemische Zugehörigkeit des Zerfallsprodukts – 40Ar, ein Edelgasisotop – der Anwendbarkeit einige Restriktionen auf.
Die Radioaktivität des K ist seit 1906 bekannt (gemessen von Campbell & Wood auf Vermutung von J. J. Thomson, 1905). Erst 1935 jedoch gelang es A. O. Nier, das Isotop 40K als
Verursacher der Radioaktivität zu identifizieren. Basierend auf theoretischen Überlegungen
von C.F. von Weizsäcker (1937), gelang Aldrich & Nier 1948 der Nachweis, daß ein Teil des
40
K tatsächlich in 40Ar zerfällt und nicht nur in 40Ca. 88.8% der 40K-Atome zerfallen unter
–
b -Emission in 40Ca, die restlichen 11.2% unter Elektroneneinfang (und 0.001% unter b+Zerfall) in 40Ar (siehe Abbildung 24).
MeV
1.6
d
40K
a
88.8% machen einen b--Zerfall
in den Grundzustand von 40Ca
(Zerfallsenergie 1.32 MeV)
b
0.16% machen einen Elektroneneinfang in den Grundzustand von
40Ar (Zerfallsenergie 1.51 MeV)
c
0.001% machen einen b+-Zerfall
in einen angeregten Zustand von
40Ar (Zerfallsenergie 0.49 MeV)
d
11.0% machen einen Elektroneneinfang in einen angeregten Zustand
40Ar (Zerfallsenergie 0.05 MeV)
1.4
c
1.2
1.0
a
0.8
0.6
b
e
f
0.4
0.2
40Ca
0.0
18
ABBILDUNG 24
19
Ordnungszahl
e f Zerfall der angeregten Zustände
von 40Ar in den Grundzustand
unter g-Emission
20
40
K erleidet einen dualen Zerfall in 40Ar und in 40Ca.
K hat 3 in der Natur vorkommende Isotope, 39K (Häufigkeit 93.2581 ±0.0029%), 40K
(0.01167±0.00004%) und 41K (6.7302±0.0029%). Das Edelgas Ar hat ebenfalls 3 natürlich
vorkommende (stabile) Isotope, deren Häufigkeit in der Atmosphäre folgendermaßen ist:
36
Ar 0.337%, 38Ar 0.063% und 40Ar 99.60%. Daraus ergibt sich ein atmosphärisches 40Ar/
36
Ar-Verhältnis von 295.5. Mehr als 99.9% des atmosphärischen Ar stammen letztlich aus
dem Zerfall von 40K. Die Isotopenzusammensetzung des Ar in Gesteinen ist nicht konstant,
sondern eine Funktion ihres K-Gehaltes, Alters und ihrer thermischen Geschichte.
31
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
3.1
Die K–Ar-Methode
Auf Grund des dualen Zerfalls von 40K muß man 2 Zerfallskonstanten unterscheiden, lb für
den l–-Zerfall in 40Ca und le für den Zerfall unter Elektroneneinfang in 40Ar. Die Addition
beider ergibt die Gesamtzerfallskonstante:
l = lb + le = 5.543´10-10 a-1.
Die derzeit international akzeptierten und verwendeten partiellen Zerfallskonstanten
betragen lb = 4.962´10-10 a-1 und le = 0.581´10-10 a-1. Demgegenüber gibt es aber nur eine
Halbwertszeit:
T = ln2/ l = 1.250 ´109 a.
Von partiellen Halbwertszeiten zu sprechen, ist sinnlos, auch wenn formal in der Zerfallsgleichung mit einer derartigen Größe gerechnet werden kann. Die Zerfallsgleichung GL 8,
auf das K–Ar-System und das K–Ca-System angewandt, lautet:
D = N´(elt – 1)
40
Ar +
40
Ca =
=
le
´
l
(
)
K e lt - 1 =
40
(
le + l b
l
)
K ´ e lt - 1 +
40
lb
l
´
(
)
K ´ e lt - 1
40
´
(
[GL 40]
)
K ´ e lt - 1
40
Hierin stellt der erste Term auf der rechte Seite den Teil des K dar (für ein gegebenes Alter
t), der in 40Ar zerfallen ist, der zweite den Teil, der in40Ca zerfallen ist. Es gilt daher:
le
´ 40K ´ e lt - 1
[GL 41]
l
Im einfachsten aller denkbaren Fälle erhält man das Alter eines Gesteins oder Minerals,
indem man GL 41 nach t auflöst:
40
(
Ar =
t=
æ
1
´ lnç
l
è
40
)
ö
Ar l
´
+ 1÷
K le
ø
40
[GL 42]
Damit dies tatsächlich ein geologisch sinnvolles Alter darstellt, muß eine Reihe von Voraussetzungen erfüllt sein. Die wichtigsten sind:
• Zur Zeit t=0 (magmatisches oder metamorphes Alter) enthielt die Probe kein 40Ar.
• Von t=0 bis heute war die Probe ein geschlossenes System für K und Ar. Das heißt, es
fand keinerlei Austausch von K und Ar mit der Umgebung statt (weder Abgabe noch
Aufnahme).
Wenn diese Bedingungen erfüllt sind, braucht man in einer Probe nur die Konzentrationen
von 40K und 40Ar zu bestimmen, um nach GL 42 das Alter zu berechnen. Für die 40KBestimmung genügt es, den Gesamtkaliumgehalt zu messen, z.B. flammenphotometrisch,
da die Isotopenzusammensetzung des K in der Natur zumindest im Rahmen der erforderlichen Meßgenauigkeit konstant ist. Das gilt selbstverständlich nicht für das Ar. Zur Konzentrationsbestimmung nach der Isotopenverdünnungsmethode muß der Probe ein Spike
zugesetzt werden; dazu wird ein Argongas benutzt, das hoch an 38Ar angereichert ist
(»99.9%). Dieser Spike wird dem Probenargon zugemischt, das durch Erhitzen im Vakuum
– meist bis zum Schmelzen – aus der Probe ausgetrieben wird.
Unter den beiden oben genannten Bedingungen ist die erste in der Regel erfüllt. Als Edelgas wird das Argon strukturell nicht oder zumindest nur sehr schwach im Kristallgitter
gebunden. Daher kann man meist davon ausgehen, daß bei der Gesteinsanatexis eine ArEntgasung des Magmas eintritt, so daß bei der späteren Kristallisation auch kein Ar zum
32
A. Radiogene Isotopensysteme
Einbau in die Minerale zur Verfügung steht. Schon bei mittelgradiger Metamorphose ist die
Entgasung von Mineralen wie Hornblenden oder Hellglimmern oft vollständig – abhängig
von der Metamorphosetemperatur und -dauer. Wenn diese Metamorphite aus Sedimenten
abgeleitet sind, enthalten die Minerale aber oft noch etwas atmosphärisches Argon aus der
sedimentären Vorgeschichte der Probe, was eine Korrektur der gemessenen 40Ar-Menge um
den atmosphärischen Beitrag erforderlich macht. Die geringe Bindung des Ar an die K-haltigen Minerale hat aber auch seine Nachteile. Selbst bei tiefen Temperaturen kann es passieren, daß das in einem K-reichen Mineral entstandene radiogene 40Ar nicht quantitativ
darin verbleibt, sondern teilweise durch Diffusion verloren geht. In anderen K-haltigen
Mineralen desselben Gesteinsverbandes kann dann der gegenläufige Effekt eintreten, daß
sie 40Ar aus der Umgebung aufnehmen. 40Ar-Überschuß wird sogar in gegenüber der Umgebung K-reichen Gesteinen beobachtet. An solchen Mineralen ermittelte Alter hätten keine
geologische Bedeutung. Im ersten Fall ergäbe sich ein zu niedriges, im zweiten Fall ein zu
hohes Alter infolge der Gegenwart von sogenanntem Überschußargon. Zu den Mineralen,
die sich nach allgemeinen Erfahrungen für die K–Ar-Datierung gut eignen, zählen
Amphibole, Biotite und Feldspäte aus vulkanischen Gesteinen sowie Amphibole und Glimmer aus Plutoniten und Metamorphiten. Gesamtgesteine sind meist unbrauchbar mit der
Ausnahme von jungen Vulkaniten, sofern sie vollkommen frisch erhalten sind.
Von einer früheren Arbeitsgruppe der Universität Bern, die sich mit der Problematik der
Datierung der alpinen Metamorphose befaßt hat, wurde in den sechziger Jahren der Begriff
der „Schließungstemperatur“ in die Isotopengeologie eingeführt, nachdem man beobachtete, daß Muskovit und Biotit aus Gesteinen von vermutlich gleich alten Einheiten charakteristische Altersvariationen zeigten, die mit dem Grad der Metamorphose zu korrelieren
schienen[21]. Und zwar sind die K–Ar- und Rb–Sr-Alter von Glimmern aus niedrig metamorphen Gesteinen höher als die aus höher metamorphen Einheiten desselben Komplexes. Es
scheint also eine charakteristische Temperatur zu geben oder, vorsichtiger gesagt, ein Temperaturintervall, unterhalb dessen der Isotopenaustausch mit der Umgebung zum Erliegen
kommt und das Mineral auch über geologische Zeiten als geschlossenes System betrachtet
werden kann.
Das Konzept der Schließungstemperatur beinhaltet, daß die Diffusion der einzige Parameter ist, der diese Temperatur bestimmt. Diffusionsprozesse von Ionen oder Atomen in
Kristallen sind thermisch aktiviert; sie gehorchen oft einer einfachen Arrhenius-Beziehung
des Typs
D = Do ´ e-E/RT
[GL 43]
(D = Diffusionskoeffizient, Do = Diffusionskoeffizient T ® ¥ [cm2/s], T in Kelvin, R = Gaskonstante [cal/(mol´K)], E = Aktivierungsenergie des Diffusionsprozesses [cal/mol]). Auf
Grund dieser exponentiellen Beziehung zwischen Diffusionskoeffizient und Temperatur
wird man annehmen dürfen, daß das Temperaturintervall, innerhalb dessen die Diffusion
praktisch zum Erliegen kommt, gering ist. Nach M.H. Dodson[22] kann die Schließungstemperatur Tc nach der folgenden iterativ zu lösenden Gleichung abgeschätzt werden:
æ -A ´ D ´ R ´ T2 ö
E
c
0
= lnç
÷
.
ç
÷
R ´ Tc
2
è
ø
E ´ T´ a
[GL 44]
Hierin ist A ein dimensionsloser Geometriefaktor (55 für eine Kugel, 27 für einen Zylinder
und 8.7 für eine ebene Schicht), a eine charakteristische Dimension des Korns, entspre.
chend dem Radius im Fall einer Kugel und T = dT / dt die zeitliche Änderung der Temperatur des Gesteins oder Minerals [K/s], bei dieser Anwendung als Abkühlgeschwindigkeit
(negatives Vorzeichen) zu interpretieren. Je rascher ein Gestein abkühlt, desto höher ist
demnach die Schließungstemperatur.
33
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
Die Diffusionskoeffizienten haben
extrem niedrige Werte – »10-14– 10-17
cm 2 /s im Fall der Sr-Diffusion in
Diopsid. Diffusionslängen oder -wege
x können mit Hilfe der Relation
x @ Dt abgeschätzt werden. Daraus
errechnet sich im Fall, daß D=10-15
cm2/s ist, eine Diffusionslänge
x»0.18cm für t = 106a = 3.15´1013s,
d.h. ein Sr-Atom im Diopsid diffundiert pro 106a »0.18cm weit.
1500
Abhängigkeit der
Schließungstemperatur von Diopsid für SrDiffusion von der
Abkühlrate
1400
Schließungstemperatur [8C]
In Abbildung 25 ist der Zusammenhang zwischen Schließungstemperatur und Abkühlgeschwindigkeit am
Beispiel der Sr-Diffusion in natürlichem Diopsid illustriert. Der geologisch relevante Bereich entspricht
Abkühlungsgeschwindigkeiten -dT/
dt von 10 o – 10 4 K/Ma, wofür die
Schließungstemperatur des Diopsids
zwischen »800 und 950°C liegt.
1300
1200
1100
1000
900
800
0
1
2
3
4
5
6
log dT/dt [K/Ma]
7
8
ABBILDUNG 25 Sr-Diffusion in Diopsid: Abhängigkeit
Das Konzept der Schließungstempe- der Schließungstemperatur von der Abkühlgeschwinratur ist in der Folgezeit zunächst digkeit. Die Berechnung der Kurve erfolgte nach der
weitgehend akzeptiert worden.
é 22440
æ dT ö ù
Inzwischen wird aber zunehmend Gleichung:
Tc [ °C] = ê
- logç ÷ ú - 273 . Sie
und auch rigoros Kritik daran geäuè dt ø û
ë 20.9
ßert. Neben der Diffusion werden die beruht auf experimentellen Untersuchungen zur SrDeformation von Gesteinen und Diffusion in natürlichem Diopsid. Angenommen wurMineralen, die eine Rekristallisation de bei den Berechnungen ein Kornradius von 0.2cm
der Minerale verursacht, und die und A=55 (Kugelgestalt des Minerals); die AktivieRolle von Fluiden auf Korngrenzen rungsenergie wurde zu 97 kcal/mol bestimmt, und D
0
für noch wichtiger gehalten. Bei
2
=
54cm
/sec.
Abwesenheit von Fluiden muß
zudem ein anderes Mineral als Reaktionspartner zur Verfügung stehen, und außerdem muß zwischen den austauschenden
Mineralen ein Ladungsausgleich bewerkstelligt werden. Villa [24] macht auf zahlreiche
Widersprüche innerhalb der originalen Kalibrierung der Schließungstemperaturen aufmerksam und auf innere Widersprüche in vielen anderen Studien. So weist er zum Beispiel
auf eine Kompilierung von Altersdaten aus den Zentralalpen hin, die anzuzeigen scheint,
daß Rb–Sr-Alter von Muskoviten höher liegen (Eozän) als U–Pb-Alter von Monaziten (Oligozän). Daraus wurde gefolgert, daß die Schließungstemperatur von Monazit für das U–PbSystem mit ca. 420 °C deutlich unterhalb der für Rb–Sr im Muskovit liegt[25], für die ca. 500
°C angenommen wurde. Villa argumentiert demgegenüber, die Muskovite seien nicht ausschließlich Neubildungen der alpinen Metamorphose und enthielten noch Anteile an herzynischem radiogenem 87Sr, so daß ihre eozänen scheinbaren Alter tatsächlich Mischalter
zwischen herzynisch und alpin seien, während die Monazite Neubildungen der Metamorphose im Oligozän wären. Gut belegt scheint immerhin, daß zonierte Monazite scharfe
Altersunterschiede zeigen, die der Zonierung entsprechen[27]. Das bedeutet, daß die Diffusion während des thermischen Ereignisses, das zur Bildung von Anwachssäumen führte,
nicht rasch genug erfolgte, um die U–Pb-Isotopenunterschiede auszugleichen. Daraus wiederum ergibt sich, daß die Schließungstemperatur des Monazits für die Diffusion von Pb
erheblich über 420 °C liegen muß. Bei der Datierung von Hellglimmern aus grünschieferbis amphibolitfaziellen Metagraniten der Alpen mittels der Ar–Ar-Methode wurde gefun-
34
A. Radiogene Isotopensysteme
den, daß die Anwesenheit von reliktischem Phengit in Hellglimmer einher geht mit ererbtem 40Ar – auch dies ein Hinweis darauf, daß selbst mittelgradige Metamorphosen nicht
unbedingt in der Lage sind, das K–Ar-System von Hellglimmer vollständig auf Null zurückzusetzen[26]. Auf der Basis seiner Neubewertung der zur Verfügung stehenden Literaturdaten gibt Villa[24] für einige Minerale und Isotopensysteme neue Schließungstemperaturen
an (Tabelle 4), die allerdings nur gelten, wenn Ionendiffusion der geschwindigkeitsbestimmende Faktor ist, Fluide nicht vorhanden sind und Rekristallisation nicht stattfindet. Ob
diese Schließungstemperaturen sinnvoll anwendbar sind, muß dann für jede Anwendung
eigens geprüft werden. Die in der Tabelle angegebenen Temperaturen sind z.B. für K–Ar in
Amphibol gegenüber früheren Annahmen unverändert geblieben, während sie für dasselbe
System in den Glimmern um 100 – 150 °C höher liegen.
TABELLE 4:
„Schließungstemperaturen“ [Tc] für einige Minerale und
Isotopensysteme[24]
Mineral
Zirkon
Biotit
Muskovit
Apatit
Amphibol
Muskovit
Titanit
Xenotim
Monazit
Granat
Zerfall
FissionTrack
K–Ar
K–Ar
U–Pb
K–Ar
Rb–Sr
U–Pb
U–Pb
U–Pb
U–Pb
Tc [°C]
350
450
500
500
550 – 650
600 – 650
680
750
770
850 – 1000
Aus diesen Daten läßt sich ablesen, daß – sofern die genannten Voraussetzungen für ihre
Anwendbarkeit auf metamorphe Gesteine erfüllt sind – die Isotopensysteme häufig schon auf
dem Höchststand der Metamorphose eingefroren sein werden. Für Bedingungen der niedrig- bis mittelgradigen Metamorphose sollte eine Datierung dann das Alter liefern, welches
der Kristallisation der für die Altersbestimmung verwendeten metamorphen Minerale ent-
Tiefe [km]
40
50
OP
vor der
Überschiebung
50
OP
40
UP
50
60
gleich nach der
Überschiebung
600
800
40
30
OP
20
5
gestörte Geotherme
Entfernung
0
50
UP
10
0
10
60
15
P [kbar]
Tiefe [km]
30
400
20
0
200
400
600
800
Tiefe [km]
20
200
(b)
100
200
300
400
500
100
200
300
400
500
10
„steady state“Geotherme
UP
0
0
Oberfläche
30
OP
5
900
0
40
10
800
60
60
15
Tiefe [km]
200
300
400
500
600
700
20
30
(a)
UP 100
10
[28]
10
0
T [8C]
20
(c)
20
16
60
40
60
UP
50
P [kbar]
80
12
40
0
10
OP
8
e
30
rm
he
eot
-G
T`
Tiefe [km]
Modell einer Orogenese
.
Eine (rasch ablaufende) Überschiebung verdoppelt die
Mächtigkeit der Kruste (b). Dadurch werden heiße Gesteine
(OP) über kalte (UP) gestapelt.
20 Ma nach dem tektonischen
Ereignis möge Hebung einsetzen (0.35 mm/a), die durch
Erosion an der Ober fläche
kompensiert wird. Dabei beschreiben die Gesteine einen
im Uhrzeigersinn gekrümmten
Druck–Temperatur–Zeit-Pfad
(c). Für die beiden Gesteinspakete UP und OP modelliert
man Pfade, die durch die blauen Kurven dargestellt sind. Die
roten Kur ven entsprechen
Geothermen, wobei die Zahlen
für die Alter in 106a nach dem
tektonischen Ereignis stehen.
Man erkennt, daß tiefere Gesteine ihre maximale Temperatur erst erheblich später erreichen als flacher gelegene. Im
Fall von UP und OP beträgt der
Zeitunterschied rund 30 Ma!
Oberfläche
P [kbar]
0
ABBILDUNG 26 Thermisches
20
4
sich entwickelnde Geothermen
und resultierender P,T-Pfad
0
0
200
400
600
800
10
0
1000
T [8C]
35
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
spricht. Erst bei der hochgradigen orogenen Metamorphose, wenn ein Gesteinspaket lange
Zeit hindurch hohen Temperaturen ausgesetzt bleibt, wäre zu erwarten, daß verschiedene
Minerale und verschiedene Isotopensysteme verschiedene Alterswerte liefern, die Punkten
auf der langsamen Abkühlungskurve des Gesteins entsprechen, also Abkühlalter darstellen.
Systematische Zonierungen der Hauptelemente von Mineralen aus solchen Gesteinen,
einer Temperaturerniedrigung entsprechend, könnten unabhängige Indizien dafür liefern.
Ergänzend sei bemerkt, daß thermische Modelle von Orogenesen zeigen, daß tiefer gelegene Gesteinspakete ihre maximale Temperatur später erreichen als flacher gelegene, wobei
der Altersunterschied leicht einige 107a erreichen kann (Abbildung 26[28]). Wenn Isotopenalter die maximale Metamorphosetemperatur anzeigen, sollten derartige Altersunterschiede häufig auflösbar sein. Andererseits zeigen viele ehemalige hoch metamorphe Komplexe Anzeichen der Anpassung an niedrigere Metamorphosegrade, z.B. durch Bildung von
Amphibolen und Biotiten in basischen Granuliten oder in Eklogiten, belegen also durch
zirkulierende Fluide verursachte chemische Reaktionen unter anderen P–T-Bedingungen.
1400
1200
e
600
er Bi
800
Ho
grob
1000
le
rnb
otit
nd
K-Ar-Alter [Ma]
Nach diesem Exkurs nun zurück
zur K–Ar-Datierung: Die unterschiedliche Eignung verschiedener Minerale sei in Abbildung 27
an einem Beispiel demonstriert,
bei dem K–Ar-Alter von Mineralen aus einem proterozoischen
Gneis an dessen Nähe zu einem
tertiären Plutonit gemessen wurden[16].
Das K–Ar-System wird heute bevorzugt für die Datierung geolo400
gisch junger Gesteine (Meso- bis
Feldspat
känozoisch) eingesetzt. Es ist oft
200
die einzige Methode, mit der das
Eruptionsalter ganz junger
(<107a) Vulkanite ermittelt wer0
den kann. Bei polymetamorphen
1
10
100
1000
10000
Gesteinen wird es die Abkühlung
Abstand vom Kontakt [m]
nach der letzten (mittelgradigen)
Metamorphose datieren oder ein ABBILDUNG 27 Variation der K–Ar-Alter von Mineralen in
Mischalter hin zu einem älteren einem Quarz-Feldspat-Biotit-Gneis nahe dem Kontakt zu
Ereignis. Bei geologisch alten Ge- einem 55 Ma alten Quarzmonzonit (Colorado Front Ransteinen nehmen die Probleme ge/U.S.A.)
von Ar-Entgasung oder Ar-Überschuß zu. Zur Datierung von Metamorphosen ist das nachfolgend beschriebene Ar–Ar-Verfahren besser geeignet. Nichtsdestoweniger hat das K–Ar-System in den 60-er Jahren wesentlich dazu beigetragen, den kanadischen Schild altersmäßig zu gliedern, indem man
acht strukturelle Provinzen unterschied, die jeweils durch eine Orogenese stabilisiert wurden. Als Beispiel sei die K–Ar-Altersstruktur der Grenville-Provinz im Osten Kanadas erwähnt (Abbildung 28[16]). Die Grenville-Orogenese im Jungproterozoikum ist gesichert einer Kollision zweier Kontinentalplatten zuzuschreiben. In der Grenville-Provinz variieren
die K–Ar-Alter systematisch um mehr als 200Ma, wobei die höchsten Alter im Westen an
der Grenze zur älteren Superior-Provinz, in der sich eine Überprägung durch die Grenville
Orogenese nicht mehr nachweisen läßt, gefunden werden. Die großen Altersunterschiede
innerhalb der Grenville-Provinz erklärt man dadurch, daß der westliche Teil früher emporgehoben wurde und damit abkühlte als der Ostrand.
Besondere Bedeutung hat das K–Ar-System für die Kalibrierung der geologischen Zeitskala
des Phanerozoikums gespielt. Sedimente lassen sich leider nur selten absolut exakt datieren, während sie biostratigraphisch sehr fein gegliedert werden können. Die absolute Kali36
A. Radiogene Isotopensysteme
brierung der Zeitskala erfolgte v.a. mit Hilfe von stratigraphisch genau eingeordneten Vulkaniten.
Die 40Ar/39Ar-Methode
Dies ist eine Variation der K–Ar-Methode, die 1966 von C.M. Merrihue & G. Turner vorgeschlagen wurde. Der K-Gehalt der Probe wird hier durch Messen ihres 39Ar-Gehaltes
bestimmt, der durch Bestrahlung in einem Kernreaktor mit schnellen Neutronen durch die
Reaktion 39K(n,p)39Ar produziert wird. 39Ar ist radioaktiv und zerfällt mit einer Halbwertszeit von 269a in 39K. Wegen dieser langen Halbwertszeit darf man das 39Ar als über den Verlauf der Ar–Ar-Isotopenanalyse stabil ansehen.
Steckt man eine Probe in einen Kernreaktor, dann werden viele Kernreaktionen ausgelöst,
vor allem (n,g)- und (n,p)-Reaktionen. Betrachtet man ein einziges Isotop eines beliebigen
Elementes dieser Probe, dann läßt sich die Zahl N der durch eine bestimmte Kernreaktion
gebildeten Nuklide (z.B. durch 39K(n,p)39Ar) nach der Gleichung
N = X ´ Dt ´ ò
¥
E = ET
berechnen, wobei X die Zahl der
Targetkerne ist (z.B. 39K), Dt die
Bestrahlungsdauer (in s), s (E)
der Wirkungsquerschnitt der
Reaktion (cm2) bei Neutronenenergie E und j(E) der Neutronenfluß (n´cm - 2 ´s - 1 ) bei der
Neutronenenergie E; integriert
wird von der Schwellenenergie
der Reaktion ET bis ¥ (oberhalb
von »15MeV geht der Neutron e n fl u ß i m R e a k t o r b e r e i t s
gegen 0). Für die Reaktion
39
K(n,p) 39 Ar) werden schnelle
(=energiereiche) Neutronen
benötigt. Die Zahl der produzierten 39Ar)-Atome erhält man,
indem man in GL 45 für X = 39K
und für N = 39Ar) setzt. Demgegenüber ist die Zahl der durch
den Zerfall von natürlichem 40K
über das geologische Alter t der
Probe gebildeten 40 Ar-Atome
gegeben durch GL 41:
Ar = le /l ´ 40K ´ (elt – 1).
40
s ( E) ´ j ( E) ´ dE
[GL 45]
1175
1 10
10 0
10 5
0
0
1125
1075
Gr
nv i
940
ll e
Fr
950
960
955
950
1095
965
950 900
870
935
t
on
0
930
1070
e
3.2
830
880
940
850
920
0
100
200
Meilen
895
ABBILDUNG 28 Metamorphosealter (in Millionen Jahren)
der Grenville-Provinz im Osten von Kanada, basierend auf
Dividiert man beide Gleichun- K–Ar-Daten granitischer Gneise
gen durcheinander, dann erhält
man:
40
Ar le
=
´
39
l
Ar
40
K 1
´
´
39
K Dt
e lt - 1
òE s ( E) j ( E) dE
[GL 46]
Mit dieser Formel läßt sich leider nicht direkt rechnen, vor allen Dingen, weil örtliche und
zeitliche Variationen des Neutronenflusses in der Bestrahlungseinrichtung eines Reaktors
nicht genau genug bekannt sind. Man kann sich jedoch damit behelfen, daß man zusammen mit den Proben bekannten Alters mehrere Proben eines Flußmonitors bestrahlt. Das
37
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
ist ein Mineral, dessen K–Ar-Alter man genau kennt. Zur Auswertung zieht man dann aus
GL 46 einen probenspezifischen Parameter J heraus, den man als
J=
l
´
le
39
40
K
´ Dt ´ ò s ( E) j ( E) dE
E
K
[GL 47]
definiert und bestimmt die J-Werte für die Flußmonitore aus Gleichung GL 46 zu
e lt - 1
Ar /39Ar
[GL 48]
40
wobei t das exakt bekannte Alter des
Minerals ist, das als Flußmonitor dient.
40
Ar ist das Argon, das während des geologischen Alters des Flußmonitors aus dem
Zerfall von 40 K entstanden ist, 39 Ar das
radioaktive Argon, das während der Reaktorbestrahlung des Flußmonitors aus dem
39
K entstanden ist. Ein Beispiel für die
Ermittlung der J-Werte ist in Abbildung 29
gegeben[29]. Das 40Ar/39Ar-Verhältnis wird
dann nach Austreiben aus der Probe
durch einen Schmelzaufschluß massenspektrometrisch bestimmt. Die örtliche
Variation des Neutronenflusses im Reaktor erfaßt man dadurch, daß man mehrere
Proben des Flußmonitors mit den Proben
zusammen bestrahlt. Man erhält auf diese
Weise für die Flußmonitore einen Satz
von J-Werten, aus denen man das für jede
der Proben unbekannten Alters spezifische J interpolieren kann. Das Alter dieser
Proben resultiert dann durch Auflösen
von GL 48 nach t.
1
Position in der Bestrahlungskapsel
J=
Flußmonitor 1
2
3
Flußmonitor 2
4
5
6
Ermittlung von J bei
Ar-Ar-Analysen
7
Flußmonitor 3
8
1.8
2
2.2
2.4
J310-2
ABBILDUNG 29 Ermittlung des Faktors J bei Ar–
Der Vorteil der Ar–Ar- über die konventio- Ar-Analysen
nelle K–Ar-Methode liegt darin, daß man
das Alter einer Probe an exakt derselben Teilprobe durch Messung eines einzigen Isotopenverhältnisses erhält. Man umgeht dadurch die Probleme, die durch eine inhomogene Verteilung von K und Ar in der Probe resultieren; zumindest wenn nur kleine Probenmengen
vorhanden sind, muß beim Teilen dieser Probe in solchen Fällen mit Fehlern gerechnet
werden. Andererseits darf nicht übersehen werden, daß die Ar–Ar-Methode sehr aufwendig
ist. Man braucht außer einem Massenspektrometer noch Zugang zu einem Reaktor; die
Proben müssen eine hohe Neutronendosis empfangen, damit das 40Ar/39Ar-Verhältnis
nicht so groß ist, daß sich meßtechnische Probleme (durch Nichtlinearität des Digitalvoltmeters des Massenspektrometers) ergeben (Günstig sind Werte zwischen »0.01 und 100).
Dadurch werden die Proben stark radioaktiv und sind unangenehm zu handhaben. Bei der
Reaktorbestrahlung selbst finden unerwünschte Nebenreaktionen statt, für die Korrekturen anzubringen sind, z.B. 42Ca(n,a)39Ar, 40K(n,p)40Ar, 41K(n,d)40Ar und 40Ca(n,n+a)36Ar.
Die letzt genannte Reaktion stört die Korrektur, die meistens für die Anwesenheit atmosphärischen Argons in den Proben durchzuführen ist, nach:
æ
ç
è
38
40
æ
Ar ö
=ç
÷
39
Ar ø Probe è
40
æ 36 Ar ö
Ar ö
295
.
5
´
÷
ç 39 ÷
39
Ar ø gemessen
è Ar ø gemessen
[GL 49]
A. Radiogene Isotopensysteme
wobei der Faktor 295.5 das 40Ar/36Ar-Verhältnis der Atmosphäre ist. Schließlich müssen bei
sehr feinkörnigen Proben (<1µm) bei der Reaktorbestrahlung selbst Rückstoßeffekte in
Betracht gezogen werden, welche die 39 Ar-Atome durch die (n,p)-Reaktion erleiden,
wodurch sie aus den Mineralkörnern entweichen können. Alles in allem wundert man sich
fast, daß die Ar–Ar-Methode ebenso verläßliche Daten liefert wie die K–Ar-Methode.
30
1800
Ar-Entgasungsverhalten eines
Granitxenoliths in Basalt
(Sierra Nevada, Kalifornien)
1400
1200
1000
r
ratu
pe
Tem
800
600
Alt
er
1
Plateaualter (entspricht dem
Eruptionsalter des Basalts)
Temperatur [8C]
scheinbares Alter [Ma]
10
1600
400
200
0.1
0
0
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
1
kumulativer Anteil des entgasten 39Ar
ABBILDUNG 30
ungewöhnliches Entgasungsverhalten eines Xenoliths aus einem Basalt
Ar–Ar-Datierungen werden meistens nach der Methode des stufenweisen Ausheizens
durchgeführt. Dabei wird das Argon in mehreren Stufen aus der Probe ausgetrieben, wobei
die Temperatur schrittweise (z.B. in 200°C-Schritten) bis zur Schmelztemperatur (oder bis
kein Argon mehr entweicht) erhöht wird. Die Ar-Isotopien werden bei jedem Schritt
gemessen, korrigiert, und ein Alter wird berechnet. Idealerweise sollten die Alter für jeden
Ausheizschritt identisch sein. Wenn das der Fall ist, dann werden das Ar–Ar- und das K–ArAlter identisch sein. Die Stärke des Ar–Ar-Systems liegt aber darin, daß man auch für
gestörte Systeme, bei denen das K–Ar-System versagt, noch verläßliche Daten erhalten
kann. Für solche Proben beobachtet man Alter, die zunächst steigen oder fallen und sich
erst bei höheren Ausheiztemperaturen auf ein konstantes Niveau einpendeln, das Plateaualter, das als das wirkliche Alter angesehen wird. Das bei tiefen Temperaturen abgegebene
Ar stammt bevorzugt aus den Randpartien der Minerale oder ist das am schwächsten
gebundene Ar. Die zu niedrigen Alter dieses bei tiefen Temperaturen abgegebenen Argons
kommen bei K-reichen Mineralen dadurch zustande, daß 40Ar aus den äußeren Bereichen
der Minerale entweicht – bei retrograden Metamorphosen z.B. oder infolge von Diffusionsprozessen bei „normalen“ Temperaturen in der Kruste; infolgedessen haben diese Zonen
ein für ihr Alter zu niedriges 40Ar/K- (und nach der Reaktorbestrahlung 40Ar/39Ar) Verhältnis. Zu hohe Alter des bei tiefen Temperaturen ausgetriebenen Argons treten bevorzugt
(aber bei weitem nicht nur) bei K-armen Mineralen auf, bei denen die Randbezirke 40Ar
durch Diffusion von „außen“ aufgenommen haben – z.B. aus benachbarten K-reichen
Mineralen; dadurch haben diese Zonen ein zu hohes 40Ar/K. Ein Beispiel für ein Plateaualter ist in Abbildung 30 für einen »100Ma alten Granitxenolith in einem »100000a alten
Basalt angeführt[30]. Bei niedriger Temperatur entgast zunächst ein Argon, das einem höheren als dem Eruptionsalter des Wirtsbasalts entspricht. Dieses locker „gebundene“ Ar
gelangte offensichtlich durch junge Diffusion in den Xenolith. Bei mittleren Temperaturen
39
Das K–Ar-Zerfallssystem (K–Ar- und Ar–Ar-Methoden)
zwischen ca. 500 und 1000 °C entgast dann ein großer Teil des gesamten Argons, für das
sich ein scheinbares Alter ergibt, das dem der Eruption des Wirtsbasalts entspricht. Bei
Temperaturen oberhalb 1000 °C entweicht dann ein immer noch erheblicher Anteil von
Argon, das einem höheren Alter entspricht; dabei handelt es sich sicherlich um Ar, das seit
der magmatischen Kristallisation des Granits gebildet wurde und das bei der Aufnahme des
Xenoliths durch den Basalt und während des raschen Transportes an die Erdoberfläche
nicht vollständig entgaste.
scheinbares Alter [Ma]
Eine neue Entwicklung der
2500
Ar-Isotopengeochemiker,
ermöglicht durch die VerEntstehungsalter
fügbarkeit einer Generation
hochempfindlicher Mas2000
senspektrometer, ist das
Laserverfahren [31] . Dabei
wird durch Laserbestrahlung ein Teil eines Mineral1500
korns verdampft. Das Ar
entgast und kann massenspektrometrisch gemessen
1000
werden. Auf diese Weise
kann man Altersprofile
über einzelne Mineralkörner gewinnen[32] und erhält
500
Informationen, die man
Eruptionsalter (394«2 Ma)
durch die normale Ar–ArKornzentren
Analyse nur vermuten
kann. So zeigt sich z.B., daß
0
man für Phlogopite aus
0
100
200
300
400
500
600
700
Xenolithen, die in KimberAbstand
vom
Rand
[
m
m]
liten innerhalb von vielleicht Tagen aus dem Erdmantel an die Erdoberflä- ABBILDUNG 31 Scheinbare Ar–Ar-Alter von drei Phlogopitkörche gelangt sind, in den nern aus einem krustalen Xenolith, der in einem Lamprophyr
Kernen noch Alter identifi- transportiert wurde (Kola-Halbinsel)
zieren kann, die dem Alter
ihrer Bildung entsprechen, während die Ränder Alter ergeben, die dem Eruptionsalter des
Kimberlits gleich sind (Abbildung 31[33]), obwohl die Temperaturen der Kimberlitmagmen
viele hundert Grad über der Schließungstemperatur der Glimmer liegen. Dies mag aber
auch darin begründet sein, daß in den Xenolithen die Phlogopite die einzigen K-Minerale
sind und unter allen Mineralen für Ar den höchsten „Verteilungskoeffizienten“ aufweisen,
so daß der Phlogopit selbst bei 1000 °C effektiv ein geschlossenes System darstellt.
Wie komplex die Altersinformationen sein können, die sich aus den Ar–Ar-Analysen eines
einzigen porphyroblastischen Muskovit-Kristalls aus einem polymetamorphen Glimmerschiefer aus dem Nordosten der USA ergeben, ist in Abbildung 32 dargestellt[34]. Der Glimmerschiefer ist während der Grenville-Orogenese zwischen ca. 1.1 und 0.8 Ga entstanden
und wurde von zwei jüngeren Metamorphosen und Deformationen erfaßt, denen die Bildung feinkörnigerer Hellglimmer und von Chloritoid zugeschrieben wird und damit eine
Wiederaufheizung auf rund 400 – 500 °C. Dennoch haben große Partien des porphyroblastischen Muskovits noch hohe Alter bewahrt, die auf eine Bildung während der GrenvilleOrogenese hindeuten. Die Diffusion bei diesen Temperaturen war offensichtlich nicht
effektiv genug, um das radiogene Argon aus dem Innern des Kristalls nach außen zu transportieren, was höhere „Schließungsalter“ als früher angenommen für Muskovit anzeigt
(vergleiche auch Diskussion auf Seite 33 bis Seite 36. Allerdings erscheint die Altersverteilung der Meßpunkte innerhalb des Kristalls nicht sonderlich systematisch.
40
A. Radiogene Isotopensysteme
397
0]
[01
934
470
551
842
800
789
1 mm
884
446
SM
838
708
855
426
680
818
720
462
892
967
600
500
638
T
893
897
85
887
0
840
790
Wachstumskante
ABBILDUNG 32
700
400
863
988
6
901
46
519
868
Alter [Ma]
418
900
[110]
914
794
max
G
709
min
A
300
1000
„Kern“
750
„Rand“
500
250
0
Entfernung [mm]
Links: Zeichnung eines Muskovit-Porphyroblasts; die feinen Linien stellen
Risse dar. Mit „SM“ sind einige bei der Analyse entstandenen Risse ausgewiesen, die Schlagspuren entsprechen. Die mit dem Laser erzeugten Krater
sind farblich ausgewiesen, wobei die Zahlen dem Alter in Ma entsprechen.
In den dunkleren (grünen) Farben sind Krater mit Altern > 750 Ma dargestellt, in den helleren (gelben) Farben Krater, für die jüngere Alter gemessen
wurden. Die jüngeren Alter treten entlang den deformierten Ecken des Kristalls auf und an einem großen Riß, der quer durch den Kristall verläuft. Die
hohen Alter kommen im Innern des Kristalls vor und entlang der Wachstumskanten unten. Rechts: Graphische Darstellung der Alter als Funktion
des Abstandes Kornmitte – Kornrand. Mit G, T und A sind drei Metamorphosen in Nordamerika bezeichnet: Grenville, Taconian, Acadian.
41
Das Rb–Sr-Isotopensystem
4.0
Das Rb–Sr-Isotopensystem
Grundlage dieses Isotopensystems ist der Zerfall von 87Rb in 87Sr unter Aussendung eines
b–-Teilchens. Als international akzeptierte Zerfallskonstante gilt derzeit ein Wert von
1.42´10-11 a-1. Vor 1977 waren sowohl 1.39´10-11a-1 als auch 1.47´10-11a-1 in Gebrauch.
Entsprechende Umrechnungen sind daher beim Vergleich älterer Literaturdaten vorzunehmen! Der wahre Wert der Zerfallskonstante könnte noch geringfügig niedriger liegen als
1.42´10-11 a-1. Diese Unsicherheiten sind darauf zurückzuführen, daß der Zerfall von 87Rb
nur von einer Zerfallsenergie von 275KeV begleitet wird, was die Messung der spezifischen
Aktivität schwierig macht.
Rb als Alkalimetall und Sr als Erdalkalimetall verhalten sich geochemisch sehr unterschiedlich und können daher bei magmatischen, metamorphen und selbst sedimentären Prozessen stark fraktionieren, was sich in einer extremen Variation der Rb/Sr-Verhältnisse zwischen fast 0 (z.B. in manchen ultrabasischen und basischen Gesteinen) und >2 äußert
(insbes. in sauren Magmatiten). Da bei der magmatischen Differentiation der generelle
Trend einer Erhöhung des Rb/Sr-Verhältnisses zu beobachten ist, eignet sich das Rb–SrSystem vor allen Dingen zur Datierung von sauren und intermediären Magmatiten und
Metamorphiten.
TABELLE 5:
Typische Rb- und Sr-Konzentrationen einiger Gesteinstypena
Gesteinstyp
Peridotit
Tholeiit
Alkalibasalt
Ca-reicher Granit (Granodiorit)
Ca-armer („normaler“) Granit
Tonschiefer
Tiefseeton
Sandstein
Karbonat
Gew.-ppm Rb
<0.2
1
50
110
170
140
110
50
3
Gew.-ppm Sr
10
100
800
500
100
250
180
50
600
a. Diese Werte können nur als grobe Hinweise gelten und tatsächlich in jedem
Gesteinstyp um ein Mehrfaches schwanken
Grundlage der Datierung ist auch wiederum die modifizierte Zerfallsgleichung GL 8:
(
)
D = N e lt - 1 ,
die für das Rb–Sr-System lautet:
87
Sr =
(
)
Rb e lt - 1
87
Anders als beim K–Ar-System kann man jedoch hier nicht davon ausgehen, daß zur Zeit t
= 0 in dem Gestein oder Mineral kein 87Sr vorhanden gewesen ist. 87Sr ist ja ein Isotop des
natürlichen Sr, das als Spurenelement bei der Bildung von Gesteinen bereits in mehr oder
weniger größeren Mengen vorhanden ist (siehe Tabelle 5). Das zur Zeit t = 0 schon vorhandene 87Sr soll im folgenden als 87Sro bezeichnet werden (Es wird auch als 87Sri bezeichnet,
wobei i für initial steht). Damit ergibt sich:
87
87
42
Srgesamt =
Srgesamt =
87
87
Sr0 +
Sr0 +
87
Srradiogen
(
)
Rb e lt - 1
87
[GL 50]
A. Radiogene Isotopensysteme
Wie schon GL 37 der Isotopenverdünnungsanalyse zeigte, mißt man in der Massenspektrometrie stets Isotopenverhältnisse und nicht die Anzahl der Atome eines Isotops. Als
Bezugsisotop wählt man dabei eines, das stabil ist und das auch nicht aus einem Zerfallsprozeß gespeist wird, d.h. dessen Anzahl in der Probe seit ihrer Bildung konstant geblieben
ist oder zumindest sein sollte. Beim Sr kämen dafür prinzipiell die Isotope 84Sr, 86Sr und 88Sr
in Frage. Konventionell benutzt man 86Sr, weil es in den meisten Proben ähnlich häufig ist
wie 87Sr, so daß man keine unhandlich großen (wie im Fall von 87Sr/84Sr) oder kleinen Verhältnisse (87Sr/88Sr) erhält. Dividiert man GL 50 durch 86Sr, dann ergibt sich:
87
86
Sr æ
=ç
Sr è
87
86
Sr ö
÷ +
Sr ø 0
87
Rb lt
e -1
Sr
86
(
)
[GL 51]
Diese Gleichung ist die Grundlage für alle Altersbestimmungen nach der Rb–Sr-Methode.
Nach Ersetzung durch die jeweiligen Isotopenverhältnisse gilt sie analog auch für Isotopensysteme wie Sm–Nd, Lu–Hf, Re–Os oder K–Ca. Diese Gleichung ermöglicht eine zweifache
Anwendung des Rb–Sr-Systems in Geo- und Kosmochemie, (a) als Mittel der Altersbestimmung, und (b) bei Kenntnis des Alters eines Gesteins dient der (87Sr/86Sr)o-Wert als Tracer zur
Aufklärung von petrogenetischen Prozessen.
4.1
Das Rb–Sr-System als Mittel der Altersbestimmung
In GL 51 stehen zwei Verhältnisse, die man messen kann, nämlich 87Sr/86Sr, das direkt aus
der massenspektrometrischen Analyse resultiert und 87Rb/86Sr, das mit Hilfe der Isotopenverdünnungsanalyse gemessen werden kann. Da mit (87Sr/86Sr)o und t aber zwei unbekannte Größen verbleiben, ist obige Gleichung für eine einzige Probe nicht zu lösen. Die
Gleichung ist dagegen lösbar, wenn man eine Serie (mindestens zwei) von genetisch
zusammengehörenden Proben analysiert – z.B. mehrere Minerale aus dem Handstück eines
magmatischen Gesteins oder mehrere Proben, aus verschiedenen Partien eines Gesteinskörpers entnommen. Man muß dabei voraussetzen, daß alle Proben der Serie
• zur selben Zeit aus einem homogenen Material entstanden sind – dann war zur Zeit t=0
das (87Sr/ 86Sr)o für alle Proben identisch – und
• daß im Anschluß an den Zeitpunkt t=0 jede der Einzelproben ein geschlossenes System
war, d.h. es erfolgte kein Elementaustausch mit der Umgebung; – bei der Abkühlung eines Granits z.B. wird bei irgendeiner Temperatur jeglicher Austausch von Sr und Rb
selbst im Mineralkornbereich zum Erliegen kommen.
Wenn diese Voraussetzungen erfüllt sind, läßt sich GL 51 als Geradengleichung der Form
Y = a + bx
auffassen, wobei x das für eine Probe gemessene 87Rb/86Sr ist und Y das aus der Geradengleichung errechnete 87Sr/86Sr and der Stelle x. Jedes Datenpaar (87Rb/86Sr, 87Sr/86Sr) bildet in
einem x–y-Diagramm einen Punkt auf (oder nahe) einer Geraden mit der Steigung (elt – 1),
aus der sich das Alter errechnen läßt. Der Schnittpunkt der Geraden mit der y-Achse ergibt
(87Sr/86Sr)o, den sogenannten Initialwert. Die Gerade heißt Isochrone, weil jede Probe auf
ihr das gleiche Alter hat. Das Diagramm heißt Isochronendiagramm oder gelegentlich nach
seinem Erfinder auch Nicolaysen-Diagramm. Im strengen Sinn kann man von einer Isochrone nur dann sprechen, wenn alle Probenpunkte innerhalb der experimentellen Fehler
darauf liegen. Vielfach wird aber die Bedingung „(87Sr/86Sr)o = identisch für alle Proben“
nicht erfüllt sein. Bei einem Granitpluton wird man z.B. nur selten davon ausgehen dürfen, daß das Magma ursprünglich völlig homogen war, da infolge der hohen Viskosität granitischer Magmen eine effektive Durchmischung nicht stattfinden kann. An den Rändern
des Plutons kann es zudem zur Aufschmelzung von und damit zur Kontamination durch
Nebengestein kommen. Eine derart verursachte zusätzliche Variation ist daher nicht
immer Anzeichen einer späteren Störung des Rb–Sr-Systems. Liegen von einer Serie die
meisten der als kogenetisch erachteten Proben nicht auf der Geraden, dann wird die Isochrone zu einer den Geochronologen höchst unbefriedigenden „errorchron“. Beispiele für
43
Das Rb–Sr-Isotopensystem
Isochrone und „errorchron“ sind in den Abbildungen 33 und 34 angegeben. Ob dem Alter,
das aus der Steigung der „errorchron“ resultiert, eine geologische Bedeutung zukommt,
muß von Fall zu Fall beurteilt werden. Die Versuchung, einer derart schlecht definierten
Geraden eine Altersrelevanz zuzusprechen, ist besonders groß bei Xenolithen der tiefen
Kruste und des oberen Erdmantels. Bei solchen Proben fehlt die stratigraphische Kontrolle,
und daher kann nur auf Grund von geochemischen und petrologischen Daten gemutmaßt
werden, ob die Xenolithe einer Serie kogenetisch sein können oder nicht.
87Sr/86Sr
Es dürfte unmittelbar
0.7052
einsichtig sein, daß ein
Sr-Isochronendiagramm für einen
Isochronenalter umso
Eklogit (Münchberger Gneisgebiet)
vertrauenswürdiger ist,
Phengit
je größer die Probense0.7048
rie ist und je mehr Daa
tenpunkte einer Pro6M
1
±
3
benserie auf der Iso39
t=
chrone liegen. Durch
0.7044
zwei Datenpunkte läßt
sich natürlich immer
Gesamtgestein
Granat
eine Gerade legen, und
Amphibol
0.7040
die Interpretation von
CpxI, II
Zweipunktgeraden als
Isochronen ist häufig
87Sr/86Sr) = 0.703952±0.000016
0
a n f e c h t b a r, z u m a l
0.7036
dann, wenn darauf
0
0.04
0.08
0.12
0.16
0.20
großartige Interpreta87
86Sr
Rb/
tionen aufgebaut werden sollen, die anderweitig nicht gestützt ABBILDUNG 33 Beispiel für eine Rb–Sr-Isochrone: Eklogit aus Münchsind.
berger Gneisgebiet
87Sr/86Sr
Die Konstruktion einer
0.7100
Isochrone erfolgt im
Schema einer „Errorchron“
einfachsten Fall durch
eine Geradenanpassung
mittels linearer Regression. Das Wesen der
0.7075
einfachen linearen
Regression ist es, Fehler
nur in einer Richtung
(meist y) und zudem
alle Fehler als gleich
groß anzunehmen. Dies
0.7050
sind jedoch keine sehr
sinnvollen Annahmen,
da sowohl das Rb/Sr- als
auch das 87 Sr/ 86 Sr-Verhältnis mit Meßfehlern
behaftet sind, die meist
0.7000
voneinander verschie0.0
0.2
0.4
0.6
0.8
1.0
1.2
den sind – in diesem
87Rb/86Sr
Fall ist der Fehler im
Rb/Sr in der Regel
ABBILDUNG 34 Bei einer „errorchron“ liegen die meisten Daten
erheblich höher als der
nicht auf der Geraden.
im 87 Sr/ 86 Sr, weil sich
der Rb-Gehalt nicht sehr präzise bestimmen läßt.
44
A. Radiogene Isotopensysteme
Zur Konstruktion von Isochronen liegen seit den späten sechziger Jahren des 20. Jahrhunderts Ansätze vor, die Fehler sowohl in x- als auch in y-Richtung berücksichtigen[35],[36].
Nach York (1969[36]) und detailliert ausgeführt bei Kullerud (1991)[37] berechnet sich die
Steigung der Isochrone zu
b=
å Wi (yi - Y ) [s y2 (xi - X ) + s x2 b (yi - Y )]
i
i
i
å Wi (xi - X ) [s y2 (xi - X ) + s x2 b (yi - Y )]
i
i
[GL 52]
i
und der Schnittpunkt mit der y-Achse (Initialwert) zu
a = Y - bX
[GL 53]
87
86
87
und
å Wi yi
Y = i
å Wi
86
Darin sind xi und yi die Meßwerte (z.B. Rb/ Sr und Sr/ Sr). X und Y stehen für die
gewichteten Mittel (Zentroide) der Regressionsgerade bezüglich x und y, errechnet zu
å Wi xi
X= i
å Wi
i
[GL 54]
i
s xi und s yi sind die analytischen Fehler für jeden Datenpunkt i bezüglich x und y. Wi
steht für die Gewichtung, die dem Datenpunkt i beigemessen wird:
Wi =
1
b
2
s x2i
[GL 55]
+ s y2i
Datenpunkte mit kleinen Fehlern werden folglich bei der Regression höher gewichtet als
solche mit großen Fehlern. Die Steigung b der Isochronengleichung läßt sich iterativ mit
der gewünschten Genauigkeit aus GL 52 ermitteln; darin sind für X und Y die Definitionen nach GL 54 in GL 52 einzusetzen. Die Iteration führt in wenigen Schleifen zum Ziel,
wenn der iterierte b-Wert als neuer Schätzwert für b verwendet wird. Anschließend läßt
sich der Initialwert nach GL 53 berechnen. Die beste Gerade ist die, für welche der nachfolgend definierte MSWD-Wert sein Minimum erreicht. Die Fehler in der Steigung und im
Initialwert ergeben sich ungefähr zu
sb = ±
1
å Wi (xi - X )
i
2
und s a = ±s b
å Wi xi2
i
å Wi
[GL 56]
i
Der Fehler in der Steigung ist demnach abhängig vom Fehler, der den Daten in x- und yRichtung zugewiesen wird (über Wi), und von der Verteilung der Datenpunkte entlang der
Geraden relativ zum Zentroid (über (xi – X )2), nicht aber davon, wie gut die Datenpunkte
auf der Isochrone liegen. Dagegen variieren die „expandierten Fehler“
exp
sb
= s b MSWD und s aexp = s a MSWD
[GL 57]
über den MSWD-Wert mit der Güte, mit welcher die Daten auf der Isochrone liegen –
genauso wie bei einer einfachen x–y-Regression. Der Parameter „MSWD“ (mean standard
weighted deviation) wird häufig verwendet, um die Qualität der Regression zu beurteilen; er
ist definiert als:
45
Das Rb–Sr-Isotopensystem
å Wi Di2
i
MSWD =
[GL 58]
n-2
dabei entspricht Di dem Abstand des Datenpunktes i von der berechneten Regressionsgeraden in y-Richtung:
(
Di = yi - a + b xi
Falls die analytischen Fehler normalverteilt sind und falls die gesamte
Streuung der Daten um die Regressionsgerade allein auf Analysenfehler
zurückgeführt werden kann, sollte
MSWD mit 95%iger Wahrscheinlich-
)
3.0
2.5
MSWD
keit in einen Bereich 1 ± 2 (n - 2) fal2.0
len, wobei n der Anzahl an Analysendaten entspricht[39],[38]. MSWD-Werte, die
1.5
erheblich größer sind, zeigen eine darüber hinausgehende Streuung der
Daten an – die Isochrone wird damit
1.0
zur errorchron – oder vielleicht auch,
daß die Analysenfehler unterschätzt
wurden. In Tabelle 6 ist für einen syn0.5
thetischen Rb–Sr-Datensatz [ 3 7 ] der
350
351
352
353
354
355
MSWD-Wert als Beispiel ermittelt und
Alter [Ma]
in Abbildung 35 als Funktion des Alters
aufgetragen worden. Der errechnete
Wert von 0.76 liegt knapp oberhalb des ABBILDUNG 35 Abhängigkeit des MSWD-Wertes
von der Zeit für den Datensatz in Tabelle 6. Der
Intervalls von 1 ± 2 (7 - 2) = 1 ± 0.63 . minimale MSWD-Wert liefert das „beste Alter“ der
Dennoch dürfte die Annahme gerecht- Isochrone.
fertigt sein, daß die Streuung der
Datenpunkte um die beste Gerade durch die Analytik erklärt werden kann und daß die
Gerade als Isochrone angesehen werden darf.
Beispiel für die Berechnung von MSWD für einen Datensatza
TABELLE 6:
Probe (i)
87
Rb/86Sr
s-87Rb/86Sr
87
Sr/86Sr
s-87Sr/86Sr
Wi
Di
Wi D2i
1
0.503
0.0025
0.72240
0.00002
1.789E+09
-0.00001
0.045
2
5.959
0.0298
0.74991
0.00002
4.400E+07
0.00014
0.918
3
6.981
0.0349
0.75504
0.00002
3.222E+07
0.00015
0.718
4
7.989
0.0399
0.75970
0.00002
2.468E+07
-0.00025
1.488
5
8.961
0.0448
0.76466
0.00002
1.965E+07
-0.00016
0.503
6
10.043
0.0502
0.77033
0.00002
1.567E+07
0.00008
0.111
7
99.725
0.499
1.21968
0.00002
1.599E+05
-0.00030
0.014
MSWD:
0.759
a. Initialwert a der Regressionsgerade ist 0.71988±0.00003; Alter ist 352.3±0.8 Ma, woraus für die
Steigung b ein Wert von 0.005015 resultiert. Für dieses Alter ergibt sich ein minimales MSWD
oder auch ein minimales S = å Wi Di2 .
i
Der MSWD-Wert kann allerdings nicht uneingeschränkt als Maß für die Qualität einer
Regressionsgerade angesehen werden. Insbesondere ist MSWD vom Alter der Proben und
46
A. Radiogene Isotopensysteme
vom Mutter/Tochter-Elementverhältnis abhängig[38], wie durch eine Betrachtung des
Gewichtungsfaktors (GL 55) abgeschätzt werden kann. In vielen Fällen ist der analytische
Fehler für x (Mutter/Tochter) erheblich größer als für y. So liegt z.B. ein typischer Fehler im
87
Rb/86Sr bei mindestens ±0.5% des Meßwertes, während der Fehler im 87Sr/86Sr nur ca.
±0.00002 bis ±0.00003 (einige 10 ppm des Meßwertes) beträgt. Daraus ergibt sich, daß
bereits nach geologisch kurzer Zeit und schon für mäßig hohe Rb/Sr-Verhältnisse der Fak2 2
2
tor b s xi gegenüber s yi dominiert. Wi wird mit steigendem Alter – und auch mit steigendem Mutter/Tochter-Verhältnis – kleiner und MSWD damit ebenfalls. Aus einer ursprünglich beträchtlichen Streuung der Daten um die Regressionsgerade über die analytischen
Fehler hinaus kann somit allein durch Alterung eine Regressionsgerade mit einer geringeren Streuung entstehen. Anders gesagt: eine Streuung der Daten, die bei geologisch jungen
Proben als Hinweis auf Probeninhomogenität gedeutet würde, könnte in geologisch alten
Proben allein der Analytik zugeschrieben werden.
Für das Mutter/Tochter-Verhältnis, z.B. 87Rb/86Sr, nimmt man in der Regel als analytischen
Fehler einen prozentualen Anteil des Meßwertes an, z.B. 0.5%; demgegenüber ist der Fehler
in einem Isotopenverhältnis wie 87Sr/86Sr kaum von seiner Höhe abhängig, sondern in
erster Näherung konstant. Aus GL 52, Seite 45 läßt sich dann ablesen, daß die Regression
über den Faktor Wi die Datenpunkte mit niedrigem Mutter/Tochter-Verhältnis höher
gewichtet als solche mit einem hohen.
87Sr/86Sr
Metamorphosealter
Was eine Isochrone
0.7052
bedeutet, läßt sich anIllustration der Sr-Isotopenentschaulich auch in eiwicklung eines Eklogits
87
86
ner Sr/ Sr – Zeit(Münchberger Gneisgebiet)
Auftragung zeigen, ei0.7048
nem sogenannten Isotopenentwicklungsgit
en
h
diagramm (AbbilP
0.7044
dung 36). Gegeben
seien 4 Minerale eines
estein
Gesteins mit sehr unGesamtg
Amphibol
terschiedlichen Rb/Sr0.7040
Ve r h ä l t n i s s e n . M i t
Cpx
Hilfe der GL 51 läßt
sich für jedes einzelne
Mineral ( 8 7 Sr/ 8 6 Sr) o
0.7036
mit den gemessenen
500 450 400 350 300 250 200 150 100 50
0
87
86
Rb/Sr- und Sr/ SrZeit [Ma]
Verhältnissen für jeden beliebigen Zeitpunkt t in der Vergan- ABBILDUNG 36 Rb–Sr-Isotopenentwicklungsdiagramm für einen
genheit zurückrech- Eklogit aus dem Münchberger Gneisgebiet
nen. Da die Minerale kogenetisch sind, erhält man einen Schnittpunkt aller 4 Geraden und
kann t (das Isochronenalter) und (87Sr/86Sr)o direkt ablesen. Was durch eine Isochrone datiert wird, ist von Fall zu Fall zu untersuchen und entscheiden.
47
Das Rb–Sr-Isotopensystem
87Sr/86Sr
In metamorphen
magmatisches
Metamorphosealter
heutige Isotopie
Gesteinen wird
Alter
(Isotopenhomogenisierung)
man mit Hilfe der
B
B
B
Rb–Sr-Methode
(sowie mit den
meisten anderen
er
Methoden) durch
m
m
i
Mineralanalysen
Gl
t
in der Regel den
pa
er
lds
m
e
Zeitpunkt der
F
Kim
Metamorphose
Gl
Anorthit
datieren*. Über die
n
estei
magmatische oder
mtg
a
s
e
G
sedimentäre Entwicklung davor
Apatit
wird man auf
diese Weise keine
Hypothetische Entwicklung der Sr-Isotopie in
gesicherten Inforeinem System mit Zweistufengeschichte
mationen mehr
erhalten können.
Zeit [Ma]
(siehe Abbildung
37). Angenommen ein Granit sei ABBILDUNG 37 Hypothetische Zweistufenentwicklung eines Gesteins; die
zur Zeit ti erstarrt. Homogenisierung durch die Metamorphose löscht im dargestellten IdealAuf Grund ihrer fall die „Erinnerung“ an die vorherige Geschichte aus. Je niedriger die Temu n t e r s c h i e d l i - peratur, je „trockener“ die Metamorphose und je weniger penetrativ die
chen Rb/Sr-Ver- Deformation ist, desto größer ist aber die Wahrscheinlichkeit, daß diese
h ä l t n i s s e w i r d Zurücksetzung der Isotopenuhr nicht vollständig erfolgt.
87
Sr/ 8 6 Sr in den
verschiedenen Mineralen und im Gesamtgestein unterschiedlich schnell wachsen. Erfolgt
irgendwann später eine Metamorphose, so werden sich infolge der Aufheizung die 87Sr/
86
Sr-Verhältnisse in den Mineralen in Richtung des Wertes des Gesamtgesteins bewegen,
und die Erinnerung an das magmatische Alter geht verloren. Durch die Metamorphose
wird also die Rb–Sr-Uhr auf 0 zurückgesetzt und wieder neu gestartet. Wenn bei der Metamorphose keine allzu hohen Temperaturen erreicht wurden und wenn die Metamorphose
„trocken“ ist, (® niedrige Diffusionsgeschwindigkeiten, Abwesenheit von Fluiden), wird
die Uhr aber möglicherweise nicht oder unvollständig zurückgesetzt (siehe auch Diskussion der Schließungstemperatur, Seite 33 und folgende). Da die Wahrscheinlichkeit, daß
eine Isotopenhomogenisierung bei der Metamorphose über große (km) Bereiche erfolgt,
kann durch weit entfernt voneinander genommene „Großproben“ eines Metamagmatits
eventuell das magmatische Alter noch rekonstruiert werden. In solchen Fällen wird man
wahrscheinlich keine Geraden erhalten, welche die strengen Bedingungen einer Isochrone
erfüllen. Wenn mehrere voneinander unabhängige Isotopensysteme (z.B. Rb–Sr und Sm–
Nd) dabei ähnliche oder gleiche Alterswerte liefern, sollte ihnen eine geologische Bedeutung zukommen.
Positive Korrelationen zwischen 87Sr/86Sr und Rb/Sr für Gesamtgesteine können allerdings
auch Mischungslinien zwischen zwei Endkomponenten darstellen, insbesondere zwischen
zwei Magmen; darauf wird in einem späteren Kapitel eingegangen (Kapitel 6.0, Seite 67).
* Es lassen sich allerdings Fälle denken, in denen eine niedriggradige Metamorphose den ehemals
magmatischen Mineralbestand weitgehend intakt gelassen hat oder wenn unter trockenen Bedingungen Mineralreaktionen unvollständig abgelaufen sind; in solchen Fällen können sich gravierende Störungen der Isotopensysteme zeigen; unter günstigen Umständen mag sich das magmatische
Alter noch abschätzen lassen.
48
A. Radiogene Isotopensysteme
4.2
Das Rb–Sr-System als Tracer
4.2.1
Die Sr-Isotopenentwicklung der Meteorite und des Erdmantels
Bei der Untersuchung magmatischer Gesteine hat sich seit den sechziger Jahren gezeigt,
daß das Rb–Sr-Isotopensystem nicht nur nützlich zur Altersbestimmung ist, sondern daß
die 87Sr/86Sr-Isotopie hilfreich als Tracer für die Aufklärung petrogenetischer Prozesse sein
kann, ähnlich wie manche Spurenelemente Aufschlüsse darüber geben können. Die kontinentale Erdkruste ist im Verlauf der Erdgeschichte letztlich durch Differentiationsprozesse
aus dem Erdmantel entstanden. Dabei haben sich sowohl Rb als auch Sr in den Gesteinen
der Erdkruste angereichert, das Rb infolge seiner größeren Inkompatibilität erheblich stärker als das Sr. D.h. die Rb- und Sr-Konzentrationen und v.a. das Rb/Sr-Verhältnis sind in der
Erdkruste wesentlich höher als im Erdmantel, und infolgedessen hat sich in der Kruste über
den Verlauf der Erdgeschichte auch ein erheblich höheres und infolge innerkrustaler Differentiation extrem variables 87Sr/86Sr herausgebildet als im Erdmantel, der eine niedrige und
vergleichsweise homogene Sr-Isotopenzusammensetzung hat.
87Sr/86Sr
Die ( 8 7 Sr/ 8 6 Sr) o -Werte
0.7010
magmatischer Gesteine
Basaltische Achondrite
bergen oft Informationen
T = 4.44«0.30Ga
über deren geochemische
Initialwert = 0.69896«0.00005
0.7005
Geschichte, insbesondere die Natur des Materials, aus dem sie entstanden sind – Kruste oder
0.7000
Mantel. Das ist deswegen
möglich, weil man aus
der Analyse von jungen
0.6995
Ozeanbodenbasalten und
kontinentalen Basalten
die heutige Sr-Isotopie
0.6990
des oberen Erdmantels
kennt. Zum anderen
kann man indirekt die SrIsotopenzusammenset0.6985
0.00
0.01
0.02
0.03
zung der Erde zur Zeit
87Rb/86Sr
ihrer Entstehung ableiten
und damit die Entwicklung des 87Sr/86Sr im Erd- ABBILDUNG 38 Der Initialwert der basaltischen Achondrite liefert
mantel über den Verlauf das initiale 87Sr/86Sr der Erde.
der
Erdgeschichte
abschätzen. Die Isotopenzusammensetzung der Erde zur Zeit ihrer Bildung ist durch die
Untersuchung von Meteoriten ableitbar. Meteorite sind Bruchstücke ehemals größerer Körper des Sonnensystems, von denen man annimmt, daß sie mehr oder weniger zeitgleich
(auf ±50 – 100Ma) mit der Erde entstanden sind. Die chondritischen Meteorite stellen
unfraktionierte Solarmaterie dar; sie sind reich an flüchtigen Komponenten und haben
infolge hoher Rb/Sr-Verhältnisse heute wesentlich höhere 87Sr/86Sr-Verhältnisse als die
Erde – d.h. die Steigung der Rb–Sr-Isochronen für die Chondrite ist groß. Ihr initiales 87Sr/
86
Sr ist daher stark zeitabhängig und wenig geeignet, ein brauchbares initiales 87Sr/86Sr für
die Erde zu liefern, da man nicht unbedingt davon ausgehen darf, daß sie exakt zeitgleich
mit der Erde entstanden. Man hat daher das initiale 87Sr/86Sr von einem anderen Meteoritentyp abgeleitet, den basaltischen Achondriten, die im Anschluß an ihre Entstehung eine
kurze Phase der chemischen Differentiation mitgemacht haben; sie müssen nämlich aus
einer Schmelze kristallisiert sein. Außerdem haben sie sehr niedrige Rb/Sr-Verhältnisse
(<0.02). Infolgedessen ist ihr 87Sr/86Sr seit ihrer Bildung nur wenig gewachsen, und Altersunterschiede zwischen ihnen und der Erde in der Größenordnung selbst von >108a wären
belanglos. Papanastassiou & Wasserburg (1969) haben aus 7 solcher basaltischer Achondrite
49
Das Rb–Sr-Isotopensystem
ein Basaltic Achondrite Best Initial von 0.69898 abgeleitet, einen Wert, der seitdem nur
minimal korrigiert worden ist (siehe Abbildung 38[40]). Man kann deswegen diesen Wert als
repräsentativ für den solaren Nebel ansehen, aus dem die Erde und andere Planeten einschließlich der Meteoritenmutterkörper entstanden sind.
Triberg-G
ranit
Am Rande sei darauf
0.725
hingewiesen, daß die
Herkunft von Meteoriten mit niedrigem Alter
0.720
Alter der magmain der Meteoritik lange
tischen Bildung
diskutiert wurde. Dies
betrifft insbes. die soge0.715
nannten SNC-Meteorite
(Shergottyites, Nakhlites, Chassignites). Das
0.710
ste
kü
sind Achondrite mit
n
i
e
nb
Kristallisationsaltern
lfe
E
um 1.3 Ga (und andeite
0.705
an
r
ren). Inzwischen glaubt
G
man, daß es sich dabei
um Stücke vom Mars
0.700
ld
Erdmantelfe
handelt, die durch
einen Meteoritenimpakt
ins
We l t a l l
0.695
geschleudert wurden.
4.0
3.0
2.0
1.0
0.0
Ein Problem bereitet die
t [Ga]
geringe Wahrscheinlichkeit, mit der solche ABBILDUNG 39 Mit Hilfe der Sr-Entwicklungskurve des Erdmantels
Brocken auf der Erde läßt sich abschätzen, ob Magmatite im wesentlichen aus dem Erdl a n d e n s o l l t e n , u n d mantel stammen oder durch Aufschmelzung von älteren Gesteinen
a u ß e r d e m i s t d e r der Kruste (Metasedimente).
Mechanismus unklar,
durch den Materie bei einem solchen Impakt der Anziehung des Mars entkommen kann.
Noch seltener sind Meteorite, die vom Mond stammen müssen und die auf den Eisfeldern
der Antarktis gefunden wurden.
87
Sr/86Sr
Mit dem 87Sr/86Sr-Initialwert der basaltischen Achondrite vor »4.5 Ga und der heutigen SrIsotopenzusammensetzung des Erdmantels von vielleicht 0.7025 sind zwei Punkte auf
einer 87Sr/86Sr – Zeitskala bekannt, zwischen denen man durch eine lineare Interpolation
die zeitliche Entwicklung des 87Sr/86Sr im Erdmantel in erster Näherung abschätzen kann.
Das ist nur eine grobe, aber dennoch genügend genaue Abschätzung, da die heutige Sr-Isotopenvariation des Erdmantels beträchtlich ist (»0.702–0.705). Andererseits weisen die
Gesteine, welche die kontinentale Erdkruste aufbauen, eine wesentlich höhere Variation
und im Schnitt erheblich höheres Rb/Sr-Verhältnis auf als typischer Erdmantel. Dadurch
hat sich in der kontinentalen Kruste im Verlauf der Erdgeschichte natürlich auch eine
wesentlich höhere 87Sr/86Sr-Variation mit einem im Schnitt erheblich höheren 87Sr/86Sr
ausgebildet als im Mantel. Mit Hilfe der initialen 87Sr/86Sr-Werte von (v.a. sauren) Magmatiten läßt sich oft entscheiden, ob sie i.w. aus älterer Erdkruste erschmolzen wurden, oder
ob an ihrer Bildung auch der Erdmantel beteiligt war.
Abbildung 39 zeigt das am Beispiel eines ca. 310Ma alten Granits aus dem Schwarzwald
und eines »2 Ga alten Granits aus Westafrika. Das initiale 87Sr/86Sr des westafrikanischen
Granits ist nicht unterscheidbar vom Erdmantel-87Sr/86Sr zu dieser Zeit; es zeigt daher an,
daß dieser Granit über Zwischenstufen wie Gabbro oder Diorit innerhalb geologisch kurzer
Zeit aus dem Erdmantel differenziert sein muß. Im Gegensatz dazu hat das initiale 87Sr/86Sr
des Triberg-Granits einen typisch krustalen Wert, der eine Beteiligung einer größeren Erdmantelkomponente sehr unwahrscheinlich macht.
50
A. Radiogene Isotopensysteme
Die Sr-Isotopenentwicklung der „bulk earth“ kann nicht so einfach abgeschätzt werden, da
das heutige 87Sr/86Sr der Erde nicht direkt bekannt ist und die Chondrite keine Hilfe bieten,
da im Vergleich zu ihnen die Erde an Rb relativ zu Sr verarmt ist. Mehr zu diesem Thema
bei der Besprechung der Nd-Sr-Isotopenkorrelation!
4.2.2
Die Sr-Isotopenentwicklung der Ozeane
Sr-Isotopenmessungen an rezenten marinen Karbonaten haben gezeigt, daß ihr 87Sr/86Sr
und damit das des Seewassers, aus dem sie i.w. durch biologische Tätigkeit ausgefällt wurden, mit 0.70910±0.00005 weltweit sehr konstant ist. Das beruht letztlich auf dem effektiven Austausch des Wassers zwischen den Weltmeeren durch Tiefen- und Oberflächenströmungen, weil die Durchmischung des Wassers der Ozeane eine Zeit von »103a erfordert,
während die sogenannte „Residenzzeit“ des Sr im Meerwasser »5´106a beträgt. Das äußert
sich in der vergleichsweise hohen Sr-Konzentration des Seewassers von ca. 8100µg/l (zum
Vergleich: Rb 120, Nd 0.0028, Sm 0.00045, Pb 0.03, U 3.3, Th 0.0004µg/l[41]). Die geographische Konstanz des 87Sr/86Sr im Seewasser nimmt man auch für die geologische Vergangenheit an.
Die Sr-Isotopenentwicklung
des Meerwassers im
Phanerozoikum
0.709
100
ABBILDUNG 40
200
300
400
500
Proterozoikum
Kambrium
Ordovizium
Silur
Devon
Karbon
Trias
Jura
Kreide
Tertiär
0.707
Perm
87Sr/86Sr
0.708
600Ma
Variation der Sr-Isotopenentwicklung des Seewassers im Phanerozoikum
Durch Analyse verschieden alter Karbonate hat man für das Phanerozoikum eine Variationskurve des Seewassers aufzustellen vermocht (siehe Abbildung 40[42]). Es zeigt sich, daß
seit dem Beginn des Kambriums die Isotopenzusammensetzung des Meerwassers nur zwischen »0.7065 und 0.709 geschwankt hat und daß etwa seit dem Mitteljura eine ständige
Erhöhung von »0.7068 auf den heutigen Wert um 0.709 zu verzeichnen ist. Kretazische bis
rezente marine Karbonate könnten daher sogar auf diese Weise datiert werden.
Was mag die Ursache der 87Sr/86Sr-Fluktuationen des Meerwassers sein? – Die im Meerwasser gelösten Salze stammen aus 3 Quellen, (a) aus einem Anteil, der durch Verwitterung
und Abtragung der Kontinente (Magmatite und klastische Sedimente) in Lösung über die
Flüsse den Weltmeeren zugeführt wird, (b) aus einer Komponente, die durch vulkanische
Aktivität, insbes. an den mittelozeanischen Rücken, ins Meerwasser gelangt und (c) aus
einem Anteil, der aus der Auflösung mariner Karbonate (inklusive älterer auf den Kontinenten) herrührt. Auch die Sr-Isotopie der Ozeane setzt sich aus diesen 3 Beiträgen zusammen:
51
Das Rb–Sr-Isotopensystem
(
87
Sr
86
Sr
)
Ozean
=
(
87
Sr
86
Sr
)
vulk.
´ jv +
(
87
Sr
86
Sr
)
kont .
´ jk +
(
87
Sr
86
Sr
)
karb.
´ jc
[GL 59]
BABI
87Sr/86Sr
wobei ji die Bruchteile
des Sr der einzelnen
0.710
Die Entwicklung der
Komponenten am Sr des
Seewasser-Strontiumisotopie
Meerwassers widerspieim Präkambrium
geln (å j i = 1). ( 8 7 Sr/
0.708
86
Sr)vulk. wird dabei
Werte zwischen »0.702
und 0.705 (meist
0.706
Se
ew
<0.7035) einnehmen,
as
87
86
se
( Sr/ Sr)kont. wird
r
0.704
>0.710 sein (durchschnittlich 0.720) und
Mante
lentwic
( 87 Sr/ 86 Sr) karb. wird im
klung
0.702
Phanerozoikum Werte
zwischen 0.7065 und
0.709 einnehmen. Die
Proterozoikum
Archaikum
0.700
Fluktuationen in der
87
Sr/86 Sr-Entwicklungs1
2
3
4Ga
kur ve des Seewassers
können dann Variationen in den relativen Bei- ABBILDUNG 41 Die Sr-Entwicklungskurve des Seewassers über den
trägen dieser 3 Kompo- Verlauf der Erdgeschichte. Die präkambrische Entwicklung ist wenenten zugeschrieben sentlich schlechter bekannt als die phanerozoische.
werden. Insbes. kann der Anstieg seit dem mittleren Jura auf erhöhten Beitrag von Sr
zurückgeführt werden, das sich aus den Gesteinen der kontinentalen Erdkruste (Granitoide, klastische Sedimente) ableitet infolge erhöhter Abtragungsrate der Kontinente, verursacht durch die jungen Orogenesen. Der Anstieg an der Wende Ordovizium-Silur kann
denselben Effekten im Anschluß an die kaledonische Orogenese zugeschrieben werden.
Da marine Karbonate im Präkambrium erheblich spärlicher werden, ist es nicht verwunderlich, daß die 87Sr/86Sr-Entwicklungskurve des Seewassers für diese Zeit schlechter
bekannt ist. Die verfügbaren Daten scheinen anzuzeigen, daß sich erst im Proterozoikum
die Seewasserkurve von der Mantelkurve zu trennen begann, d.h. Verwitterung und Abtragung älterer kontinentaler Kruste spielte im Archaikum keine wesentliche Rolle, verglichen
mit den Beiträgen aus vulkanischer Tätigkeit und Abtragung junger Kruste. Insgesamt
scheint also die 87Sr/86Sr-Isotopie des Seewassers zeitverzögert ein relativ empfindlicher
Indikator der Großtektonik auf der Erde zu sein.
52
A. Radiogene Isotopensysteme
5.0
Das Sm–Nd-System
5.1
Allgemeines
Das Sm–Nd-System ist eine der neueren Methoden der Geochronologie; sie wurde Mitte
der siebziger Jahre von G.W. Lugmair in die Kosmochemie eingeführt.
Natürliches Sm besteht aus 7 Isotopen mit den Massenzahlen 144, 147, 148, 149, 150, 152
und 154. 147Sm hat eine Häufigkeit von 15.0Atom% und zerfällt mit einer Halbwertszeit
von 106 Ga unter a-Emission in stabiles 143Nd, das am Aufbau des natürlichen Nd zu ca.
12.2% beteiligt ist. Ebenfalls radioaktiv ist 146Sm, das wegen seiner kurzen Halbwertszeit
von 103 Ma aber nur in der Frühzeit des Sonnensystems existierte[43]; sein a-Zerfall in
142
Nd führte zu kleinen Variationen im Verhältnis 142Nd/144Nd von bis zu»20 ppm im
Archaikum[44]. Nd hat 7 natürlich vorkommende Isotope, welche die Massenzahlen 142,
143, 144, 145, 146, 148 und 150 haben. Die Zerfallsgleichung für dieses System lautet:
143
Nd =
(
143
Nd
)
0
(
)
+ 147Sm e lt - 1
[GL 60]
Als Referenzisotop dient konventionell 144Nd, das nicht Produkt eines Zerfallsprozesses ist:
143
Nd æ 143Nd ö
=ç
÷ +
144
Nd è 144 Nd ø 0
147
144
Sm lt
e -1
Nd
(
)
[GL 61]
0.13
0.12
Ionenradien [nm]
Ionenradien für
sechsfache Koordination
Eu2+
Ionenradien für
achtfache Koordination
0.11
0.10
REE3+
Ce4+
0.09
0.08
La
ABBILDUNG 42
Ce
Pr
Nd
Sm Eu
Gd Tb
Dy Ho
Er
Tm Yb
Lu
Variation der Ionenradien der Seltenen Erden
Sm und Nd sind beide Elemente der Seltenen Erden (REE), einer Gruppe von sich chemisch
sehr ähnlich verhaltenden Elementen. Sie treten bis auf zwei Ausnahmen (Ce4+ und Eu2+)
in der Natur nur dreiwertig auf und unterscheiden sich dann ausschließlich durch ihre
Ionenradien, die vom leichtesten der Elemente (La) zum schwersten (Lu) systematisch
abnehmen (siehe Abbildung 42). Der Ionenradius von Nd3+ in Sechserkoordination in
einem Kristallgitter beträgt 0.0983nm, der von Sm3+ 0.0958nm, und demzufolge passen Sm
und Nd geringfügig unterschiedlich gut oder schlecht auf die Gitterpositionen der
53
Das Sm–Nd-System
gesteinsbildenden Minerale, was im Diagramm auf der nächsten Seite anhand der Verteilungskoeffizienten zwischen Kristall und einer Schmelze für verschiedene Minerale dargestellt ist. Diese chemische Ähnlichkeit hat für die Anwendung des Sm–Nd-Systems in der
Isotopengeochemie sowohl Vor- als auch Nachteile. Ein großer Vorteil ist, daß sich die REE
geochemisch ziemlich stabil verhalten; zudem ist ihre Geochemie gut untersucht. Die
wesentliche Fraktionierung von Sm und Nd findet bei Hochtemperaturprozessen statt, d.h.
vor allem bei magmatischen Prozessen der partiellen Aufschmelzung und der fraktionierten Kristallisation. Bei der Gesteinsmetamorphose scheinen Sm–Nd-Fraktionierungen über
einen größeren als Handstückbereich selten zu sein, solange die Metamorphose im trockenen Zustand erfolgt; und bei sedimentären Prozessen tritt keine nennenswerte Fraktionierung von Sm und Nd auf. Im Gegensatz dazu verursacht die Gesteinsverwitterung beim
Rb–Sr-System eine erhebliche Trennung von Rb und Sr, weil die Minerale mit niedrigem
Rb/Sr-Verhältnis (Pyroxene, An-reicher Feldspat, Amphibole) rascher verwittern als die mit
hohem Rb/Sr (Glimmer, K-reiche Feldspäte).
10
relativ zu Basaltschmelzen
Beispiele für die Variabilität der SEVerteilungskoeffizienten für
Minerale in basaltischen Schmelzen
at
Gran
1
Augit
0.1
Plagiokla
s
0.01
it
on
e
Pig
in
Oliv
0.001
0.0001
La
ABBILDUNG 43
Ce
Pr
Nd
Sm
Eu
Gd
Tb
Dy
Ho
Er
Tm
Yb
Lu
REE-Verteilungskoeffizienten zwischen Mineralen und koexistierenden
Schmelzen
Die große chemische Ähnlichkeit von Sm und Nd bringt jedoch auch wesentliche Nachteile mit sich, denn geringe Sm–Nd-Fraktionierungen, das heißt eine geringe Spreizung der
x-Achse des Isochronendiagramms und geringe Wachstumsgeschwindigkeit von 143Nd/
144
Nd im Verlauf der Zeit, zumal noch die Halbwertszeit von 147Sm außerordentlich hoch
ist. Die gesamte Sm/Nd-Variation in Gesteinen bewegt sich mit wenigen Ausnahmen nur
zwischen »0.10 – 0.80; sie liegt in den Gesteinen, welche die kontinentale Erdkruste aufbauen, meistens niedriger als der „bulk-earth“-Punkt und macht weniger als einen Faktor
4 zwischen dem minimalen und dem maximalen Wert aus (siehe Abbildung 44). Dagegen
ist die Variation der Rb/Sr-Verhältnisse um mehr als eine Größenordnung höher. Aus der
geringen Variation im Sm/Nd in Kombination mit der langen Halbwertszeit von 147Sm
ergibt sich, daß die natürlichen Isotopenvariationen des 143Nd/144Nd in Gesteinen sehr
gering sind. Basische und ultrabasische Gesteine haben im Schnitt höhere Sm/Nd-Verhältnisse als saure. Das Sm–Nd-System eignet sich daher zur Altersbestimmung vor allem von
Basiten und Ultrabasiten, insbesondere wenn sie auch noch geologisch alt sind. Solche
54
A. Radiogene Isotopensysteme
Gesteine zeichnen sich oft durch niedrige Rb/Sr-Verhältnisse aus, und so ergänzen sich
beide Systeme bei der Geochronologie recht gut.
Tabelle 7 gibt als Ergänzung zu Abbildung 44 typische Sm- und Nd-Gehalte für einige
Gesteinstypen an. Es ist zu betonen, daß die Variation innerhalb einzelner Gesteinstypen
sehr groß sein kann; hoch differenzierte Granite z.B. können sogar SE-Gehalte im subppm-Bereich enthalten.
TABELLE 7:
Mittlere Sm- und Nd-Gehalte einiger Gesteinstypen
Gestein
Peridotit (Lherzolith
Peridotit (Harzburgit)
MOR-Basalt
Alkalibasalt
Phonolith
Kimberlit
Granodiorit
Granit
Tonschiefer
Grauwacke
ppm Sm
0.2
0.005
3.5
7
14
8
6
8
10
5
ppm Nd
0.5
0.020
10
40
80
70
30
40
60
25
147
Sm/144Nd
0.24
0.15
0.21
0.11
0.11
0.07
0.12
0.12
0.10
0.12
Die Isotopenent147Sm/144Nd
wicklung des Nd ist
0
0.1
0.2
0.3
0.4
0.5
0.6
in Abbildung 45 der
des Sr schematisch
gegenübergestellt,
klastische + chemische Sedimente
in der die IsotopenzusammensetzunGranitoide
gen gegen die Zeit
aufgetragen sind.
Anorthosite
Für beide Isotopensysteme ist als RefeAlkalibasalte
Sm-Nd-Variation
renz die Entwickverschiedener
lungslinie der Erde
MORBs
Gesteinstypen
(als ein homogenes
Reservoir betrachPeridotite
tet, identisch mit
unfraktioniertem
Erdmantel) einge- 0
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
tragen. Wir stellen
Sm/Nd
uns ein Teilvolumen
dieses Reservoirs
vor, das vor 2 Ga ABBILDUNG 44 Variation des Verhältnisses Sm/Nd in Gesteinen
eine partielle Aufschmelzung erfahren möge. Im Rb–Sr-System ist das Rb das für die Silikate, die den Erdmantel aufbauen, inkompatiblere Element; es reichert sich daher bei der
partiellen Aufschmelzung in den Schmelzen (Basalten) an und bei fraktionierter Kristallisation in den Restschmelzen. Der betrachtete Erdmantel, dem die Schmelze entzogen wird,
hat anschließend ein niedrigeres Rb/Sr-Verhältnis von fast 0, und infolgedessen wächst
sein 87Sr/86Sr nur noch langsam an (Das verdeutlicht, daß sich ultrabasische Gesteine für
eine Rb–Sr-Datierung nicht gut eignen.), während es in der Schmelze, die als Basalt oder
Gabbro oder Diorit erstarren möge, wesentlich rascher wächst als in unfraktioniertem Erdmantel. 87Sr/86Sr=0.7025 ist ein typischer Wert für Erdmantel unter den Ozeanen, 87Sr/
55
Das Sm–Nd-System
86
Sr>0.715 typisch für viele Gesteine der kontinentalen Erdkruste. Im Sm–Nd-System ist
das Nd das für Erdmantelminerale inkompatiblere Element. Daher verläuft die Entwicklung der Nd-Isotope in vielen Gesteinstypen derjenigen der Sr-Isotope umgekehrt. Als Beispiel diene wiederum ein Stück bulk-earth oder Erdmantel, der vor 2 Ga partiell aufgeschmolzen werde. Da sich auf Grund ihrer größeren Inkompatibilität die leichten REE in
der Teilschmelze über die schweren anreichern werden, hat die Teilschmelze ein Sm/Nd <
bulk-earth und der residuale Erdmantel ein Sm/Nd > bulk-earth. Dementsprechend wird
im Anschluß an den Aufschmelzprozeß das 143Nd/144Nd im residualen Erdmantel rascher
wachsen als im unfraktionierten Mantel und dort wieder rascher als in der ehemaligen Teilschmelze. Im Verlauf der Erdgeschichte ist die kontinentale Erdkruste durch eine Reihe von
Differentiationsprozessen – z.B. in den Inselbögen – durch Extraktion aus dem Erdmantel
entstanden. Man kann daher in diesem Diagramm die „mantle melt“ auch durch kontinentale Erdkruste ersetzen, und „depleted mantle“ steht für den größten Teil des Erdmantels sowohl unter den Ozeanen als auch unter den Kontinenten. Unfraktionierter Erdmantel scheint dagegen bei Differentiationsprozessen nicht mehr in Erscheinung zu treten; ob
es noch Relikte davon im oberen Erdmantel gibt, ist ungewiß. Die für t=0 angegebenen
Werte sind als typisch für den heutigen ozeanischen Erdmantel (»0.5132) bzw. für 2 Ga alte
Kruste (»0.5115–0.5120) gewählt. Die gesamte Nd-Isotopenvariation in Gesteinen auf der
Erde liegt bis auf wenige obskure Ausnahmen zwischen »0.510 und 0.5135, macht also nur
knapp 7‰ aus. Bei den Sr-Isotopen ist die untere Begrenzung ungefähr durch einen Wert
von »0.701 gegeben (alte Granulite oder Eklogite), während eine Obergrenze kaum anzugeben ist. Schließt man granitische Gesteine mit ihren hohen Rb/Sr-Verhältnissen aus und
wählt anstatt dessen 0.740 als hohen Wert für klastische Sedimente (z.B. Devontonschiefer
aus dem Rheinischen Schiefergebirge), dann erhält man schon »5.5% als Mindestvariation.
Granite können in Extremfällen 87Sr/86Sr-Werte bis über 2 erreichen.
0.514
0.716
hypothetisches
Schmelzereignis vor 2Ga
0.712
te
La
0.510
elz
hm
lsc
elp
ar
tia
0.708
an
t
ia
art
Ma
e
elz
hm
lsc
M
sid
re
ul
„b
lp
nte
rth“
„bulk-ea
Lu
0.704
residualer Mantel
0.700
-2
-1.5
-1
t [Ga]
ABBILDUNG 45
“ La Lu
rth
a
ke
0.511
0.509
-2.5
e
an
rM
Lu
ua
La
le
0.512
87Sr/86Sr
143Nd/144Nd
l
0.513
Reaktion des Sm-Nd- und des
Rb-Sr-Isotopensystems auf ein
partielles Schmelzereignis im
Erdmantel
-0.5
0 -2.5
-2
-1.5
-1
-0.5
0
t [Ga]
Das Sm–Nd-System verhält sich bei Aufschmelzprozessen im Erdmantel umgekehrt wie das Rb–Sr-System.
Mit einem modernen Massenspektrometer kann man bequem 87Sr/86Sr-Unterschiede von
»75 ppm auflösen (»±0.000050) und 1 4 3 Nd/ 1 4 4 Nd-Unterschiede von »50 ppm
(»±0.000025); die individuellen statistischen Meßfehler liegen, wenn sie niedrig sind, bei
weniger als der Hälfte dieser Werte.
56
A. Radiogene Isotopensysteme
Woher kennt man die Entwicklungslinie der Nd-Isotope in der „bulk earth“? Nur durch
Analogieschluß, indem man davon ausgeht, daß die Entwicklung des 143Nd/144Nd-Verhältnisses in der Erde identisch ist mit der vieler Meteorite, insbesondere derjenigen der Chondrite. Da die REE refraktäre Elemente sind, die bei der Kondensation der Erde aus dem
Solarnebel nicht fraktionierten, nimmt man an, daß die Erde die REE in chondritischen
Häufigkeitsverhältnissen enthält. Die anschließende chemische Segregation in den metallischen Erdkern und den Erdmantel hat nur dazu geführt, daß sich die REE im Erdmantel
gegenüber den Chondriten um rund einen Faktor 1.5 anreicherten. Im Gegensatz dazu ist
– infolge seiner Flüchtigkeit – weniger Rb verglichen mit Sr in die Erde bei ihrer Kondensation eingetreten als in die undifferenzierte Solarmaterie (Chondrite), so daß die Erde ein
wesentlich niedriger als chondritisches Rb/Sr hat. Um die 143Nd/144Nd-Entwicklungsgerade
zu bestimmen, benötigt man den Initialwert (143Nd/144Nd)o des Sonnensystems bei der
Entstehung der Erde vor »4.56 Ga, der identisch sein sollte mit dem der Meteorite, die zu
dieser Zeit entstanden sind, d.h. der Chondrite oder Achondrite. Nun haben Chondrite
definitionsgemäß eine chondritische REE-Verteilung, d.h. ein nahezu konstantes Sm/Nd.
Das gilt auch für die meisten Achondrite. Man hat daher entweder die Möglichkeit, mit
dem heutigen 143Nd/144Nd und ihrem Sm/Nd-Verhältnis das 143Nd/144Nd auf die Zeit vor
»4.56 Ga zurückzurechnen, Alter die v.a. die U–Th–Pb-Chronologie als Alter der Meteorite
und damit vermutlich auch der Erde nahelegt. Die bessere Lösung ist aber die, das Alter der
internen Äquilibrierung der Meteorite zu bestimmen, d.h. Mineralisochronen zu messen.
Dazu eignen sich nur die Achondrite, deren Minerale – im Gegensatz zu denen aus Chondriten – eine genügend große Sm/Nd-Fraktionierung zeigen, da sie ehemals im Gleichgewicht mit einer Schmelze standen, also eine Hochtemperaturfraktionierung erlebt haben.
G.W. Lugmair wählte ursprünglich den Achondriten Juvinas aus, für den er ein (143Nd/
144
Nd)o von 0.50670±10 (bias corrected) bei einem Alter von 4.56±0.08 Ga erhielt. Dieser
Wert ist durch Analyse weiterer Achondrite verfeinert worden, und als bester Initialwert
gilt ca. 0.50663 bei einem Alter von 4.60 Ga[45]. Der heutige 143Nd/144Nd-Wert der Chondrite liegt bei »0.512638. Daraus resultiert nach GL 61 ein 147Sm/144Nd-Verhältnis von
0.1967 (ºSm/Nd von 0.3254)[46]. Damit ist die Nd-Isotopenentwicklungskurve der Erde
vollständig bestimmt.
In den meisten Veröffentlichungen wird die Nd-Isotopenzusammensetzung nicht nur als
143
Nd/144Nd, sondern zusätzlich als eNd (eChur, ebulk-earth, eJuv) angegeben. Damit ist die relative Abweichung (in 10000stel) der Nd-Isotopie einer Probe von der Isotopie einer Bezugsprobe gemeint, für die das 143Nd/144Nd einer Probe mit chondritischem Sm/Nd gewählt
wird, also Chondrite (Chur) oder die Erde (bulk-earth) oder – früher – der Achondrit Juvinas (Juv). Dessen 147Sm/144Nd beträgt jedoch nur 0.1936 und daher ist sein 143Nd/144Nd
heute mit 0.512566 etwas niedriger als das der Chondrite oder der Erde. Der e-Wert läßt
sich berechnen nach:
é
e = êê
êë
(
(
143
é
e=ê
ê
êë
143
Nd
(
143
Nd
144
Nd
144
Nd
144
Nd
)
)
Probe
Bezugsreservoir
Nd
)
0.512638
Probe
ù
- 1úú ´ 10 4
úû
ù
- 1ú ´ 10 4
ú
ûú
[GL 62]
[GL 63]
Eine Probe mit 143Nd/144Nd>0.512638 hat daher ein positives, eine solche <0.512638 ein
negatives eNd (z.B. MORB mit 0.5132 Þ 11.0, ein Tonschiefer mit 0.5120 Þ -12.4.
eNd(T) steht für das eNd einer Probe, zurückgerechnet auf eine Zeit t vor heute. Um z.B.
eNd(500Ma) ausrechnen zu können, müssen das 143Nd/144Nd der betrachteten Probe und
das der „bulk-earth“ auf 500Ma vor heute zurückgerechnet werden.
57
Das Sm–Nd-System
Die Angabe einer relativen Isotopenzusammensetzung findet man unter anderem auch
beim Sr (eUR, UR= uniform reservoir), Hf (eHf), W (eW), Os (gOs als Prozentabweichung) sowie
als Promilleabweichung d bei den stabilen Isotopen (d18O, d13C).
Während die e-Angabe für die Hf-Isotope immerhin den Vorteil hat, daß man sich nur Zahlen zwischen vielleicht -20 und +20 merken muß, und die e-Angabe für das Sr gänzlich
überflüssig ist, hat sie beim Nd einen ganz realen und sinnvollen Hintergrund. Während
nämlich die eNd-, eChur- oder ebulk-earth-Werte, die von verschiedenen Labors angegeben werden, direkt miteinander vergleichbar sind, ist das für die 143Nd/144Nd-Verhältnisse nicht
der Fall. Das liegt an unterschiedlichen Normierungen der Meßwerte (siehe Kapitel 7.0,
Seite 75). Für einige Laboratorien (insbesondere California Institute of Technology, University of California–Berkeley, NASA-Houston) ergibt sich ein Wert von 143 Nd/ 144 Nd =
0.511847 für das Bezugsreservoir, der anstelle von 0.512638 in GL 63 einzusetzen ist.
5.2
Sm–Nd – Anwendung zur Datierung
Auf Grund der langen Halbwertszeiten von 147Sm und der geringen Sm/Nd-Fraktionierung
eignet sich das Sm–Nd-Isotopensystem bevorzugt zur Datierung von geologisch alten (präkambrischen) Gesteinen. Hier gilt es als stabiler als das Rb/Sr-System, weil die REE weniger
mobil sind als Rb und weil Sm und Nd weniger voneinander fraktionieren als Rb und Sr.
Mit der Analyse von Gesamtgesteinen scheint man oft durch die Metamorphosen „hindurchschauen“ zu können und magmatische Ereignisse zu datieren. Wie bereits früher
erwähnt, eignet sich das Sm–Nd-System vor allem zur Datierung mafischer Gesteine, da
diese sich durch höhere Sm/Nd-Verhältnisse und damit rascheres Wachstum des 143Nd/
144
Nd auszeichnen als saure Gesteine.
0.513
0.512
143Nd/144Nd
Metabasalt
„Bimodal Suite –
Ancient Gneiss
Complex“, Swaziland
Metabasalt
Dioritgneis
t = 3417«34Ma
«Nd(t) = 1.1«0.6
saurer Gneis
0.511
Tonalitgneis
Monzonitgneis
0.510
0.509
Initialwert: 0.508249±31
0.508
0.00
0.05
0.10
0.15
0.20
0.25
147Sm/144Nd
ABBILDUNG 46
Sm–Nd-Isotopenbeziehungen für eine bimodale Suite von archaischen
Gneisen in Swaziland
Abbildung 46 für die Bimodal Suite[47] des Ancient Gneiss Complexes im südlichen Afrika gibt
aber auch einen Einblick in die Problematik von Sm–Nd-Gesamtgesteinsdatierungen. Die
Datenpunkte liegen exakt auf einer Geraden; überzeugende Hinweise für eine Mischungslinie gibt es nicht. Darf man die Gerade daher als Isochrone betrachten? Problematisch
58
A. Radiogene Isotopensysteme
sieht es nämlich mit der Erfüllung einer anderen Voraussetzung für das Vorliegen einer
Isochrone aus: Die Proben variieren von sauren Gneisen bis hin zu Gesteinen mit basaltischer Pauschalzusammensetzung. Sind die Proben dann kogenetisch? Diese Frage ist
sicherlich zu verneinen, und man muß sich fragen, was die vermeintliche Isochronenbeziehung dann bedeuten kann. Es ist denkbar, daß die Gesteinssuite innerhalb geologisch
kurzer Zeit aus einem von der Nd-Isotopie einigermaßen homogenen Mantel differenzierte; die Stadien zwischen Kristallisation des Basaltmagmas und Granitoidbildung (z.B.
durch Aufschmelzung anderer aber gleich alter in der tiefen Kruste kristallisierter Basalte
oder durch fraktionierte Kristallisation von Basaltmagmen) waren so kurzlebig, daß die
Gesteine innerhalb des zeitlichen Auflösungsvermögens der Methode gleich alt erscheinen. Sm–Nd-Isochronenbeziehungen, die derart verschiedene Gesteinstypen umfassen,
werden in ihrer Interpretation notwendigerweise umstritten bleiben. Wegen der großen
geochemischen Ähnlichkeit von Sm und Nd verhält sich dieses Isotopensystem aber zweifellos stabiler als das Rb–Sr-System gegenüber sekundären Veränderungen, z.B. Aufheizungen im Zuge einer Metamorphose. So liefert das Rb–Sr-System für dieselben Proben aus
dem Ancient Gneiss Complex keine akzeptable lineare Beziehung (Abbildung 47). Andererseits sollte gerade diese Diskrepanz Anlaß geben, sorgsam zu prüfen, ob die linearen Sm–
Nd-Beziehungen vielleicht durch Magmenmischung erworben wurden (siehe auch Kapitel
6.0, Seite 67).
87Sr/86Sr
Zur Aufnahme von Sm–
0.95
Nd-Mineralisochronen
„Bimodal Suite –
eignen sich unter den
Ancient Gneiss
saurer Gneis
MonzonitMineralen in Magmatiten
0.90
Complex“,
Swaziland
gneis
vor allem Pyroxen-Plagioklas-Paragenesen, weil
Pyroxene vergleichs0.85
weise hohe und Plagioklase sehr niedrige Sm/
Nd-Verhältnisse haben.
0.80
In metamorphen Gesteinen ist der Granat das
wichtigste Mineral für
0.75 MetaTonalitgneis
Sm–Nd-Datierungen; er
basalt Dioritgneis
kann Sm extrem hoch
Metabasalt
über Nd in sein Gitter
0.70
einbauen und hat damit
0
1
2
3
4
5
6
zumindest potentiell eine
87Rb/86Sr
ähnlich große Bedeutung
wie die Glimmer für das
Rb–Sr-System. Ein Bei- ABBILDUNG 47 Die Rb–Sr-„Isochrone“ für dieselbe Suite ist wespiel einer Mineraliso- sentlich schlechter definiert.
chrone ist in Abbildung
48 für einen Eklogit aus dem Münchberger Gneisgebiet aufgeführt[48]. Die Sm/Nd-Fraktionierung von Granat ist in diesem Beispiel so hoch, daß sich möglicherweise sogar deren
Wachstum ansatzweise rekonstruieren läßt. Die genaue Rekonstruktion scheitert daran,
daß für die Analyse eine Anzahl von Körnern benötigt wird; dabei ist die Auftrennung in
verschiedene Wachstumszonen beim Auslesen von Hand schwierig.
Zweipunktisochronen sind für Metamorphite recht beliebt geworden, die aus Datenpunkten für das Gesamtgestein und Granat bestehen. Das mag ausreichend sein, solange das
Gestein mineralogisch und texturell äquilibriert ist, d.h. solange nicht Minerale oder Texturen vorhanden sind, die in verschiedenen Entwicklungsphasen des Gesteins entstanden
sind. So wurde z.B. bei Untersuchung eines Übergangs von Gabbro in Eklogit gefunden,
daß Minerale aus mineralogisch und texturell sich im Ungleichgewicht befindenden
Gesteinen nicht auf eine Gerade im Sm–Nd-System fallen; die Minerale mit extremen Sm/
59
Das Sm–Nd-System
Nd- und 143Nd/144Nd-Verhältnissen bilden vielmehr die Ecken eines Dreiecks, in das
irgendwo die Zusammensetzung des Gesamtgesteins fällt[49]. Potentielle Probleme mögen
sich auch z.B. ergeben, wenn unter trockenen Bedingungen Granate diffusionskontrolliert
vor allem auf Kosten von Plagioklasen wachsen und Klinopyroxene auf Kosten von
Amphibolen (oder bereits im Ausgangsgestein vorhanden waren und sich nur chemisch an
die neuen P–T-Bedingungen anpassen). Plagioklase haben sehr niedrige Sm/Nd-Verhältnisse und entwickeln im Lauf der geologischen Zeit entsprechend niedrige Nd-Isotopien.Da Diffusion allein nicht sehr effektiv sein wird, die Isotopenzusammensetzungen bei
der Metamorphose zu homogenisieren, könnte der Granat auf diese Art seine Geschichte
mit einem niedrigeren 143Nd/144Nd beginnen als die übrigen Minerale des Gesteins.
Beträchtliche Unsicherheit besteht in der Frage, bei welchen Temperaturen der Nd-Isotopenaustausch in Granat zum Erliegen kommt. Vielfach wird davon ausgegangen, daß die
„Schließungstemperatur“ in Granaten aus Eklogiten und Granuliten bei »800 – 1000°C
liegt[50],[51],[52]; damit würde die Temperatur der Granatkristallisation angezeigt. Angenommen wird dabei, daß die mit Hilfe verschiedener Geothermometer abgeleitete Temperatur
des Gesteins die Nd-Schließungstemperatur angibt. Nach einer anderen Ansicht sind Sm–
Nd-Alter von Mineralen aus Granuliten, die i.w. durch Granat bestimmt werden, jedoch
Abkühlalter[53]. Diese Interpretation gründet sich auf den Befund, daß das U–Pb-System
von Mineralen aus denselben Gesteinen oder zumindest demselben Gebiet z.T. signifikant
höhere Alter liefert. Nach der Diskussion auf Seite 33 und folgenden wird von Fall zu Fall
zu prüfen sein, inwieweit Texturen, Mineralzonierungen und Reaktionsgefüge Hinweise
auf die Kristallisationsabfolge der Minerale und die Abkühlungs- und Deformationsgeschichte der Gesteine liefern und damit eine Erklärung für mit unterschiedlichen Isotopensystem gewonnene unterschiedliche Alter.
0.522
Eklogit Weißenstein
(Münchberger Gneisgebiet)
«Nd(t) = 8.3«0.2
0.520
Granat
(Ränder)
t = 395«4Ma
Granat (Ränder)
143Nd/144Nd
t = 384«2Ma
0.518
0.5140
Granat (Kerne)
Cpx II
0.5136
0.516
0.5132
Amphibol
Cpx I
Gesamtgestein
0.5128
0.514
Cpx II
0.0
0.1
0.2
0.3
0.4
0.5
0.6
0.512
0
1
2
3
4
147Sm/144Nd
ABBILDUNG 48
60
Sm–Nd-Mineralisochrone für Eklogite aus dem Münchberger Gneisgebiet.
Die Granate sind chemisch zoniert; ihre Kerne scheinen etwas älter zu sein
als die Ränder.
A. Radiogene Isotopensysteme
5.3
Nd-Isotope als Tracer und die Korrelation zwischen Sr- und NdIsotopen
Infolge der unterschiedlichen Inkompatibilitäten von Mutter und Tochter in den Isotopensystemen Rb–Sr und Sm–Nd findet man in den Gesteinen des Erdmantels und solchen, die
sich durch partielle Aufschmelzung daraus ableiten, meistens eine inverse Korrelation zwischen ihren Rb/Sr- und Sm/Nd-Verhältnissen. Da im Verlauf der Erdgeschichte verschiedene Teile des Erdmantels eine Reihe von Magmenextraktionsprozessen unterschiedlichen
Ausmaßes erfahren haben, hat sich infolge der über lange Zeit unterschiedlichen Sm/Ndund Rb/Sr-Verhältnisse in den Gesteinen des Erdmantels eine grob inverse Korrelation zwischen den Sr- und den Nd-Isotopen ausgebildet, den man als den mantle array bezeichnet
hat; diese Bezeichnung wird jedoch nur noch selten verwandt, weil das Korrelationsband
mit der Zahl der zur Verfügung stehenden Analysen immer breiter wurde. Danach ist der
ozeanische Erdmantel, aus dem die MOR-Basalte stammen, zeitintegriert stark an inkompatiblen Elementen verarmt, verglichen mit dem Mantel, aus dem sich die Basalte der
Ozeaninseln wie Hawaii oder Samoa ableiten (siehe Abbildung 97, Seite 129; der mantle
array entspricht darin ungefähr dem Feld von MORB und dem von Hawaii) oder wie der
Mantel, der an der Bildung der Basalte der Inselbögen beteiligt war (in Abbildung 97 nicht
dargestellt, um den möglichen Einfluß durch Assimilation kontinentaler Kruste zu eliminieren).
verarmt
10
Feld der Sr-NdKorrelation
ozeanischer Basalte
Relation zwischen Sr- und NdIsotopenzusammensetzung der
kontinentalen Erdkruste
„bulk-earth“
0
-10
(Se
«Nd
dim
en
angereichert
-20
te,
arc
ha
isc
Gr
an
he
ito
ide
phanerozoische
Kruste mit hohem
Rb/Sr (Granitoide,
Sedimente)
Kru
ste
,M
eta
mi
th
mo
rph
oh
ite
-30
alte Kruste mit
niedrigem Rb/Sr
(Granulite)
-40
em
Rb
/Sr
au
ße
rG
ran
uli
ten
)
-50
0.700
0.710
0.720
87
ABBILDUNG 49
0.730
0.740
0.750
86
Sr/ Sr
Variation von Sr- und Nd-Isotopien in Gesteinen der kontinentalen Kruste.
Die Pfeile geben die Richtung der Änderung der Isotopien als Funktion der
(nicht spezifizierten) geologischen Zeit wieder. Das flächig markierte Feld
gibt die ungefähren Begrenzungen für Gesteine der kontinentalen Kruste
an. Im Bereich links und oberhalb der gestrichelten sich im bulk-earth-Punkt
kreuzenden Linien liegt das Feld der zeitintegriert an Nd relativ zu Sm und
Rb relativ zu Sr verarmten Gesteine (bzw. Quellregionen der Gesteine, insbesondere der Erdmantel), im Bereich rechts und unterhalb dieser Linien das
Feld der zeitintegriert angereicherten Materialien, insbesondere die konti61
Das Sm–Nd-System
nentale Oberkruste. Die beiden übrigen Quadranten sind seltener belegt;
links unten liegen insbesondere alte Granulite, die zwar eine relative Anreicherung der leichten REE zeigen, aber Rb-arm sind und damit ein sehr kleines Rb/Sr haben; rechts oben liegt z.B. stark hydrothermal alterierte
Ozeankruste.
Die heutige Nd-Isotopie der chondritischen Meteorite von »0.512638 kann auch für die
Erde als gültig angenommen werden, weil man davon ausgehen kann, daß die Erde, als ein
einziges homogenes Reservoir betrachtet, Sm und Nd in chondritischem Verhältnis enthält. Aus der Korrelation der Sr- und Nd-Isotope für ozeanische Basalte folgt, daß dem
chondritischen 143Nd/144Nd-Wert ein 87Sr/86Sr-Verhältnis von »0.7045 – 0.7052 entspricht,
das man in erster Näherung als Sr-Isotopie der Gesamterde ansehen kann – vorausgesetzt
die Sr-Isotopie der Erdkruste ist davon nicht zu weit entfernt, und es gibt im tieferen Erdmantel keine Reservoire, die nicht an der Produktion von Basaltmagmen beteiligt waren
und völlig andere Rb/Sr-Verhältnisse haben.
Die Gesteine, welche die kontinentale obere Erdkruste aufbauen (Granitoide, klastische
Sedimente), zeichnen sich durch eine außerordentlich hohe Variation ihrer Rb/Sr-Verhältnisse aus, während ihre Sm/Nd-Verhältnisse einander sehr ähnlich sind. Infolgedessen
wird für diese Gesteine auch keine Korrelation mehr zwischen 87Sr/86Sr und 143Nd/144Nd
beobachtet (mit der eventuellen Ausnahme von genetisch zusammengehörenden
Gesteinskomplexen), was besonders deutlich am Beispiel von Granitoiden und deren
metamorphen Äquivalenten wird (siehe Abbildung 49, die nach verschiedenen Literaturdaten zusammengestellt ist).
Da die Fraktionierung von Sm und Nd in der Natur sehr gering ist, verglichen mit der von
Rb und Sr, kann man aus dem 143Nd/144Nd eines Gestein oft einen ganz groben Altershinweis ablesen. Abbildung 49 zeigt z.B., daß präkambrische Granitoide bzw. Gneise
143
Nd/144Nd<0.5120 haben, phanerozoische Granitoide und Gneise von durchweg >0.5120
– vorausgesetzt sie sind nicht durch Assimilation oder Aufschmelzung von geologisch alter
Kruste entstanden. Diese grobe Korrelation zwischen 143Nd/144Nd und dem Alter kann
man quantitativ als sogenanntes Modellalter ausdrücken.
5.4
Modellalter
Der Begriff des Modellalters ist nicht für ein bestimmtes Isotopensystem definiert sondern
allgemein. Unter einem Modellalter versteht man die Zeit, zu der ein Gestein dieselbe Isotopenzusammensetzung hatte wie das Material, das zum Vergleich herangezogen wird, in
der Regel das (hypothetische) Material, aus dem das interessierende Gestein entstanden ist.
Falls sich die Isotopie des Bezugsreservoirs halbwegs linear mit der Zeit entwickelt, kann
man das Modellalter als durch eine Zweipunktisochrone bestimmbar ansehen; der zweite
Datenpunkt ist das heutige Sm/Nd- und 143Nd/144Nd-Verhältnis (bzw. Rb/Sr und 87Sr/86Sr,
analog für andere Isotopensysteme) des Bezugsreservoirs. Voraussetzung für die Berechnung eines vernünftigen Modellalters ist daher, daß man eine begründete Annahme für die
Isotopie des Ausgangsmaterials machen kann. Meist wird das nur schwer möglich sein,
weil dieses Material nicht zugänglich ist. So wird bei einem Granit, der durch Aufschmelzung von kontinentaler Unterkruste entstanden ist, das Ausgangsmaterial nicht zur Beprobung zur Verfügung stehen, auch wenn potentiell hochmetamorphe Al-reiche Metapelite
der Umgebung in Verdacht stehen, die Restite dieses Prozesses zu sein. Außerdem ist die
Isotopie der Kruste ziemlich heterogen, was sicherlich auch für die Quellregion der Granite
gilt. Sm–Nd-Modellalter werden daher meist anders berechnet (Abbildung 50):
Es gibt eine Reihe von Indizien dafür, daß im Lauf der Erdgeschichte die kontinentale Kruste letztlich durch Differentiationsprozesse aus dem Erdmantel gebildet worden ist. Man
nimmt daher meist an, daß der zweite Modellpunkt der Isochronen der Erdmantel ist, und
zwar nicht chondritischer, sondern ein als Folge der Differentiationsprozesse an inkompatiblen Elementen verarmter Erdmantel. Das so berechnete Modellalter wird auch oft, insbesondere wenn es sich um klastische Sedimente handelt, als crustal residence age bezeich-
62
A. Radiogene Isotopensysteme
net. Dieser Ausdruck beinhaltet, daß man nicht davon ausgehen darf, das betrachtete
Gestein sei direkt aus dem Erdmantel entstanden. Ein Sediment kann z.B. aus der Verwitterung von anderen Sedimenten entstanden sein, die ihrerseits bereits aus anderen Sedimenten hervorgegangen sind, die wiederum Verwitterungsprodukte von Granitoiden sind
etc. Daß man dennoch im Fall des Sm–Nd-Isotopensystems auch für ein solches Beispiel
noch ein vernünftiges Modellalter erhalten kann, ergibt sich daraus, daß mit der Bildung
und Umlagerung von Sedimenten keine wesentliche Fraktionierung des Sm/Nd-Verhältnisses einhergeht, so daß auch das Sm/Nd von solchen umgelagerten Sedimenten noch
repräsentativ ist für das ihres ehemals magmatischen Ausgangsgesteins.
0.5130
tel
n
ma
m
rar
ve
0.5120
ob
ter
er
ir
rvo
ese
Modellalter
1
t [Ga]
eis
ogn
Orth
0.5105
1.5
E
i
(pr
riti
nd
o
ch
a
rdm
Metamorphosealter
0.5115
0.5110
ABBILDUNG 50
tiv
mi
sR
e
sch
l)
nte
rd
E
rer
e
Modellalter
143Nd/144Nd
0.5125
Illustration eines Modellalters:
Die Isotopie der interessierenden Probe wird
zeitlich zurückgerechnet, bis ihre Entwicklungskurve sich mit der Entwicklung eines Modellreservoirs schneidet.
0.5
Metamorphosealter
0
Ob ein Modellalter sinnvoll ist, hängt davon ab, wie sinnvoll die Wahl des
Modellreservoirs ist, gegen welches das Alter der interessierenden Probe errechnet wird.
Wenn Modellalter irgendeine geologische Bedeutung haben sollen, muß eine Reihe von
Bedingungen erfüllt sein[54]:
1.
2.
3.
Die Wahl des Modellpunktes muß sinnvoll sein. Die Wahl von chondritischem (unfraktioniertem) Erdmantel als Modellpunkt kann genauso sinnvoll oder sinnlos sein
wie die Wahl von an inkompatiblen Elementen verarmtem Erdmantel. Bei Wahl von
unfraktioniertem Erdmantel werden die Nd-Modellalter für Granitoide etc. (Gesteine
mit Sm/Nd < chondritisch) niedriger sein als bei Wahl von ozeanischem Erdmantel.
Die Isotopenentwicklung, d.h. sowohl Sm/Nd als auch 143Nd/144Nd von interessierendem Gestein und dessen Ausgangsmaterial (z.B. dem verarmten Erdmantel) muß genügend voneinander abweichen, so daß in einem 143Nd/144Nd – Zeit-Diagramm der
Schnittpunkt der beiden Isotopenentwicklungslinien wohl definiert ist. Da basische
Gesteine, insbesondere wenn sie höhere Aufschmelzgrade des Erdmantels repräsentieren, oft relativ hohe Sm/Nd-Verhältnisse haben, lassen sich für Basite nur selten solche
Modellalter ableiten.
Die Isotopenentwicklung des Modellreservoirs muß hinlänglich bekannt sein. Das ist
für den oberen Erdmantel der Fall. Die Isotopenentwicklung kann aber nicht als völlig
linear mit der Zeit angenommen werden, da die großen Krustenbildungsprozesse episodisch und nicht kontinuierlich verliefen. Eine ganz grobe Abschätzung der Isotopen63
Das Sm–Nd-System
entwicklung des verarmten Erdmantels kann nach der empirischen Formel eNd(t) =
0.25t2 – 3t + 8.5 [T = Alter in Ga] vorgenommen werden[55]. Man wird aber nicht davon
ausgehen dürfen, daß zu jedem Zeitpunkt überall die Isotopenzusammensetzung des
Erdmantels identisch ist, weil die Verarmung an inkompatiblen Elementen episodisch
und lokalisiert, insbesondere bei Orogenesen, ist.
Für die praktische Berechnung des Nd-Modellalters mit dem verarmten Erdmantel als
Bezugsreservoir eignet sich diese Abschätzung der Nd-Isotopie des Mantels nicht besonders, da die resultierende Gleichung nur iterativ lösbar wird. Man kann alternativ
auch von einer zeitlich linearen Änderung der Nd-Isotopie des verarmten oberen Erdmantels ausgehen, weil der Beitrag des quadratischen Gliedes der Gleichung gering ist.
Da das Modellalter die Zeit ist, zu der die interessierende Probe dieselbe Isotopie hatte
wie das Bezugsreservoir, gilt:
æ 143Nd ö
æ 147 Sm ö
æ 143Nd ö
æ 147 Sm ö
lt
lt
e
1
=
ç 144 ÷
ç 144 ÷
ç 144 ÷
ç 144 ÷ e - 1
è Nd ø dm è Nd ø dm
è Nd ø Probe è Nd ø Probe
(
)
(
)
æ 147 Sm ö
æ 147 Sm ö
æ 143Nd ö
æ 143Nd ö
lt
lt
e
1
e
1
=
ç 144 ÷
ç 144 ÷
ç 144 ÷
ç 144 ÷
è Nd ø Probe
è Nd ø dm è Nd ø Probe
è Nd ø dm
(
)
(e
lt
(
)
-1 =
)
æ 143Nd ö
æ 143Nd ö
ç 144 ÷ - ç 144 ÷
è Nd ø dm è Nd ø Probe
æ 147 Sm ö
æ 147 Sm ö
ç 144 ÷ - ç 144 ÷
è Nd ø dm è Nd ø Probe
ù
é æ 143Nd ö
æ 143Nd ö
ú
ê ç 144 ÷ - ç 144 ÷
ú
1 ê è Nd ø dm è Nd ø Probe
1
t = ln ê 147
+ ú
l ê æ Sm ö
æ 147 Sm ö
ú
- ç 144 ÷
ú
ê çè 144Nd ÷ø
Nd
è
ø
dm
Probe
û
ë
4.
5.
[GL 64]
mit dm = „depleted mantle“, dessen 143Nd/144Nd mit » 0.5131 und 147Sm/144Nd mit
0.22 angesetzt werden kann.
Der Differentiationsprozeß muß innerhalb kurzer Zeit ablaufen, d.h. Zwischenstufen
der Differentiation mit einem vom Endprodukt sehr verschiedenen Sm/Nd-Verhältnis
und damit unterschiedlicher Wachstumsgeschwindigkeit des 143Nd/144Nd dürfen nur
geologisch kurze Zeit bestanden haben. Wenn sich z.B. aus dem Erdmantel zuerst ein
Gabbro bildet und daraus erst einige 100Ma später der Granit, dessen Modellalter man
errechnen will, dann wird dieses Modellalter, je nachdem ob der Gabbro ein höheres
oder niedrigeres Sm/Nd-Verhältnis hatte als der Granit, niedriger oder höher ausfallen
als das wahre crustal residence age.
Bei späteren krustalen Prozessen, z.B. sedimentärer Umlagerung, tritt keine Änderung
des Sm/Nd ein, was sich genauso auswirken würde wie unter 4.) beschrieben.
In Anbetracht der vielen Unbekannten, die in die Berechnung der Modellalter eingehen,
darf man nicht erwarten, auf diese Weise geologisch genau definierte Alter zu erhalten,
sondern wird schon einige 100Ma als Unsicherheit zulassen müssen. Zur genauen Datierung ist das Verfahren daher unbrauchbar mit Ausnahme der seltenen Fälle, in denen die
Isotopenzusammensetzung des Bezugsreservoirs nicht kritisch für die Altersberechnung ist
(Z.B. werden im Rb–Sr-System Modellalter von Glimmern meist recht exakt das geologische Alter ihrer magmatischen oder metamorphen Entstehung widerspiegeln infolge ihrer
extrem hohen Rb/Sr-Verhältnisse. Für 87Rb/86Sr = 10 und 87Sr/86Sr = 0.900, ist t = 1.39 Ga,
wenn das Modellreservoirs ein 87Rb/86Sr = 0 und 87Sr/86Sr = 0.700 hat; es liegt bei 1.34 Ga
für Modellwerte von 87Rb/86Sr = 0.1 und 87Sr/86Sr = 0.710).
64
A. Radiogene Isotopensysteme
«Nd(t)
Mit Hilfe der
5
Nd-ModellalterInitiale Nd-Isotopien krustaler
systematik hat
Gesteine aus Mitteleuropa
kaleman
z.B.
0
donisch
Metamorphite
erschlossen,
1.4Ga
herzynisch
Granitoide
daß die kontiSedimente
nentale Kruste
-5 1.7G
a
in Mitteleuropa
(Gneise, Grani2.0Ga
toide, klasti-10
sche Sedimente)
überwiegend
„crustal resi-15
dence ages“ von
2.5Ga
»1.6 – 2.0 Ga
aufweist (in
-20
Abbildung 51
für Granitoide
3.0Ga
und Gneise dar-25
gestellt[56]) und
600
400
200
0
daß das mittlere
t [Ma]
Alter der kontinentalen Kruste weltweit um ABBILDUNG 51 Initiale Nd-Isotopien der kontinentalen Kruste Mitteleuropas.
Die Geraden stellen die Entwicklung der initialen e-Werte dar, die für Kruste
ca. 2 Ga liegt.
im Mittel zu erwarten ist, die zu den angegebenen Zeiten durch Differenzierung aus dem Erdmantel entstanden ist.
Nd-Modellalter, relativ zu verarmtem Erdmantel [Ma]
Bei der Analyse von Grani3500
toiden, die potentiell aus
Zusammenhang zwischen
den verschiedensten AusNd-Modellalter und
gangsgesteinen entstehen
3000
geologischem Alter für
können, ist die ModellalterGranitoide
systematik zuweilen auch
2500
noch zu etwas anderem
nütze (siehe Abbildung
52[57] mit zusätzlichen
2000
Daten aus [55], [56], [57],
[58]). Wenn man das NdModellalter gegen das geo1500
logische Alter aufträgt,
stellt man fest, daß die Differenz dieser beiden „Alter“
1000
umso größer ist, je jünger
die Granitoide sind, auch
500
wenn die Relation für hohe
Alter zugegebenermaßen
nur mit wenigen Daten
0
belegt ist. Bis vor »2 Ga
0
500
1000
1500
2000
2500
3000
3500
sind geologisches und
geologisches Alter [Ma]
Modellalter mehr oder
weniger identisch. D.h.
jene alten Granite müssen ABBILDUNG 52 Die Nd-Modellalter phanerozoischer Granitoide
innerhalb geologisch kur- sind meist wesentlich höher als die geologischen Alter, weil sie in
zer Zeit durch Differentia- der Regel nur eine geringe I-Typ-Komponente aufweisen.
tion aus dem Erdmantel entstanden sein. Dagegen gibt es unter den phanerozoischen Gra-
65
Das Sm–Nd-System
nitoiden offensichtlich alle Übergänge zwischen solchen, die innerhalb kurzer Zeit aus
dem Erdmantel differenziert sein müssen und solchen, die vollständig durch Aufschmelzung älteren Krustenmaterials entstanden sind.
Initiales «Nd
Dieser Befund läßt sich
10
auch am Beispiel der
Nd-Isotopie des Erdmantels
mesozoisch-känoNd-Isotopenzusammenzoischen Batholithe
5
setzung der Granitoide
im Westen der USA
im Westen der U.S.A.
von Kalifornien bis
Utah demonstrieren
0
(siehe Abbildung 53).
Nd
Die Bildung dieser
-Is
-5
ot
Batholithe steht im
op
ie
Zusammenhang mit
de
rK
der Subduktion der
ru
-10
ste
p a z i fi s c h e n P l a t t e
un
te
unter den nordamerirh
al
-15
b
kanischen Kontinent.
10
km
In der Abbildung sind
die initialen eNd-Werte
-20
dieser Granitoide (also
eNd zur Zeit ihrer IntruKalifornien
Nevada
Utah
-25
sion) gegen die Entfer0
200
400
600
800
1000
1200
nung von der Westkm Entfernung von der Pazifikküste
küste aufgetragen.
Entlang der Westküste
fi n d e t m a n h o h e ABBILDUNG 53 Variation der initialen Nd-Isotopien von Granitoiden
initiale eNd-Werte, die im Westen der U.S.A. als Funktion des Abstands von der (ehemaligen)
fast dem des verarm- Subduktionszone
ten ozeanischen oberen Erdmantels entsprechen. Diese Granitoide enthalten daher fast ausschließlich Erdmantel-Nd. Die initialen eNd-Werte sinken in Richtung Inland und sind im Osten von Nevada
nicht mehr unterscheidbar von den Werten, die man für die kontinentale Erdkruste dort
annimmt, d.h. dort ist kein Einfluß des Erdmantels (bzw. in diesem Fall der subduzierten
ozeanischen Kruste) in den Granitoiden mehr zu erkennen; die Bildung dieser Granitoide
kann daher nicht mehr in Zusammenhang mit der Subduktion gestellt werden. Diese
Abbildung macht jedoch auch die Grenzen der Modellalterberechnung deutlich: Offensichtlich gibt es unter den Granitoiden alle Übergänge zwischen solchen, die sich aus dem
Erdmantel und solchen, die sich aus der kontinentalen Kruste ableiten. D.h. die Batholithe
entlang der Westküste hätten TDM»0; was in guter Näherung ihrem geologischen Alter entspräche, die im Osten von Utah hätten TDM, die in guter Näherung dem tatsächlichen „crustal residence age“ in dieser Region entspräche (»1.8 – 2.5 Ga), während alle übrigen Alter
reine Mischalter wären ohne jegliche geologische Bedeutung.
66
A. Radiogene Isotopensysteme
6.0
Zweikomponentenmischungen
Lineare Beziehungen in einem Isochronendiagramm brauchen nicht immer Alterssignifikanz zu haben, sondern können auch durch Mischen von 2 Komponenten erzeugt werden,
die unterschiedliche Isotopenzusammensetzungen und Elementverhältnisse aufweisen.
Beispiele für Mischungsvorgänge in der Natur sind Magmenkontamination durch Assimilation von Nebengestein, Mischung verschiedener Magmen, die Bildung von Sedimenten
aus Gesteinen unterschiedlicher Herkunft oder die Durchmischung von Fluß-, See- und
Ozeanwasser.
Für die Mischung von 2 Komponenten A und B definieren wir einen Mischungsparameter
f als
f = a / (a+b)
ay
[analog für >2 Komponenten: fy =
å
ay
[GL 65]
; å fy = 1 ], wobei a und b die Massen der beiy
y = A,B¼
den Komponenten in der Mischung darstellen, d.h. f ist der Bruchteil von A in der
Mischung M der Masse m = a + b. Die Konzentration eines beliebigen Elementes X in dieser
Mischung ist gegeben durch die Massenbilanzgleichung
xM = xA ´ f + xB ´ (1 – f) = f ´ (xA – xB) + xB
[für beliebig viele Komponenten: xM =
[GL 66]
å (xy fy ) ] oder, nach f aufgelöst
y = A,B¼
f = (xM – xB) / (xA – xB)
[GL 67]
mit xA und xB = Konzentration des Elements X in Komponente A bzw. B. Betrachtet man
zusätzlich ein zweites Element Y, so gilt dafür eine analoge Gleichung:
f = (yM – yB) / (yA – yB)
[GL 68]
Durch Gleichsetzen der beiden Gleichungen GL 67 und GL 68 läßt sich der Mischungsparameter f eliminieren, und es ergibt sich
(xM – xB) / (xA – xB) = (yM – yB) / (yA – yB)
[GL 69]
yM = [(xM – xB) / (xA – xB)] ´ (yA – yB) + yB
yM = [(xM – xB) ´ (yA – yB) + yB ´ (xA – xB)] / (xA – xB)
yM = (xM ´ yA – xM ´ yB – xB ´ yA + xB ´ yB + xA ´ yB – xB ´ yB) / (xA – xB)
y M = xM ´
y A - y B xA y B - xB y A
+
xA - xB
xA - xB
[GL 70]
In einem Plot yM gegen xM ist dies die Gleichung einer Geraden, da in einer Zweikomponentenmischung die Elementkonzentrationen der Endglieder Konstanten sind.
GL 66 ist auch gültig für den Fall, daß die beiden Komponenten A und B nicht nur verschiedene Elementkonzentrationen, sondern auch unterschiedliche Isotopenzusammensetzungen aufweisen. Die Anzahl der Atome i des Isotops I (z.B. 87Sr) in der Mischung M
ergibt sich zu:
iM =
xA hIA N Av f xB hIB N Av (1 - f )
+
WA
WB
[GL 71]
67
Zweikomponentenmischungen
wobei h die Häufigkeit des Isotops I im Element X und W das Atomgewicht des Elements
X in den beiden Komponenten A und B sowie NAv die Avogadro-Zahl sind, z.B. für Sr:
87
SrA h87 A N Av f SrB h87B N Av (1 - f )
+
WA
WB
SrM =
Eine analoge Gleichung gilt für die Zahl der Atome j eines zweiten Isotops J desselben Elements, z.B. 86Sr:
86
SrA h86 A N Av f SrB h86 B N Av (1 - f )
+
.
WA
WB
SrM =
Dividiert man die Gleichungen für iM und jM durcheinander, dann resultiert:
(
(
)
)
(xA hIA N Av f ) WA + xB hIB N Av (1 - f ) WB
æ iö
ç ÷ = RM =
è jø M
xA hJA N Av f WA + xB hJB N Av (1 - f ) WB
(
RM =
)
(xA hIA f ) WA + (xB hIB (1 - f )) WB
(xA hJA f ) WA + (xB hJB (1 - f )) WB
[GL 72]
z.B. für 87Sr/86Sr:
æ
ç
è
87
86
(
(
)
)
(SrA h87A f ) WA + SrB h87B (1 - f ) WB
Sr ö
.
÷ =
Sr ø M ( SrA h86 A f ) WA + SrB h86 B (1 - f ) WB
In der Regel gilt für die Atomgewichte WA » WB und oft für die Häufigkeit des Isotops j (z.B.
im Fall von Nd, Hf, Os und meist sogar für Sr) hJA » hJB (Z.B. für 87Sr/86Sr von 0.700 und
0.800 differiert die Häufigkeit des 86Sr um weniger als 1% und die Atomgewichte sogar nur
um 0.08%.). Mit diesen Näherungen vereinfacht sich GL 72 zu:
RM
1
xA hIA f + xB hIB (1 - f )
W
=
1
xA hJA f + xB hJB (1 - f )
W
[
[
RM =
RM =
]
]
xA hIA f + xB hIB (1 - f )
[
]
hJ xA f + xB (1 - f )
xA hIA f
[
]
hJ xA f + xB (1 - f )
+
xB hIB (1 - f )
[
]
hJ xA f + xB (1 - f )
Das Isotopenhäufigkeitsverhältnis hIA/hJ ist identisch mit RA und hIB/hJ = RB und der Nenner
der Gleichung [xA ´ f + xB ´ (1 – f)] = xM nach GL 66, also:
RM = RA f
xA
x
+ RB (1 - f ) B
xM
xM
[GL 73]
Diese Gleichung kann benutzt werden, um die Isotopenzusammensetzung von Zweikomponentenmischungen für beliebige f-Werte zu berechnen.
æ
Für Sr ergibt sich: ç
è
87
86
æ
Sr ö
÷ =ç
Sr ø M è
87
86
SrA æ
Sr ö
÷ f Sr + ç
Sr ø A
è
M
87
86
SrB
Sr ö
÷ (1 - f ) Sr
Sr ø B
M
Zur Eliminierung des Mischungsfaktors f wird GL 73 nach f aufgelöst:
68
A. Radiogene Isotopensysteme
RM = RA f
RM - RB
xA
x
x
+ RB B - RB f B
xM
xM
xM
æ
xB
x
x ö
= f ç RA A - RB B ÷
xM
xM
xM ø
è
RM - RB xB / xM
RA xA / xM - RB xB / xM
f =
1 xM ( RM xM - RB xB )
f =
f =
1 xM ( RA xA - RB xB )
( RM xM - RB xB )
( RA xA - RB xB )
[GL 74]
Dies, mit GL 67 gleichgesetzt, ergibt:
xM - xB ( RM xM - RB xB )
,
=
xA - xB
( RA xA - RB xB )
und daraus resultiert, nach RM aufgelöst:
( xM - xB )( RA xA - RB xB ) = R
M
xA - xB
RM = RB xB
RM
(R
=
B
xM - RB xB
( xM - xB )( RA xA - RB xB )
xA - xB
+
xM ( xA - xB )
xM ( xA - xB )
) (
xA xB - RB xB2 + RA xA xM - RB xB xM - RA xA xB + RB xB2
)
xM ( xA - xB )
RM =
( RB xA xB - RA xA xB ) + ( RA xA xM - RB xB xM )
xM ( xA - xB )
RM =
RM =
1
xM
xA xB ( RB - RA )
xM ( xA - xB )
+
xM ( RA xA - RB xB )
xM ( xA - xB )
é xA xB ( RB - RA ) ù ( RA xA - RB xB )
ú+
ê
( xA - xB )
êë ( xA - xB ) úû
[GL 75]
z.B. für Sr:
æ 87 Sr ö
ç 86 ÷
è Sr ø M
ì
éæ 87 Sr ö
æ 87 Sr ö ù ü æ 87 Sr ö
æ 87 Sr ö
ïï SrA SrB êç
÷
ç 86 ÷ ú ïï ç 86 ÷ SrA - ç 86 ÷ SrB
86
êëè Sr ø B è Sr ø A úû ý è Sr ø A
è Sr ø B
1 í
=
ï
ï+
SrM ïî
( SrA - SrB )
( SrA - SrB )
ïþ
Dies ist die Gleichung einer Hyperbel, wenn man RM gegen xM aufträgt:
RM = a/xM + b
oder eine Geradengleichung, wenn man RM gegen 1/xM aufträgt:
69
Zweikomponentenmischungen
RM = (1/xM) ´ a + b
[GL 76]
0.735
0.735
Endglied B:
150ppm Sr;
87Sr/86Sr = 0.730
87
Sr/86Sr
0.730
Illustration einer
Zweikomponentenmischung
0.730
0.725
0.725
0.720
0.720
0.715
0.715
0.710
0.710
0.705
0.705
Endglied A:
350ppm Sr;
87Sr/86Sr = 0.7025
0.700
150
200
250
ppm Sr
ABBILDUNG 54
300
0.700
350 0.003 0.004
0.005
0.006
0.007
1/ppm Sr
Beispiel für eine Zweikomponentenmischung der Sr-Isotope
Mit einer derartigen Auftragung läßt sich testen, ob sich eine lineare Beziehung in einem
Isochronendiagramm als Mischungslinie interpretieren läßt. Das ist besonders wichtig für
errorchrons, da kaum zu erwarten ist, daß exakt lineare Beziehungen durch Mischungsvorgänge in magmatischen und metamorphen Systemen hergestellt werden. Assimilation von
Fremdgestein durch ein Magma wird kaum zu homogenen Mischungen führen vielleicht
mit Ausnahme von extrem heißen Magmen. Wenn sich die Daten in einem gewöhnlichen
Isochronendiagramm ungefähr auf einer Geraden aufreihen und sich Isotopenverhältnisse
und Konzentrationen (des Elements, welches das Tochternuklid enthält, also z.B. Sr) entlang der Geraden gleichsinnig verändern, liegt ein genügend hoher Anfangsverdacht vor,
um zu testen, ob nicht vielleicht eher eine Mischungslinie vorliegt. Wenn neben der Zweikomponentenmischung auch Prozesse der fraktionierten Kristallisation ablaufen – sicherlich eine plausible Annahme – dann wird die Fraktionierung zudem eine Änderung der
Elementverhältnisse in Kumulaten und Restschmelzen gegenüber der Ausgangsschmelze
verursachen. Im Verlauf der geologischen Zeit können dann aber die linearen Beziehungen
völlig zerstört werden, welche die Mischung belegen. So wird z.B. in pyroxenreichen
Kumulaten die Nd-Isotopie wegen des höheren Sm/Nd-Verhältnisses rascher wachsen als
in der Ausgangsschmelze, während die Sr-Isotopie infolge des sehr niedrigen Rb/Sr hinter
derjenigen der Schmelze zurückbleibt. In einem plagioklasreichen Kumulat wird die Sr-Isotopie wegen des niedrigen Rb/Sr kaum noch wachsen und die Nd-Isotopie wegen des niedrigen Sm/Nd langsamer als in der Ausgangsschmelze. Zum Test auf eine Zweikomponentenmischung müssen daher die Isotopien aller Gesteine auf die vermutete Zeit
zurückgerechnet werden, zu welcher der Mischungsvorgang ablief. Dies ist auch generell
dann sinnvoll, wenn die Mutter/Tochter-Verhältnisse (z.B. Rb/Sr) groß sind und das Alter
hoch ist, da bereits auf diese Weise ursprüngliche Heterogenitäten innerhalb einer Probenserie verdeckt werden können (kleineres MSWD über die geringere Gewichtung Wi der
Datenpunkte allein auf Grund des Alters – siehe GL 58, Seite 46). Ist dieses Alter unbe-
70
A. Radiogene Isotopensysteme
kannt, sollten die Isotopenzusammensetzungen auf verschiedene Alter zurückgerechnet
werden. Dasjenige, für welches sich dabei die beste Korrelation zwischen der Isotopenzusammensetzung und dem Kehrwert des Elementgehaltes (z.B. 1/Nd) ergibt, dürfte dann als
wahrscheinlichstes Alter der Mischung angesehen werden.
In Diagrammen, in denen zwei Verhältnisse radiogener Isotope gegeneinander aufgetragen
werden, z.B. 143Nd/144Nd – 87Sr/86Sr oder 176Hf/177Hf – 143Nd/144Nd, ergeben sich keine
Mischungsgeraden sondern Mischungskurven, die nach Gleichung GL 73 berechnet werden können:
RM = RA f
xA
x
+ RB (1 - f ) B ,
xM
xM
bzw. da xM = x A f + xB (1 - f ) :
RM =
RA xA f + RB xB (1 - f )
xA f + xB (1 - f )
.
Eine Auftragung von zwei Isotopenverhältnissen gegeneinander hat Vorteile gegenüber der
Auftragung eines Verhältnisses gegen eine Konzentration, weil so z.B. Effekte der fraktionierten Kristallisation minimiert werden können (Änderung der Elementgehalte), welche
die Assimilation von Nebengestein durch ein Magma begleiten. Indirekt bleibt aber auch
hier die Konzentrationsabhängigkeit nach GL 73 bestehen. Eine beginnende Ausscheidung
von Plagioklas aus einem Magma wird z.B. den Sr-Gehalt der Restschmelze verringern, so
daß sich anschließend die Assimilation von radiogenem Nebengestein stärker auf die SrIsotopie der Restschmelze auswirken wird als vor der Plagioklasfraktionierung. Als Folge
wird die Mischungslinie ihre Krümmung ändern. Die Notwendigkeit einer Korrektur der
Isotopien auf das Alter der Mischung bleibt bestehen, weil fraktionierte Kristallisation
natürlich auch hier über die Änderung der Mutter/Tochter-Elementverhältnisse im Lauf
der Zeit die Isotopien beeinflußt.
0.706
„Eruptierte Mantelisochrone“ für
Tholeiite der Ozeaninseln und
Ozeanböden
Ga
0.704
t
.5
»1
87
Sr/86Sr
0.705
0.703
0.702
0
0.02
0.04
0.06
87
ABBILDUNG 55
0.08
86
0.10
0.12
0.14
0.16
Rb/ Sr
Sr-Isotopien einer Reihe von ozeanischen Basalten streuen um eine Gerade,
deren Steigung einem Alter um 1.5 Ga entspricht.
71
Zweikomponentenmischungen
Abbildung 54 illustriert eine Zweikomponentenmischung an einem hypothetischen Beispiel. Auch bei Auftragung gegen das Rb/Sr-Verhältnis anstatt gegen 1/Sr ergibt sich eine
lineare Beziehung im Fall von Mischungslinien, weil die Endglieder jeweils nur mit einem
Faktor multipliziert werden.
Ein berühmtes Beispiel einer Pseudoisochronenbeziehung aus der Literatur ist das der
„eruptierten Mantelisochronen“, deren Signifikanz in den 1970-er Jahren diskutiert wurde
(Abbildung 55[61]). Es zeigte sich, daß Rb–Sr-Daten für verschiedene ozeanische Tholeiite
regional gemittelt entlang einer errorchron streuen, deren Steigung einem Alter von »1.5 –
2 Ga entspricht. Da Tholeiite Produkte hoher Aufschmelzgrade des Erdmantels sind, sollten sich Rb quantitativ und Sr nahezu quantitativ in der Schmelze befinden, d.h. die Tholeiite sollten das Rb/Sr-Verhältnis des Erdmantels haben, aus dem sie erschmolzen wurden.
Die Sr-Isotopie ändert sich bei der Aufschmelzung nicht. Das „Isochronenalter“ könnte
dann irgendein Fraktionierungsereignis im Erdmantel datieren. Anfang der achtziger Jahre
wurde diese Hypothese aber beiseite gelegt, weil es wahrscheinlicher wurde, daß die lineare
Beziehung im Rb–Sr-Isochronendiagramm die Vermischung verschiedener Mantelreservoire durch Konvektion in der Asthenosphäre wiederspiegelt, so daß das „Alter“ irgendein
mittleres Alter der Verarmung an inkompatiblen Elementen im Erdmantel anzeigt. Auch
das mittlere Alter der kontinentalen Erdkruste liegt um 2 Ga.
0.5140
Komatiite und Tholeiite
(Abitibi Belt, Kanada)
t = 2826«64Ma
eNd(t) = 2.7±0.3
0.5130
zum Vergleich:
U-Pb-Zirkonalter
ist 2697±1Ma
143
Nd/144Nd
0.5135
0.5125
Komatiite
Tholeiite
0.5120
0.15
0.17
0.19
147
0.21
144
Sm/
ABBILDUNG 56
0.23
0.25
0.27
Nd
Komatiite aus dem Abitibi-Belt scheinen eine wohl definierte Sm–Nd-Isochrone zu bilden, deren Alter allerdings nicht in Einklang mit der Geologie
und mit U–Pb-Zirkondatierungen zu bringen ist.
Andere Isochronen sind nicht so einfach als Mischungslinien zu umzuinterpretieren. So
reihen sich z.B. Komatiite und Tholeiite aus dem Abitibi-Belt in Ontario (Hudson Bay) auf
einer Geraden auf, deren Steigung einem Alter von 2826±64 Ma entspricht (Abbildung 56).
Zirkone aus dazitischen Tuffen stratigraphisch unter der Komatiit–Tholeiit-Serie ergeben
aber ein ca. 125 Ma jüngeres Alter, das als das maximale magmatische Alter der Komatiite
angesehen wird[62]. In Abbildung 57 sind die Nd-Isotopien auf verschiedene Zeiten zurückgerechnet und gegen den Kehrwert der Nd-Konzentration aufgetragen. Die Streuung der
Daten um eine Gerade ist für 2697 Ma (das Zirkon-Alter) und 2826 Ma nicht nennenswert
verschieden, so daß eine Wahrheitsfindung auf diesem Weg nicht möglich erscheint und
72
A. Radiogene Isotopensysteme
man der Interpretation der Geländegeologen bezüglich der Korrektheit der stratigraphischen Abfolge und der Ansprache der dazitischen Tuffe vertrauen muß. – In jedem Fall ist
darauf zu achten, daß eine Isochrone nicht allein auf Grund ihrer Statistik (niedriges
MSWD) bewertet werden sollte, sondern zusätzlich ist eine adäquate, d.h. geologisch sinnvolle, Probenahme der Gesteinsserie von Interesse sicherzustellen.
0.5095
260
a
0M
0.5094
2697
Ma
Komatiite und Tholeiite
(Abitibi Belt, Kanada):
Hinweise auf
Magmenmischung?
0.5092
143
Nd/144Nd
0.5093
2826 Ma
0.5091
2900 Ma
0.5090
0.5089
0.0
0.1
0.2
0.3
0.4
0.5
1/Nd
ABBILDUNG 57
Dieselben Gesteine wie in Abbildung 56 liefern in einem Mischungsdiagramm keine klaren Hinweise für oder gegen das Ereignis einer Zweikomponentenmischung vor ca. 2700 Ma (Größe der Symbole entspricht
ungefähr dem Analysenfehler). Wenn das magmatische Alter der Komatiit–
Tholeiit-Serie tatsächlich bei rund 2700 Ma liegt, hätte das Endglied mit der
höheren Nd-Isotopie den niedrigeren Nd-Gehalt (entsprechend dem höheren 1/Nd) gehabt; dies ist plausibel.
73
Zweikomponentenmischungen
Anhang:
GL 71 ist auch für beliebig viele Komponenten A, B,… gültig:
iM =
xA hIA N Av f A xB hIB N Av f B xC hIC N Av f C
+
+
+¼
WA
WB
WC
Z
iM =
fy
å xy hIy N Av W
Z
jM =
desgleichen für jM:
[GL 77]
y
y =A
fy
å xy hJy N Av W
so daß RM =
RM =
,
y
y =A
fy ö
iM æ Z
= ç å xy hIy N Av
Wy ÷ø
jM è y = A
Z
fy ö
iM æ
= ç N Av å xy hIy
Wy ÷ø
jM è
y =A
æ Z
fy ö
ç å xy hJy N Av W ÷
y ø
èy = A
[GL 78]
Z
æ
fy ö
ç N Av å xy hJy W ÷
y ø
è
y =A
Da WA » WB » WC » … »W (d.h. die Atomgewichte der verschiedenen Phasen sind identisch), vereinfacht sich die Gleichung zu:
RM =
iM æ 1
=
jM çè W
ö
Z
å xy hIy fy ÷
ø
y =A
æ 1
çW
è
Z
ö
å xy hJy fy ÷
y =A
ø
Da außerdem hJA » hJB » hJC »…. » hJ (d.h. z.B. die prozentualen Häufigkeiten von 86Sr in den
verschiedenen Phasen sind identisch):
RM =
ö
iM æ Z
= ç å xy hIy fy ÷
jM è y = A
ø
RM =
hIy ö
iM æ Z
= ç å xy
fy ÷
hJ
jM è y = A
ø
Z
Nach GL 67 ist
å xy fy
Z
æ
ö
h
ç J å xy fy ÷
è y =A
ø
(
æ Z
ö
ç å xy fy ÷
èy = A
ø
)
= xM und hIy / hJ = Ry , also:
y =A
RM =
ö
1 æ Z
xy fy Ry ÷
å
ç
xM è y = A
ø
was für beliebig viele Komponenten identisch ist mit GL 73.
74
[GL 79]
A. Radiogene Isotopensysteme
7.0
Die Massenfraktionierung
Die leichten und flüchtigen Elemente (H, He, Li, C, N, O, Ne, S) erfahren auf Grund der
unterschiedlichen Massen ihrer stabilen Isotope eine gut meßbare Fraktionierung in der
Natur, die mit zunehmender Massendifferenz steigt und mit zunehmender Masse sinkt.
Oft verwechselt wird damit die Isotopenvariation der schwereren Elemente, die auf radioaktiven Zerfallsprozessen beruht. So tauchte z.B. des öfteren in der Literatur die Frage auf,
ob Isotopenvariationen von Basalten tatsächliche Isotopenvariationen ihrer Quellregionen
im Erdmantel widerspiegeln oder nicht vielmehr als Folge der Aufschmelz- oder Differentiationsprozesse erklärt werden können. Meßbare natürliche Isotopenfraktionierungen der
meisten für die Geochronologie wichtigen Elemente scheinen tatsächlich nicht aufzutreten, mögen aber bei weiter verbesserter Meßtechnik durchaus erfaßbar sein. Selbst, wenn
es sie gäbe, hätten sie aber auf das Ergebnis der Isotopenanalysen keinerlei Einfluß, weil
jede Massenfraktionierung – sei sie natürlich oder bei der Analyse auftretend – durch eine
Korrektur der Massenspektrometerdaten eliminiert wird. Eine signifikante massenabhängige Fraktionierung der Isotope, die stets korrigiert werden muß, findet nämlich bei
der Messung im Thermionenmassenspektrometer statt.
Beim Abdampfen von der heißen Oberfläche des Re-, Ta- oder W-Filaments im Hochvakuum der Ionenquelle eines Massenspektrometers gehen die leichteren Isotope eines
Elements bevorzugt in die Gasphase über, weil Bindungen zwischen schweren Isotopen
geringfügig fester sind als die zwischen leichten Isotopen. Von den vier stabilen Sr-Isotopen mit den Massenzahlen 84, 86, 87 und 88 verdampft das 84Sr am leichtesten und das
88
Sr am schwersten (und das 87Sr schwerer als das 86Sr). Von den sieben Nd-Isotopen verdampft das 142Nd am leichtesten und das 150Nd am schwersten und 143Nd leichter als
144
Nd. Da eine massenspektrometrische Messung oft einige Stunden dauert und die Menge
der Probe kein „unendliches“ Reservoir darstellt, wird die auf dem Filament verbleibende
Restprobe kontinuierlich isotopisch schwerer (das Atomgewicht nimmt zu); desgleichen
wird das in die Gasphase eintretende Isotopengemisch, das mit ständig schwererem Isotopengemisch auf dem Filament ins Gleichgewicht tritt, ständig schwerer. D.h. im Verlauf
einer Messung wird das 87Sr/86Sr-Verhältnis einer Probe kontinuierlich steigen, das 143Nd/
144
Nd kontinuierlich fallen. Als ganz groben Richtwert kann man sich merken, daß sich die
Isotopenfraktionierung bei einer solchen mehrstündigen Messung in der Größenordnung
von 1‰ pro Masseneinheit ändert. Dies, in Relation gesetzt zu den »7‰ der heutigen
Variation des 143Nd/144Nd in der Natur, zeigt, daß eine massenspektrometrische Messung
nicht viel nützt, wenn man die Massenfraktionierung nicht korrigieren würde. Eine Probe
mit einem 143Nd/144Nd-Verhältnis von 0.512638 könnte z.B. zu Beginn einer Messung
einen Wert von 0.5130 liefern, zu Ende von 0.5125; eine Probe mit einem 87Sr/86Sr von
0.7040 könnte zu Beginn einen Wert von 0.7035 ergeben, zu Ende von 0.7042. Die Korrektur der Massenfraktionierung wird mit Hilfe zweier Isotope vorgenommen, die nicht aus
Zerfallsprozessen gespeist werden, und deren Verhältnis daher konstant ist. Daraus folgt,
daß für ein Element, welches nur aus zwei natürlichen Isotopen besteht, von denen eines
zum Zweck der Isotopenverdünnungsanalyse mit einem Spike angereichert wird, keine
Korrektur der Massenfraktionierung vorgenommen werden kann. Beim Sr bleiben für die
Fraktionierungskorrektur die Isotope 84Sr, 86Sr und 88Sr übrig, und konventionell wählt
man das Verhältnis 86Sr/88Sr zur Korrektur. Nach zahlreichen Messungen an Proben natürlichen Strontiums wurde für das 86Sr/88Sr-Verhältnis ein Wert von 0.1194 gewählt, mit dem
die Sr-Fraktionierung von jeder Arbeitsgruppe korrigiert wird. Zudem gibt es mehrere internationale Standards für Sr-Isotopenmessungen, gegen welche die eigenen Analysen ständig
geprüft werden. Die 87Sr/86Sr-Analysen aller Laboratorien sind daher direkt miteinander
vergleichbar. Diese Korrektur trägt jeder massenabhängigen Fraktionierung Rechnung –
der im Massenspektrometer und auch eventuellen Fraktionierungen in der Natur oder bei
der Ionenaustauscherchemie zur Abtrennung des Elementes von Interesse. Übrig bleibt der
nicht massenabhängige Anteil, also der durch den radioaktiven Zerfall verursachte.
75
Die Massenfraktionierung
Beim Nd konnte man sich dagegen nicht auf eine derartige Korrektur einigen, sondern es
werden von verschiedenen Isotopenlabors zwei miteinander konkurrierende Korrekturen
der Isotopenfraktionierung verwandt. Bei beiden Normierungen wird entweder das Verhältnis 146Nd/144Nd oder – von den Gruppen, welche die Nd-Messung mit dem Metalloxid
durchführen – das Verhältnis 148NdO/144NdO benutzt. Die große Mehrzahl der Arbeitsgruppen benutzt die Korrektur
146
Nd/144Nd = 0.7219 º 148NdO/144NdO = 0.242436
[GL 80]
eine Minderheit (vornehmlich Wissenschaftler aus dem Umfeld von G.J. Wasserburg und
J.D. DePaolo am Caltech in den 1970-er Jahren) die Korrektur
148
NdO/144NdO = 0.243969
[GL 81]
143
144
Als Folge davon sind die von der zweiten Gruppe veröffentlichten
Nd/ Nd-Daten um
gut 1.5‰ niedriger als die der ersten Gruppe. Der Wert des „bulk-earth“-Bezugsreservoirs
beträgt nach der zweiten Normierung 0.511847. Will man die Werte der zweiten Normierung in die der ersten umrechnen, muß man sie mit dem Verhältnis 0.512638/0.511847
multiplizieren. Alle in diesem Skript vorgestellten 143Nd/144Nd-Daten beziehen sich auf die
Korrektur nach GL 80. Diese etwas chaotischen Zustände in der Nd-Isotopengeochemie
sind vor allem für Nichteingeweihte nicht zu durchschauen. Die Angabe der Nd-Isotopenzusammensetzung in der e-Form hat dagegen den Vorteil, daß die verschiedenen Labors
die 143Nd/144Nd-Werte auf ihren „bulk-earth“-Wert normieren, wodurch die unterschiedlichen Fraktionierungskorrekturen eliminiert werden. Daten, die als eNd, ebulk–earth oder
eCHUR angegeben sind, sind daher direkt miteinander vergleichbar. Nicht vergleichbar sind
dagegen (die nur in den frühen Jahren verwendeten) eJuvinas-Werte, weil hier die Normierung auf eine Probe mit niedrigerem 143Nd/144Nd als das eines chondritischen Reservoirs
erfolgte (als Folge des unterchondritischem Sm/Nd-Verhältnisses dieses Achondriten).
eJuvinas-Werte sind um »1.3e-Einheiten höher als die übrigen e-Werte.
Als Beispiel einer Massenfraktionierung ist die Änderung der Verhältnisse von 86Sr/88Sr und
87
Sr/86Sr über den Verlauf einer Messung in Abbildung 58 dargestellt.
Die Korrektur der Massenfraktionierung kann im einfachsten Fall mit einer linearen Funktion erfolgen, d.h. es wird angenommen, daß die Fraktionierung pro Masseneinheit konstant ist, also z.B. für das Paar 142Nd–146Nd genausogroß ist wie zwischen 146Nd und 150Nd
und viermal so hoch wie zwischen 143Nd und 144Nd oder zwischen 84Sr und 86Sr genauso
groß ist wie zwischen 86Sr und 88Sr. Tatsächlich werden bei genügend präzisen Messungen
kleine Abweichungen von der Linearität beobachtet, die durch einen nicht linearen (exponentiellen) Anteil in der Korrektur behoben werden. Unter Annahme von Linearität – die
komplexeren Rechnungen werden erst danach vorgestellt – kann die Fraktionierungskorrektur folgendermaßen vorgenommen werden:
1.
Wahl eines Isotopenverhältnisses Mi/Mj zur Korrektur der Fraktionierung, wobei Mi
und Mj die Massenzahlen der Isotope darstellen; Mj ist das Referenzisotop, z.B. 86Sr oder
144
Nd;
Beispiele: 146/144 beim Nd, 88/86 beim Sr;
76
A. Radiogene Isotopensysteme
0.1210
0.1205
86Sr/88Sr
gemessen
86Sr/88Sr
0.1200
86Sr/88Sr
0.1195
korrigiert
0.1190
0.1185
0.1180
0.708
87Sr/86Sr
0.706
87Sr/86Sr
korrigiert
0.704
0.702
87Sr/86Sr
0.700
gemessen
0.698
0
50
100
150
Meßblock
ABBILDUNG 58
200
250
300
Zeit
Beispiel für die Änderung der Meßwerte der Sr-Isotope einer Probe infolge
der Massenfraktionierung über den Verlauf einer massenspektrometrischen
Messung; die Änderung tritt auf, weil die Masse des Sr auf dem Filament relativ klein ist und sich über die Messung ständig verringert. Zum Ende der
Messung hin, wenn das Sr weitgehend verbraucht ist, kann seine Isotopenzusammensetzung daher besonders schwer werden, entsprechend niedrigen Werten für das gemessene 86Sr/88Sr und hohen 87Sr/86Sr-Verhältnissen.
77
Die Massenfraktionierung
Das obere Teildiagramm zeigt die Variation der gemessenen Verhältnisse
von 86Sr/88Sr (kleine Quadrate), die per Konvention auf das wahre Verhältnis
von 0.1194 korrigiert werden (durchgezogene Linie). Im unteren Teildiagramm sind die Meßwerte für 87Sr/86Sr als kleine Quadrate dargestellt. Mit
Hilfe der Korrektur für 86Sr/88Sr aus dem oberen Teildiagramm werden die
87
Sr/86Sr-Werte korrigiert (zackige blaue Kurve). Die durchgezogene gestrichelte Linie bei 87Sr/86Sr = 0.70326 stellt den Mittelwert dieser korrigierten
Werte für die gesamte Messung dar.
2.
Berechnung der Fraktionierung a = Fraktionierungsfaktor pro Masseneinheit, Dmij =
Massendifferenz zwischen Mi und Mj:
(
(
)
)
Std
é
ù
ö
1 ê M i M j Std
1 æ Rij
ú
a=
-1 =
ç meas - 1÷
ú Dmij è Rij
Dmij ê M i M j
ø
meas
ë
û
[GL 82]
wobei meas für gemessen (measured) und Std für Standard stehen möge, z.B. für Sr: D =
88–86=2 (oder ganz genau: die Differenz der exakten Atommassen); Rij steht für das
ù
1 éê (88 86)Standard
- 1ú mit (88/86)Std =
2 ê (88 86) gemessen
ú
û
ë
(88Sr/86Sr) im Standard = 1/0.1194 (in allen Proben identisch, so daß dieses Verhältnis
für die Fraktionierungskorrektur beliebiger Proben verwendet wird); aSr wird i.a. zu Beginn der Messung >0 sein;
Isotopenverhältnis zwischen i und j und a Sr =
ù
1 éê (146 144)Standard
- 1ú ,
2 ê (146 144) gemessen
ú
ë
û
wobei (146/144)Std = 0.7219 in allen Proben identisch ist; dieser Wert kann daher zur
Nd-Fraktionierungskorrektur benutzt werden; aNd= wird zu Beginn der Messung ebenfalls positiv sein;
Korrektur der Isotopenverhältnisse:
für Nd: D = 146–144 = 2; a Nd =
3.
z.B. für 143Nd/144Nd: (143Nd/144Nd)calc = (143Nd/144Nd)meas ´ (1 + a´Dm143-144); calc
möge für korrigiert stehen; wenn a bei Meßbeginn positiv und Dm = -1 ist, wird der
korrigierte Wert sinken;
für 87Sr/86Sr: (87Sr/86Sr)calc = (87Sr/86Sr)meas ´ (1 + a´Dm87-86); da a und Dm beide positiv
sind, steigt der korrigierte Wert;
für 84Sr/88Sr: (84Sr/88Sr)calc = (84Sr/88Sr)meas ´ (1 + a´Dm84-88); a ist bei Meßbeginn positiv
und Dm = -4; das korrigierte Isotopenverhältnis sinkt gegenüber dem Meßwert.
Bei dieser linearen Korrektur geht man davon aus, daß die Massenfraktionierung proportional zur Massendifferenz ist und unabhängig von der Masse selbst. Tatsächlich sollte aber
eine zusätzliche inverse Abhängigkeit von der Masse bestehen. Bei hoch präzisen Analysen
insbesondere der leichten Elemente oder von Elementen mit großer Massendifferenz der
Isotope kann es dann notwendig werden, dieser Abhängigkeit durch eine exponentielle
Korrektur Rechnung zu tragen, z.B. im Fall der Analyse der Ca-Isotope[63].
Die oben dargestellte lineare Korrektur ist lediglich ein vereinfachter Fall einer Potenzfunktion (englisch: „power law“), die sich allgemein folgendermaßen formulieren läßt:
Rijcalc = Rijmeas (1 + a )
Dmij
Logarithmiert und aufgelöst ergibt sich für den Fraktionierungsfaktor a:
78
[GL 83]
A. Radiogene Isotopensysteme
æ Rijcalc ö
1
lnç meas ÷ = ln(1 + a )
Dmij è Rij ø
1
æ Rijcalc ö Dmij
a = ç meas ÷
-1
è Rij ø
[GL 84]
Entwickelt man GL 83 als Taylor-Reihe, erhält man:
(
)
(
)(
)
ù
é
Dmij Dmij - 1 2 Dmij Dmij - 1 Dmij - 2 3
Dmij
Rijcalc = Rijmeas ê1 +
a+
a +
a + ¼ú
1!
2!
3!
ú
ê
û
ë
[GL 85]
Das dritte Glied in der Klammer ist für kleine Werte von a bereits klein gegen das zweite,
so daß man die Reihe unter dieser Voraussetzung schon nach dem zweiten Glied abbrechen darf*. Nach a aufgelöst ist diese Gleichung dann identisch mit GL 82 (wenn man
berücksichtigt, daß für das Isotopenpaar, das zur Fraktionierungskorrektur verwendet wird,
Std und calc identisch sind), entspricht also der linearen Korrektur. Das bedeutet, daß die
Korrekturen nach dem linearen Gesetz und dem power law meist identische Ergebnisse liefern. Formuliert man eine analoge Gleichung für ein zweites Isotopenverhältnis zwischen
j und k (wobei mj das mittelschwere der drei Isotope sein möge), und bricht sie nach dem
zweiten Glied ab:
(
Rjkcalc = Rjkmeas 1 + Dm jk a
)
[GL 86]
löst die nach dem zweiten Glied abgebrochene GL 85 nach a auf und setzt in GL 86 ein,
dann ergibt sich:
Rjkcalc
Rjkmeas
= 1+
ö
Dm jk æ Rijcalc
ç meas - 1÷
Dmij è Rij
ø
[GL 87]
In einer Auftragung von Rjkcalc Rjkmeas gegen Rijcalc Rijmeas ist dies die Gleichung einer Geraden, deren Steigung zwar abhängig vom Verhältnis der Massendifferenzen, aber unabhängig von der Masse der Isotope ist. Bei exakt gleicher Massendifferenz zwischen i–j und j–k,
z.B. für 40Ca/44Ca und 44Ca/48Ca, wenn lediglich ganze Massenzahlen eingesetzt werden,
vereinfacht sich GL 87 zu
Rjkcalc Rjkmeas = Rijcalc Rijmeas
d.h. nach dem linearen Gesetz und auch dem power law ist die Massenfraktionierung allein
von der Massendifferenz abhängig; nicht lineare Effekte werden vernachlässigt.
Gerade für das Beispiel der Ca-Isotope ist jedoch bekannt, daß ein lineares oder fast lineares
Gesetz nur eine unzureichende Korrektur der Massenfraktionierung liefert und daß anstatt
dessen eine Funktion verwendet werden muß, bei der die Massenfraktionierung auch von
der Masse selbst abhängt[63],[64],[65]. Zu diesem Zweck wird eine Funktion verwendet, bei der
die Masse im Exponenten steht („exponential law“), z.B. eine Gleichung der Form
* Zum Beispiel errechnet man für einen hohen Wert von a von 1‰ und eine maximale Differenz der
Ca-Isotope von 8 zwischen 48Ca und 40Ca für das zweite Glied in der Klammer 0.08 und für das dritte Glied 0.0028, also ein Verhältnis von knapp 29.
79
Die Massenfraktionierung
Rijcalc
=
æm ö
i
÷
è mj ø
amj
Rijmeas ç
=
æ m j + Dmij ö
÷
mj
è
ø
amj
Rijmeas ç
[GL 88]
Auch hieraus läßt sich durch Auflösen a errechnen:
æ Rijcalc ö
æm ö
lnç meas ÷ = a m j lnç i ÷
è mj ø
è Rij ø
(
calc
Rijmeas
1 ln Rij
a=
´
mj
ln mi m j
(
)
[GL 89]
)
1.015
1.010
korrigiert/gemessen
1.005
für 86Sr/87Sr
1.000
0.995
für 86Sr/88Sr
0.990
0.985
0.985
0.990
0.995
84Sr/86Sr
ABBILDUNG 59
80
1.000
1.005
1.010
1.015
84
86
korrigiert/ Sr/ Srgemessen
Auf der Basis desselben Datensatzes wie in Abbildung 58 sind die Verhältnisse (86Sr/88Srcalc)/(86Sr/88Srmeas) sowie (86Sr/87Srcalc)/(86Sr/87Srmeas) gegen
(84Sr/86Srcalc)/(84Sr/86Srmeas) aufgetragen, wobei die Isotopenverhältnisse
nur linear (» power law) nach GL 86 korrigiert wurden. Die Daten zeigen für
86
Sr/88Sr eine minimale Abweichung von einer Geraden mit einer Steigung
von 1 (und noch weniger von der Steigung 1/2 für 86Sr/87Sr), was bedeutet,
daß eine lineare Korrektur die Fraktionierung nicht vollständig beschreibt.
A. Radiogene Isotopensysteme
Als Reihe entwickelt, ergibt sich für GL 88:
Rijcalc
é
=
Rijmeas ê1 + a
êë
Dmij - a
Dmij2
2mj
+a
2
Dmij2
2
ù
+ ¼ú
úû
[GL 90]
Diese vier Glieder in der Klammer genügen in der Regel für eine Fraktionierungskorrektur.
Der dritte Term in der Klammer in dieser Gleichung tritt in GL 85 nicht auf. Er vermindert
den Korrekturfaktor in der Klammer gegenüber dem power law um einen Betrag, der umgekehrt proportional zur Masse ist*. Der Wert für die Fraktionierungskorrektur wird zudem
abhängig vom gewählten Isotopenverhältnis eines Elementes sein; zum Beispiel wird er für
die Ca-Isotope für das Paar 44Ca–40Ca etwas größer sein als für das Paar 48Ca/44Ca. Als
andere mögliche Korrekturfunktion für die Massenfraktionierung könnte man an eine
Abwandlung des Rayleighschen Destillationsgesetzes denken mit einem Fraktionierungsfaktor umgekehrt proportional zur Quadratwurzel aus der Masse.
Ob eine lineare Fraktionierungskorrektur oder eine nach dem power law genügt, muß von
Fall zu Fall getestet und entschieden werden; ein striktes Rezept für die Anwendung gibt es
nicht. Das exponential law sollte die besseren Korrekturen liefern bei Elementen mit geringen Massen und/oder großen Massendifferenzen der Isotope, während bei großen Massen
und geringen Massendifferenzen keine nennenswerten Unterschiede zwischen den verschiedenen Korrekturverfahren zu erwarten sind. Welche Massen in die Gleichungen einzusetzen sind, ist ebenfalls nicht von vornherein klar. Falls zum Beispiel ein Elementoxid
vom Filament abdampft und nicht ein Metall, könnte Einsetzen der Massen der Oxide eine
bessere Korrektur liefern als Einsetzen der Massen der Isotope des Elementes.
Isotopenfraktionierungen dieser Art treten bei der Messung von gasförmigen Spezies nicht
auf, bzw. sie werden unterdrückt, z.B. dadurch, daß das Gas in das Einlaßsystem „viskos“
strömt. Dabei behindern sich die verschiedenen Moleküle durch Kollision gegenseitig so
sehr, daß die leichteren Moleküle einer Gasspezies keine größere Geschwindigkeit erreichen als die schweren.
Eine Diskriminierung zwischen verschiedenen Isotopen eines Elementes tritt dagegen in
ICP-MS-Geräten auf, und zwar auf Grund des Raumladungseffektes (space–charge effect),
das ist die gegenseitige Abstoßung der Kationen im Ionenstrahl, sei es noch im Plasma oder
vor allem beim Übergang ins Hochvakuum des Spektrometers[66]. Dies hat den bevorzugten Durchtritt der schwereren Ionen zur Folge[67]. Die Massenfraktionierung bei der ICP-MS
ist größer als bei der TIMS, sollte aber dafür über den Verlauf einer Messung hinweg konstant bleiben, weil die Probe kontinuierlich ins Plasma eingebracht wird. Für eine Reihe
von Elementen scheint die Abhängigkeit des Korrekturfaktors von der Massenzahl einer
linearen Funktion zu gehorchen (Abbildung 60). Das läßt sich z.B. dazu nutzen, daß man
zur Analyse der Pb-Isotopenverhältnisse der zu messenden Probe Tl zumischen kann. Der
Korrekturfaktor wird nach GL 83 zu
1 + a Tl =
RijStd
1
´ meas
Dmij Rij
bestimmt, wobei das Verhältnis RijStd für 205Tl/203Tl mit 2.3871 in allen Proben auf der Erde
nahezu konstant ist (siehe aber auch [68]). Der Korrekturfaktor ist für Pb nur minimal kleiner, und die Regressionsgerade in Abbildung 60 kann dazu dienen, (1+aPb) genügend
genau zu ermitteln.
* Für dasselbe Beispiel wie zuvor errechnet man für den dritten Term 0.01´82/44 = 0.0145, was gegenüber dem zweiten Term (0.08) nicht vernachlässigbar ist (Verhältnis von 5.5).
81
Die Massenfraktionierung
Einige Elemente gehorchen der Regressionsgeraden nicht. Dies sind die Edelmetalle Os
und Ru und vielleicht auch Re. Eine Möglichkeit, diese Abweichung zu erklären, liegt in der
erheblichen Flüchtigkeit von Os und Ru als Tetroxide. In diesem Fall wäre denkbar, daß die
leichten Isotope bevorzugt vom Strom der Ar+-Ionen des Plasmas aufgenommen werden
und in das Massenspektrometer gelangen. Ob in diesem Fall die Anwendung des exponentiellen Gesetzes sinnvoller ist, gegebenenfalls unter Einsetzen der Massen der Tetroxide, ist
nicht untersucht worden.
1.030
Ru
1.025
Korrekturfaktor
Rb
Sr
C = -1.329310-4m + 1.0356
1.020
1.015
Nd
Re
Os
Hf
1.010
Tl
Pb
1.005
1.000
80
ABBILDUNG 60
82
100
120
140
160
Massenzahl
180
200
220
Abhängigkeit der Korrekturfaktoren von der Massenzahl für ICP-MS-Messungen[67]. Für jedes Element wurden die Korrekturfaktoren nach dem power
law bestimmt. Sie entsprechen (1 + a) in GL 83. Mit mehr als 2% pro Masseneinheit bei Rb und Sr und noch ca. 0.8% bei Tl und Pb ist die Fraktionierung je Masseneinheit beträchtlich höher als bei der TIMS. Die Elemente Ru
und Os sind von der Regression ausgenommen; ihre Korrekturfaktoren liegen deutlich über der Korrekturgeraden. Korrekturfaktoren und Regressionsgerade sind charakteristisch für einen ICP-MS-Typ, und die jeweiligen
Meßbedingungen und gelten daher nicht generell.
A. Radiogene Isotopensysteme
8.0
Das Lu–Hf-Isotopensystem
Lu besteht aus den beiden natürlich vorkommenden Isotopen 175Lu (natürliche Häufigkeit
97.4%) und 176Lu (natürliche Häufigkeit 2.6%). Die Lu–Hf-Methode macht sich den b–-Zerfall von 176Lu mit einer Halbwertszeit von 35.3 Ga in 176Hf zunutze. Das natürliche Hf
besteht aus den 6 Isotopen 174Hf (Häufigkeit 0.162%), 176Hf (5.206%), 177Hf (18.606%),
178
Hf (27.297%), 179Hf (13.629%) und 180Hf (35.100%). Das leichteste der Hf-Isotope ist
schwach radioaktiv, kann jedoch wegen der extrem langen Halbwertszeit von »2´1015a als
über das Alter der Erde stabil angesehen werden. Zur Relativangabe benutzt man im Lu–HfSystem das Isotop 177Hf. Die Zerfallsgleichung lautet daher:
176
Hf æ 176 Hf ö
=ç
+
÷
177
Hf è 177 Hf ø initial
176
177
Lu l176 t
e
-1
Hf
(
)
[GL 91]
Lu ist das schwerste und kleinste Element der Seltenen Erden, deren geochemisches Verhalten gut bekannt ist. Es tritt in der Natur nur dreiwertig auf. Seine Konzentration in Gesteinen übersteigt nur selten 1ppm. Das geochemische Verhalten des Hf ähnelt sehr stark dem
des Zr. Das bedingt, daß Zr und Hf in der Natur stets zusammen vorkommen und sich chemisch nur schwer trennen lassen. Die Hf-Gehalte der meisten Gesteine liegen unter
»20ppm und liegen oft um eine Größenordnung über denen des Lu. Dadurch und infolge
der langen Halbwertszeit des 176Lu sind die Hf-Isotopenvariationen in der Natur leider nur
wenig höher als die der Nd-Isotope.
TABELLE 8:
Lu- und Hf-Gehalte sowie Lu/Hf-Verhältnisse von Gesteinen und
Mineralen
Chondrite
Achondrite
MORB
kontinentale Basalte
granitische Gesteine
Sandsteine, Quarzite
Tonschiefer
rote Tiefseetone
Zirkon
Granat
ppm Lu
0.033
0.25
0.5 (0.1–1)
0.25 (0.1–0.7)
0.5
0.05–0.5
0.15–0.8
0.8–3
10–100
0.5–5
ppm Hf
0.14
1.25
2.5 (1–15)
4 (2–20)
7
0.5–20
1–7
3–5
10000
<1
176
Lu/177Hf
0.033
0.028
0.005–0.05
0.002–0.02
0.010
0.001–0.04
0.01–0.03
0.03–0.1
<0.002
>0.1
Lu und Hf sind refraktäre Elemente, die sich geochemisch stabil, d.h. wenig mobil verhalten. Ihre wesentliche Fraktionierung findet – wie beim Sm–Nd-System – bei der Magmenbildung und ihrer Kristallisation statt. Zusätzlich dazu werden Lu und Hf aber auch noch
bei der Sedimentbildung fraktioniert, und zwar dadurch, daß Zirkon mit im Durchschnitt
1% Hf und sehr niedrigem Lu/Hf-Verhältnis extrem verwitterungsresistent ist und sich in
grobkörnigen klastischen Sedimenten anreichert. Bei partiellen Aufschmelzprozessen im
Erdmantel und der Fraktionierung basischer Magmen verhält sich das Hf ähnlich inkompatibel wie das Sm, während Lu deutlich weniger inkompatibel ist. Die in der Natur beobachtete Fraktionierung zwischen Lu und Hf ist daher größer (rund doppelt so hoch) als die
zwischen Sm und Nd. Tabelle 8 vermittelt einen Überblick über die Konzentrationen von
Lu und Hf in wichtigen Gesteinen und einigen Mineralen:
Gesteine mit hohen Lu/Hf-Verhältnissen, in denen im Lauf der Zeit das 176Hf/177Hf rasch
wachsen könnte, sind relativ selten. Unter den häufigeren Mineralen in der Natur haben
83
Das Lu–Hf-Isotopensystem
Granate ein sehr hohes Lu/Hf-Verhältnis. Unter den Akzessorien werden diejenigen, welche die schweren REE, nicht aber Zr und Hf konzentrieren (z.B. Xenotim, Gadolinit, hohe
Lu/Hf-Verhältnisse aufweisen.
Wegen der geringen Isotopenvariationen müssen an Hf-Isotopenanalysen hohe analytische Anforderungen gestellt werden. Es kann daher nicht verwundern, daß frühe Untersuchungen am Lu–Hf-System um 1958 von W. Herr und Mitarbeitern[69] nur dem Zweck dienten, durch Untersuchung von REE-reichen Erzen die Zerfallskonstante des 177 Lu zu
bestimmen. Erst 1980 gelang es J. Patchett & M. Tatsumoto vom US Geological Survey in
Denver, eine Methode zur präzisen Hf-Isotopenanalyse mittels Thermionenmassenspektrometrie zu entwickeln. Derzeit wird diese Methode nur von wenigen Laboratorien auf der
Welt eingesetzt. Ein erhebliches Problem dabei liegt nämlich darin, daß die Ionenausbeute
sehr gering ist. Das Verhältnis der Ionen, die auf dem Auffänger (Faraday) des Massenspektrometers registriert werden, zu den Ionen, die auf das Filament geladen werden, beträgt
nur »1/30000, während z.B. bei der Nd-Isotopenanalyse eine um zwei Zehnerpotenzen größere Ionenausbeute erreichbar ist (sogar drei Zehnerpotenzen, wenn Nd als Oxid gemessen
wird). Die geringe Ionenausbeute beim Hf bedingt, daß für eine Messung mit der erforderlichen Präzision eine Hf-Menge von »1µg vorhanden sein sollte, mindestens das Zehnfache dessen, was für eine Standard-Nd-Isotopenanalyse nötig ist. Für terrestrische Proben
wird das meist keine Probleme bereiten (Ausnahme: Mineralanalysen), für die Analyse
extraterrestrischen Materials wegen dessen beschränkter Verfügbarkeit jedoch schon. Die
Schwierigkeiten der Hf-Isotopenanalyse liegen vor allem darin begründet, daß extrem
hohe Temperaturen erforderlich sind, um das Hf von den verwendeten Re-Filamenten
abzudampfen, Temperaturen bei denen das Re selbst schon ziemlich flüchtig ist.
0.292
0.290
Lu-Hf-Isochrone für Eukrite zur
Bestimmung der Zerfallskonstanten
Für t = 4.55Ga resultiert
eine Halbwertszeit von
35.3±1.4Ga
0.288
176Hf/177Hf
Moama
0.286
0.284
0.282
Moore County
Serra de Magé
Pa
sam
on
te
Juvinas
Nuevo Laredo
Sioux County
ALHA 77302
B
éré
Stannern
ba
0.280
0.00
ABBILDUNG 61
0.02
0.04
0.06
176Lu/177Hf
0.08
0.10
0.12
Lu–Hf-Isochrone für Eukrite, eine Gruppe von Meteoriten, die in ihrer Frühgeschichte eine magmatische Differenzierung erfahren haben.
Das erste Projekt von Patchett & Tatsumoto war in einer Umkehrung der Altersbestimmungsmethode die Bestimmung der Zerfallskonstanten von 176Lu mittels einer Gruppe
von achondritischen Meteoriten, den Eukriten, deren magmatisches Bildungsalter durch
die U–Pb-, Rb–Sr- und Sm–Nd-Chronologie mit 4.55 Ga gut bekannt ist. (siehe Abbildung
84
A. Radiogene Isotopensysteme
61[70]). Daraus resultierten eine Zerfallskonstante l von (1.94±0.07)´10-11 a-1 und das
initiale Hf-Isotopenverhältnis des Sonnensystems – also auch der Erde – mit 176Hf/177Hf =
0.27978±9. Infolge der geringen Variation im Lu/Hf-Verhältnis ist der Fehler dieser Zerfallskonstanten groß. Eine neue indirekte Bestimmung, bei denen U–Pb-Alter irdischer Proben
zugrunde gelegt wurden, ergaben l = (1.865±0.015)´10-11 a-1, also einen um etwa 4% niedrigeren Wert[71], der aber gut mit einigen Ergebnissen direkter Bestimmungen des b–-Zerfalls[72] übereinstimmt. Es ist bislang jedoch nicht gesichert, daß dieser neue Wert mit dem
Alter des Sonnensystems kompatibel ist, denn eine Isochrone für Eukrite[73] ist eher mit
einem Wert von 1.93´10-11 a-1 zu vereinbaren, der aus einer g–g-Koinzidenzmessung des b–
-Zerfalls resultiert[74].
Die Analyse der Hf-Isotope mittels ICP-MS, die mit einem Magnetsektormassenspektrometer und Multikollektor als Auffänger gekoppelt ist[18], hat eine deutlich verbesserte Präzision der Daten mit sich gebracht und als Folge der hohen Temperaturen der Anregung im
Plasma eine drastische Reduzierung der benötigten Probenmenge auf ca. 25 ng. Das hat
dazu geführt, daß sich das Lu–Hf-Isotopensystem inzwischen stark steigender Wertschätzung erfreut. Es ist mit dieser Technik jetzt auch möglich, Chondrite zu analysieren (Abbildung 62[75]). Eine präzise Isochrone konnte allerdings nicht erhalten werden, weil die Lu/
Hf-Fraktionierung sehr gering ist. Allerdings streuen die Daten einigermaßen vernünftig
um die Isochrone für die Eukrite.
0.2835
Lu-Hf-Isotopie
von Chondriten
0.2825
176
Hf/177Hf
0.2830
0.2820
Eukrit-Isochrone
0.2815
0.026
0.028
0.030
0.032
0.034
0.036
0.038
0.040
176
Lu/177Hf
ABBILDUNG 62
Lu–Hf-Isotopensystematik der Chondrite[75]. Zur Orientierung ist die Isochrone für Eukrite eingetragen[70]. Die Fehler im 176Hf/177Hf sind zumeist ungefähr so groß wie die Symbole und wurden nur aufgetragen, wenn sie
erheblich größer waren.
Zur Datierung eignet sich das Lu–Hf-System infolge der geringen Lu/Hf-Fraktionierung vorwiegend für proterozoische und ältere Gesteine. Tatsächlich spielt das Lu–Hf-System in der
Geochronologie erst in den letzten Jahren durch die Multikollektor-ICP-MS-Technik
85
Das Lu–Hf-Isotopensystem
zunehmend eine Rolle. Pettingill & Patchett[78] haben eine Lu–Hf-Gesteinsisochrone vor
allem deswegen gemessen, um die generelle Brauchbarkeit des Systems zu testen. Dabei
handelt es sich um die Amîtsoq-Gneise in West-Grönland (Abbildung 63), die bereits im
Rb–Sr-Kapitel erwähnt wurden. Das Alter ist im Rahmen seines relativ großen analytischen
Fehlers identisch mit dem Rb–Sr-Alter. Die Lu–Hf-Isochrone ist jedoch vergleichsweise
schlecht definiert und eher als „errorchron“ zu bezeichnen. In Zirkonen wird das 176Hf/
177
Hf wegen deren niedrigem Lu/Hf-Verhältnis praktisch eingefroren sein, und Zirkone
sind daher gut geeignet, das initiale Hf-Isotopenverhältnis eines Gesteins zu liefern, während man beim Sm–Nd-System das initiale 143Nd/144Nd nur durch Aufnahme einer Isochrone erhält. Man kann daher durch Analyse von Zirkonen aus Gesteinen unterschiedlichen
Alters terrestrische Hf-Isotopenvariationen studieren, ohne das genaue Alter des Gesteins
selbst zu kennen. Die Lu/Hf-Fraktionierung der Gesteine des Amîtsoq-Komplexes ist
gering, kann aber als typisch für die Gesteine angesehen werden, welche die kontinentale
Kruste aufbauen.
0.2825
Amîtsoq-Gneise/Grönland
t = 3.55«0.22Ga
176
Hf/177Hf
0.2820
0.2815
0.2810
Zirkone
0.2805
0.2800
0
0.005
0.010
0.015
176
Lu/
ABBILDUNG 63
0.020
0.025
177
Hf
Lu–Hf-Isochrone der Gneise von Amîtsoq in Grönland
Scherer et al.[76] haben Granate auf ihre Verwendbarkeit zur Lu–Hf-Datierung untersucht.
Ihre Resultate legen nahe, daß die „Schließungstemperatur“ von Granat für das Lu–HfSystem etwas höher liegt als die für Sm–Nd. Vorsicht ist geboten, wenn die Granate Einschlüsse von Zirkon enthalten, weil dieses Mineral hohe Hf-Gehalte aufweist und man
nicht sicher sein kann, daß Granat und Zirkon sich bei t = 0 (Bildungsalter) im Hf-Isotopengleichgewicht befunden haben. Auch für Granate aus Hochdruckgesteinen der Walliser
Alpen wurde gefunden, daß ihr Lu–Hf-Alter signifikant über dem Sm–Nd-Alter liegt[77]. Die
Ursache wird von den Autoren in der prograden Wachstumsdauer der Granate gesehen. Es
wird argumentiert, daß infolge der großen Kompatibilität des Lu für Granat – der LuGehalt nimmt vom Kern zum Rand ab – die Lu–Hf-Alter die Kerne der Granate stärker
gewichten als die Ränder.
86
A. Radiogene Isotopensysteme
Der wesentliche Nutzen des Lu–Hf-Systems liegt derzeit (noch) in der Anwendung als Tracer. D.h. man mißt die Isotopenzusammensetzung von Gesteinen bekannten Alters, um so
die chemische Differenzierung der Erde über den Lauf ihres Alters von »4.55 Ga zu verfolgen. Auch die Hf-Isotopie läßt sich bequemerweise in der e-Form angeben:
é
e Hf = ê
ê
êë
(
(
176
176
177
Hf
177
Hf
176
Hf
Hf
)
)
Probe
Chondrite
ù
- 1ú ´ 10 4
ú
ûú
[GL 92]
177
Zur Ermittlung des chondritischen
Hf/ Hf wählten Patchett und Tatsumoto den C2Chondriten Murchison. Sein 176 Hf/ 177 Hf ist in 4.55 Ga vom Initialwert der Eukrite
(0.27978±9) infolge seines 176Lu/177Hf-Verhältnisses von 0.0334 (= Lu/Hf von 0.240) auf
0.28286 heute angewachsen. Zur Fraktionierungskorrektur der Massenspektrometermessungen wird das Verhältnis 179Hf/177Hf mit 0.7325 verwendet. Das heutige chondritische 176Hf/177Hf-Verhältnis wird inzwischen auf Grund der größeren Datenbasis von Blichert-Toft & Albarède[75] zu 0.282772 angesetzt.
Im folgenden werden drei Beispiele angeführt, um die Tracer-Anwendung des Lu–HfSystems zu demonstrieren.
8.1
Die Hf-Isotopensignatur des subozeanischen oberen Erdmantels
Im Lu–Hf-System sind – wie im Sm–Nd-System, aber im Gegensatz zum Rb–Sr-System – die
Tochternuklide (bzw. -elemente) des radioaktiven Zerfalls inkompatibler bei Magmenbildungsprozessen als die Mutternuklide (bzw. -elemente). Man wird daher vermuten dürfen,
daß Nd- und Hf-Isotope positiv und Sr- und Hf-Isotope negativ korreliert sind. Und tatsächlich wurden solche Beziehungen auch gefunden (siehe Abbildung 64[79]), auch wenn
die Variation im Detail komplizierter sein mag.
0.2836
Ozeanboden- und
Ozeaninselbasalte
B
Galapago
«Hf = 18
OR
OR
s
0.2832
h
Ta
0.2830
it
M
M
176Hf/177Hf
0.2834
B
«Nd = 0
«Nd = 10
0.2838
i
s
go
a
lap
Ga
«Hf = 0
0.2828
Kerguelen
ABBILDUNG 64
0.5126
143
hi
ti
bulk-earth
Kerguelen
0.2826
0.2826
0.5122
Ta
0.5130
Nd/144Nd
0.5134
0.702
0.704
0.706
87Sr/86Sr
0.708
Die Korrelation zwischen Hf-, Sr- und Nd-Isotopen in ozeanischen Basalten
Basalte von ozeanischen Spreizungszentren (MORB) haben die höchsten 143Nd/144Nd- und
Hf/177Hf-Verhältnisse und die niedrigsten 87Sr/86Sr-Verhältnisse aller Basalttypen. Sie
müssen deshalb aus einem Reservoir im Erdmantel stammen, das integriert über alle geologische Zeit die höchsten Verhältnisse von Sm/Nd und Lu/Hf und das niedrigste Rb/SrVerhältnis hatte. Das kann man als Folge früherer Magmenextraktionsprozesse ansehen.
176
87
Das Lu–Hf-Isotopensystem
Für MORB kann man sich als einfachen Zusammenhang zwischen Nd- und Hf-Isotopie die
Faustformel
eHf » 1.5 – 2eNd
[GL 93]
merken. Basalte der ozeanischen Inseln müssen demgegenüber eine andere Entwicklungsgeschichte haben. Sie nehmen einen weiten Bereich in den Isotopendiagrammen ein, der
auch die Zusammensetzung des unfraktionierten Erdmantels umfaßt, was aber nicht auf
Ableitung aus solch primitivem Material schließen läßt, sondern komplexe Mischungsprozesse verschiedener Ausgangsmaterialien erfordert, z.B. von verschiedenen Mantelreservoiren oder von Mantel- und Krustenmaterial. Aus dem linken Teildiagramm ist ferner
zu ersehen, daß der bulk-earth-Punkt etwas unterhalb des durch MORB und OIB aufgespannten mantle array liegen. Blichert-Toft & Albarède[75] haben daher argumentiert, daß es
der Erde ein weiteres Reservoir neben dem verarmten Erdmantel und der kontinentalen
Kruste geben muß, und schlagen vor, daß dies subduzierte Basalte sein können.
8.2
Die Hf-Isotopenentwicklung der Erde
Auch für das Lu–Hf-System kann die Erde wieder als chondritisches Reservoir angesehen
werden, ihre Hf-Isotopenentwicklung also gleich der des C2-Meteoriten Murchison gesetzt
werden. In Abbildung 65[79] sind die initialen 176Hf/177Hf-Verhältnisse krustaler Gesteine
(auf der Basis von Gesamtgesteins- oder Zirkonanalysen) gegen das Bildungsalter dieser
Gesteine aufgetragen, zusammen mit der chondritischen Entwicklungslinie. Die gegenwärtige Hf-Isotopenvariation des Erdmantels macht ca. 20e-Einheiten aus von »0 – 20, was
einem zeitintegriert chondritischen bis zu einem wesentlich höher als chondritischen Lu/
Hf-Verhältnis entspricht. Gesteine der kontinentalen Erdkruste mit Bildungsaltern >»3 Ga
haben chondritische initiale 176Hf/177Hf-Verhältnisse; diese Gesteine sind daher aus einem
damals noch weitgehend undifferenzierten Erdmantel extrahiert worden.
0.284
Variation der initialen
Hf-Isotopenverhältnisse
(aus Gesamtgesteinen und
Zirkonen)
176
Hf/177Hf
0.283
0.282
heutiger
Erdmantel
0.281
0.280
«Hf:
+20
+10
0
-10
aus Ereignissen intensiver Krustenbildung
aus Intraplattenvulkaniten
0.279
4.55
ABBILDUNG 65
4
3
t [Ga]
2
1
0
initiale Hf-Isotopien von Magmatiten über den Verlauf der Erdgeschichte
Kruste, die während der großen Krustenbildungsepisoden zwischen »2.8 Ga und heute
gebildet wurde, ist demgegenüber meist aus einem an Hf relativ zu Lu verarmten Erdmantel entstanden mit eHf-Werten bis »+10. Eine markante Zunahme der initialen eHf-Werte
88
A. Radiogene Isotopensysteme
vom späten Archaikum bis heute ist jedoch nicht ersichtlich. Die hohen eHf-Werte stammen überwiegend aus der Analyse von Zirkonen. Aus U–Pb-Isotopenuntersuchungen weiß
man aber, daß viele solcher Zirkone diskordant sind, d.h. daß sie irgendwann einmal nach
ihrer Bildung Pb relativ zu U verloren haben müssen. Es kann daher nicht ausgeschlossen
werden, daß während eines solchen (metamorphen) Ereignisses auch das Hf-Isotopensystem der Zirkone beeinflußt wurde, z.B. durch Austausch mit hoch radiogenem Hf aus
einem REE-reichen und Hf-armen Mineral wie Monazit, Titanit, Allanit oder Apatit. Dann
wäre ihre Hf-Isotopie eine Mischung, und die Zirkone wären bei einem zu hohen Alter in
die Abbildung eingetragen. Auch durch parallele Analyse von U–Pb und Lu–Hf an solchen
Zirkonen konnte diese Ungereimtheit nicht aufgelöst werden.
Ein weiteres Problem resultiert aus der Revision der Zerfallskonstanten auf den Wert von
1.865´10-11 a-1. Damit wird das initiale 176Hf/177Hf der Erde höher, und eine Reihe von
archaischen Zirkonen erhält negative eHf-Werte[80], sollte also aus Gesteinen stammen, die
über beträchtliche Zeit hinweg an Hf über Lu relativ zur Gesamterde angereichert waren.
Dies wiederum würde die Existenz krustaler Blöcke schon während der ersten ca. 250 Ma
der Erdgeschichte nahelegen. Obwohl in archaischen Quarziten Westaustraliens gefundene Zirkone U–Pb-Alter bis 4.3 oder gar 4.4 Ga zeigen[81],[82], ist nicht klar, inwieweit dies
die Existenz größerer Mengen an Erdkruste erfordert. Der generellen Vergleichbarkeit geochronologischer Daten wegen wäre es zweifellos angebracht, die Werte der Zerfallskonstanten vieler Isotopensysteme kritisch zu evaluieren und gegebenenfalls neue Bestimmungen
mit den inzwischen vorhandenen Techniken vorzunehmen[83].
8.3
Hinweise von den Hf-Isotopen auf das Ausmaß des globalen Recycling
Tiefe
[km]
IAB
CFB
OIB
MORB
kontinentale
Lithosphäre
100
200
ozean.
Lithosphäre
300
400
500
600
alte ozeanische Lithosphäre
670
ABBILDUNG 66
Cartoon zur Illustration von Subduktion der ozeanischen Lithosphäre bis zur
670 km-Diskontinuität und Recycling alter subduzierter Lithosphäre
Magmen, die in Subduktionszonen aufdringen, können chemische Komponenten sowohl
aus der subduzierten Ozeankruste als auch dem Mantelkeil darüber enthalten. Daß die
basaltische Ozeankruste z.T. subduziert wird, steht außer Frage. Was allerdings lange Zeit
kontrovers diskutiert wurde, ist die Frage, ob die Sedimentauflage der Ozeankruste mit subduziert wird bzw. ob ihr Anteil mengenmäßig so bedeutsam ist, daß sie im Laufe der Zeit
durch Homogenisierung mit Mantelperidotit eine meßbare Isotopenverschiebung im Mantel verursacht oder ob die Menge an subduzierten Sedimenten so gering ist, daß sie die che-
89
Das Lu–Hf-Isotopensystem
mische und Isotopenentwicklung des Erdmantels nicht beeinflußt. Subduktionszonenbasalte haben einige chemische Charakteristika, z.B. hohe Ba/La- und La/TaVerhältnisse, die dadurch erklärt werden können, daß an ihrer Bildung tonige Sedimente
beteiligt waren. Diese Hypothese wird auch durch die Sr- und Nd-Isotopenzusammensetzung solcher Basalte gefordert.
176
Lu/177Hf
In Diskussionen über die Erdmantelentwicklung spielen die
Lu/Hf- und Sm/Nd0.08
Basalte der ozeanischen Inseln
Verhältnisse von
[OIB] wie Hawaii oder Samoa
Sedimenten
Mn-Knollen,
eine große Rolle. Ozeanische
Rote Tone
Inseln liegen weit entfernt von
0.06
kontinentaler Kruste. Trotzdem
entspricht die Isotopenzusammensetzung ihrer Basalte nicht
der von Basalten ozeanischer
0.04
Rücken. Der Mantel, aus dem
Erde
die Ozeaninseln entstanden,
muß vielmehr zeitintegriert
Tone,
weniger stark an inkompatiTonschiefer
0.02
blen Elementen verarmt gewesen sein (also an Rb relativ zu Sr
oder Hf relativ zu Lu) als der
Sande
Mantel, aus dem MORB ent0
standen. Nach einer in der
Fachwelt populären Vorstel0
0.05
0.1
0.15
0.2
147
144
lung sollen daher die Quelle
Sm/ Nd
von Ozeaninselbasalten ozeanische Kruste (Basalt + etwas
Sediment) ± Peridotit sein, die ABBILDUNG 67 Lu/Hf- und Sm/Nd-Verhältnisse verschiedesubduziert wurde und sich an ner ozeanischer Sedimente
der Grenze oberer/unterer Erdmantel in einer Tiefe von »670km (oder gar an der Mantel/
Kern-Grenze) ansammelte, dort einige 100Ma stabil war, bis sie sich durch radioaktive Wärmeproduktion gegenüber ihrer Umgebung soweit aufgeheizt hatte, daß sie instabil wurde
und aufzusteigen und schließlich aufzuschmelzen begann[84].
Wenn diese Hypothese richtig ist, muß man zumindest in günstigen Fällen auf Grund der
Hf-Nd-Isotopensystematik die sedimentäre Komponente nachweisen können, da Tiefseesedimente, welche die subduzierte Sedimentkomponente darstellen sollten, außergewöhnliche Hf-Nd-Isotopien über den Verlauf von 0.5 – 2 Ga entwickeln würden. Schaut man sich
die Lu/Hf- und Sm/Nd-Verhältnisse von ozeanischen Sedimenten an(Abbildung 67[85]),
dann stellt man fest, daß deren 147Sm/144Nd nur relativ wenig schwankt (»0.10 – 0.16).
Gewöhnliche Tonschiefer und Tone haben zudem auch ein eng begrenztes Lu/Hf, das im
Mittel dem halben chondritischen Verhältnis entspricht. Sande weisen das niedrigste Lu/
Hf auf, weil sich in ihnen der durch Verwitterungsprozesse praktisch unzerstörbare Zirkon
mit seinem hohen Hf-Gehalt von »1% anreichert. Rote Tiefseetone und Mn-Knollen haben
im Vergleich zu normalen Tonen hohe REE-Gehalte bei identischen Hf-Konzentrationen,
und als Folge davon hohe und sehr variable Lu/Hf-Verhältnisse. Dadurch wird in roten
Tiefseetonen in geologischer Zeit ein wesentlich radiogeneres 176Hf/177Hf eingestellt als in
anderen Sedimenten. Biogene Sedimente (Kalke, Kieselschiefer) scheinen noch höhere Lu/
Hf-Verhältnisse zu haben; infolge niedriger Konzentrationen beider Elemente dürfte ihre
176
Hf/177Hf-Signatur jedoch als Komponente der subduzierten Kruste nicht mehr zu erkennen sein. Geht man davon aus, daß dieselben Prozesse der Produktion von ozeanischer
Kruste an mittelozeanischen Rücken und ihrer Zerstörung in Subduktionszonen seit mindestens dem frühen Proterozoikum vor »2 Ga vorherrschend waren wie heute, dann läßt
sich abschätzen, ob die Hf- und Nd-Isotopien von Ozeaninselbasalten durch eine
90
A. Radiogene Isotopensysteme
Mischung von ozeanischer Kruste (±verarmtem ozeanischem Mantelperidotit) und Tiefseesedimenten erklärt werden können. Wie Abbildung 68 erkennen läßt[85], ist dies weder
durch Mischen von MORB mit 1 – 2 Ga alten roten Tiefseetonen noch durch Mischen von
MORB mit einem Durchschnitt an pelagischen Sedimenten möglich (Mischung von alten
Komponenten ist erforderlich, weil das globale Recycling sicherlich solche Zeiträume in
Anspruch nimmt). Die letzt genannte Mischung für »2 Ga alte ozeanische Kruste würde
entlang der gezeigten Mischungslinie erfolgen. Eine Mischung, welche die Nd- und Hf-Isotopenvariation der Ozeaninselbasalte erklären würde, bestünde aus verarmtem Mantelperidotit (bzw. ozeanischer Kruste) + pelagischen Sedimenten + Sanden mit niedrigem Lu/Hf,
die durch Trübeströme vom Kontinentalhang in die Tiefsee gelangen könnten. Diese
Mischung müßte jedoch in einem engen Mengenverhältnis der sedimentären Komponenten erfolgt sein, was sehr schwer realisierbar scheint, weil pelagische Sedimente und Turbidite an unterschiedlichen Orten abgelagert werden (in der Tiefsee bzw. vor dem Kontinentalhang) können und nicht gleichzeitig subduziert werden müssen. Damit stellen die
Ozeaninselbasalte wohl keine solche Mischung von altem verarmtem Mantel und alten
Sedimenten dar. In Kapitel 12.2, Seite 120 wird diese Frage nochmals aufgerollt.
40
«Hf
1 extremer
MORB
Tiefseeton
Ø Tiefseeton
2
20
Mischung von
pelagischem Sediment
mit Erdmantel
t=
t=2Ga
0
Ozeaninselbasalte
Ø
-20
pe
Se lagis
dim ch
en es
t
0
3
-40
Mischung von Turbidit +
pelagisches Sediment
(Verhältnis 1.2:1) mit
Erdmantel
t=2Ga
t=2Ga
4 turbiditischer Sandstein
-60
-40
ABBILDUNG 68
-30
-20
-10
Modell zur Erklärung
der Entstehung von
Ozeaninselbasalten
0
10
«Nd
20
Hf- und Nd-Isotope ozeanischer Sedimente und von Ozeaninselbasalten
91
Das La–Ce-System
9.0
Das La–Ce-System
Ein Zerfallssystem, das erst in den 1980-er Jahren auf seine Nutzbarkeit für die Geochronologie untersucht worden ist, ist das La–Ce-System[86]. Auf Grund eines ungünstig niedrigen
Mutter-Tochter-Verhältnisses beim Zerfall, gekoppelt mit einer kleinen Zerfallskonstante,
wird man davon ausgehen dürfen, daß es auch in den kommenden Jahren keine größere
Bedeutung erlangen wird.
Natürliches La besteht aus den beiden Isotopen 138La (natürliche Häufigkeit 0.089%) und
139
La (99.911%). 138La ist schwach radioaktiv und zerfällt unter Elektroneneinfang in 138Ba
(das mit 71.66% das mit Abstand häufigste Ba-Isotop ist) sowie unter b–-Aussendung in
138
Ce. Da Ba in Gesteinen und Mineralen fast stets erheblich häufiger ist als La, scheidet das
Zerfallssystem La-Ba für die Geochronologie weitgehend aus. Eine potentielle Ausnahme
bilden Minerale der leichten REE, z.B. Bastnäsit[87]. Ce besteht aus den 4 stabilen Isotopen
136
Ce (Häufigkeit 0.193%), 138Ce (0.25%), 140Ce (88.48%) und 142Ce (11.07%).
La und Ce sind die beiden leichtesten Elemente der Seltenen Erden. La tritt in der Natur
nur dreiwertig auf, während das Ce unter oxidierenden Bedingungen – vor allem bei den
Prozessen der Verwitterung und Sedimentbildung, selten aber auch in Meteoriten – zusätzlich vierwertig vorkommen kann. Das chondritische La/Ce-Häufigkeitsverhältnis beträgt
0.31/0.808=0.38; dies entspricht einem 138La/138Ce-Verhältnis von 0.38´(0.089/138.91)/
(0.25/140.12) = 0.138. Viele Gesteine der kontinentalen Erdkruste sowie basaltische bis
kimberlitische Magmatite haben La/Ce > chondritisch und dürften daher potentiell die
best geeigneten Studienobjekte für die La–Ce-Datierung sein.
Die partiellen Zerfallskonstanten und die Halbwertszeit von 138La sind noch nicht sehr
genau bekannt. Als beste Werte können gelten[86]:
le = (4.59±0.33)´10-12 a-1
lb = (2.58±0.25)´10-12 a-1
l = le + lb » 7.2´10-12 a-1,
woraus eine Halbwertszeit von »97´109a folgt, die vergleichbar ist mit der von 147Sm.
Tanaka & Masuda bezogen ihre Massenspektrometerdaten auf das häufige Isotop 142Ce,
während eine andere Arbeitsgruppe[88] dem 136Ce den Vorzug gibt, das eine ähnlich niedrige Häufigkeit hat wie 138Ce. Die Zerfallsgleichung lautet im Fall der Division durch 142Ce:
138
lb
Ce æ 138Ce ö
= ç 142 ÷
+
142
Ce è Ce ø initial l
138
La l138t
e
-1
Ce
142
(
)
[GL 94]
Das System ist bislang nur in einem Fall auf seine Brauchbarkeit für Datierungszwecke hin
untersucht worden, und zwar für Gabbros aus dem Bushveld Komplex in Südafrika (siehe
Abbildungen 69 und 70). Das Alter ist innerhalb des Fehlers nicht unterscheidbar von Sm–
Nd- und Rb–Sr-Altern. Infolge der niedrigen La/Ce-Verhältnisse und der kleinen partiellen
Zerfallskonstante ist die Variation des Ce-Isotopenverhältnisses jedoch winzig und damit
der Fehler des Isochronenalters hoch.
Eine andere Arbeit beschäftigte sich mit der Möglichkeit, mit Hilfe des La–Ce-Systems in
Magmatiten Kontaminationen durch die Aufschmelzung und Inkorporation von alter kontinentaler Kruste nachzuweisen[88]. In diesem Fall liegen die beobachteten Ce-Isotopenvariationen am Rand des derzeitigen Auflösungsvermögens der Massenspektrometrie.
92
A. Radiogene Isotopensysteme
0.02290
Gabbros Bushveld
t = 2390±480Ma
Plag 1
Bulk
0.02286
138
Ce/142Ce
0.02288
Cpx 2
Plag 2
Cpx 1
0.02284
0.02282
0.001
0.002
0.004
0.003
0.005
0.006
La/142Ce
138
La–Ce-Isochrone für Gesteine der Bushveld-Lagenintrusion; der große statistische Fehler zeigt, daß das La–Ce-System nicht besonders zur Datierung
basischer Magmatite geeignet ist.
ABBILDUNG 69
0.513
Gabbros Bushveld
Cpx 2
t = 2050±90Ma
Cpx 1
Bulk
0.511
143
Nd/144Nd
0.512
Plag 1
Plag 2
0.510
0.00
0.10
0.20
147
Sm/144Nd
ABBILDUNG 70
Zum Vergleich: Sm–Nd-Isochrone der Gesteine vom Bushveld
93
Das K–Ca-System
10.0
Das K–Ca-System
40
K erfährt einen dualen Zerfall: Unter Elektroneneinfang zerfallen »10.5% der 40K-Atome
in 40Ar und liefern damit die Grundlage der K–Ar-Datierung. Die übrigen »89.5% zerfallen
unter b–-Emission in 40Ca, das mit 96.9821% am Aufbau des natürlichen Ca beteiligt ist. Ca
verfügt noch über 5 weitere stabile Isotope mit den Massenzahlen 42Ca (natürliche Häufigkeit 0.6421%), 43Ca (0.1334%), 44Ca (2.0567%), 46Ca (0.0031%) und 48Ca (0.1824%). Die
Massendifferenz zwischen 40Ca und 44Ca beträgt immerhin »10%, und daher findet man
beim Ca geringe, aber meßbare massenabhängige natürliche Fraktionierungen[63]; darauf
wird bei den stabilen Isotopen auf Seite 243 kurz eingegangen.
Obwohl die Zerfallskonstante lb des 40K eine für die Geochronologie günstige Größenordnung hat, ist die K–Ca-Methode zur Altersbestimmung nur in Ausnahmefällen geeignet.
Das liegt daran, daß die meisten Gesteine und Minerale ein sehr niedriges 40K/40Ca-Verhältnis haben, denn 40K ist am Aufbau des natürlichen K nur mit 0.01167% beteiligt, und
sowohl K als auch Ca sind Hauptelemente in den Gesteinen der Erdkruste. Die Angabe der
Massenspektrometerdaten erfolgt relativ zum Isotop 42Ca. Die Zerfallsgleichung lautet
dann:
40
40
42
42
Ca æ
=ç
Ca è
lb
Ca ö
+
÷
Ca ø initial l
40
K l40t
e
-1
Ca
42
(
)
[GL 95]
mit lb = 4.962´10-10 a-1 Þ t1/2 = 1.25´109a.
152.0
Biotit
Pikes Peak-Granit
(Colorado)
40
Ca/42Ca
151.8
t = 1041±32Ma
151.6
K-Feldspat
151.4
151.2
Gesamtgestein
Plagioklas
151.0
0
0.2
0.4
0.6
40
0.8
1
1.2
1.4
42
K/ Ca
ABBILDUNG 71
K–Ca-Alter des Pikes Peak-Komplexes
Einer der wenigen Fälle, in denen die K–Ca-Methode bislang zur Datierung verwendet
wurde, ist der des Pikes Peak Granitstocks in Colorado[89], für den Plag, Gesamtgestein, 2
Kalifeldspatfraktionen und Biotit ein Alter von 1041±32Ma lieferten (Abbildung 71). Die
Altersbestimmung mit dieser Präzision konnte nur gelingen, weil Minerale wie Biotit und
Kalifeldspat hohe K-Gehalte bei niedrigen Ca-Gehalten haben (z.B. der analysierte Biotit:
5.786%K, 0.0833%Ca). Bei der Berechnung stellte sich heraus, daß der Initialwert der
94
A. Radiogene Isotopensysteme
Isochrone mit 40Ca/42Ca = 151.024±16 vor »1 Ga identisch ist mit dem primordialen Verhältnis der Chondrite und dem Verhältnis junger, aus dem Erdmantel stammender
Gesteine. D.h. die 40Ca/42Ca-Entwicklungskurve der Erde weist eine Steigung von 0 auf,
weil das K/Ca-Verhältnis der Erde offensichtlich so niedrig ist, daß der Zerfall von 40K keinen Einfluß auf die Isotopenzusammensetzung des Ca der Erde in den »4.6 Ga ihrer
Geschichte hat.
Auch für das 40Ca/42Ca läßt sich wieder ein e-Parameter definieren:
e Ca
é
=ê
ê
êë
(
(
40
40
42
Ca
Ca
Ca
42
Ca
)
)
Probe
chondritisch
ù
- 1ú ´ 10 4
ú
úû
[GL 96]
Abbildung 72 illustriert schematisch die Entwicklung der Ca-Isotopie in Kruste und Mantel
und vermittelt einen Einblick, welche Isotopenunterschiede sich eventuell auflösen lassen[89]. Taylor & McLennan zufolge liegt das K/Ca-Verhältnis der „bulk crust“ bei »1/4, das
der Oberkruste bei »1 – 2. Danach wären im Durchschnitt selbst für alte (»3.5 Ga) kontinentale Kruste nur eCa-Werte von weniger als +10 zu erwarten. Das K–Ca-Isotopensystem
eignet sich daher nur in wenigen Ausnahmefällen zur Datierung.
40
Kruste mit
K/Ca = 7
Hypothetische Entwicklung der CaIsotopien in der Erdkruste als Folge
von Differentiationsereignissen
35
30
Differentiationsereignisse
«Ca
25
20
Kru
ste
mi
t
a=
K /C
5
15
Kruste mit
K/Ca = 5
10
mit K/C
Kruste
5
0
a=1
Mantel (K/Ca = 0.01)
4.5
4.0
3.5
3.0
2.5
2.0
1.5
1.0
0.5
0.0
t [Ga]
ABBILDUNG 72
Ca-Isotopenentwicklungskurven von Erdmantel und Erdkruste
95
Die Re–Os-Methode
11.0
Die Re–Os-Methode
Natürliches Re besteht aus den beiden Isotopen 185 Re mit einer Häufigkeit von
37.398±0.016% und 187Re (62.602±0.016%). 187Re ist radioaktiv und zerfällt unter b–-Emission in 187Os. Die direkte Bestimmung der Halbwertszeit von 187Re durch Messung der b–Strahlung ist sehr schwierig, weil die Zerfallsenergie nur »2.6KeV beträgt. Ein gangbarer
Weg ist daher – wie bei der Bestimmung der Halbwertszeit von 176Lu – eine Gesteinsserie
gut bekannten Alters zu nehmen und die Halbwertszeit aus der Steigung der Isochrone zu
bestimmen. Hirt et al. (1963)[90] bestimmten die Halbwertszeit zu (4.3±0.5)´1010a durch
Analyse von Molybdänglanzen bekannten Alters. Dieser Wert stimmt innerhalb des Fehlers überein mit dem derzeit besten durch die indirekte Isochronenmethode bestimmten
Wert von (4.56±0.11)´1010a, woraus ein l = (1.52±0.04)´10-11a-1 resultiert[91].
187Os/192Os
Auf direktem Wege
wurde die Halb2.5
wertszeit 1989
Bestimmung der
dagegen
zu
Halbwertszeit von 187Re
(4.23±0.13) ´1010a
2.0
ermittelt [ 9 2 ] . Die
dabei angewandte
Methode sei hier
1.5
kurz skizziert: In
mehreren Parallelexperimenten, die
sich über ca. 5
1.0
Jahre erstreckten,
wurden je ca. 2kg
187Re
Steigung = 192 ´ l
hochkonzentrierte
0.5
Os
HReO 4 (entsprechend »1kg Re)
von Os-Verunrei0.0
nigungen weitge0
200
400
600
800
1000
1200
1400
1600
hend gereinigt,
Tage
indem das Os in
der Lösung mit
HJO4 in einem O3/ ABBILDUNG 73 direkte Bestimmung der Halbwertszeit von Re
O 2 -Strom oxidiert
und dann abdestilliert wurde; dabei verbleiben »0.5 – 0.8ng Os je kg Re in der HReO4Lösung. Die gereinigte HReO4-Säure wurde tiefgefroren und in unregelmäßigen Abständen
(150 – 400 Tage) wurde nach Auftauen ein Aliquot entnommen, aus dem das Os in ngMengen wieder durch Destillation abgetrennt und mit einer ICP-MS auf die Isotopenzusammensetzung 187Os/190Os bzw. 187Os/192Os untersucht wurde. Für die Auswertung gilt
dann die Zerfallsgleichung, z.B.
187
187
192
Os æ 187Os ö
=ç
+
÷
Os è 192Os ø t = 0
192
Re l187 t
e
-1
Os
(
)
Da die Halbwertszeit von 187Re sehr groß ist gegen die Dauer der Halbwertszeitbestimmung
(»5a), kann vereinfachend geschrieben werden:
187
Os æ 187Os ö
ȍ
+
÷
192
Os è 192Os ø t = 0
187
Re
´ l187 t
Os
192
Das 192Os stammt aus der unvollständigen Abtrennung vom Re vor Beginn des Experiments. Da 187Re ein riesiges Reservoir im Vergleich zu 192Os ist, ändert sich das Verhältnis
96
A. Radiogene Isotopensysteme
187
Re/192Os im Verlauf des Experiments im Rahmen der Meßgenauigkeit nicht. Bei Auftragung von t gegen das Verhältnis 187Os/192Os ergibt sich die Steigung zu187Re/192Os ´ l. Die
Genauigkeit, mit der die Zerfallskonstante oder damit die Halbwertszeit bestimmt werden
kann, hängt danach von der Präzision ab, mit der187Re/192Os gemessen werden kann. In
Abbildung 73 ist ein Beispiel einer der Messungen gegeben.
Natürliches Os besteht aus den 7 stabilen Isotopen 184Os (mittlere Häufigkeit 0.0239
Atom%), 186 Os (1.600%), 187 Os (1.510%), 188 Os (13.286%), 189 Os (16.251 8 %), 190 Os
(26.369%) und 192Os (40.9579%). Als Bezugsisotop zur Angabe der Massenspektrometerdaten benutzt man 186Os, woraus sich die Zerfallsgleichung ergibt als
187
Os æ 187Os ö
=ç
+
÷
186
Os è 186Os ø initial
187
186
Re l187 t
e
-1
Os
(
)
[GL 97]
1992 ist eine Arbeitsgruppe dazu übergegangen, das Verhältnis 187Os/188Os anstatt des Verhältnisses 187Os/186Os zu benutzen[94]. 187Os/188Os soll präziser zu messen sein; außerdem
hat 188Os weniger isobare Interferenzen. Vor allem aber stammt 186Os selbst in geringem
Maße aus dem Zerfall des langlebigen 190Pt (ca. 4.5´1011a[95]). Dieses ist zwar am Aufbau des
natürlichen Platins nur zu ca. 0.0122% beteiligt; dennoch kann es in Erzen der Platinoide
bei hohen Pt/Os-Verhältnissen, z.B. in den Cu-Erzen von Sudbury[96], einen meßbaren Beitrag zum 186Os liefern. Anstelle von GL 97 erhält man dann:
187
187
188
Os æ 187Os ö
=ç
+
÷
Os è 188Os ø initial
188
Re l187 t
e
-1
Os
(
)
[GL 98]
Das 187Os/188Os-Verhältnis läßt sich durch Multiplikation mit 8.309 einfach in 187Os/186Os
umrechnen.
Infolge der geringen geochemischen Häufigkeit von Os und Re in der Natur hatte die Re–
Os-Methode bis vor wenigen Jahren keine große Bedeutung in der Geo-/ Kosmochronologie. Ihre Anwendung beschränkte sich auf Spezialfälle, in denen einfachere Methoden versagten oder sich der große Aufwand wissenschaftlich vertreten läßt. Ein gutes Beispiel für
den ersten Fall ist die Datierung von Fe-Meteoriten, in denen die Konzentrationen von Sr,
Nd oder Hf verschwindend gering sind. 1988 gelang jedoch eine entscheidende Verbesserung der massenspektrometrischen Os-Messung, als K.G. Heumann fand, daß sich wesentlich intensivere Strahlströme erzielen lassen, wenn man Os nicht als Kation Os+, sondern
als Anion OsO3– mißt[97]. Das von Heumann skizzierte Verfahren wurde am Caltech soweit
entwickelt, daß es inzwischen zur Routinemessung geologischer Proben dienen kann[93].
Danach wird die Probe, zusammen mit Ba(NO3)2, auf ein Pt-Filament geladen. Das Barium
reduziert die Elektronenaustrittsarbeit (die Wahrscheinlichkeit dafür, daß ein Atom als Ion
die heiße Filamentoberfläche verläßt) des Pt-Filaments und dient, ähnlich wie La, als Elektronenemitter (und der Sauerstoff des nach Erhitzen des Filaments verbleibenden BaO
wohl als O-Donator). Zur Analyse müssen die Polarität des Elektromagneten des Spektrometers und des power supply für die Beschleunigungsspannung umgekehrt werden. 4ng Os
lieferten dabei stabile Ionenströme von »3´10-12A über etwa eine Stunde, was die Bestimmung der Os-Isotopie mit einer Genauigkeit von ca. ±2‰ auf dem Faraday zuläßt; 70pg Os
können noch mit ±5‰ 2s-Fehler auf einem Sekundärionenvervielfacher gemessen werden. Os und Re können auf dasselbe Filament geladen werden, weil die Verhältnisse von
ReO 4– / ReO3– > 250 sind und damit i.a. tolerierbare Masseninterferenzen bilden. Damit ist
das Re–Os-Isotopensystem jetzt auch der gewöhnlichen Massenspektrometrie zugänglich
und erfordert nicht mehr den Einsatz von high-tech-Maschinen (Resonanzionenmassenspektrometer[98], Beschleunigermassenspektrometer[99]). Sicherlich wird das Re–Os-System
in der Zukunft eine größere Bedeutung erlangen als bisher.
Re verhält sich geochemisch ähnlich wie Mo und reichert sich daher in molybdänhaltigen
Mineralen hoch über seinen geochemischen Durchschnitt an. So wurden in Molybdän-
97
Die Re–Os-Methode
glanzen Re-Gehalte zwischen einigen ppm und mehr als 1% gemessen. Da Mo-Minerale
arm an Os sind, können die Os-Isotopien solcher Minerale extrem radiogen sein. Bei partiellen Aufschmelzprozessen im oberen Erdmantel scheint sich das Re wie ein mäßig inkompatibles Element zu verhalten; für ozeanische Basalte besteht eine gute Korrelation zu den
schweren REE[100].
Als Element der Pt-Gruppe ist Os stark siderophil und kommt vor allem als Mineral Osmiridium vor sowie in Cu- und Ni-Sulfiden vornehmlich ultrabasischer Gesteine. Os scheint
sich bei der partiellen Aufschmelzung des Erdmantels weitgehend kompatibel zu verhalten. Die Häufigkeitsverhältnisse von Re und Os variieren daher in Erdmantel und Erdkruste
sehr stark. Tabelle 9 mag einen Überblick darüber geben:
TABELLE 9:
Re- und Os-Gehalte verschiedener Gesteinstypen
Gesteinstyp
Chondrite
Fe-Meteorite
Granat- und Spinellperidotite (südl.
Afrika)[101]
Komatiite, Tholeiite (Gorgona/Kolumbien)[102]
Ozeaninselbasalte[103]
[104]
klastische Sedimente
ppb Re
57 (30 - 80)
2500 (5 – 50000)
0.02 – 2
ppb Os
660 (300 – 900)
30000 (7 – 50000)
1–7
1 – 2.3
1.0 – 6.5
0.06 – 0.5
0.1 – 10
0.01 – 0.35
£0.1
1.5
Re-Os-Isotopie der Meteorite
Initialwert (4.55Ga): 0.806±0.006
1.4
187
Os/186Os
1.3
1.2
1.1
1.0
Eisenmeteorite
Mesosiderit
Chondrite (Metallphase)
0.9
0.8
0
ABBILDUNG 74
2
4
187
6
8
Re/186Os
Re–Os-Isochrone für verschiedene Typen von Meteoriten[105],[91]
Die extrem niedrigen Re- und Os-Gehalte der Silikatgesteine dürften eine Konsequenz des
siderophilen bzw. chalcophilen Charakters dieser Elemente sein, weswegen sie vermutlich
im Metallkern der Erde hoch angereichert sind. Infolge der sehr unterschiedlichen Re/Os-
98
A. Radiogene Isotopensysteme
Verhältnisse in Erdmantel und -kruste wird man erwarten, daß die Os-Isotopien dort sehr
verschieden voneinander sind.
6
Entwicklung der Os-Isotopie in
Erdmantel und Erdkruste
5
4
O
6
18
Osmiridium
e/
R
Laurit
te
m
s
ru
K
2
ky
ns
ef
Re
re
Me
Witwa
tersran
orite
1.04
Ural
1
Mete
Papua-Neuguinea
it
Australien
3
7
18
10
Australien
187
Os/186Os
0
s=
d
0
4
3
2
1
0
t [Ga]
ABBILDUNG 75
Os-Isotopenentwicklungskurve des Erdmantels
Jagersfontein
1.2
0.
9G
a
N. Lesotho
Premier
2.
4«
Kimberlit
(Bellsbank)
Kontamination durch Kimberlit
1.0
187
Os/
186
Os
1.1
0.9
Granat- und Spinellperidotite, südliches Afrika
0.8
0
ABBILDUNG 76
5
187
Re/186Os
10
15
Re–Os-Isotopenzusammensetzung von Gesteinen des Erdmantels
Bei der Bestimmung der Halbwertszeit von 187Re nach der Isochronenmethode durch Luck
& Allègre (1980)[105] stellte sich heraus, daß Eisenmeteorite, Steineisenmeteorite und die
Metallphasen aus Chondriten auf derselben Isochrone liegen (siehe Abbildung 74) und
daher zur selben Zeit oder innerhalb eines relativ kurzen Zeitintervalls von »100Ma ent99
Die Re–Os-Methode
standen sein müssen. Der Schnittpunkt der Isochrone mit der Ordinate liefert das initiale
187
Os/186Os des Sonnensystems vor »4.55 Ga mit 0.806±0.006.
187Os/188Os
187Os/188Os
Die Os-Isotopen0.140
entwicklungskurve des ErdmanRe-Os-Isotopensystematik
tels (bzw. der Erde)
von
Peridotiten aus den Pyrenäen
0.135
wurde von Luck &
Allègre (1982) dadurch bestimmt,
0.130
daß sie Os-haltige
Minerale aus Ul0.125
t r a m a fi t e n v e r schiedenen Alters
analysierten [106] .
0.120
In diesen Minera187
len ist das
Os/
186
Os infolge des
0.115
niedrigen Re/OsVe r h ä l t n i s s e s
praktisch einge0.110
froren seit der Zeit
0.0
0.1
0.2
0.3
0.4
0.5
ihrer Kristallisa187Re/188Os
tion (siehe Abbildung 75). Nach
0.140
diesen Untersuchungen liegt das
Korrelation von Os-Isotopen mit Al
187
Os/186Os des
für Peridotite aus den Pyrenäen
0.135
Mantels heute bei
1.040±0.010.
Kombiniert mit
0.130
dem Initialwert
des Sonnensystems, ergibt sich
0.125
daraus ein 187 Re/
186
Os-Verhältnis
0.120
von 3.3 bzw. ein
Re/Os-Verhältnis
von 0.082 (Um0.115
rechnungsfaktor:
187
Re/ 186 Os = Re/
Os´40.2). Messun0.110
gen an chondriti0
1
2
3
4
5
schen Meteoriten
%Al2O3
[107]
zufolge
, liegt
deren mittleres
187
Os/186Os heute ABBILDUNG 77 Re–Os-Isotopendiagramm [oben] bzw. Al–187Os/188Osbei »1.06 (entspre- Korrelation [unten] für Peridotite aus den Pyrenäen[108]
chend
einem
187
Os/188Os von 0.1276). Granat- und Spinellperidotite aus südafrikanischen Kimberliten
zeigen 187Os/186Os-Verhältnisse zwischen 0.91 und 1.07 (Walker et al., 1989[101]) und
schwanken damit nicht sehr stark um den nominellen Mittelwert des heutigen Erdmantels
(Abbildung 76). Die meisten Daten liegen unter dem chondritischen Wert und zeigen an,
daß die Peridotite bei einem hypothetischen Schmelzereignis Re bevorzugt über Os verloren haben. Ihre Re–Os-Modellalter liegen um 2.5 Ga.
100
A. Radiogene Isotopensysteme
Eifel
187
kanadische Kordillere
Os/188Os
187
Os/188Os
Reisberg und Lorand [ 1 0 8 ]
0.135
haben gefunden, daß sich
zwischen dem Al-Gehalt von
alpinotypen Peridotiten und
ihrer Os-Isotopie bessere Korkanadische Kordillere
0.130
relationen ergeben als zwi9/2
(Peslier et al., 2000)
MHP7
schen dem Re/Os-Verhältnis
und der Os-Isotopie (AbbilIb/8
dung 77). Sie argumentierten, daß der Al-Gehalt ein
0.125
Indikator für den Aufschmelzgrad ist, da Al in denjenigen Mineralen des ErdIb/3
mantels beheimatet ist, die
bevorzugt in die Schmelze
0.120
Dreiser Weiher
eintreten und sich das Cr/Al(Meisel et al., 1996)
Ib/2
Verhältnis der residualen
Peridotite mit zunehmendem Aufschmelzgrad konti0.115
nuierlich erhöht. Das Re/Os0
10
20
30
40
50
60
70
80
Verhältnis kann demgegenppb
Lu
über durch sekundäre Pro0.135
zesse (Metasomatosen)
infolge der Mobilität des Re
Os-Isotopen-Modellalter des
0.130
erhöht oder zumindest unsylithosphärischen Erdmantels
stematisch verändert werden,
0.125
so daß die Re–Os-Systematik
der Peridotite keine verwertbaren Altersinformationen
0.120
konserviert haben müssen.
Os
We n n m a n d e n A c h s e n 0.115
-Is
ot
abschnitt der Al–187Os/188Osop
d
en
Korrelation als Initialwert
es
0.110
en
Er
eines magmatischen Ereigdm twi
an cklu
nisses interpretiert, als „Bil0.105
te
ng
ls
dungsalter“ des subkontinentalen lithosphärischen
0.100
Mantels nach Differenzierung aus einem primitiven
0.095
Mantel, dann läßt sich aus
0
1
2
3
4
der ErdmantelentwicklungsAlter
[Ga]
kurve das ungefähre Alter
abschätzen, im Fall der Peridotite aus den Pyrenäen von ABBILDUNG 78 Korrelation zwischen Os-Isotopien und den
knapp 2.5 Ga. Ähnlich wie Al Gehalten an schweren REE am Beispiel des Lu für Erdmantellassen sich auch die schwe- xenolithe aus dem Westen Kanadas[109] und der Eifel[110],[112]
ren REE, z.B. Lu verwenden (oberes Diagramm). Aus der Korrelation ergeben sich initiale
(Abbildung 78). Die Qualität Os-isotopien, mit denen sich im unteren Diagramm über die
der Korrelation ist überra- Entwicklungskurve des Erdmantels Modellalter konstruieren
schend gut. denn die schwe- lassen, gut 1 Ga im Fall Kanadas und gut 1.5 Ga im Fall der
r e n R E E , O s u n d ( d a s Eifel.
ursprüngliche) Re sind
sicherlich in verschiedenen Phasen der Erdmantelgesteine beheimatet (schwere REE weitgehend in den Klinopyroxenen und untergeordnet in den Orthopyroxenen, das Os eher in
Sulfiden, möglicherweise auch in Form metallischer Legierungen; Re keine Informatio-
101
Die Re–Os-Methode
nen). Für die kanadische Kordillere argumentieren Peslier et al. (2000)[109], daß die krustalen Teile der Lithosphäre in der Region sowohl höhere als auch niedrigere Alter aufweisen,
so daß die Beziehung zwischen Kruste und oberstem Mantel dort möglicherweise tektonisch bedingt ist.
187Os/186Os
In den Partialschmelzen des Erdmantels
Tholeiite, Gorgona
5
wird sich Re über Os in
Island
(Kolumbien)
Abhängigkeit vom Aufschmelzgrad mehr oder
weniger stark anrei4
chern. In der Tat haben
tertiäre komatiitische
Schmelzen von Gorgona Island im Pazifik
3
vor Kolumbien niedrigere 1 8 7 Re/ 1 8 6 Os-Vert=88«4Ma
hältnisse (7 – 50) als
2
tholeiitische Basalte
(300 – 2700) derselben
Insel [ 1 0 2 ] . Auf Grund
dieser extremen Frak1
tionierung werden sich
0
500
1000
1500
2000
2500
3000
in Basalten im Verlauf
187Re/186Os
der Zeit rasch sehr
radiogene Isotopien
einstellen, und damit ABBILDUNG 79 Re–Os-Isochrone für Basalte
sollten sich im Prinzip
mit der Re–Os-Methode auch mesozoische und selbst tertiäre Vulkanite datieren lassen. Für
die Tholeiite von Gorgona Island wurde eine präzise Isochrone erhalten, deren Alter die
Entstehung dieser Gesteine angeben sollte (siehe Abbildung 79).
Da Gesteine der kontinentalen Erdkruste ein sehr hohes Re/Os-Verhältnis aufweisen, woraus altersabhängig ein sehr radiogenes 187Os/186Os resultieren kann, eignet sich das Os-Isotopenverhältnis potentiell, um die Kontamination von basischen Magmen durch alte Kruste nachzuweisen.
Die Fraktionierung von Re und Os ist um Größenordnungen höher als die zwischen Sm
und Nd; die resultierenden 187Re/186Os-Verhältnisse zeigen sogar größere Variationen als
die 87Rb/86Sr-Verhältnisse. Die Os-Isotopie wird daher bequemerweise, ähnlich wie die des
Nd, relativ zum Erdmantel angegeben, hier allerdings als prozentuale Abweichung:
g Os
é
=ê
ê
êë
(
(
187
Os
187
Os
)
Os)
186
186
Os
Probe
Mantel
ù
é
- 1ú ´ 100 bzw. g Os = ê
ú
ê
úû
êë
(
(
187
Os
187
Os
)
Os)
188
Os
Probe
188
Mantel
ù
- 1ú ´ 100
ú
ûú
[GL 99]
Eine Analyse von Peridotitxenolithen verschiedener Kontinente führte Meisel et al. (1997)
über eine Extrapolation zum Schluß, der primitive Erdmantel habe heute ein 187Os/188Os
von mindestens 0.1290±0.0009, vergleichbar den Enstatitchondriten, aber etwas höher als
der Wert für kohlige Chondrite (0.1258±0.0005)[110]. Dem Wert von 0.1290 für 187Os/188Os
entspricht 1.072 für 187Os/186Os; diese Werte, die in GL 99 einzusetzen wären, liegen etwas
über denen, die ursprünglich abgeleitet worden waren.
Es ist inzwischen aus der Analyse von Peridotiten gut belegt, daß der obere Erdmantel zwar
ein chondritisches Ir/Os, aber um ca. 30 – 50% erhöhte Pt/Ir-, Rh/Ir- und Pd/Ir-Verhältnisse
aufweist[111], obwohl Os und Ir als die am stärksten kompatiblen dieser Elemente gelten.
Generell liegen die Gehalte der Elemente der Platingruppe [PGE] um mehr als drei Zehner-
102
A. Radiogene Isotopensysteme
potenzen über denjenigen, die erwartet würden, wenn die Trennung der Erde in eine silikatische und eine Metallphase vor »4.5 Ga unter ungefähren Gleichgewichtsbedingungen
erfolgt wäre (Niedrigdruckfraktionierung nahe der frühen Erdoberfläche). Als Erklärung für
die zu hohen PGE-Gehalte des Erdmantels ist die late veneer-Hypothese vorgeschlagen worden, nach der die überschüssigen PGE durch Meteoriteneinfall nach der Separation des
Erdkerns auf die Erde gelangt sein könnten. Die Alter der großen Krater auf dem Mond gelten als Hinweis für die Plausibilität einer solchen Erklärung. Allerdings lassen sich die heutigen PGE-Verhältnisse des Erdmantels nicht mit dem Einfall chondritischer Meteorite
(»1% der Masse der Erde!) erklären, sondern allenfalls mit einer selektiven Addition der
fraktionierten Eisenmeteorite; dies erscheint wenig plausibel. Eine Alternative bildet die
Vermischung von Material des äußeren Erdkerns mit unterstem Erdmantel in der D''Region, dem möglichen Quellgebiet tiefer Plumes, die den oberen Erdmantel allmählich an
PGE angereichert haben[113]. In Analogie zu den Eisenmeteoriten müßte der flüssige äußere
Kern an Pt und Pd relativ zu Os und Ir angereichert sein, weil Os und Ir infolge hoher
Metall/Metallschmelze-Verteilungskoeffizienten bei der allmählichen Kristallisation des
festen inneren Erdkern bevorzugt über Pt und Pd in diesen festen Kern gewandert sein sollten[111]. Wenn dem so ist, sollte das zeitintegriert hohe Pt/Os-Verhältnis im flüssigen äußeren Kern durch den a-Zerfall von 190Pt ein etwas erhöhtes 186Os/188Os erzeugt haben, das
sich in günstigen Fällen in Plume-Basalten nachweisen lassen mag. Bislang ist dies nicht
gelungen, weil die Isotopenunterschiede wegen der extrem langen Halbwertszeit von 190Pt
sehr gering sein werden.
Ein Problem, das
man – letztlich
K/T-Grenzton
nicht eindeutig –
durch Anwendung
der
R e – O s - M e - kontinentale Kruste
thode zu lösen versucht hat, ist die
rezente Mn-Knollen
Natur des Ereignisses an der Kreide/
Tertiär-Grenze. SeErdmantel
dimente, die an der
K/T-Grenze sowohl
im marinen als
Meteorite
auch im kontinentalen Milieu abgela1
10
100
gert wurden, zeich187
186
Os/ Os
nen sich weltweit
durch eine Anreicherung von Plati- ABBILDUNG 80 Os-Isotopenverhältnisse verschiedener Gesteine im Zunoiden erheblich sammenhang mit der K/T-Grenze
über den lokalen
geochemischen Untergrund aus. Eine populäre Hypothese ist, daß dies auf den Einschlag
eines »10km großen Meteoriten (oder noch größeren Asteroiden) zurückzuführen ist, während andere Hypothesen terrestrische Ursachen geltend machen. Proben des K/T-Grenztons weisen 187Os/186Os-Verhältnisse auf, wie man sie auch in Meteoriten findet (siehe Abbildung 80[114]), während typische kontinentale Erdkruste zehnfach höhere Verhältnisse
hat. Obwohl dieser Befund die extraterrestrische Hypothese zu stützen scheint, kann nicht
unterschieden werden zwischen extraterrestrischem Os und Erdmantel-Os. Im letzteren
Fall wäre dann allerdings eine gewaltige vulkanische Aktivität auf der Erde an der K/TGrenze erforderlich, wobei platinoidhaltige Gase in die Stratosphäre gelangen müßten, um
sich weltweit auszubreiten. Dabei ist vor allem auf den Dekkan-Vulkanismus in Indien hingewiesen worden, wobei jedoch unklar bleibt, wie „stiller“ basaltischer Vulkanismus große
Mengen an Gasen in die Stratosphäre schleudern kann. Explosiver saurer Vulkanismus, der
i.w. an Subduktionszonen geknüpft ist, trägt zwar große Mengen an Staub in die Strato103
Die Re–Os-Methode
sphäre, bringt dagegen nicht die erforderlichen Mengen an Platinoiden mit. Daß es an der
Kreide/Tertiär-Grenze den Einschlag eines extraterrestrischen Objektes gegeben haben
muß, ist inzwischen durch andere Argumente erhärtet, z.B. durch eine kleine Isotopenanomalie beim Cr[115].
Durch die Analyse von metallreichen Sedimenten aus Bohrkernen im Pazifik haben
Peucker-Ehrenbrink et al. (1995) versucht, die Meerwasserentwicklungskurve der Os-Isotope
über die vergangenen 80 Ma zu rekonstruieren (Abbildung 81[117]). Dabei wird angenommen, daß die beste Annäherung an die Os-Isotopie des Meerwassers erhalten wird durch
die Analysen von karbonatreichen Sedimenten, die bei rascher Sedimentation entstanden
sind oder durch eine Ätzung klastischer Sedimente mit einer sauren Peroxidlösung, bei der
das an Fe-Mn-Oxihydroxide gebundene Os herausgelöst wird. Aus der Abbildung ist zu
ersehen, daß 187Os/186Os an der K/T-Grenze mit einem Wert von nur wenig größer als 1 ein
Minimum aufweist und anschließend rasch wieder ansteigt. Auch wenn sich die Autoren
klar für einen Impakt als Quelle des unradiogenen Os aussprechen, bleibt festzustellen, daß
infolge der relativ schlechten zeitlichen Auflösung Erdmantel-Os nicht völlig ausgeschlossen werden kann.
1.2
10
Gesamtsedimentprobe
Lösung nach milder Ätzung
der Gesamtprobe
Lösung nach starker Ätzung
der Gesamtprobe
1.0
0.8
187
0.6
Os/188Os
6
187
Os/186Os
8
4
0.4
2
0.2
0
20
40
60
80
Alter [Ma]
ABBILDUNG 81
104
Variation der Os-Isotopenzusammensetzung in metallreichen pazifischen Sedimenten über die vergangenen 80 Ma[117]. Die größeren der Kreise und
Quadrate stehen für Karbonate, die während großer Sedimentationsraten
gewachsen sind. Es wird angenommen, daß solche Proben die beste Annäherung an die Os-Isotopie des Meerwassers darstellen. Die schlechteste Annäherung stellen Gesamtanalysen klastischer Sedimente dar (kleinere
Quadrate), bei denen die Wahrscheinlichkeit groß ist, daß ihre Os-Isotopie
durch einen Anteil an Mikrometeoriten zu niedrig ausfällt. Das Band der
Meerwasserkurve wurde daher bevorzugt durch die karbonatreichen Sedimente gelegt.
A. Radiogene Isotopensysteme
12.0
Die U,Th–Pb-Methoden
Der Zerfall von 238U, 235U und 232Th in 206Pb, 207Pb und 208Pb bildet die Grundlage für eine
ganze Reihe von mehr oder weniger wichtigen Methoden der Geo- und Kosmochemie. Zu
den frühesten, inzwischen aufgegebenen Methoden der Geochronologie gehören die UHe-Methode, bei der die Mengen an He und U in einem Mineral ermittelt werden, und die
chemische U–Pb- bzw. Th–Pb-Methode, bei der die Konzentrationen an diesen Elementen
in einer Probe gemessen werden und zudem angenommen wird, alles Pb stamme aus dem
U- bzw. Th-Zerfall. Die Isotopenmethoden hingegen erfreuen sich wieder großer Wertschätzung, nachdem man erkannt hat, daß auch Rb–Sr und Sm–Nd als Chronometer viele
Tücken haben und daß die U,Th–Pb-Methoden Informationen liefern, die mit anderen Isotopensystemen nicht zu erhalten sind. Die Entwicklung hoch auflösender SekundärionenMassenspektrometer (Ionensonden) und Laserablations-ICP-MS-Geräte, mit denen sich die
Pb-Isotopenzusammensetzung an einzelnen Mineralkörnern messen läßt, wird diese
Renaissance sicherlich noch verstärken.
Das Th-Isotop 232Th sowie die Isotope 235U und 238U sind die schwersten in der Natur noch
vorkommenden primordialen Nuklide. 5 weitere Th-Isotope (227, 228, 230, 230, 234) und
ein U-Isotop (234) treten in sehr geringen Konzentrationen in den 3 Zerfallsreihen auf.
U und Th gehören zur Gruppe der Actiniden, die sich chemisch ähnlich wenig unterscheiden wie die REE (In beiden Gruppen werden die f-Orbitale der Elektronenhülle aufgefüllt,
4f bei den Seltenen Erden, 5f bei den Actiniden). U und Th treten in der Natur vierwertig
auf. Der Unterschied ihrer Ionenradien beträgt dann »5% (U4+ 1.00Å, Th4+ 1.05Å für 8er
Koordination), und beide Elemente können sich in den Kristallstrukturen von Mineralen
zum Teil ersetzen. Unter oxidierenden Bedingungen – d.h. vor allem im sedimentären
Milieu – kann U jedoch sechswertig vorkommen und bildet dann das Uranylion UO22+ ,
dessen Salze in wäßrigen Lösungen im Gegensatz zu den U4+-Verbindungen meist gut
löslich sind. Da Th nicht oxidierbar ist, kann unter solchen Bedingungen eine weitgehende
chemische Trennung beider Elemente in der Natur erfolgen, eine Eigenschaft, die man sich
bei der Datierung durch die Ungleichgewichtsmethoden zunutze macht. Vor allem in den
Ozeanen tritt Uran sechswertig auf und ist dann besser löslich als Th, so daß chemische
Sedimente (Karbonate) Th/U-Verhältnisse <1 haben können, während das kosmische Verhältnis und das vieler terrestrischer Gesteine um 4 liegt.
Das Schwermetall Pb tritt in der Natur fast nur zweiwertig auf, selten – unter stark oxidierenden Bedingungen – auch vierwertig. Der Ionenradius von Pb2+ ist beträchtlich höher als
der von U4+ oder Th4+ (Pb2+ in 8er Koordination 1.29Å, in 6er Koordination 1.19Å), und so
verhalten sich U/Th und Pb geochemisch sehr unterschiedlich. Pb, sofern es keine eigenen
Minerale, insbesondere Sulfide, bildet, tritt als Spurenelement in K-haltige Minerale – insbes. Kalifeldspäte – ein, während sich U und Th vornehmlich in Akzessorien von Gesteinen
finden, z.B. Allanit, Titanit, Epidot, Apatit, Monazit und Zirkon.
Tabelle 10 gibt grobe Anhaltspunkte über die Pb-, Th- und U-Gehalte verschiedener
Gesteine und Minerale (zusammengestellt nach [118] und [16]).
Da Pb, Th und U hoch inkompatible Elemente für die Paragenesen des uns zugänglichen
Erdmantels sind (mit Ausnahme der jedoch meist bleiarmen Sulfide), sind sie in den
Gesteinen der Erdkruste hoch angereichert.
Die Gleichungen, die den Zerfall von U und Th beschreiben, lassen sich wie folgt zusammenfassen:
238
U ® 206Pb + 8 4He + 6b–
235
[GL 100]
U ® 207Pb + 7 4He + 4b–
[GL 101]
Th ® 208Pb + 6 4He + 4b–
[GL 102]
232
105
Die U,Th–Pb-Methoden
TABELLE 10:
Pb-, Th- und U-Gehalte von Gesteinen und Mineralen
ppm Pb
1.0
0.4
Chondrite
Achondrite
primitiver Erdmantel
MORB
Alkalibasalte
Granitoide
Sandsteine
Tone
Allanit
Apatit
Epidot
Titanit
Zirkon
Monazit
Feldspäte
0.5–1.5
0.4–10
23 (2–150)
14 (2–50)
1–80
10–10000
3–300
(Amazonit –1%!)
1–100
Biotit
ppm Th
0.04
0.36
0.094
0.5
8
22
4
3 – >>20
1000 – 20000
50 – 250
200
100 – 1000
100 – 10000
2% – 20%
0.5 – 10
ppm U
0.01
0.07
0.026
0.2
1.5
5
1.5
4 – >180
30 – 1000
10 – 100
20 – 200
10 – 700
100 – 6000
500 – 3000
0.1 – 10
0.5 (–50?)
1(–50?)
In diesen 3 natürlichen Zerfallsreihen entstehen als intermediäre Tochterprodukte 43 Isotope von 12 Elementen. Keines dieser Nuklide ist Mitglied von mehr als einer Zerfallsreihe.
In Tabelle 11 sind wichtige Daten der natürlich vorkommenden U- und Th-Isotope zusammengestellt:
TABELLE 11:
Halbwertszeiten und Zerfallskonstanten der wichtigsten U- und ThIsotope
Isotop
238
U
235
U
234
U
232
Th
Häufigkeit (%)
99.2743
0.7200
0.0057
100.00
Halbwertszeit
4.468´109a
0.7038´109a
2.47´105a
14.010´109a
Zerfallskonstante
1.55125´10-10 a-1
9.8485´10-10 a-1
2.806´10-6 a-1
4.9475´10-11 a-1
234
U tritt als intermediäres Zerfallsprodukt in der 238U-Reihe auf und ist infolge seiner langen Halbwertszeit im natürlichen U noch mit »57ppm vertreten.
Verglichen mit der Halbwertszeit der Mutternuklide, sind die Halbwertszeiten aller intermediären Tochternuklide vernachlässigbar klein. Die längstlebigen Zwischenprodukte treten in der 238U-Zerfallsreihe auf mit 234U, 230Th (75000a) und 226Ra (1600a). Auf Grund dieser Eigenschaft läßt sich auf die Zerfallsreihen das Gesetz des säkularen Gleichgewichts
anwenden, das besagt, daß pro Zeiteinheit von jedem der intermediären Nuklide genausoviele Atome gebildet werden wie Atome zerfallen und wie Atome des Mutternuklids zerfallen, d.h. die Aktivitäten aller Nuklide sind gleich groß:
N1l1 = N2l2 = … = Nnln
[GL 103]
In offenen Systemen, z.B. in Magmenkammern oder in den Ozeanen, kann es jedoch
infolge der unterschiedlichen chemischen Natur der Zwischenprodukte und der Mutternuklide zu einer Störung dieses säkularen Gleichgewichts kommen, d.h.GL 103 gilt nicht
106
A. Radiogene Isotopensysteme
mehr. Mit den damit verbundenen Problemen und Möglichkeiten beschäftigen sich die
Ungleichgewichtsmethoden, für die man zur Messung der Isotopenverhältnisse mit einem
a-Detektor auskommt und nicht unbedingt ein Massenspektrometer benötigt. Minerale
und Gesteine dagegen sollten – zumindest bei niedriger Temperatur – ähnlich geschlossene
Systeme bilden wie für die anderen Isotopensysteme, mit der Einschränkung, daß durch
die Vielzahl der Zerfälle innerhalb der U- und Th-Zerfallsreihen in den betroffenen Kristallgittern vergleichsweise hohe Konzentrationen von Gitterstörungen geschaffen werden.
Natürliches Pb besteht aus den vier stabilen Isotopen 204Pb, 206Pb, 207Pb und 208Pb mit im
Mittel folgenden Häufigkeiten: 1.48%, 23.6%, 22.6% und 52.3%. Sie können von Gesteine
zu Gestein oder Mineral zu Mineral jedoch extrem davon verschieden sein. Lediglich 204Pb
hat keinen Anteil, der aus einem natürlichen Zerfallsprozeß gebildet ist; es ist deshalb das
einzige Isotop, das sich zur „Normierung“ der Massenspektrometerdaten eignet. Leider
fehlt beim Pb ein zweites natürliches Isotop, das nicht durch Zerfallsprozesse nachgebildet
wird, so daß keine exakte Korrektur der Massenfraktionierung der Spektrometerdaten vorgenommen werden kann. Zum Glück sind die Isotopenvariationen beim Pb wesentlich
größer als beim Nd oder Hf, so daß dieser Nachteil meist keine wesentliche Einschränkung
bedeutet. Abhilfe kann hier die Methode des Doppelspikes schaffen, bei welcher der zu
messenden Probe eine exakt bekannte Menge eines Spikes zugesetzt wird, der aus 2 Pb-Isotopen besteht, von denen eines das künstlich hergestellte 205Pb ist mit einer Halbwertszeit
von »3´107a.
12.1
Die U–Pb- und Th–Pb-Isochronenmethoden
Für jede der 3 Zerfallsreihen kann eine eigene Zerfallsgleichung formuliert werden, die
erwartungsgemäß die Form haben:
206
Pb æ
=ç
204
Pb è
206
207
207
Pb æ
=ç
204
Pb è
208
204
Pb æ
=ç
Pb è
Pb ö
+
÷
204
Pb ø initial
238
204
235
Pb ö
+
÷
204
Pb ø initial
204
208
232
204
Pb ö
+
÷
Pb ø initial
U l238 t
e
-1
Pb
(
)
[GL 104]
U l235 t
e
-1
Pb
[GL 105]
Th l232 t
e
-1
Pb
[GL 106]
204
(
(
)
)
Man kann daher im Prinzip aus einer massenspektrometrischen Bestimmung der Pb-Isotopenverhältnisse und einer Konzentrationsbestimmung von Pb, Th und U drei voneinander
unabhängige Altersdaten errechnen und hat auf diese Weise eine interne Kontrolle der
Ergebnisse, wie sie keine der anderen Methoden zu bieten hat. Wenn die drei Alter innerhalb der Analysenfehler identisch sind, kann man sicher sein, irgendein geologisches
Ereignis datiert zu haben.
Früher hat man versucht, mit Hilfe dieser 3 Gleichungen Modellalter zu berechnen. Dazu
eignen sich theoretisch U,Th-reiche, Pb-arme Minerale, insbes. Zirkon, aber auch Titanit,
Monazit, Uraninit oder Apatit. Solche Minerale haben bei ihrer Entstehung nur sehr wenig
Pb inkorporiert, so daß sie – wenn sie aus alten Gesteinen stammen – hohe 206Pb/204Pb-,
207
Pb/204Pb- und 208Pb/204Pb-Verhältnisse haben. Wenn man davon ausgeht, daß diese
Minerale bei ihrer Entstehung Pb mit einer „normalen“ irdischen Isotopenzusammensetzung eingebaut haben, dann macht man durch Erraten der initialen 206Pb/204Pb-, 207Pb/
204
Pb- und 208Pb/204Pb-Verhältnisse keinen allzu großen Fehler. Tatsächlich zeigt sich aber,
daß die nach dieser Methode berechneten Alter meist diskordant sind. Man muß daher
annehmen, daß die Minerale im Lauf ihrer geologischen Geschichte keine geschlossenen
Systeme waren oder eine komplexe Entstehungsgeschichte mit mehreren Wachstumsphasen hatten.
107
Die U,Th–Pb-Methoden
Etwas sicherer ist die Methode der 206Pb/204Pb–207Pb/204Pb-Analyse, die bereits 1939 von
A.O. Nier eingeführt wurde. Dabei werden GL 104 und GL 105 kombiniert:
207
204
Pb æ
-ç
Pb è
206
Pb æ
-ç
204
Pb è
207
204
Pb ö
÷
Pb ø initial
206
Pb ö
÷
204
Pb ø initial
(
(
)
)
l235 t
-1
U e
= 238
U e l238 t - 1
235
[GL 107]
Auf der linken Seite dieser Gleichung steht das Verhältnis des radiogenen Anteils (207Pb/
204
Pb)/(206Pb/204Pb) = (207Pb/206Pb)rad., das man errechnen kann, wenn man von den
gemessenen 207Pb/204Pb- und 206Pb/204Pb-Verhältnissen ein angenommenes initiales Verhältnis subtrahiert. Auf der rechten Seite der Gleichung steht mit dem heutigen Verhältnis
235
U/238U eine Konstante für fast alle terrestrischen Proben (Ausnahmen: Proben, in denen
in Naturreaktoren ein Abbrand des 235U erfolgte) und Meteorite (=1/137.88). D.h. man
braucht zur Altersberechnung nach GL 107 weder die U-Isotopenzusammensetzung noch
die Konzentrationen von U und Pb zu analysieren. Aber auch die derart berechneten Alter
von Zirkonen etc. scheinen oft keine geologische Bedeutung zu haben, auch wenn meist
t207/206 > t207 > t206 ist und damit näher am tatsächlichen Alter.
Mit den Gleichungen GL 104 – GL 106 läßt sich natürlich auch nach der gewöhnlichen
Isochronenmethode arbeiten. Jedoch zeigt sich selbst hier, daß das U–Pb-System in Gesteinen wie Granitoiden oft gestört ist, vermutlich weil die Gesteine bereits bei einsetzender
chemischer Verwitterung an der Erdoberfläche rasch U-Verluste erleiden. Ätzversuchen
zufolge ist das U oft auf den Mineraloberflächen konzentriert und läßt sich leicht ablösen,
wohl weil es meist sechswertig ist. Da das Th–Pb-System resistenter gegen solche Verwitterungseinflüsse ist, gelingen Datierungen nach dieser Methode des öfteren.
Die Gründe für die häufigen Störungen der U–Pb- und Th–Pb-Systeme liegen sicherlich
darin, daß der Zerfall von U bzw. Th nach Pb mit einer hohen Zerfallsenergie und vielen
Einzelzerfällen verbunden ist, die eine hohe Konzentration an Gitterstörungen in den
betroffenen Mineralen erzeugen und die Minerale dann anfällig gegenüber Elementverlust
oder chemischen Austausch mit der Umgebung machen. In anderen isotopengeochemisch
bedeutsamen Zerfallssystemen gibt es dagegen nur einen Zerfallsprozeß, der zudem
wesentlich energieärmer ist. Darüber hinaus verhalten sich U und Th chemisch erheblich
anders als Pb, so daß zudem noch sehr große Elementfraktionierungen in der Natur erzeugt
werden können, ähnlich wie bei Rb und Sr zu beobachten.
Auch die Pb–Pb-Isochronenmethode nach GL 107 hat sich des öfteren zur Datierung von
Gesteinen als geeignet erwiesen. Da auf der linken Seite dieser Gleichung das Verhältnis
(207Pb/206Pb)rad. steht, das sich über lange geologische Zeit seit der Bildung des Gesteins entwickelt hat, wirken sich junge – z.B. durch die Verwitterung an der Erdoberfläche verursachte – U- oder Pb-Verluste hier nicht aus. Für das Alter t eines Gesteins ist die rechte Seite
von GL 107 eine Konstante m:
m=
1
e l235 t - 1
´ l t
137.88 e 238 - 1
[GL 108]
Dann wird
207
204
207
Pb æ
-ç
Pb è
207
204
Pb
= m´
204
Pb
108
æ
Pb
-m´ç
Pb
è
206
æ
Pb ö
-m´ç
÷
204
Pb ø initial
è
206
Pb ö
= m´
÷
Pb ø initial
206
Pb æ
+ç
204
Pb è
207
206
204
204
204
Pb ö
÷
Pb ø initial
Pb ö
÷
Pb ø initial
A. Radiogene Isotopensysteme
207
204
Pb
= m´
Pb
206
204
Pb
+C
Pb
[GL 109]
Dies ist die Gleichung einer Geraden, wenn man die gemessenen Verhältnisse 207Pb/204Pb
und 206Pb/204Pb gegeneinander aufträgt. Aus der Steigung m der Geraden kann das Alter t
des Gesteins nach einer Iterationsmethode ermittelt werden.
12.1.1
Konkordia und Diskordia
Die Pb–Pb-Methode hat ihre Grenzen dort, wo ein System bereits vor geologisch langer Zeit
gestört wurde. Der klassische Fall ist der des magmatischen Gesteins, das irgendwann
metamorph überprägt wurde. Da man bei den U- und Th-Zerfallsreihen aber auf 2 oder
sogar 3 voneinander unabhängige Zerfallssysteme zurückgreifen kann, lassen sich auch
Gesteine mit solchen Mehrstufenentwicklungen noch datieren. Dazu bedient man sich der
in den Gesteinen vorkommenden U- und/oder Th-haltigen Akzessorien, wobei den Zirkonen eine besondere Bedeutung zukommt. Zirkone finden sich in vielen Gesteinstypen
magmatischer, metamorpher und sedimentärer Herkunft; sie kristallisieren bzw. wachsen
vorzugsweise in sauren Magmatiten und Metamorphiten und finden sich in geringen Konzentrationen selbst in basischen Magmatiten, normalerweise jedoch nicht in Ultramafiten.
Zr4+ hat mit 0.84Å für Achterkoordination einen Ionenradius, der gut 15% geringer ist als
der von U4+ und gut 20% niedriger als der von Th4+. ZrSiO4 ist zudem isotyp mit USiO4 und
ThSiO4. U ist daher für die Zirkonstruktur noch halbwegs kompatibel, Th aber bereits weit
weniger; und daher haben Zirkone i.a. hohe U/Th-Verhältnisse und oft hohe U-Gehalte
von einigen 100ppm oder mehr. Pb dagegen ist erheblich zu groß für die Zirkonstruktur,
und folglich haben Zirkone bei ihrer Kristallisation sehr niedrige Pb-Gehalte und sehr hohe
U/Pb-Verhältnisse, was im Verlauf geologischer Zeiten zu sehr radiogenen Pb-Isotopenzusammensetzungen führt. Die Inkompatibilität des Pb macht den Zirkon dennoch nicht so
anfällig für Pb-Mobilität bei Metamorphosen, wie das im folgenden dargestellte Konzept
von Konkordia und Diskordia vermuten läßt.
Wenn man zwei Zerfallssysteme benutzt, z.B. 238U–206Pb – 235U–207Pb, dann läßt sich nicht
nur die Zeit eines –hypothetischen oder realen – Pb-Verlustes bestimmen, sondern auch
noch ein früheres Alter, vorausgesetzt, der Pb-Verlust war nicht total.
Mit Hilfe des von G. W. Wetherill 1956 eingeführten Konkordia-Diagramms[119] lassen sich
noch geologisch relevante Alter für Proben berechnen, die eine Zweistufenentwicklung
mitgemacht haben. Zur Ableitung des Konkordia-Diagramms löst man GL 104 und GL 105
nach (elt – 1) auf:
206
206
Pbradiogen
238
U
206
=
Pb - 206Pbinitial
=
238
U
204
Pb - 207Pbinitial
=
235
U
204
Pbradiogen
235
U
207
=
204
Pb ö
÷
Pb ø initial
238
U
204
Pb
207
207
206
Pb æ
-ç
Pb è
Pb æ
-ç
Pb è
207
204
Pb ö
÷
Pb ø initial
235
U
204
Pb
Trägt man GL 111 gegen GL 110 auf, indem man
(e
l238 t
)
= e l238 t - 1
[GL 110]
= e l235 t - 1
[GL 111]
(
)
- 1 und e l235 t - 1 berechnet,
dann erhält man eine Kurve, die sogenannte Konkordia, deren Krümmung auf den
unterschiedlichen Halbwertszeiten von 235U und 238U beruht. Proben mit einer Einstufen-
109
Die U,Th–Pb-Methoden
207
entwicklung haben
Pbradiogen
206
Pbradiogen
-Verhältnisse, die auf die Konkordia plotten,
238
U
U
von der man dann das Alter ablesen kann (siehe Abbildung 82):
235
–
Wie verhält es sich nun mit einem Zirkon, der lange nach seinem magmatischen Wachstum noch eine Metamorphose erleidet? Wie bereits erwähnt, ist Pb für die Zirkonstruktur
inkompatibel im Gegensatz zum Uran. Der Zirkon wird daher bei der Wiederaufheizung
einen Pb-Verlust erleiden können. Das ist in Abbildung 83 illustriert. Trägt man die Anzahl
der 206Pb-Atome gegen die Anzahl der 207Pb-Atome auf, dann möge Punkt A den Anfangspunkt vor Pb-Verlust repräsentieren.
0.8
3.5
Konkordia
3.0
2.5
0.4
2.0
206
Pbrad./238U
0.6
1.5
0.2
1.0
0.0
Die Zahlen auf der Konkordia
geben das Alter in Ga an.
0.0
0
5
10
15
20
25
30
207
Pbrad./235U
ABBILDUNG 82
Auf der Konkordia liegen die Pb-Isotopien aller Proben mit einer Einstufenentwicklung. Jedem Punkt auf der Konkordia entspricht exakt ein Alter, das
sich durch die aufgetragenen Exponentialfunktionen ergibt.
Da man wohl davon ausgehen kann, daß 206Pb und 207Pb nicht fraktionieren, wird durch
den Pb-Verlust das Verhältnis 206Pb/207Pb nicht geändert, d.h. der Pb-Verlust vollzieht sich
entlang der Geraden durch A und den Koordinatenursprung. Punkt B repräsentiert dann
eine Probe, die 1/4, Punkt C eine Probe, welche die Hälfte ihres Bleis verloren hat. Division
von 206Pb durch 238U und von 207Pb durch 235U (Dies sind die Achsen des Konkordia-Diagramms!) führt zu einer Ähnlichkeitstransformation der Abbildung (238U/235U = konstant
auf der Erde zu jeder gegebenen Zeit), d.h. die Gerade durch A, B und C geht in eine neue
Gerade durch A', B' und C' über. Das bedeutet, daß rezenter Bleiverlust (ohne Isotopenfraktionierung) im Konkordia-Diagramm entlang einer durch den Koordinatenursprung
gehenden Geraden in Richtung Ursprung verläuft.
110
A. Radiogene Isotopensysteme
206Pb
206Pb/238U
A'
A
B
B'
C'
C
207Pb
207Pb/235U
Pb-Verlust vollzieht sich entlang einer Geraden; die Pb/U-Verhältnisse fallen
in ähnlicher Weise auf eine transformierte Gerade.
ABBILDUNG 83
0.5
2.5
A
0.4
206Pb
238U
rad./
2.0
B
0.3
1.5
0.2
1.0
0.1
0.5
C
0.0
0
2
4
6
207Pb
ABBILDUNG 84
8
10
12
235U
rad./
Zur Zeit eines Pb-Verlustes liegen Proben mit unterschiedlichen Anteilen an
Pb-Verlust auf einer Diskordia, die durch den Ursprung des Koordinatensystems geht.
Das ist in der Abbildung 84 dargestellt. Punkt A repräsentiert darin eine Probe ohne Bleiverlust; Punkt B stellt eine Probe dar, die 1/3 ihres Bleis verloren hat und Punkt C eine
Probe, die ihr Blei vollständig verloren hat. Der obere Schnittpunkt der Geraden mit der
Konkordia – in diesem Fall identisch mit Punkt A – gibt das Alter des Systems an (in diesem
Beispiel 2.5 Ga), der untere Schnittpunkt – in diesem Fall identisch mit Punkt C – das Alter
111
Die U,Th–Pb-Methoden
des Bleiverlusts (hier: 0 Ga). Da alle potentiellen Proben auf der Geraden (mit Ausnahme
von A und C) diskordante Alter haben, nennt man die Gerade Diskordia. Im Normalfall
wird der Bleiverlust sicherlich nicht rezent stattfinden, sondern irgendwann in der geologischen Vergangenheit durch eine Metamorphose verursacht worden sein. Wandelt man
das obige Beispiel derart ab, daß das „Alter“ des Systems 3.5 Ga beträgt und der Bleiverlust
vor 1 Ga stattfand – als das System also 2.5 Ga alt war – dann werden in der letzten Milliarde Jahre die Verhältnisse 206Pbrad/238U und 207Pbrad/235U in allen Proben wieder angewachsen sein; die Proben A (kein Bleiverlust) und C (totaler Bleiverlust) bewegen sich dann
weiter entlang der Konkordia nach A' und C', Punkt B (ein Drittel Bleiverlust) auf einer
Kurve unterhalb der Konkordia nach B'. Die Daten aller dieser Proben liegen heute auf
einer Geraden, welche die Konkordia bei t=1 Ga und t=3.5 Ga schneidet, d.h. beide Alter
sind datierbar. Das ist schematisch in Abbildung 85 dargestellt. Aus diesem Diagramm läßt
sich der Anteil des radiogenen Bleis, der bei der Metamorphose zum Zeitpunkt t' nicht verloren gegangen ist, als das Verhältnis F der Strecken B,C/A,C berechnen, was identisch ist
mit dem Verhältnis der Strecken B'C'/A'C'. Der Bruchteil des bei der Metamorphose verloren gegangenen Bleis läßt sich entsprechend berechnen als das Verhältnis (1–F)= A,B/A,C
oder A'B'/A'C'.
0.8
3.5
A'
Konkordia
206Pb
238U
rad./
0.6
rdia
3.0
ko
Kon
2.5
B'
A
ia
ord
k
Dis
0.4
2.0
B
1.5
0.2
1.0
Die Zahlen auf der Konkordia
geben das Alter in Ga an.
C'
0.5
C
0.0
0
5
10
15
207
ABBILDUNG 85
20
25
30
Pbrad./235U
Wenn das Ereignisses des Pb-Verlustes geologische Zeit zurückliegt, liegen
die betroffenen Proben auf einer neuen Diskordia, deren unterer Schnittpunkt mit der Konkordia das Alter des Pb-Verlustes angibt.
Im folgenden soll eine mathematische Betrachtung der Diskordia-Entwicklung durchgeführt werden in Anlehnung an die obigen Beispiele, d.h. „Alter“ des Systems t=3.5 Ga, Bleiverlust vor t'=1 Ga, t"=heute, Probe A kein Bleiverlust, Probe B = 1/3 Bleiverlust, Probe C totaler Bleiverlust. Mit f werde das Verhältnis (Atome Pb nach Verlust/Atome Pb vor Verlust)
bezeichnet. Der Bleiverlust möge sich innerhalb einer geologisch vernachlässigbar kurzen
Zeitspanne DtM vollziehen. Betrachten wir die Isotopenentwicklung zum Zeitpunkt t',
unmittelbar vor dem Bleiverlust. Dann ist:
112
A. Radiogene Isotopensysteme
206
(v = vorher)
207
Pbv =
[
238
Pbv =
Uv ´ e
[
235
Uv ´ e
l238 (t -t ' )
]
-1
[GL 112]
]
l235 (t -t ' )
-1
[GL 113]
Unmittelbar nach dem Bleiverlust ergibt sich (n = nachher):
206
Pbn = f ´ 206Pbv
[GL 114]
207
Pbn = f ´ 207Pbv
[GL 115]
In der letzten Milliarde Jahre sind an radiogenem Blei neu hinzugekommen (h = heute):
[
U [e
206
Pbn -h =
238
207
Pbn -h =
235
Uh e
h
]
) -1
]
l238 (t ' -t ")
l235 (t ' -t "
-1
[GL 116]
[GL 117]
Die heute in den Proben vorhandenen Mengen an Pb ergeben sich aus der Summierung
von GL 114 und GL 116 bzw. GL 115 und GL 117:
206
206
Pbn +
[
´ [e
206
Pbn -h = f ´ 206Pbv +
]
) -1 +
]
Pbh = f ´ 238U v ´ e
l238 (t -t ' )
Pbh = f ´ 235U v
l235 (t -t '
206
207
Pbh =
-1 +
[
U [e
238
Uh e
235
h
206
Pbn -h
]
) -1
]
l238 (t ' -t ")
l235 (t ' -t "
-1
[GL 118]
[GL 119]
Da man bei diesem Modell davon ausgeht, daß während der Phase des Bleiverlustes das U
immobil bleibt, läßt sich Uv berechnen zu:
l t ' -t ''
U v = Uh ´ e ( )
[GL 120]
Damit wird GL 118:
206
Pbh = f ´ 238U h ´ e
206
206
Pbh =
Pbh =
206
æ
ç
è
{
238
Uh f ´ e
{ [
238
Uh f ´ e
Pbh =
206
l238 (t ' -t '' )
238
[
´ e
l238 (t ' -t '' )
l238 (t -t ' )
[
´ e
[
l238 (t ' -t '' ) + (t -t ' )
{ [
Uh f ´ e
l238 (t -t '' )
]
-1 +
l238 (t -t ' )
[
238
Uh e
][
-1 + e
l238 (t ' -t ")
l238 (t ' -t ")
]}
-1
}
] - e l238 (t '-t '') ] + [e l238 (t '-t ") - 1]
-e
l238 (t ' -t '' )
] + [e l
238
]}
(t ' - t " ) - 1
Pb ö
l238 (t -t '' )
l
l
t ' -t ''
t ' -t "
- e 238 ( ) + e 238 ( ) - 1
÷ =f ´ e
U øh
[
238
æ
und analog: ç
è
207
][
]
[GL 121]
Pb ö
l235 (t -t '' )
l
l
t ' -t ''
t ' -t "
- e 235 ( ) + e 235 ( ) - 1
÷ =f ´ e
U øh
235
[
]
-1
][
]
[GL 122]
Für das konkrete Beispiel gilt also:
113
Die U,Th–Pb-Methoden
æ
ç
è
206
Pb ö
1Ga
1Ga
l238 (3.5Ga)
l
l
- e 238 ( ) + e 238 ( ) - 1
÷ =f ´ e
U øh
[
238
][
[und analog für
æ
ç
è
207
]
Pb ö
÷ ]
U øh
235
Mit Hilfe der Gleichungen GL 121 und GL 122 läßt sich also die heutige Lage der Datenpunkte im Konkordia-/Diskordia-Diagramm berechnen, was für die Punkte A', B' und C'
nun geschehen soll:
1.
Probe A, die kein Pb verloren hat und sich entlang der Konkordia nach A' in der letzten
Milliarde Jahre entwickelt hat:
f=1Þ
æ
ç
è
206
æ
ç
è
206
Pb ö
l238 (t -t '' )
l
l
t ' -t ''
t ' -t "
- e 238 ( ) + e 238 ( ) - 1
÷ =e
U øh
238
Pb ö
l238 (t -t '' )
- 1 = e l238 t - 1 (da t " = 0 )
÷ =e
U øh
238
æ
und analog: ç
è
2.
Pb ö
l235 (t -t '' )
- 1 = e l235 t - 1
÷ =e
U øh
235
Probe C, die einen vollständigen Pb-Verlust erlitten hat und sich entlang der Konkordia von C nach C' in den vergangenen 109a entwickelt hat:
f=0Þ
æ
ç
è
206
Pb ö
l238 (t ' -t ")
- 1 = e l238 t ' - 1 (da t " = 0 )
÷ =e
U øh
238
æ
ç
è
3.
207
207
Pb ö
l235 (t ' -t ")
- 1 = e l235 t ' - 1
÷ =e
U øh
235
Probe B, die 1/3 ihres Bleis verloren hat und sich in den vergangenen 109a nach B' entwickelt hat:
Man löst GL 122 nach f auf:
f =
æ
ç
è
207
Pb ö
l235 (t ' -t ")
-1
÷ - e
U øh
l
l
t -t ''
t ' -t ''
e 235 ( ) - e 235 ( )
[
235
]
setzt in GL 121 ein:
æ
ç
è
æ
ç
è
114
206
Pb ö
÷ =
238
U øh
æ
ç
è
207
206
Pb ö
÷ =
238
U øh
æ
ç
è
207
Pb ö
l235 (t ' -t ")
-1
÷ - e
U øh
l
l
l
t -t ''
t ' -t ''
t ' -t "
´ e 238 ( ) - e 238 ( ) + e 238 ( ) - 1
l235 (t -t '' )
l235 (t ' -t '' )
e
-e
235
[
]
[
][
]
Pb ö
l238 (t -t '' )
l
l
l
l
t ' -t ''
t ' -t "
t -t ''
t ' -t ''
- e 238 ( ) - e 235 ( ) - 1 ´ e 238 ( ) - e 238 ( )
÷ ´ e
U øh
l
-t"
t '+ e 238 ( ) - 1
l235 (t -t '' )
l235 (t ' -t '' )
e
-e
235
[
][
][
]
[
]
A. Radiogene Isotopensysteme
æ
ç
è
206
æ
Pb ö
÷ =ç
238
U øh è
[
][
][
l
l
l
t ' -t "
t -t ''
t ' -t ''
l
l
t -t ''
t ' -t ''
e 235 ( ) - 1 ´ e 238 ( ) - e 238 ( )
Pb ö
e 238 ( ) - e 238 ( )
l
t ' -t "
+ e 238 ( ) - 1
÷ ´
235
l
t -t ''
l
t ' -t ''
U ø h e l235 (t -t '') - e l235 (t ' -t '')
e 235 ( ) - e 235 ( )
207
]
bzw. wegen t" = 0:
æ
ç
è
206
æ
Pb ö
÷ =ç
238
U øh è
(
) (
) (
e l235 t ' - 1 ´ e l238 t - e l238 t '
Pb ö
e l238 t - e l238 t '
´
+ e l238 t ' - 1
÷
235
U ø h e l235 t - e l235 t '
e l235 t - e l235 t '
207
)
[GL 123]
Für festes t und t' ist dies aber wieder die Gleichung einer Geraden der Form:
æ
ç
è
206
æ
Pb ö
÷ =ç
238
U øh è
207
Pb ö
÷ ´m+b
U øh
235
D.h. verschiedene Proben mit variablen Bleiverlusten zur selben Zeit t' liegen heute
auf einer Geraden im Konkordia-/Diskordia-Diagramm. Da die heutigen Pb/U-Verhältnisse meßbar sind, bleiben t und t' als einzige Unbekannte in GL 123. Man benötigt
daher mindestens 2 Proben, um diese beiden Schnittpunktsalter zu ermitteln. Diese
Ableitung gilt auch, wenn nicht nur Blei, sondern auch Uran mobil ist. Definiert man
g als das Verhältnis der Uranatome nach zu vor dem (metamorphen) Ereignis, dann ist
Un = g ´ Uv
l t ' -t ''
U n g = Uh ´ e ( ) g
Damit wird GL 120:
und folglich GL 121:
æ
ç
è
206
Pb ö
f
l238 (t -t '' )
l
l
t ' -t ''
t ' -t "
- e 238 ( ) + e 238 ( ) - 1
÷ =g´ e
U øh
238
[
][
]
Durch Auflösen der analogen Gleichung für 207Pb/235U nach f/g und Einsetzen in die
obige Gleichung läßt sich dann wieder zeigen, daß bei Auftragung von 207Pb/235U gegen 206Pb/238U eine Gerade resultiert.
Die Bedingung, daß eine Probenserie bei einer Metamorphose z.T. ihr Pb vollständig
behält, z.T. vollständig verliert, ist in der Praxis sicherlich eher die Ausnahme denn die
Regel. Glücklicherweise erfahren Zirkone aus demselben Gestein und unter den gleichen
p,T-Bedingungen jedoch (scheinbar) variable Pb-Verluste, so daß die Konstruktion der Diskordia und damit die Berechnung sowohl des Metamorphose- als auch des magmatischen
Alters ermöglicht wird. In dem (seltenen) Fall, daß die Zirkone ihr Pb bei der Metamorphose vollständig verlieren, wäre jede Erinnerung an das magmatische Alter ausgelöscht.
Das Ausmaß des Pb-Verlustes scheint von solchen Faktoren wie Korngröße, U-Gehalt oder
Anzahl der Gitterstörungen infolge der radioaktiven Strahlung abzuhängen. Je höher der
Gehalt an radioaktiven Elementen und je älter der Zirkon, desto stärker wird das Gitter
gestört; aus derart gestörten Bereichen geht das Uran dem Zirkon bevorzugt verloren. Es sei
daran erinnert, daß Diffusion allein kein effektiver Mechanismus ist, um Ionen aus einem
Kristall an die Kornoberfläche zu transportieren, solange sie nicht von Rekristallisation
begleitet wird (Seite 33 und folgende).
Mittels des Konkordia-/Diskordia-Diagramms kann nicht unterschieden werden zwischen
Pb-Verlust und U-Gewinn. Beides würde zu einer Erniedrigung des Pbrad/U-Verhältnisses
führen. Da Pb in den Zirkonen jedoch wesentlich inkompatibler ist als U, wird man davon
ausgehen dürfen, daß die Vorstellung eines bevorzugten Pb-Verlustes korrekt ist. Manchmal fallen Mineraldaten auch über die Konkordia. Das kann bei Monazit passieren, obwohl
dieses Mineral in der Regel wenig diskordant ist oder unter die Konkordia fällt (z.B. [27],
[121]). Solch außergewöhnliches Verhalten kann dadurch erklärt werden, daß Th für
Monazit wesentlich kompatibler ist als U (Th-Gehalte von Monazit sind leicht eine Größenordnung höher als die U-Gehalte). Dann wird der Monazit bei seinem Wachstum das
115
Die U,Th–Pb-Methoden
aus dem 238U-Zerfall stammende 230Th (sofern es z.B. in einer zirkulierenden fluiden Phase
zur Verfügung steht) erheblich bevorzugt über den das säkulare Gleichgewicht der 238UZerfallskette repräsentierenden Anteil einbauen. Als Folge erwirbt der Monazit einen höheren Gehalt an 206Pb, als es seinem U-Gehalt entspricht (R. Romer, persönliche Mitteilung,
2001). Im radioaktiven Gleichgewicht ergibt sich 230Th/238U aus dem Verhältnis der beiden
Zerfallskonstanten zu 1.68´10-5. Dieser Effekt wird daher nur bei geologisch jungen Monaziten ausgeprägt sein können, bei denen das gesamte überschüssige 230Th (Halbwertszeit
ca. 7.52´104a) bereits in 206Pb zerfallen ist, während der Zerfall von 238U noch keine großen
Mengen an radiogenem Pb nachgeliefert hat.
Konkordias lassen sich im Prinzip auch mit den Verhältnissen 206Pbrad/238U – 208Pbrad/232Th
bzw. 207Pbrad/235U – 208Pbrad/232Th darstellen. Im ersten Fall hätte die Konkordia jedoch eine
geringere Krümmung als im gewöhnlichen Diagramm, weil sich die Halbwertszeiten von
238
U und 232Th weniger unterscheiden als die von 235U und 238U; im zweiten Fall wäre die
Krümmung sogar größer. Der Nachteil bei dieser Art von Auftragung ergibt sich jedoch daraus, daß mit U und Th zwei Elemente beteiligt sind, die sich in den Mineralstrukturen
nicht gegenseitig vollständig ersetzen können und evtl. sogar verschiedene Gitterpositionen einnehmen, so daß nicht angenommen werden kann, daß sie sich bei Metamorphosen gleich mobil oder immobil verhalten.
Ein größeres Problem bei der Bestimmung der Diskordia-Alter von Zirkonen insbesondere
aus Metamorphiten ergibt sich ausgerechnet daraus, daß Zirkone extrem resistente Minerale gegenüber der Verwitterung sind. Es ist intuitiv einsichtig, daß Sedimente Zirkonpopulationen enthalten werden, die aus dem gesamten Liefergebiet stammen und daher
natürlich ganz unterschiedliche Entstehungsalter haben können. Bei der Gesteinsmetamorphose werden diese Zirkone weiterwachsen; außerdem werden sich unter Umständen
neue Zirkone bilden. Auf Grund der Morphologie (Tracht und Habitus) und der inneren
Struktur (Anwachssäume, Zonierungen) lassen sich oft die verschiedenen Zirkontypen aus
Metamorphiten unterscheiden. Zonierungen sind gut mit der Methode der Kathodolumineszenz* erkennbar. Fraglich ist allerdings, ob man in Körnerseparaten, die aufgelöst
und analysiert werden, die verschiedenen Generationen von Zirkonen strikt auseinanderhalten kann. Während der untere Schnittpunkt zwischen Konkordia und Diskordia von
Zirkonen aus solchen Metamorphiten auch dann mit dem Metamorphosealter in der Regel
ein geologisches Ereignis datieren wird, stellt der obere Schnittpunkt in solchen Fällen ein
bloßes Mischalter dar.
Diese Schwierigkeiten versucht man, durch Analyse einzelner Zirkonkörner zu umgehen.
Es ist aus vielen derartigen Analysen klar geworden, daß die verschiedenen Domänen
zonierter Zirkone (siehe z.B. [122]) und auch zonierter Monazite (z.B. [27]) scharfen Alterssprüngen entsprechen, was die Notwendigkeit unterstreicht, Punktanalysen einzelner Körner zu machen. Die neuen Daten zeigen zudem, daß Zirkone und andere Minerale seltener
in hohem Maß diskordant sind, als aus der Analyse von Körnerseparaten abgeleitet; der diskordante Charakter solcher Separate ergibt sich vielmehr aus der Gesamtanalyse zonierter
Minerale und/oder von Mineralen, die verschiedenen Ursprungs sind. Stark diskordante
Zirkone sind allerdings auch bekannt, überraschenderweise sogar aus niedrigst-metamorphen Gesteinen[123]. In dem zitierten Beispiel wurde ihr Pb-Verlust bei Temperaturen von
nur 150 bis 200 °C der Zirkulation von stark salzhaltigen Lösungen zugeschrieben, durch
welche das Pb aus den metamikten† Zonen der Zirkone herausgelöst wurde.
* Dabei wird die Probe (polierter Dünnschliff) durch Elektronenbestrahlung zum Leuchten angeregt.
Die Lumineszenz ist abhängig von Materialeigenschaften wie Chemismus, Kristallbau und Kristallbaufehlern.
† Zirkone und einige andere Minerale, die U und Th in größeren Mengen einbauen können, erfahren
abhängig von der Konzentration der radioaktiven Elemente und ihrem Alter eine teilweise bis vollständige Zerstörung des Kristallgitters; dabei erwirbt der Zirkon eine ausgeprägte dunkle Farbe. Solche metamikten Zirkone sind viel leichter im Labor aufzulösen als farblose Zirkone.
116
A. Radiogene Isotopensysteme
Nach einer – nicht idealen, aber keinen zusätzlichen hohen apparativen Aufwand erfordernden – Methode der Einzelkornanalyse werden die Körner in ein Bändchen eines Doppelfilamentes eingewickelt[120]. Bei der sukzessiven Ausheizung dampft zunächst das am
lockersten gebundene (vielleicht von den Kornrändern und Störzonen) Blei ab, zum
Schluß das am stärksten gebundene Blei. Ähnlich wie bei der Ar–Ar-Methode erhält man
idealerweise ein Altersplateau, das dem „wahren“ Alter des Zirkons entsprechen wird. Ein
erheblicher Nachteil des Verfahrens ist, daß man keine Informationen über die U- und ThGehalte des Zirkons und damit die U,Th/Pb-Verhältnisse erhält; die Altersinformation
resultiert dann aus 207Pb/206Pb-Verhältnissen.
Quadrupollinse
Magnetanalysator
Austrittsspalt
Energieanalysator
Primärionenmassenspektrometer
Duoplasmatron
(Primärionenquelle)
Blende
Hohl- O2-Gas
kathode
sekundärer Ionenstrahl
Faraday-Becher
„Source“-Schlitz
Extraktionslinsen für
Sekundärionen
S
optisches Mikroskop
ABBILDUNG 86
elektrostatische
Kondensorlinse
primärer
Ionenstrahl
elektrostatische
Objektivlinse
Probe
Funktionsprinzip einer Ionensonde
Ein wesentlich eleganteres, aber auch viel kostspieligeres Verfahren ist die Verwendung
einer Ionensonde, die zur Gruppe der Sekundärionen-Massenspektrometer gehört. Die vorstehende Skizze zeigt den schematischen Aufbau eines solchen Großgerätes[124]. Dabei wird
die Probe mit einem Strahl möglichst monoisotopischer Ionen (z.B. 16O–) beschossen. Die
Ionen werden in einem „Duoplasmatron“ erzeugt, einem Gerät, in welches das Gas bei
niedrigem Druck (z.B. 0.1 Torr) in eine Hohlkathode eingelassen wird. In der Hohlkathode
wird eine Bogenentladung erzeugt, die das Gas ionisiert. Die Ionen werden auf »15 – 30kV
beschleunigt und in ein Massenspektrometer mit niedriger Auflösung geführt, um den
monoisotopischen Ionenstrahl zu separieren. Die Probe wird mit Strahlströmen von typischerweise einigen 10nA beschossen (Strahldurchmesser einige µm). Dabei wird ein kleiner
Teil der Probe verdampft, und es entsteht lokal ein Plasma aus einer Vielzahl von Ionen,
Moleküloxiden und Molekülionen. Die gewünschte Spezies wird in einem hoch auflösenden doppelfokussierenden Massenspektrometer (Kombination aus elektrischem und
magnetischem Sektorfeld) ausgeblendet und registriert. Bei der Analyse von Zirkonen
ergibt sich eine Vielzahl von Masseninterferenzen (z.B. 94,96Zr2O, 176HfO2, Zr2Si, 176Hf28Si).
so beträgt z.B. die Masse von 176HfO2 175.9417 + 2´15.9949 = 207.9315; demgegenüber
liegt die Masse von 208Pb bei 207.9766. Daher sind extrem hohe Auflösungen des Massenspektrometers erforderlich, um die Pb-Isotope exakt zu messen. Derzeit sind vor allen Dingen die Ionensonde SHRIMP* und ihre Nachfolgemodelle leistungsfähig genug dazu. Die
SHRIMP wurde an der Australian National University gebaut und betrieben[125], typischerweise mit einer Massenauflösung M/DM von 6500 (M = Masse, DM = Breite des Massenpeaks
* Sensitive High-Resolution Ion MicroProbe
117
Die U,Th–Pb-Methoden
des Ions bei ca. 10% der Höhe). Abbildung 87 zeigt die kommerziell vertriebene SHRIMP II.
Die Laserablation entwickelt sich derzeit allerdings rasch zu einem vergleichbar leistungsfähigen Gerät, das den Ionensonden für die U–Pb-Datierung erhebliche Konkurrenz
macht. Dabei wird ein kleines Volumen der Probe durch Beschuß mit einem Laserstrahl
(Durchmesser einige 10 µm, das ist größer als bei der Ionensonde) verdampft und in die
Plasmafackel eines ICP-Massenspektrometers geleitet[126].
Die Ionensonde SHRIMP der Australian National University eignet sich zur
Analyse der Pb-Isotopenzusammensetzung von Zirkonen. Mit ihrer Hilfe und
den nachfolgenden Geräten wurden wichtige Beiträge zur Geochronologie
vor allem des Archaikums geleistet.
ABBILDUNG 87
Zur Datierung von Th- oder U-reichen Mineralen, die bei ihrer Kristallisation keine nennenswerten Mengen an Pb aufnehmen, genügt im Prinzip bereits die Bestimmung der Konzentrationen von U, Th und Pb. Gute Erfahrungen wurden mit Monazit gesammelt, der
sich mit der Elektronenstrahlmikrosonde bequem analysieren läßt[127],[128],[129]. Monazit
enthält typischweise einige Prozent Th bei einem höheren Verhältnis von Th/U als das
Gestein, in dem er kristallisiert ist. In polymetamorphen Gesteinen lassen sich damit Informationen über die Phasen des Wachstums dieses Minerals machen. Die Präzision der
Daten erreicht zwar nicht diejenige der Isotopenmethoden, ist aber für Übersichtsaufnahmen ausreichend. Ein Vorteil der Mikrosondenanalytik besteht – neben der weiten Verfügbarkeit der Geräte – in der hohen Ortsauflösung (1–2 µm Durchmesser des Elektronenstrahls), die eine detaillierte Kartierung einzelner Körner ermöglicht, und auch in der
Schnelligkeit. Monazite aus polymetamorphen Gesteinen erweisen sich oft als chemisch
und hinsichtlich ihres Alters zoniert[129],[130], wobei die Zonierung außerordentlich komplex und folglich schwer zu deuten sein kann (Abbildung 88). Monazit ist ein in Gneisen
und Glimmerschiefern sowie in Granitoiden weit verbreitetes akzessorisches Mineral, so
daß die Methode prinzipiell eine breite Anwendung finden könnte. Einschränkend ist
jedoch zu bemerken, daß man mit der Elektronenstrahlmikrosonde keinerlei Möglichkeit
hat zu verifizieren, daß das Mineral bei seiner Bildung tatsächlich kein Pb enthalten hat.
Das Alter erhält man durch iteratives Lösen der kombinierten Zerfallsgleichungen von Th
und U:
Pbtotal »
208
Pbrad + 207Pbrad + 206Pbrad =
(
)
Th e l232 t - 1 +
232
(
)
U e l235 t - 1 +
235
(
)
U e l238 t - 1
238
[GL 124]
Dazu sind die Th-, U- und Pb-Gehalte (Gewichtsprozent) aus der Mikrosondenanalyse in
atomare Anteile umzurechnen. Dabei ist zu berücksichtigen, daß das Atomgewichtes von
Pb eine Funktion der Th- und U-Gehalte sowie des Alters der Probe ist. Bei der iterativen
Lösung von GL 124 erhält man jedoch rasch eine beliebig gute Übereinstimmung zwischen
vorgegebenem Alter (mit dessen Hilfe das Atomgewicht berechnet wird) und iterativ ermitteltem Alter. Eine gleichwertige, von Kenntnis des Atomgewichts von Pb unabhängige For118
A. Radiogene Isotopensysteme
mulierung erhält man[128], wenn man bedenkt, daß sich die einzelnen atomaren Anteile
des Pb berechnen lassen zu
2726622 Ma
(n = 34)
2032618 Ma
(n = 98)
2023627 Ma
(n = 26)
<1965 Ma
1966–2119 Ma
2120–2622 Ma
2715626 Ma
(n = 22)
2623–2759 Ma
>2760 Ma
ABBILDUNG 88 Th–U–Pb-Alter in einem Monazitkorn (großer Durchmesser ca.
0.45 mm) aus einem migmatischen Gneis von der Elfenbeinküste[129]. Jeder
Punkt entspricht einer Mikrosondenanalyse. Das Korn ist offensichtlich alters–
zoniert, wobei die Kerne höhere Alter haben als die Ränder.
206
Pbrad =
[
206
Pb
A206
] ( A = Atomgewicht)
usw. (Konzentrationen in eckigen Klammern). Der atomare Anteil an
dem U-Gehalt und der Isotopenhäufigkeit von 238U (f238) zu
238
U = f238 ´ U = f238 ´
Damit läßt sich z.B. der Term für
206
238
U ergibt sich aus
[U ]
AU
206
Pbrad =
Pb in GL 124 umschreiben als
[
206
Pb
A206
]=f
238
´
[U ] ´
AU
(e
l 238 t
)
-1
und GL 124 wird zu
[Pbtotal ] » [ 208 Pbrad ] + [ 207 Pbrad ] + [ 206 Pbrad ]
=
A208 ´ [Th ] l 232 t
A ´ [U ] l 235 t
A ´ [U ] l 238 t
e
- 1 + f235 ´ 207
e
- 1 + f238 ´ 206
e
-1
ATh
AU
AU
(
)
(
)
(
)
[GL 125]
119
Die U,Th–Pb-Methoden
12.2
Die Pb–Pb-Methoden („gewöhnliches Blei“ oder „common lead“)
Die bisherigen Methoden beschäftigten sich mit der U,Th–Pb-Datierung von Proben mit
hohem U/Pb-Verhältnis, d.h. Proben mit sehr radiogener Pb-Isotopenzusammensetzung.
Es lassen sich jedoch auch Altersinformationen aus Proben mit U/Pb»0 gewinnen, vor
allem Pb-haltigen Sulfiden. In derartigen Proben ist die Pb-Isotopie „eingefroren“, und die
Alter haben lediglich den Charakter von – zuweilen geologisch sinnvollen – Modellaltern.
Die Pb-Isotopenzusammensetzung von magmatischen und metamorphen Gesteinen kann
zudem als geochemischer Tracer nützlich sein.
Bereits A.O. Nier berichtete 1938, daß das Atomgewicht des Pb aus Bleiglanzen verschiedener Herkunft verschiedene Isotopenzusammensetzungen hat[131]. 1941 schlugen Nier, R.W.
Thompson & B.F. Murphey vor, daß die Ursache dieser Isotopenvariationen darin liegt, daß
das Pb in den Bleiglanzen eine Mischung aus „Urblei“ darstellt, wie es bei der Kondensation der Erde vorlag, und radiogenem Blei[132]. Dieser Vorschlag hat sich als sehr fruchtbar
erwiesen und führte unmittelbar zu Versuchen, über die Pb-Isotopenzusammensetzung das
Alter der Meteorite und der Erde zu ermitteln. Der mathematische Formalismus ist als Holmes-Houtermans-Modell bekannt, das unabhängig voneinander von A. Holmes*[133] und
F.G. Houtermans[134] 1946 formuliert wurde. Das Holmes-Houtermans-Modell basiert auf
der Voraussetzung, daß die Erde bei ihrer Bildung homogen zusammengesetzt war, d.h. U,
Th und Pb hatten überall die gleichen Häufigkeiten, und die Pb-Isotopenzusammensetzung war überall gleich. Anschließend änderten sich die Verhältnisse Pb/U und Pb/Th
durch Differentiationsprozesse innerhalb kurzer Zeit, so daß sich mehrere Reservoire ausbildeten. In diesen aber änderten sich diese Verhältnisse nur noch infolge des radioaktiven
Zerfalls, nicht aber durch weitere Fraktionierungen in neue Reservoirs. Schließlich wurden
bei Erzbildungsprozessen Pb einerseits und U–Th andererseits vollständig voneinander
getrennt, und die Pb-Isotopie hat sich in den Pb-Mineralen seitdem nicht mehr geändert.
Diese Voraussetzungen scheinen für die Erde nicht sehr realistisch gewählt zu sein. Dennoch hat das Holmes-Houtermans-Modell in den 1950-er und 1960-er Jahren weite
Anwendung gefunden. Bezeichnet man das Alter der Erde mit t0, dann ergibt sich die
bekannte Zerfallsgleichung in der Formulierung für die Evolutionskurve der Erde:
æ
ç
è
206
204
æ
Pb ö
=ç
÷
Pb ø heute è
206
204
æ
Pb ö
+ç
÷
Pb ø initial è
238
204
U ö
e l238 t0 - 1
÷
Pb ø heute
(
)
[GL 126]
æ 206 Pb ö
æ 238U ö
wobei ç 204 ÷
die Isotopie des Urbleis ist und ç 204 ÷
das Verhältnis in der Erde.
Pb ø initial
Pb ø heute
è
è
Wenn in einem solchen Reservoir in der Erde zur Zeit t durch einen Erzbildungsprozeß Pb
vollständig von U und Th getrennt wird, dann hat sich in diesem Pb-Mineral die Pb-Isotopie seit der Zeit t nicht mehr geändert, und von obiger Gleichung muß der Anteil
206
æ 238U ö
Pb
l238 t
e
1
subtrahiert
werden,
der
dem
Anteil
entspricht, der von t bis
ç 204 ÷
204
Pb ø heute
Pb
è
heute entstanden wäre, wenn die Trennung von Pb und U+Th nicht stattgefunden hätte:
(
æ
ç
è
)
206
æ
Pb ö
÷ =ç
204
Pb ø t è
æ
ç
è
206
204
206
æ
Pb ö
+ç
÷
204
Pb ø initial è
æ
Pb ö
÷ =ç
Pb ø t è
206
204
238
æ
U ö
e l238 t0 - 1 - ç
÷
204
Pb ø heute
è
æ
Pb ö
+ç
÷
Pb ø initial è
(
238
204
)
238
204
U ö
e l238 t - 1
÷
Pb ø heute
U ö
e l238 t0 - e l238 t
÷
Pb ø heute
(
(
)
)
[GL 127]
* englischer Geologe (1890–1965) in Durham und Edinburgh; Holmes schlug auch Konvektionsströmungen in der tiefen Erde als Ursache von A. Wegeners Kontinentverschiebungen vor.
120
A. Radiogene Isotopensysteme
GL 126 ist lediglich ein Spezialfall dieser Gleichung, wenn die Separation des Bleis „heute“
(t = 0) stattgefunden hat.
Analoge Gleichungen können für 207 Pb 204 Pb und 208 Pb 204 Pb formuliert werden. Für
die Isotopenverhältnisse und die heutigen Elementverhältnisse werden früher die folgenden – im Zeitalter des Computers weitgehend verschwundenen – Abkürzungen benutzt:
æ
ç
è
„Urblei“:
206
204
Pb ö
= a 0 (oder a0 )
÷
Pb ø initial
æ
ç
è
æ
ç
è
207
204
Pb ö
= b 0 (oder b0 )
÷
Pb ø initial
208
204
æ
ç
è
Verhältnisse zur Zeit t:
Pb ö
= g 0 (oder c0 )
÷
Pb ø initial
20¢6
204
207
æ
ç
è
204
æ
ç
è
Pb ö
÷ = a (oder a )
Pb ø t
Pb ö
÷ = b (oder b )
Pb ø t
208
204
Pb ö
÷ = g (oder c )
Pb ø t
heutige Verhältnisse:
æ
ç
è
238
204
U ö
=m
÷
Pb ø heute
æ
ç
è
232
Th ö
=w
÷
Pb ø heute
æ
ç
è
204
232
Th ö
=k
÷
U ø heute
238
Damit lassen sich die Gleichungen schreiben als:
(
a t = a 0 + m e l238 t0 - e l238 t
bt = b 0 +
(
)
m
e l235 t0 - e l235 t
137.88
(
)
[GL 128]
)
(
g t = g 0 + w e l232 t0 - e l232 t = g 0 + mk e l232 t0 - e l232 t
[GL 129]
)
[GL 130]
Die Werte a0, b0 und g0 („Urblei“) wurden aus der Analyse von Troilit (FeS) aus dem Eisenmeteoriten Canyon Diablo ermittelt[135]. Troilit ist praktisch U- und Th-frei, enthält jedoch
etwas Pb, dessen Isotopenzusammensetzung praktisch eingefroren ist. Als beste Initialwerte für das Sonnensystem zur Zeit seiner Bildung gelten heute[136]:
a0 = 9.3066
b0 = 10.293
g0 = 29.475.
Der µ-Wert läßt sich durch die Kombination von GL 128 und GL 129 eliminieren:
(
(
e l235 t0 - e l235 t
bt - b 0
1
=
a t - a 0 137.88 e l238 t0 - e l238 t
)
)
[GL 131]
121
Die U,Th–Pb-Methoden
40
35
Das Alter der Meteorite
(C. Patterson, 1956)
Nuevo Laredo
30
a)
5G
.0
60
.55
25
do
(t
=4
hr
oc
Ge
c
20
e
on
Mo
207Pb/204Pb
Für t=0, d.h. rezente Trennung von
Pb und U, ist dies vergleichbar mit
GL 107 (in der t0 durch t ersetzt war),
und in jener Form wurde sie von C.
Patterson zur Ermittlung des Alters
der Meteorite benutzt durch Analyse
von 3 Stein- und 2 Eisenmeteoriten [137] (siehe Abbildung 89). Die
Gleichung läßt sich dann umschreiben zu
Meeressediment
bt = m a t - m a 0 + b0
= m at + C
15
[GL 132]
10
Dies ist die Gleichung einer Geraden
in den Koordinaten at und bt; aus
ihrer Steigung
(
(
e l235 t0 - e l235 t
1
m=
137.88 e l238 t0 - e l238 t
)
)
Forest City
Canyon
Diablo
Henbury
10
15
20
25
30
35
206Pb/204Pb
40
45
50
ABBILDUNG 89 Der 1995 verstorbene C. Patterson be-
stimmte das Alter der Meteorite und, in Analogie, das
Alter der Erde.
18
Holmes-Houtermans-Modell
für verschiedene m-Werte
m=10
16
m=9
m=7
m=6
14
m=5
207
Pb/204Pb
m=8
e
n
ro
ch
o
Ge
12
Die Punkte auf den Kurven für die
verschiedenen m-Werte geben die
berechnenten Isotopenverhältnisse
in Abständen von jeweils 0.5Ga an.
Urblei
10
8
10
12
14
16
18
20
206
Pb/204Pb
ABBILDUNG 90
122
Die Pb-Isotopenentwicklung der Erde nach dem Modell von Holmes und
Houtermans für verschiedene Verhältnisse von U/Pb. Die Pb-Isotopenzusammensetzung von Lagerstätten darf nach diesem Modell nicht rechts
der Geochronen liegen. Auf der Geochronen läge Pb, das heute vom U abgetrennt wurde.
A. Radiogene Isotopensysteme
läßt sich dann das Alter errechnen, und C ist eine Konstante. Patterson erhielt dabei ein
Alter von 4.55±0.05 Ga, das bis heute Gültigkeit hat und durch andere Methoden bestätigt
wurde. Patterson vermutete außerdem, daß die Erde dasselbe Alter hat wie die Meteorite.
Um diese Hypothese zu testen, analysierte er die Pb-Isotopenzusammensetzung einer
Probe eines rezenten ozeanischen Sediments, von dem er annahm, daß es einen halbwegs
repräsentativen Durchschnitt für terrestrisches Blei darstellt. Er fand, daß es ebenfalls auf
die Isochrone der Meteorite fällt und sah dadurch seine Hypothese bestätigt. Obwohl auch
diese Meinung heute nicht mehr bezweifelt wird, hatte Patterson mit seiner Wahl des Sedimentes jedoch auch einiges Glück, denn längst nicht alle ozeanischen Sedimente haben
ein Modellalter von »4.55 Ga. Diese Gerade heißt Geochrone, weil alle terrestrischen und
Meteoritenproben mit t=0, deren Pb-Isotopie sich durch ein Einstufenmodell beschreiben
läßt, auf diese Isochrone plotten. Je höher das U/Pb-Verhältnis einer Probe, desto radiogener sind natürlich ihre 206Pb/204Pb- und 207Pb/204Pb-Verhältnisse.
Die Gleichungen GL 128 und GL 129 können benutzt werden, um 206Pb/204Pb und 207Pb/
Pb bei gegebenem U/Pb-Verhältnis für beliebige Zeit t der Trennung einer Pb-Probe von
U zu berechnen. Abbildung 90 zeigt dies an Hand der fest gewählten Werte µ = 5 – 10; die
meisten terrestrischen Einstufenbleie liegen zwischen den Kurven für µ = 8 und µ = 10. Es
ergeben sich Kurven, die vom Punkt (a0, b0) des Urbleis ausgehen. Zur Orientierung ist
auch noch die Geochrone in dieses Bild eingetragen.
204
18
Holmes-Houtermans-Modell
für verschiedene m-Werte
und verschiedene Alter t
2G
a
a
16
m=10
1G
3G
a
m =9
m =7
m=6
14
)
m=5
4Ga
207
Pb/204Pb
m =8
e
n
ro
0
(t=
Ga
h
oc
Ge
12
Urblei
10
8
10
12
14
206
Pb/
ABBILDUNG 91
16
18
20
204
Pb
Pb-Isotopenentwicklung der Erde nach dem Holmes-Houtermans-Modell für
verschiedene U/Pb-Verhältnisse und für verschiedene Zeiten des vollständigen Pb-Verlustes dargestellt.
Nun kann man im nächsten Schritt hingehen und die Zeit t der Separation von Pb und U
konstant lassen und (206Pb/204Pb)t und (207Pb/204Pb)t nach GL 128 und GL 129 durch Variation von µ berechnen. Für t=1, 2 bzw. 3 Ga ergeben sich Isochronen, die ebenfalls vom
123
Die U,Th–Pb-Methoden
Urblei-Punkt ausgehen und welche die Kurven mit den unterschiedlichen µ-Werten
schneiden (Abbildung 91). Es ergibt sich auf diese Weise ein Netz, aus dem sich das Pb–PbModellalter einer Probe aus deren 207Pb/204Pb- und 206Pb/207Pb-Werten ablesen läßt, die in
günstigen Fällen (wenn die Annahme des Einstufenmodells zutrifft) dem tatsächlichen
Alter des Pb-Minerals entspricht. Wenn das Alter t derart bestimmt ist, kann mit Hilfe von
Gleichung GL 130 das scheinbare (232Th/204Pb)t = w der Quellregion des Pb-Minerals (für
t=0 heute) errechnet werden. Da die µ-Werte der meisten Einstufenbleiproben zwischen »8
und 10 liegen und w typischerweise zwischen »30 und 40, erhält man Th/U-Verhältnisse
zwischen »2.9 und 4.85, Werte also, die um das terrestrische Th/U » 4 in relativ engem
Bereich streuen.
18
Stacey-Kramers-Modell der PbIsotopenentwicklung der Erde
a
2G
a
[zum Vergleich ist das Holmes-Houtermans-Modell ebenfalls eingetragen]
16
m=10
1G
3G
a
m =9
m =7
Stacey-KramersEntwicklung
m=6
14
)
m=5
4Ga
207
Pb/204Pb
m=8
=0
Ga
t
e(
on
hr
oc
Ge
12
t=3.7Ga (Zeit der Erhöhung von m)
Urblei
10
8
10
12
14
206
Pb/
ABBILDUNG 92
16
18
20
204
Pb
Das Modell von J. Stacey und J. Kramers kann radiogenere Pb-Isotopien von
Pb-Lagerstätten erklären als das von Holmes und Houtermans.
Die Annahme einer Einstufenentwicklung des terrestrischen Bleis (also konstantes U/Pb
zwischen t0 und t, dann vollständige Trennung des Bleis von Uran (und Th) ist nur in seltenen Fällen gegeben, und das Pb vieler Lagerstätten ist radiogener als es dem Einstufenmodell entspricht. Das heißt nichts anderes, als daß deren Pb–Pb-Modellalter in der
Zukunft liegen, denn Isotopenzusammensetzungen rechts der Geochronen sind mit dem
Holmes-Houtermans-Modell nicht erklärbar. Es hat nicht an Versuchen gefehlt, auch die
Isotopie von Lagerstätten-Pb mit offensichtlicher Mehrstufenentwicklung zu datieren. Ein
bekanntes Modell ist das von Stacey & Kramers (1975). Danach entwickelte sich das Pb in
der Erde zwischen 4.57 Ga und 3.7 Ga mit einem µ von 7.192 und w = 32.208. Durch geochemische Prozesse wurden diese Verhältnisse vor 3.7 Ga in den Reservoiren, aus denen
die uns heute verfügbaren Gesteine stammen, auf 9.735 bzw. 36.837 erhöht, und,
bestimmt durch diese Verhältnisse, entwickelten sich die Pb-Isotope bis heute ohne weitere
Störung. d.h. Pb, das zu einer beliebigen Zeit t zwischen 3.7 Ga und 0 von U und Th
getrennt wurde, stammt aus einem solchen Reservoir. Dieses (krustale) Reservoir mit µ =
124
A. Radiogene Isotopensysteme
9.735 und w = 36.837 hat heute die Isotopenzusammensetzung 206Pb/204Pb =18.700, 207Pb/
Pb = 15.628 und 208Pb/204Pb =38.63. t läßt sich dann analog GL 131 berechnen:
204
(
(
’
e l235 t0 - e l235 t
bt - b 0’
1
=
a t - a 0’ 137.88 e l238 t0’ - e l238 t
(
(
’
e l232 t0 - e l232 t
g t - g 0’
=k
’
a t - a 0’
e l238 t0 - e l238 t
)
)
[GL 133]
)
)
[GL 134]
41.0
Tubuai
40.5
Samoa
208
Pb/204Pb
40.0
39.0
38.5
38.0
St. Helena
Tristan da
Cunha
39.5
Komoren
Azoren
Kerguelen
MORB des
Indischen
Ozeans
Gesellschaftsinseln
Galapagos
37.5
Hawaii
37.0
atlant. und pazif. MORB
17
17.5
18
18.5
19
19.5
20
21
21.5
22
Geoc
h
Gesellschaftsinseln
[Franz. Polynesien]
Samoa
[SW-Pazifik]
15.7
Kerguelen
[Südindik]
15.6
207
Pb/204Pb
15.8
15.5
20.5
St. Helena
[Südatlantik]
rone
36.5
Tubuai [Franz.
Polynesien]
Komoren [Indik]
Azoren [Atlantik]
MORB des
Indischen
Ozeans
Galapagos [Ostpazifik]
Tristan da Cunha [Südatlantik]
Hawaii
15.4
atlant. und pazif. MORB
17
17.5
18
18.5
19
19.5
20
206
204
Pb/
ABBILDUNG 93
20.5
21
21.5
22
Pb
Pb-Isotopenzusammensetzungen von Basalten ozeanischer Spreizungszentren und von Ozeaninseln (zusammengestellt nach Literaturangaben in
[138], [139] und [140])
125
Die U,Th–Pb-Methoden
mit t 0’ =3.7 Ga, a 0’ = 11.152, b 0’ = 12.998 und g 0’ = 31.230. k kann berechnet werden,
nachdem t aus GL 133 ermittelt wurde. Für Proben konstanten Alters erhält man in einem
207
Pb/204Pb – 206Pb/204Pb oder 208Pb/204Pb – 206Pb/204Pb –Plot eine Gerade, welche die nach
Stacey & Kramers spezifizierte terrestrische Pb-Entwicklungskurve bei t 0’ = 3.7 Ga und dem
Modellalter t der Proben schneidet (siehe Abbildung 92).
Der Befund, daß viele Proben krustalen Bleis* radiogener sind, als es durch das HolmesHoutermans- oder Stacey-Kramers-Modell beschrieben wird, hatte früher zu der Vermutung geführt, daß das komplementäre Reservoir zu der Erdkruste – also ein Reservoir,
das links der Geochrone liegt – der Erdmantel ist, vorausgesetzt, der darstellende Punkt der
Erde liegt auf der Geochrone. Wie Abbildung 93 zeigt, kann das jedoch nicht sein, denn
auch ozeanische Basalte liegen fast ausnahmslos rechts der Geochrone, haben also radiogenere Bleiisotopenzusammensetzungen als für die bulk-earth angenommen. Das wird als
das Pb-Paradox bezeichnet. Danach bleiben als potentielle komplementäre Reservoire
noch übrig der Erdkern (über dessen Pb-Gehalt sich sinnvoll wohl nichts sagen läßt) oder
die kontinentale Unterkruste (Granulite), die oft niedrige Konzentrationen an U und Th
aufweist. Die Unterkruste scheint jedoch, soweit das aus Xenolithen erschließbar ist, nur in
Ausnahmefällen unradiogene 206Pb/204Pb-Isotopien zu haben (z.B. [141], [142], [143]) mit
Ausnahme von Xenolithen in Vulkaniten, die durch alte Kratongebiete eruptieren[144], wie
Abbildung 94 erkennen läßt. In der Massenbilanz mag die Unterkruste eine Pb-Isotopie
haben, die tatsächlich links der Geochronen liegt; ob das allerdings ausreicht, das Pb-Paradox aufzulösen, ist eher unwahrscheinlich; Rudnick & Goldstein (1990) haben für die
Gesamtkruste eine Zusammensetzung errechnet, die etwas rechts der Geochrone liegt.
9
m=
Ge
och
ron
e
15.8
207Pb/204Pb
(4.
57G
a)
16.0
Massif Central
Eifel
Lesotho
15.6
RB
MO
Lashaine
(Tanzania)
Arizona
15.4
m=
8
Kilbourne
Hole (New
Mexico)
15.2
m=238U/204Pb
Nordostaustralien
Pb-Isotopenzusammensetzung
von Granulitxenolithen der
kontinentalen Unterkruste
15.0
15
ABBILDUNG 94
16
17
18
206Pb/204Pb
20
Die Pb-Isotopenzusammensetzung der kontinentalen Unterkruste; das Feld
von MOR-Basalten ist zum Vergleich eingetragen.
* Das sind dann in der Regel Proben aus der kontinentalen Oberkruste.
126
19
A. Radiogene Isotopensysteme
Die Isotopendaten für Basalte der mittelozeanischen Rücken, die bis Anfang der achtziger
Jahre vorhanden waren, ließen einige lokale Besonderheiten erkennen, nämlich das Vorhandensein relativ radiogener Pb- und Sr-Isotopien von Basalten des Indischen und des
südwestlichen Pazifischen Ozeans (Abbildung 95[145], Abbildung 93). Zunächst glaubte
man, diese „Dupal-Anomalien“* seien Merkmale der ozeanischen Basalte der südlichen
Hemisphäre. Es scheint aber so, daß die Anomalie tatsächlich auf den Indischen Ozean
und die westliche Umrandung des Pazifiks beschränkt ist, während Basalte vom Mittelatlantischen Rücken und East Pacific Rise in ihrer Isotopie nicht zu unterscheiden sind.
Man darf daher annehmen, daß diese Anomalie ein Charakteristikum der Mantelkonvektionszelle unter dem Indischen Ozean ist, die erst durch die Subduktionszonen im westlichen Pazifik begrenzt wird[145]. Die Ursache der anomalen Isotopenzusammensetzungen ist
nicht klar, könnte aber wohl in einer Beimischung von Material alter kontinentaler Lithosphäre zur Quellregion der Basalte liegen[139], z.B. von Sedimenten†. Das Material (oder die
Zumischung) muß geologisch alt sein, weil das 207Pb/204Pb im Indik höher ist als in den
beiden anderen Ozeanen. Das 207Pb stammt aus dem Zerfall von 235U, von dem infolge seiner gegenüber 238U erheblich geringeren Halbwertszeit heute nur noch geringe Mengen
vorhanden sind. Zur Verdeutlichung mag man sich die Krümmung der Kurven für verschiedene µ-Werte über den Verlauf der Zeit in Abbildung 90, Seite 122, ansehen; eine geologisch junge Erhöhung von µ produziert im Lauf der Zeit nur noch eine vergleichsweise
geringe Erhöhung von 207Pb/204Pb.
0.5132
40
TongaInselbogen
pazifischer
MORB
Tonga-Inselbogen
39
indischer
MORB
0.5130
r
he
sc B
i
d R
in O
M
0.5128
0.5126
Sr-Nd-Pb-Isotopenzusammensetzung
einiger ozeanischer Basalttypen
38
pazifischer
MORB
37
0.705
Tonga-Inselbogen
15.6
0.704
indischer
MORB
indischer
MORB
0.703
pazifischer
MORB
pazifischer
MORB
0.702
ABBILDUNG 95
17
15.5
18
19
17
206Pb/204Pb
18
19
207Pb/204Pb
TongaInselbogen
87Sr/86Sr
208Pb/204Pb
143Nd/144Nd
0.5134
15.4
15.3
Die Sr-, Nd- und Pb-Isotopenzusammensetzung ozeanischer Basalte
* Akronym für Dupré & Allègre, die darauf zuerst aufmerksam machten[146]
† Feinkörnige klastische Sedimente haben sehr viel höhere Pb-Gehalte als Basalte und meist sehr unterschiedliche Isotopien; die Pb-Isotopien sind daher gut geeignet, um in Subduktionszonenmagmen Kontaminationen durch (subduzierte) Sedimente aufzuzeigen, z.B. in den Antillen[147].
127
Die U,Th–Pb-Methoden
ellsc
haft
ai
aw
H
eln
en
sins
l
ue
rg
Ke
87Sr/86Sr
Ges
Die weite Pb-Isotopenvaria.708
tion von OIB (Abbildung 93)
ist sehr markant. Zusammen
EM I
EM II
mit Variationen bezüglich der
.707
Sr- und Nd-Isotopie (Abbildungen 96 und 97) hat sie
.706
Anlaß zur Definition von drei
Endgliedern gegeben, die als
EM I (enriched mantle I), EM II
.705
(enriched mantle II) und
HIMU (high µ) bezeichnet werden [148] . EM I ist durch eine
.704
niedrige Nd-Isotopie ausgewiesen, gekoppelt mit relativ
PREMA
St. H
elen
unradiogenem 2 0 6 Pb/ 2 0 4 Pb
a
.703
MORB
und einem hohen Anteil von
HIMU
radiogenem 208Pb zu 206Pb[139].
DMM
Beispiele neben Kerguelen im
17 17.5 18 18.5 19 19.5 20 20.5 21 21.5 22
südlichen Indik sind Pitcairn
206Pb/204Pb
im Südpazifik und Tristan da
Cunha im Südatlantik. EM II
hat das höchste 8 7 Sr/ 8 6 Sr, ABBILDUNG 96 Sr-Pb-Isotopenvariation der Basalte einiger
gekoppelt mit relativ hohem Ozeaninseln, die vermeintliche oder tatsächliche Endglieder
207
Pb/206Pb. Als Beispiel kann definieren. Die Isotopien dieser Basalte scheinen zusammen
n e b e n d e n f r a n z ö s i s c h e n mit denen der MOR-Basalte in das PREMA (prevalent mantle)
Gesellschaftsinseln im zentra- genannte Feld zu konvergieren[148]. DMM steht für depleted
len Südpazifik noch Samoa MORB mantle.
genannt werden. HIMUOzeaninseln wie St. Helena, die Austral-Inseln (Tubuai und andere) Französisch Polynesiens oder mit Einschränkung die Azoren schließlich sind durch das zeitintegriert höchste
238
U/204Pb und das niedrigste 87Sr/86Sr ausgewiesen. In erweiterten REE-Diagrammen (siehe
auch im REE-Skript Kapitel 6.2.3, Seite 134) werden U und Th bei den inkompatibelsten
Elementen neben Nb aufgetragen, das Pb aber als deutlich weniger inkompatibles Element
bei den leichten REE, entsprechend der Reihenfolge für die partielle Aufschmelzung des
Erdmantels. In solchen Diagrammen zeigen sowohl MORB als auch OIB negative Pb-Anomalien, während Gesteine der kontinentalen Kruste eine positive Pb-Anomalie aufweisen;
beide Reservoire können daher als in erster Näherung komplementär für den Pb-Gehalt,
bezogen auf primitiven Erdmantel, angesehen werden, nicht aber für die Pb-Isotopie. In
MORB, EM I, EM II und der kontinentalen Kruste sind die normierten Th,U/Pb-Verhältnisse nahe 1; nur in HIMU liegen sie wesentlich darüber. Per Saldo haben demnach Th, U
und Pb in der Summe ungefähr identische „Verteilungskoeffizienten“ für die Kruste–Erdmantel-Differenzierung. Als Folge weisen Kruste (zumindest die kontinentale Oberkruste)
und Mantel (und seine Partialschmelzen) ähnliche Pb-Isotopien auf.
i
Eine mögliche Lösung für dieses Pb-Paradox wurde von A. W. Hofmann[139] vorgeschlagen.
Danach werden zunächst U, Th und Pb bei der Partialschmelzenbildung im Erdmantel entsprechend ihren experimentell einigermaßen bekannten Verteilungskoeffizienten in die
Basaltmagmen übertreten, d.h. Pb weniger stark als U und Th. Zusätzliches Pb (sicherlich
auch neben kleineren Mengen an U und Th) wird aber sekundär aus den Basalten durch
hydrothermale Prozesse an mittelozeanischen Rücken und bei der Subduktion herausgelöst. Dieses Pb verbleibt letztlich in der kontinentalen Erdkruste. Der Mehrstufenprozeß
der Fraktionierung bewirkt, daß zufällig die „Verteilungskoeffizienten“ von U, Th und Pb
zwischen Kruste und Mantel ähnlich groß sind.
128
A. Radiogene Isotopensysteme
i
ai
«Nd
aw
H
Man wird vermutlich anneh12
men dürfen, daß Zwei- oder
DMM
Mehrkomponentenmischun10 MORB
gen die plausibelste Erklärung
für die Isotopenvariationen
8
der ozeanischen Basalte sind.
Eine Kontamination durch
6
PREMA
a
kontinentale Kruste ist dabei
len
e
.H
nur für den EM II-Typ zuläs4
St
Ge
se
sig; dies ergibt sich aus den
HIMU
llsc
ha
Isotopendaten in Kombina2
fts
ins
tion mit einer negativen Nbeln
[139]
.
Anomalie dieses OIB-Typs
0
EM II
Hart et al. (1992) [149] haben
die Isotopendaten ozeani-2
scher Basalte einer statistischen Analyse unterzogen
-4
und festgestellt, daß sich der
EM I
weitaus größte Anteil der
.702
.703
.704
.705
.706
.707
.708
Variation (97.5%) durch die
87Sr/86Sr
87
86
drei Verhältnisse Sr/ Sr,
143
Nd/144Nd und 206Pb/204Pb
b e s c h r e i b e n l ä ß t . Z u d e m ABBILDUNG 97 Nd-Sr-Isotopenvariation der Basalte einiger
beobachteten sie, daß in einer Ozeaninseln und von MORB mit Bezeichnung der Lage der
Prismendarstellung mit den Endglieder[148]
Ecken DMM – HIMU – EM I –
EM II viele Trends für individuelle Suiten in Richtung die Basis des Prismas weisen zwischen DMM und HIMU (Abbildung 98). Auf Grund dieses Befundes definierten sie eine
neue Komponente namens FOZO (focal zone) mit 87Sr/86Sr = 0.7025, eNd um +9 und 206Pb/
204
Pb um 19.5, welche sie im unteren Erdmantel ansiedeln wollen. Von der Kern/MantelGrenze aufsteigende Plumes, die gerne als Quelle der OIB angesehen werden, könnten bei
ihrem Aufstieg solches Material inkorporieren. Es ist allerdings nicht klar, ob eine solche
Komponente für die Massenbilanz der Erde erforderlich oder zumindest zulässig ist.
Ke
ue
rg
le
n
P
Wa itcairn
lvis
Der Befund, daß viele
EM 1
Gesteine Pb-Isotopien
Sr
rechts der Geochrone
EM 2
haben, heißt natürlich, daß
das Pb – wie bereits gezeigt
Samoa
– eine MehrstufenentwickTristan da Cunha
lung erlebt hat. Im folgenden wird für eine ZweistuNd
fenentwicklung
die
Kapverden
mathematische Behandlung beschrieben. Das Blei
Kamerun-Linie
Gesellschaftsmöge sich zwischen t0, dem
St. Helena
inseln
Alter der Erde, und t1 dem
Holmes-HoutermansMangaia
Modell entsprechend mit
MORB
(Franz. Polynesien)
einem Wert µ1 entwickeln.
FOZO
Zur Zeit t1 soll dem Gestein
DMM
HIMU
U (und Th) zu- oder fortgeführt werden, d.h. der µ98 Prismendarstellung der 87Sr/86Sr-, 143Nd/144NdWert ändert sich. Zwischen ABBILDUNG
206
204
[149],[140]
t1 und t2 wächst die Pb-Iso- und Pb/ Pb-Zusammensetzung von OIB und MORB
topie dann mit dem neuen µ2-Wert weiter an; bei t2 findet die Trennung von U,Th und Pb
Az
or
en
Haw
aii
Pb
129
Die U,Th–Pb-Methoden
statt. Zufuhr von Pb würde die Betrachtung komplizieren, weil vorhandenes und zugeführtes Pb wohl kaum dieselbe Isotopie gehabt haben werden. Zum Zeitpunkt t1 hätte die Probe
dann die folgende Pb-Isotopie gehabt:
(
)
a t1 = a 0 + m1 e l238 t0 - e l238 t1
Von t1 bis t2 ist das 206Pb/204Pb dann weiter angewachsen auf a t 2 :
(
)
(
a t2 = a 0 + m1 e l 238 t0 - e l 238 t1 + m2 e l 238 t1 - e l 238 t2
)
oder
(
a t2 = a t1 + m2 ´ e l 238 t1 - e l 238 t2
)
[GL 135]
und analog für 207Pb/204Pb:
bt2 = b0 +
m1
m2
e l 235 t0 - e l 235 t1 +
e l 235 t1 - e l 235 t2
137.88
137.88
(
)
(
m2
e l235 t1 - e l235 t 2
137.88
Durch Kombination von GL 135 und GL 136 erhält man:
bt 2 = bt1 +
bt 2 - bt1
a t 2 - a t1
=
)
(
)
[GL 136]
(
(
)
)
[GL 137]
e l235 t1 - e l235 t 2
1
137.88 e l238 t1 - e l238 t 2
Dies ist aber wieder die Gleichung einer Geraden in den Koordinaten von 206Pb/204Pb ( a t 2 )
und 207Pb/204Pb ( bt 2 ) mit der Steigung
(
(
e l235 t1 - e l235 t 2
1
m=
137.88 e l238 t1 - e l238 t 2
also
)
)
bt 2 = ma t 2 - ma t1 + bt1 .
Eine Serie kogenetischer Proben, die sich nur in ihren µ2-Werten unterscheidet, hat dann
Pb-Isotopenzusammensetzungen, die auf eine Gerade fallen, die für µ2 = 0 durch den Punkt
( a t1 , bt1 ) auf der Wachstumskurve mit dem früheren µ1-Wert geht. Eine solche Gerade ist
eine sekundäre Isochrone. Letztlich kommt es nicht darauf an, wie oft dem System U und
Th zu- oder abgeführt oder Pb abgeführt wird; datierbar ist das jeweils letzte Ereignis, das
zur Homogenisierung der Pb-Isotope kogenetischer Gesteine geführt hat. Werden solche
U,Th-haltigen Proben heute untersucht, dann ist t2 = 0 und die Gleichung reduziert sich zu
bt 2 - bt1
a t 2 - a t1
(
(
)
)
e l235 t1 - 1
1
=
137.88 e l238 t1 - 1
[GL 138]
In den Abbildungen 99 und 100 ist ein solches Modell dargestellt, um die Pb-Isotopie von
Proben zu erklären, die radiogener sind, als es der Geochrone entspricht. Aufgetragen sind
im vorigen Diagramm drei Pb–Pb-Entwicklungskurven mit µ = 6, 8 und 10, die dem Holmes-Houtermans-Modell gehorchen. Vor 2 Ga mögen Proben, die sich bis dahin mit µ = 8
entwickelten, eine Zufuhr von U (oder Abfuhr von Pb), also eine Erhöhung von µ auf 12
bzw. 16 erfahren. Diese Gesteine hätten dann heute eine 206Pb/204Pb-Isotopie entwickelt,
die weit rechts der Geochrone liegt. Abbildung 100 zeigt zwei sekundäre Isochronen, eine,
130
A. Radiogene Isotopensysteme
für welche die Trennung von U und Pb heute stattgefunden hat, und eine mit einer U–PbTrennung vor 1 Ga. Beide Isochronen schneiden die Kurve der Holmes-Houtermans-Entwicklung für µ = 8 in einem Punkt, der die initiale Pb-Isotopenzusammensetzung des
Systems angibt. Die Pb-Isotopie ausgewählter MOR-Basalte streut in einem solchen Pb–PbDiagramm um eine Gerade mit einer Steigung 0.121, was einem Alter von »2 Ga entspricht, wenn die Gerade als sekundäre Isochrone und nicht als Mischungslinie interpretiert wird, was genauso möglich wäre[150].
18
Modell einer zweistufigen
Entwicklung der Pb-Isotope
m=16
16
m=12
14
t=
1G
a
a
8
m=
t=
2G
207Pb/204Pb
10
m=
Zweistufenblei
6
m=
)
=0
Ga
t
e(
on
hr
oc
Ge
12
10
8
ABBILDUNG 99
10
12
14
16
206Pb/204Pb
18
20
22
Modell einer zweistufigen Pb-Isotopenentwicklung zur Erklärung von radiogeneren Pb-Isotopien in Gesteinen, als es dem Holmes-Houtermans-Modell
entspricht. In der Zeichnung ist angenommen, daß sich eine Pb-Probe zwischen 4.57 Ga und 2 Ga mit einem µ-Wert von 8 nach dem Holmes-Houtermans-Modell entwickelt. Dann soll durch Zufuhr von U der µ-Wert auf 12
bzw. 16 erhöht werden. Mit diesen Werten wachsen die Pb-Isotopenverhältnisse in den Proben bis heute weiter an.
Um die Pb-Isotopenzusammensetzung bleiarmer Proben zu messen (z.B. ozeanische
Basalte), muß man sehr hohe Vorsichtsmaßnahmen im Labor treffen. Das betrifft sowohl
die Probenaufbereitung als auch die chemischen Separationen. Das hat seine Ursache
darin, daß Pb ein allgegenwärtiges Element ist. Seit 1923 wird Pb-Tetraethyl als Antiklopfmittel dem Benzin zugesetzt, und bis 1965 waren dadurch bereits 2.6´106t weltweit in die
Atmosphäre geblasen worden, was einer Menge von »5mg Pb pro m2 Erdoberfläche entspricht. Diese anthropogene Belastung durch das toxische Schwermetall erstreckt sich auf
alle Kontinente und die obersten Schichten der Ozeane (bis einige 100m). Es ist u.a. den
Arbeiten und Bemühungen des schon erwähnten C. Patterson am Caltech zu verdanken,
131
Die U,Th–Pb-Methoden
daß in den USA bereits in den siebziger Jahren die Katalysatoren eingeführt wurden, die
den Zusatz von Pb zum Benzin überflüssig gemacht haben.
16.0
Modell einer zweistufigen
Entwicklung der Pb-Isotope
m=16
15.8
m=12
207Pb/204Pb
1Ga
t=0
t= 0
15.6
ld
-Fe
1Ga
t=0
B
OR
M
15.4
2Ga
sekundäre
Pb-Pb-Isochronen
Geoc
hron
15.2
e (t=
HolmesHoutermansEntwicklung
mit m=8
0 Ga
)
1Ga
15.0
14
ABBILDUNG 100
132
15
16
17
18
206Pb/204Pb
19
20
21
Die Pb-Isotopie von MOR-Basalten läßt sich durch eine mehrstufige Entwicklung erklären. Dies ist ein Ausschnitt aus Abbildung 99, in den zum Vergleich
das Feld der MORB eingetragen ist.
A. Radiogene Isotopensysteme
13.0
Die Fission-Track-Methode
Bei Beobachtung einer Mit Neutronen bestrahlten Probe unter dem Elektronenmikroskop
beobachteten E.C.H. Silk & R.S. Barnes[151] 1959 Spuren, die durch den Rückstoß der Spaltkerne entstanden waren. Dabei bewegen sich diese Spaltkerne einige µm durch den Kristall
und verursachen Gitterstörungen. P.B. Price & R.M. Walker[152],[153] fanden dann 1962, daß
die Spuren durch Ätzung des Materials mit geeigneten Chemikalien soweit vergrößert werden können, daß sie unter dem Lichtmikroskop als Kanäle sichtbar werden. Price & Walker
beobachteten solche „Fission-Tracks“ auch in natürlichem Glimmer und erkannten, daß
diese Spuren fast ausschließlich durch die Spontanspaltung von 238U entstehen. Dabei werden pro U-Atom Energien von »200 MeV frei, von denen sich ein beträchtlicher Teil auf die
beiden Spaltproduktkerne verteilt, die infolge ihres Rückstoßes Gitterdefekte von ca. 10µm
Länge erzeugen. Price & Walker (1963) berichteten, daß man auf Grund der Dichte der
Spaltspuren in einem Material dessen Alter bestimmen kann, wenn man zusätzlich den UGehalt mißt[154]. Dieser Vorschlag wurde sofort aufgegriffen und hat zur Entwicklung der
Spaltspurenmethode als Verfahren der Altersbestimmung geführt. Sie hat ihre Stärken v.a.
in der Meteoritik und bei der Altersbestimmung von Mondproben gezeigt, ist aber auch für
einige Fragestellungen zur Datierung irdischer Gesteine geeignet. Spezialist auf diesem
Gebiet ist in Deutschland G.A. Wagner (MPI Heidelberg).
238
U erleidet außer
dem a-Zerfall noch
eine Spontanspaltung, für welche die
Zerfallskonstante an
Hand von Proben
bekannten Alters
(Minerale, künstliche
U-haltige Gläser)
bestimmt wurde. Als
bester Wert gilt heute
lf
=(8.46±0.06)
´10-17a-1. Sie ist vernachlässigbar klein
gegenüber der a-Zerfallskonstanten des
238
U (l f /l a »5´10 -7 ).
Auch 235U und 232Th
erleiden eine Spontanspaltung; außerdem können sie Neutronen einfangen,
die bei der Spontan- ABBILDUNG 101 Spaltspuren in Titanit aus einem Syenit aus Burundi.
spaltung des 238U frei Die Ätzung erfolgte 15 Minuten bei 25°C in einer Mischung aus HF,
werden. Alle diese HCl, HNO3 und H2O. Die schräg von oben nach unten verlaufende LiBeiträge sind jedoch nie ist eine Zwillingsgrenze.
gegenüber der 238 USpontanspaltung völlig vernachlässigbar (falls es sich nicht gerade um ein U-Erz handelt);
und man kann daher, zumindest in irdischen Proben, alle Spaltspuren dem Spontanzerfall
des 238U zuordnen.
Das Fission-Track-Alter einer Probe läßt sich folgendermaßen bestimmen: Man zerschneidet oder zersägt das Material und legt damit eine innere Oberfläche im Zentrum des Minerals oder Glases frei, in der sich Spaltspuren finden sollten, die durch 238U-Zerfall innerhalb
eines kleinen Volumens symmetrisch in beiden Seiten der Schnittfläche entstanden sind
133
Die Fission-Track-Methode
(4p-Geometrie). Eine der Schnittflächen wird poliert; kleine Proben können z.B. in EpoxyHarz eingebettet und dann heruntergeschliffen werden. Dann erfolgt die Ätzung, bei Apatit z.B. mit HNO3, bei Titanit (siehe Abbildung 101[155]) mit HF, bei Zirkon mit NaOH. Nun
wird auf der geätzten Fläche eine statistisch ausreichende Zahl von Spaltspuren auf einer
bestimmten Fläche ausgezählt. Schließlich mißt man noch die U-Konzentration mit einer
geeigneten Methode. Dazu wird die Probe in einen Kernreaktor gesteckt. Dabei erleidet das
235
U eine Spaltung durch Neutroneneinfang und erzeugt seinerseits Tracks, die ausgezählt
werden können. Will man dessen Spaltspuren ebenfalls im Mineral oder Glas messen, müssen die 238U-Spuren durch Erhitzen und Tempern des Materials vor der Reaktorbestrahlung
durch Verheilen entfernt werden. Sonst wäre eine Unterscheidung zwischen 238U- und
235
U-Fission-Tracks nicht möglich. Nach der Reaktorbestrahlung wird die Probe dann weiter abgeschliffen und eine neue Oberfläche poliert, auf der die induzierten Spaltspuren ausgezählt werden. Eine Alternative ist, daß man die polierte Oberfläche des untersuchten
Materials mit einer empfindlichen Folie abdeckt (U-freier Muskovit oder Kunststoff) und
dann im Reaktor bestrahlt. Die Folie dient dabei als externer Monitor, in der Tracks erzeugt
werden, die sich anschließend auszählen lassen. Diese Tracks stammen jedoch nur aus der
Spaltung des 235U, das sich an und nahe der Oberfläche des zu untersuchenden Materials
befindet, also nur auf einer Seite (2p-Geometrie). Dafür ist eine Korrektur mit Hilfe eines
Geometriefaktors vorzunehmen.
Die Berechnung des Alters der Probe kann jetzt folgendermaßen erfolgen: Die Anzahl der
Zerfälle D von 238U (betrachtet wird also nur der Zerfall von U, nicht die Bildung des stabilen Endprodukts Pb) in einem cm3 Probenvolumen innerhalb einer Zeit t ergibt sich aus
der bekannten Zerfallsgleichung zu:
D=
(
)
U e la t - 1
238
[GL 139]
wobei 238U die Anzahl der heute noch vorhandenen Atome pro cm3 Probe ist. Der Zerfall
durch Spontanspaltung kann in Relation zum a-Zerfall vernachlässigt werden. Der Anteil
fs von 238U, das durch Spontanspaltung zerfällt, ergibt sich durch Multiplikation von D mit
dem Verhältnis lf/la:
fs =
lf
(
)
U e la t - 1
238
la
[GL 140]
Ein kleiner Anteil j der Spuren wird die polierte Oberfläche kreuzen und kann ausgezählt
werden. Die Flächendichte (Tracks pro cm2) der durch die Spontanspaltung hervorgerufenen Spuren auf dieser Oberfläche ist dann gegeben durch:
(
r s = f s j = l f la
)
(
)
U e la t - 1 j
238
[GL 141]
Eine ähnliche Betrachtung ist noch für das 235U anzustellen. Die Anzahl fi der durch die
Neutronenbestrahlung im Reaktor verursachten 235U-Spaltungen je cm3 Probe ergibt sich
zu:
fi = 235U s F
[GL 142]
wobei 235U die heutige Anzahl der Atome je cm3 Probe ist, s ist der Spaltwirkungsquerschnitt des 235U für thermische Neutronen (580.2 barn); und F ist die Neutronendosis, welche die Probe je cm2 erhält. Der Anteil der entstandenen Spuren, die eine neue durch
Abschleifen freizulegende Materialoberfläche kreuzen, ergibt sich durch Multiplikation
von GL 142 mit demselben Faktor j wie in GL 141:
ri = f i j =
235
U s Fj
Durch Division von GL 141 und GL 143 läßt sich der Faktor j eliminieren:
134
[GL 143]
A. Radiogene Isotopensysteme
rs lf
=
ri la
(
)
la t
U e -1
235
U sF
238
[GL 144]
Dies, nach t aufgelöst, ergibt:
t=
ær l
1
lnç s a
la è ri l f
ö
U
s F + 1÷
U
ø
235
238
[GL 145]
wobei la = 1.55125´10-10a-1, lf = (8.46±0.06)´10-17a-1, s = 580.2 barn und 235U/238U= 1/
137.88. Die Neutronendosis F wird mit Hilfe eines Flußmonitors (z.B. Metallfolie aus Co
oder Au) bestimmt. rs und ri werden ausgezählt. Wünschenswert ist ein Verhältnis rs/ri »
1, was sich durch Variation der Neutronendosis F erreichen läßt.
t ist ein Alter unter den Voraussetzungen, daß
a) die Spaltspuren des 238U seit ihrer Bildung stabil geblieben, d.h. nicht partiell ausgeheilt
sind;
b) die untersuchten Minerale oder Gläser genügend klar und einschlußfrei sind, um ein
sicheres Auszählen der Spuren zu erlauben;
c) das U in den Materialien völlig homogen verteilt ist;
d) sich das Ätzverfahren genau reproduzieren läßt zum Auszählen der Tracks von 238U und
U;
235
nur wenn c) und d) gegeben sind, ist der Faktor j in GL 141 und GL 145 identisch;
e) die U-Konzentration in den Mineralen oder Gläsern hoch genug ist, um eine statistisch
signifikante Anzahl von Spaltspuren auszuzählen.
In Anbetracht der vielen Variablen, die in GL 145 eingehen, ist es nicht verwunderlich, daß
Alter, die auf diese Weise erhalten werden, eine Genauigkeit von nur ±5 – 10% haben. Am
schwierigsten ist die Neutronendosis F zu bestimmen, aber selbst lf ist wesentlich schlechter bekannt als la. Nach einem Vorschlag von Hurford & Green (1982+1983)[156],[157] benutzt
man daher heute oft Mineralstandards, die man zusammen mit der Probe im Reaktor
bestrahlt. Das Alter des Mineralstandards muß durch andere Methoden gut bekannt sein.
Außerdem muß gewährleistet sein, daß das Gestein, aus dem diese Minerale stammen, sehr
rasch abgekühlt ist und später nie wieder über die Ausheiltemperaturen der Fission-Tracks
aufgeheizt wurde. Diese Voraussetzungen werden nur durch Vulkanite erfüllt, und es sind
hauptsächlich Zirkone, die infolge ihrer relativ hohen Temperatur für die Ausheilung der
Spuren als Standards Verwendung finden. Bei diesem Standardverfahren wird aus GL 145
ein sogenannter z-Parameter herausgelöst, der die am schlechtesten absolut bestimmbaren
sowie konstante Größen beinhaltet:
x=
sF
lf
235
U
U
238
[GL 146]
Aus GL 145 wird damit:
t=
ær
ö
1
lnç s la x + 1÷
la è ri
ø
[GL 147]
z wird dann mit Hilfe des Standards bestimmt, d.h. bei jeder Reaktorbestrahlung werden
Standards zusammen mit den Proben unbekannten Alters bestrahlt und z nach GL 144
errechnet:
135
Die Fission-Track-Methode
x=
e la t - 1 æ ri ö
ç ÷
la è r s ø Standard
[GL 148]
worin t das bekannte Alter des Standards ist. Diesen Wert für z setzt man dann in GL 147
ein, um das unbekannte Alter der Proben zu ermitteln. Diese Prozedur erinnert stark an das
bei der 40Ar/39Ar-Analyse angewandte Verfahren. Ein Nachteil dieses Verfahrens ist, daß die
Homogenität der verfügbaren Mineralstandards naturgemäß nicht gewährleistet werden
kann; vor allem aber sind solche Minerale nur in geringen Mengen verfügbar. Alternativ
werden daher synthetische U-haltige Gläser als Standards verwandt.
0%
100%
0%
Jahre
100%
Mit der Fission-Track-Me500 400 300 200
100
50
8C
thode können also geologi1000000
sche Alter bestimmt werden,
genauso wie mit anderen radiometrischen Verfahren.
Titanit
Apatit
10000
Beim Vergleich der FissionTrack-Alter mit z.B. K–Ar-,
Rb–Sr- oder Sm–Nd-Altern
wird besonders augenfällig,
100
daß Alter nicht gleich Alter
ist. Bei Metamorphiten und
Plutoniten sind die Spalt1
spurenalter stets erheblich
jünger als die der anderen
Methoden. Das liegt daran,
daß die Fission-Tracks in den
0.01
meisten Mineralen im Lauf
geologischer Zeit bereits bei
sehr niedrigen Temperatu0.0001
ren kürzer werden und
schließlich verschwinden –
die Fission-Track-Uhr wird
auf Null zurückgestellt. Die 0.000001
Geschwindigkeit, mit der
1
1.5
2
2.5
3
3.5
diese Gitterdefekte bei gege1000/T [K]
bener Temperatur ausheilen,
variiert von Mineral zu Mineral, so daß verschiedene ABBILDUNG 102 Ausheilung von Fission Tracks in Apatit und TiMinerale aus einem Meta- tanit. Gezeigt sind Ausheilkurven (durchgezogene Teile: gemesmorphit oder Plutonit völlig sen, gestrichelt: extrapoliert), oberhalb derer 100% der Spuren
verschiedene Fission-Track- ausheilen bzw. unterhalb derer alle Spuren erhalten bleiben. So
Alter haben können. Wenn heilen z.B. alle Tracks in Apatit schon aus, wenn dieses Mineral
man die Ausheiltemperatu- 1Ma auf Temperaturen oberhalb »175°C erhitzt wird, während
ren für verschiedene Mine- beim Titanit dafür schon mehr als 400°C erforderlich sind.
rale bei verschiedenen
Abkühlgeschwindigkeiten
kennt, läßt sich damit etwas über die Abkühlgeschichte eines Gesteinskomplexes ablesen.
Als thermisch aktivierter Prozeß kann man die Gitterausheilung durch eine Art von Arrhenius-Gleichung beschreiben:
t = A eU
kT
[GL 149]
wobei t die Ausheilzeit ist, A eine Konstante, U die Aktivierungsenergie [z.B. in eV], k die
Boltzmann-Konstante [8.6171 ´ 10-5 eV/Kelvin] und T die absolute Temperatur. In logarithmierter Form
136
A. Radiogene Isotopensysteme
ln(t) = ln(A) + U/kT
400
350
Schließungstemperatur [8C]
ist dies die Gleichung einer Geraden,
wenn man ln(t) gegen 1/T aufträgt.
Ein Beispiel dafür ist in Abbildung
102 für Apatit und Titanit gezeigt.
Wird Titanit demnach für 106a auf
250°C aufgeheizt, so überleben die
Fission Tracks alle noch; bei Aufheizung auf »420°C sind jedoch alle
Tracks in derselben Zeit verschwunden. Für Apatit liegen die entsprechenden Temperaturmarken erheblich niedriger, nämlich bei »50 bzw.
gut 150°C. Die Spaltspuren in Titaniten können also eine niedriggradige
Metamorphose in Grünschieferfazies noch überleben, während die
Tracks im Apatit schon bei der Diagenese ausheilen bzw. das Endstadium der Abkühlung nach einer
Metamorphose markieren.
[GL 150]
Titanit
t
Grana
300
n
Zirko
Epidot
250
Titanit
Allanit
Allanit
200
Muskov
150
blende
Horn
100
Epidot
it
pit
Phlogo
t
Apati
Biotit
50
0
0.1
1
10
100
Ähnlich wie bei anderen radiogenen
Abkühlgeschwindigkeit
[8C/Ma]
Isotopensystemen kann man auch
bei der Fission-Track-Methode von
einer Schließungstemperatur reden, ABBILDUNG 103 Abhängigkeit der „Schließungstemdie wiederum von der Abkühlge- peratur“ (Erhaltung von 100% aller Tracks) von der Abschwindigkeit eines Gesteinskom- kühlrate für verschiedene Minerale. Für einige Minerale
plexes abhängt. Auch dabei wird das existieren sehr unterschiedliche Daten von diversen Ausehr unterschiedliche Ausheilver- toren, vornehmlich wohl, weil unterschiedliche Ätzvermögen der Tracks in verschiedenen fahren angewendet wurden, mit denen teilweise verMineralen deutlich. Leider sind, wie heilte Spuren sichtbar gemacht werden können oder
Abbildung 103 zeigt, die Literaturda- nicht.
ten z.T. nicht sehr konsistent. Das
liegt vermutlich daran, daß zur Bestimmung dieser auf experimentellen Daten beruhenden
Kurven unterschiedliche Verfahren angewandt wurden, um die Tracks anzuätzen und so
die Ausheilrate zu messen. Außerdem stellen diese Daten natürlich Extrapolationen der
Labordaten auf die Abkühlgeschwindigkeiten in der Natur dar. Was jedoch auf jeden Fall
aus der Abbildung hervorgeht, ist, daß Titanit, Zirkon, Granat und Epidot hohe Ausheiltemperaturen für die Spaltspuren haben, Apatit und Biotit außerordentlich niedrige. Systematische Untersuchungen an natürlichem Zirkon[158] erweisen die Spaltspuren sogar als
noch stabiler als zuvor geglaubt, nämlich bis ca. 350 °C.
Diese Schließungstemperaturen können, zusammen mit entsprechenden Daten für andere
Isotopensysteme und Abschätzungen geothermischer Gradienten, verwandt werden, um
die Heraushebungsgeschwindigkeiten von Gesteinskomplexen nach tektonischen Ereignissen und Metamorphosen zu rekonstruieren. So wurde z.B. für das Gotthardt-Massif in
den Alpen eine durchschnittliche Heraushebung um »500m pro 106a für die letzten »10Ma
errechnet[159], für die Nanga Parbat-Region im Himalaya sogar um »800m pro 106a[160].
137
Die Fission-Track-Methode
Tiefe [m]
0.3mm/a
Generell läßt sich festAlter [Ma]
stellen, daß die Fis10
20
30
40
50
60
70
80
sion-Track-Methode
die letzten Punkte auf
der Abkühlkurve eines
Gesteinskomplexes
500
definiert. Geologische
Ereignisse, also z.B.
der Höchststand einer
1000
Metamorphose oder
die Kristallisation
eines Magmatits, kön1500
nen daher auf diese
Weise nicht bestimmt
werden mit der Aus608C
2000
nahme der Erstarrung
von Vulkaniten. Der
praktische Nutzen der
2500
Methode für die Geowissenschaften hält
sich daher in Grenzen.
3000
Das läßt sich noch an
Abbildung 104 ver1008C
deutlichen, welche die
3500
Altersverteilung in der
Vorbohrung des Kontinentalen Tiefbohr4000
programms in der
Oberpfalz zeigt [ 1 5 5 ] . ABBILDUNG 104 Fission-Track-Alter in Gesteinen der Vorbohrung der
Danach hat die Aus- KTB
wertung der Längen
der Spaltspuren in Apatiten ergeben, daß die Altersdaten der obersten ca. 2000m des Profils
als Abkühlung innerhalb der letzten »65Ma mit einer Heraushebungsrate von etwa 300m
pro Ma gedeutet werden können. Der steile Abfall der Alter unterhalb 2000m Tiefe ist auf
eine teilweise Ausheilung der Spaltspuren oberhalb »60°C der „Schließungstemperatur“
des Apatits zu deuten. An der Basis des Bohrkerns der Vorbohrung bei knapp 4000m liegt
das Spaltspurenalter bei nur noch etwa 6 Ma!
138
A. Radiogene Isotopensysteme
14.0
Die Ungleichgewichtsmethoden
Beim Zerfall von U und Th in Pb tritt eine ganze Reihe von Zerfallsprodukten auf, die
Nuklide anderer Elemente sind. Wenn die Systeme geschlossen sind, stellt sich nach einigen Halbwertszeiten des längstlebigen Zwischenprodukts das sogenannte „säkulare Gleichgewicht“ in, bei dem die Aktivitäten Ai = li Ni aller Nuklide gleich sind. Im festen Zustand
und bei niedrigen Temperaturen sind die Voraussetzungen für geschlossene Systeme
sicherlich in der Regel erfüllt. Wenn sich Th und U und ihre Folgeprodukte jedoch in
Lösung befinden, kann es wegen der unterschiedlichen chemischen Eigenschaften der Zerfallsprodukte zu Fraktionierungen kommen, vor allem natürlich dann, wenn die Halbwertszeiten der Zwischenprodukte mindestens im Bereich der Dauer der (geo)chemischen
Prozesse liegen, denen sie unterworfen sind. Das sind in den drei natürlichen Zerfallsreihen nur vier Isotope, die in der Tabelle aufgeführt sind. Drei dieser Isotope kommen in
der 238U-Zerfallsreihe vor, eines in der 235U-Reihe, keines in der Th-Reihe. In die Tabelle
wurde noch das 210Pb aufgenommen, das infolge seiner niedrigen Halbwertszeit Anwendungen bei der Datierung von Schnee und Eis sowie von rezenten Sedimentablagerungen
findet. Die für die Geochemie wichtigsten der Ungleichgewichtsdatierungen beruhen auf
der Trennung von U und Th in der Natur. Diese Methoden werden vorwiegend bei der
Datierung von chemischen (Karbonaten), seltener von klastischen Sedimenten angewandt
und als Tracer für die Aufklärung von Magmenbildungsprozessen. Die Lebensdauer der
Ungleichgewichte beschränkt die Einsetzbarkeit der Verfahren auf das Quartär, einen Zeitbereich also, in dem die meisten anderen Isotopenmethoden (Rb-Sr, Sm-Nd, U,Th-Pb) versagen. Voraussetzung für die Anwendbarkeit der Ungleichgewichtsmethoden ist, daß ein
ehemals bestehendes Ungleichgewicht in einer flüssigen (wäßrige Lösungen) oder
Schmelzphase bei der Bildung von Gesteinen und Mineralen in diese übernommen wurde
und sich anschließend im nun geschlossenen System in Richtung auf ein neues säkulares
Gleichgewicht zu entwickeln begann.
Nuklid
Halbwertszeit [a]
l [a-1]
234
2.48´105
7.52´104
1.622´103
3.248´104
22.26
2.794´10-6
9.217´10-6
4.272´10-4
2.134´10-5
3.11´10-2
U
230
Th
226
Ra
231
Pa
210
Pb
Durch Kernwaffenversuche und die Tschernobyl-Katastrophe in die Umwelt gelangt, sind
die Radionuklide 90Sr (Halbwertszeit 28.64a) und 137Cs (Halbwertszeit 30.17a), die mit
hohen Isobarenausbeuten von rund 6% bei der Spaltung von 235U mit thermischen Neutronen entstehen und selektiv in der Biosphäre angereichert werden, indem sich Cs ähnlich wie K und Sr ähnlich wie Ca verhält. Auf Lebewesen üben sie durch hochenergetische
ß--Zerfälle eine gewebeschädigende Wirkung aus. In den Umweltwissenschaften liefern sie
Zeitmarker für den Beginn des Atomzeitalters. Zudem lassen sich über ihre Ausbreitung die
atmosphärische und marine Zirkulation verfolgen.
Für die Datierung mittels der Ungleichgewichtsmethoden bedarf es im Prinzip keines Massenspektrometers. Man begnügte sich lange mit der Messung der Aktivitäten mit einem aDetektor. Die quantitative Messung von a-Strahlung ist allerdings infolge der extremen
Absorptionseffekte nicht einfach (a-Strahlen werden bereits durch ein Blatt Papier quantitativ absorbiert.). Zudem sind die Zählraten durchweg niedrig, was lange Meßzeiten erfordert. Das führt dazu, daß die Meßdaten mit größeren statistischen Fehlern behaftet sind als
massenspektrometrische Daten. Seit den späten achtziger Jahren werden Datierungen mittels der Ungleichgewichtsmethoden zunehmend mit Thermionenmassenspektrometern
durchgeführt[161]; diese Technik dominiert seit Mitte der neunziger Jahre des 20. Jahrhunderts. Eine Problematik dabei besteht darin, daß man sehr große Isotopenverhältnisse
139
Die Ungleichgewichtsmethoden
bestimmen muß. Z.B. entspricht einem 230Th/238U-Aktivitätsverhältnis von 1 ein Isotopenverhältnis von l1N1 = l2N2 Þ 230Th/238U = [1.55125´10-10a-1/9.217´10-6a-1] = 1.7´10-5, was
eine Messung mit verschiedenen Detektoren nötig macht (Faraday für intensive Signale,
Photomultiplier als Ionenzähler für kleine Signale; dabei ist die Linearität des Multipliers
kritisch – dies ist die Proportionalität zwischen der Anzahl an Ionen, die auf den Detektor
treffen, zur Anzahl an registrierten Ionen). Die Verwendung eines Spikes, z.B. von 229Th
(Halbwertszeit 7880a) für die 230Th–238U-Ungleichgewichtsbestimmung kann evtl. das Problem entschärfen. Andererseits weisen die a-spektrometrischen Analysen eine Ungenauigkeit von immerhin einigen Prozent auf. Die massenspektrometrische Analyse hat gegenüber der a-Spektrometrie tatsächlich eine Steigerung in der Präzision (Reproduzierbarkeit)
der Analyse um etwa eine Zehnerpotenz gebracht bei einer ebenfalls ca. zehnfachen Reduzierung der Probenmengen. Mit Hilfe der Datierung von Korallen und Höhlensintern hat
man auf diese Weise die Klimageschichte des Tertiärs wesentlich besser auflösen können,
als dies zuvor der Fall war[162]. Dennoch ist die Genauigkeit einer massenspektrometrischen
Analyse nicht unbedingt viel höher als die der a-Spektrometrie[163].
Die folgende Darstellung ist weitgehend auf die a-spektrometrischen Methoden
beschränkt; die praktische Durchführung einer solchen Datierung durch eine der
Ungleichgewichtsmethoden gestaltet sich dabei kurz folgendermaßen[164]:
• Die zu untersuchende Probe wird in geeigneter Weise aufgeschlossen.
• Um die chemische Ausbeute des Trennverfahrens kontrollieren zu können, werden der
Lösung Isotopenspikes zugefügt, bei der Datierung nach dem 230Th/234U-Verfahren z.B.
Spikes von 232U und 228Th.
• Mit Ionenaustausch- und Extraktionsverfahren werden U einerseits und Th andererseits
chemisch so rein wie möglich abgetrennt.
• U und Th werden dann separat auf Edelstahlscheiben elektrolytisch abgeschieden; die
chemischen Ausbeuten des von Hennig benutzten Trennverfahrens liegen für U zwischen 50 – 80%, für Th bei »30 – 60%.
• Die Messung wird mit einem a-Spektrometer vorgenommen, das ähnlich aufgebaut ist
wie ein g-Meßplatz. Als Detektor wird ein Silizium-Oberflächengrenzschichtzähler verwandt; das ist eine dünne Scheibe eines N-dotierten (elektronenverarmten) hochohmigen Reinstsiliziumkristalls, auf der auf der Oberseite eine äußerst dünne Au-Schicht
aufgedampft wurde, auf der Rückseite eine Al-Schicht. Da ein Teil der Elektronen aus
dem Au in das Si wandert, bildet sich an der Kontaktfläche beider Elemente ein geringes
Potential aus, das der Sperrschicht einer Diode entspricht. Die Schichtdicke dieser Oberflächensperrschicht läßt sich erheblich vergrößern, wenn man an die Au-Schicht ein negatives Potential anlegt. Die mit Al bedampfte Rückseite des Detektors liegt an Masse.
Ein a-Teilchen, das in die Oberflächensperrschicht eintritt, verliert seine Energie vorwiegend durch Ionisation des Siliziums, also durch Erzeugung von Elektronen und Elektronenlöchern. Bei Raumtemperatur sind zur Erzeugung eines Elektronen/
Elektronenloch-Paares im Si 3.62eV nötig, so daß pro a-Teilchen von 4 – 4.5MeV Energie »106 Elektronen/Loch-Paare gebildet werden.
Die Messung muß natürlich im Vakuum erfolgen, da die a-Teilchen in Luft sehr rasch
gebremst würden.
Abbildung 105 zeigt Beispiele für a-Spektren von U und Th. Infolge der chemischen Reinheit der Fraktionen können die für die Altersbestimmung nötigen Nuklide anhand ihrer aMaximalenergien leicht identifiziert werden.
14.1
Geschichtliche Anmerkungen
Die Entdeckung des radioaktiven Ungleichgewichts zwischen Uran und einem langlebigen
Tochterprodukt in der Natur geht auf den Anfang des 20. Jahrhunderts zurück, als Joly
fand, daß Tiefseesedimente ungewöhnlich hohe Gehalte an 226Ra aufweisen, dessen Ursache später einem Überschuß an 230Th („Ionium“) durch dessen „Sedimentation“ am Mee-
140
A. Radiogene Isotopensysteme
resboden zugeschrieben wurde, ohne daß man diesen reinen a-Strahler direkt messen
konnte[165]. Dabei zeigte sich auch, daß diese Anomalie auf die oberflächennahen – also
jüngsten – Sedimentschichten beschränkt ist und daß bereits in einigen m Tiefe der Sedimentkerne wieder radioaktives Gleichgewicht zwischen 238U und 230Th besteht. Diese frühen Messungen von Ra wurden durch Registrierung der b– und g-Strahlung gemacht.
Im folgenden werden die Methoden
im einzelnen besprochen. Eckige
Klammern [ ] oder der Buchstabe A
mit einer tiefgestellten Zahl kennzeichnen dabei die Aktivitäten der
betrachteten Proben.
14.2
Die 210Pb-Methode
In der 238 U-Zerfallsreihe entsteht
intermediär das Edelgas 2 2 2 Rn.
Infolge seiner vergleichsweise langen
Halbwertszeit von »3.8d entweicht
es aus Gesteinen und Gewässern in
die Atmosphäre mit einer mittleren
Geschwindigkeit von »45 Atomen
pro Minute und cm2 Landoberfläche.
Es zerfällt über eine Serie von kurzlebigen Zwischenprodukten in 210Pb,
das wiederum mit einer mittleren
Verweildauer von »10d durch Regen
und Schnee aus der Atmosphäre ausgeschieden wird und sich dann im
200
300
Kanal
232U
300
234U
238U
200
Impulse
Komplementär dazu gibt es die
230
Th–238U- und die 230Th–234U-Methoden, bei denen das Alter eines
Materials aus einem Unterschuß an
230
Th errechnet wird. Analog funktioniert eine 231Pa–235U-Methode[167]. Sie hat jedoch gegenüber
den zuvor genannten den großen
Nachteil, daß infolge der geringen
Häufigkeit von 235U die Aktivitäten
dieser Nuklide wesentlich niedriger
sind als die von 238U und seinen Zerfallsprodukten. Die 210Pb-Methode[168] schließlich eignet sich wegen der niedrigen Halbwertszeit von
»22a nur für die Datierung von sehr
jungen Prozessen.
100
100
224Ra
0
228Th
224Ra
230Th
400
Impulse
Leistungsfähige a-Spektrometer, mit
denen es gelang, das Ionium direkt
zu bestimmen, wurden erst in den
fünfziger Jahren konstruiert. Dies
führte dann rasch zur Entwicklung
der Datierung von ozeanischen Sedimenten nach der Ioniummethode, bei
der ein Alter aus dem Überschuß von
230
Th über 238U errechnet wird[166].
200
0
100
200
300
Kanal
(Energie)
ABBILDUNG 105 a-Spektrum der U-Isotope (oberes
Diagramm) bzw. der Th-Isotope (unteres Diagramm)
eines Sinterkalkes aus der Petralona-Höhle in Griechenland; Aus 166.3g Sinterkalk wurden U und Th
chemisch abgetrennt und 23.5h bzw. 26.6h mit einem a-Spektrometer gemessen. Die chemische Ausbeute der Trennung betrug in beiden Fällen ca. 50%.
Das 2 3 4 U/ 2 3 8 U-Aktivitätsverhältnis wurde zu
1.134±0.033 bestimmt, das Aktivitätsverhältnis von
230
Th/234U zu 0.930±0.045 und die a-Aktivität von
230
Th zu 6.59±0.23 Zerfälle pro Gramm und Stunde
(umgezeichnet nach Hennig, Diss. Köln 1979)
141
Die Ungleichgewichtsmethoden
Eis von Gletschern, in Seen und den Oberflächenschichten der Ozeane wiederfindet und
natürlich auch in lebende Materie eingebaut werden kann. Sofern sich in den Materialien,
in die es eingebaut wird, kein Uran befindet, klingt es dann mit seiner Halbwertszeit von
22.26a ab und erlaubt die Datierung mancher Materialien, vorausgesetzt die Anfangsakti0
vität A210
ist bekannt oder kann aus einer Serie von zusammengehörenden Proben errech-
net werden. Da 210Pb nur einen b-Zerfall (zum 210Bi) mit einer Maximalenergie von 20KeV
macht, benutzt man zur Messung die 1.2MeV-Linie von 210Bi.
Die Basis der Altersbestimmung nach dieser Methode ist wieder das Zerfallsgesetz, diesmal
als Aktivität geschrieben:
0
A210 = A210
´ e - lt
mit A210 = Aktivität von
210
Pb
1000
0
A210
0
k e r n d e r I n i t i a l w e r t A210
durch A210 an der Oberfläche
des Kerns annähern. Aus der
Annahme einer konstanten
Niederschlagsrate
a = h/t
[dph/kg]
210 Pb-Aktivität in
Schnee der Antarktis
210 Pb-Aktivität
pro Gewichtseinheit und
= Aktivität zur Zeit der Ablagerung der Probe. Bei der Datierung von Schnee und Eis
nimmt man an, daß sich im
Zeitraum der Anwendbarkeit
dieser Methode (»100a) an
einem gegebenen Ort die mittlere jährliche Niederschlagsmenge nicht geändert hat und
der mittlere Eintrag von 210Pb
gleich geblieben ist. Dann läßt
sich in einem Schnee- oder Eis-
[GL 151]
Base Roi
Baudouin
100
a = 45±3 cm/Jahr
(70°26'S,
24°19'O)
10
a = 6±1 cm/Jahr
Südpolstation
1
0
500
1000
1500
2000
2500
3000
Tiefe in cm (umgerechnet auf Wasser)
[GL 152]
ABBILDUNG 106 Aus der Aktivität von 210Pb in Niederschlag
(h = Länge des Bohrkerns, läßt sich die Niederschlagsmenge errechnen.
h = 0 ist die rezente Oberfläche
des Eis- oder Schneekerns; t = Alter) läßt sich GL 151 dann umformulieren zu:
0
ln A210 = ln A210
- lh / a
[GL 153]
Dies ist eine Geradengleichung in den Koordinaten ln (A210) und h mit der Steigung -l/a.
Wenn die obigen Voraussetzungen erfüllt sind (Konstanz der Niederschlagsmenge und
damit konstante A210-Einbringung ins Eis), werden die Daten für einen Bohrkern tatsäch0
lich auf eine Gerade plotten, aus der man dann A210
als Achsenabschnitt für h = 0 und
über die Steigung das Alter der jeweiligen Partie des Bohrkerns ermitteln kann. Die 210PbMethode wurde z.B. verwendet, um die mittleren jährlichen Niederschlagsmengen in der
Antarktis zu bestimmen. Ein Beispiel dafür ist in Abbildung 106 gezeigt[171].
Basierend auf dem Befund, daß 210Pb aus Süß- und Meerwasser rasch (mit einer mittleren
Residenzzeit in der Größenordnung von 1a) durch bio- und geochemische Prozesse entfernt wird, hat man auch versucht, rezente Sedimentbildungen mit dieser Methode zu
datieren, jedoch zunächst mit relativ bescheidenem Erfolg[168]. Das Problem besteht darin,
daß nicht nur 210Pb aus der Atmosphäre in das Wasser eingebracht wird, sondern ein Teil
142
A. Radiogene Isotopensysteme
zusätzlich – im Wasser und im Sediment – aus dem Zerfall von
„kogenetischen“ Serie von Sedimenten (gleiches
Messung von
14.3
0
A210
226
Ra entsteht. In einer
) kann dieser Anteil jedoch durch
226
Ra ermittelt werden (z.B. [169], [170]).
Die Ionium-Methode
Bei den Prozessen der Verwitterung wird
234U
238U
das Uran im oxidierenden Milieu in den
2.483105a
sechswertigen Zustand überführt und liegt 4.513109a
2+
b
dann meist als Uranylion UO 2 (im Meer234Pa
wasser wahrscheinlich als Uranylkarbo1.18min
natkomplex) vor, während Th nur vierb
a
a
wertig in der Natur auftritt. Das hat zur
Folge, daß das Th ziemlich immobil bleibt
b
234Pa
und rasch wieder aus dem Wasser entfernt
6.7h
wird, indem es in sekundäre Minerale ein230Th
gebaut oder an authigene Minerale adsor- 234Th
biert wird. Uran hingegen gelangt in die
24.1d
7.523104a
Ozeane und bleibt über lange Zeit in gelöster Form. Das drückt sich in seiner langen
a
Residenzzeit von »5´105a im Ozeanwasser
aus, während die des Thoriums bei nur
»300a liegt, d.h. ein Th-Ion wird im Mittel
226Ra
nach 300a aus dem Wasser ausgeschieden
1622a
und in eine feste Phase eingebaut, ein U5a, 4b
Ion erst nach einer halben Million Jahren.
Daher kommt es, daß im Meerwasser relativ viel U gelöst ist (»3ppb) und nur sehr
206Pb
wenig Th (<0.0015ppb), was einem 232Th/
238
U-Verhältnis von »0.0005 entspricht,
während das Verhältnis in den Gesteinen ABBILDUNG 107 Zerfallsschema von 238U
der Erdkruste im Durchschnitt bei knapp 4
liegt[41]. Durch den Zerfall von 238U entstehen im Meerwasser die relativ langlebigen Isotope 234U und 230Th (Ionium), nach dem in Abbildung 107 gezeigten Schema[172]. Aus dem
230
Th/232Th-Verhältnis der Ozeane läßt sich abschätzen, daß »1/4 des Ioniums dem Meerwasser direkt vom Land über Flüsse zugeleitet wird. Das so entstandene oder eingebrachte
Ionium wird dann rasch aus dem Meerwasser entfernt und am Meeresboden in neue Minerale (Zeolithe, Baryt, Karbonate) eingebaut oder an Detritus adsorbiert. Seine Aktivität
klingt dann mit der Halbwertszeit von »75200a ab, vorausgesetzt die Menge des in diese
Minerale eingebauten oder adsorbierten Urans ist vernachlässigbar gering. Das Alter der
Ablagerung eines marinen Sediments läßt sich mittels des Aktivitätsverhältnisses der ThIsotope A230/A232 der Mineralneubildungen errechnen. Voraussetzung dafür ist, daß beide
Th-Isotope als selbe chemische Spezies im Wasser vorliegen und in gleichen Verhältnissen
in die Minerale eingebaut werden, in denen sie im Wasser vorliegen. Außerdem muß man
von einem lokal konstanten 230Th/232Th-Verhältnis des Seewassers über mehrere 105a, der
Anwendbarkeit des Verfahrens, ausgehen. Schließlich darf das Th im Sediment nicht mobil
sein. Davon kann in der Regel ausgegangen werden; es wurde jedoch gefunden, daß das
Mutternuklid des Ioniums, 234U, im Sediment unter bestimmten Umständen mobil sein
kann[173]. Eine Schwierigkeit der analytischen Praxis ist, daß man zwei Th-Komponenten
voneinander trennen muß, nämlich den kleinen Teil, der aus dem Meerwasser entfernt
wurde und den großen Teil, der im Detritus (Feldspäte, Quarz, z.T. Tonminerale) von den
Kontinenten in die Ozeane gelangt ist. Das macht man, indem das Sediment mit heißer
HCl behandelt wird in der Hoffnung, so nur das adsorptiv gebundene Th oder Th in Mineralneubildungen herauszulösen[174].
143
Die Ungleichgewichtsmethoden
Wenn Th, aber kein U aus dem Meerwasser in authigene Minerale eingebaut oder an Detritus adsorbiert wird, klingt die Aktivität des Ioniums nach der einfachen Zerfallsgleichung
ab:
0
A230 = A230
´ e - l 230t
A230 é A230 ù
- l 230t
=ê
ú ´e
A232 ë A232 û 0
[GL 155]
Ähnlich wie bei einem Eiskern bei der
210
Pb-Methode sollte man in einem
Sedimentkern an der Sedimentoberfläche das höchste Aktivitätsverhältnis
messen ([A 230 /A 232 ] 0 ), das nach der
Tiefe zu kontinuierlich abnimmt. Definiert man die Sedimentationsgeschwindigkeit a wiederum als
log(230Th/232Th)A
Als Referenzisotop benutzt man bei der
Aktivitätsmessung 232Th, das innerhalb
der Anwendbarkeit der Ioniummethode als stabil angesehen werden
kann[175]:
[GL 154]
1
2
3
4
a = h/t
Tiefe im Bohrkern
(h = Tiefe unter der Sediment-WasserGrenzfläche), erhält man als Geradengleichung:
ABBILDUNG 108 Variabilität der 230Th/232Th-Aktivitätsverhältnisse mit der Tiefe von Sedimentbohrkernen. Typ 1 ist das normale Muster, das einer konéA ù
éA ù
lh
ln ê 230 ú = ln ê 230 ú [GL 156] stanten Sedimentationsrate entspricht. Typ 2 ist ein
ë A232 û
ë A232 û 0 a
normales Muster mit einer Änderung der SedimenWenn das hier gemachte einfache tationsgeschwindigkeit. Das konstante AktivitätsverModell gültig ist, sollten die Meß- hältnis von Typ 3 im oberen Teil des Profils wird
punkte eines Sedimentkerns in einem durch bohrende Organismen am Meeresboden erDiagramm ln[A 230 /A 232 ] – h auf eine zeugt, was eine Durchmischung der oberen cm beGerade fallen, d.h. ln[A230/A232] linear wirkt. Typ 4 schließlich zeigt an, daß 230Th durch
mit der Tiefe abnehmen. Das ist nach den Zerfall von U nachgebildet wird, bis sich das raGoldberg & Koide [174] tatsächlich oft dioaktive Gleichgewicht der Zerfallskette eingestellt
der Fall und als Fall 1 in Abbildung hat.
108 gezeigt.
Darüber hinaus gibt es jedoch Fälle, in denen genau das gegenteilige Verhalten beobachtet
wird (Fall 4). Das ist darauf zurückzuführen, daß hier Ionium durch Zerfall aus 234U in den
Sedimenten entsteht. GL 154 gilt dann offensichtlich nicht. Die Gesamtaktivität des Ioniums in der HCl-lösbaren Form setzt sich dann aus zwei Komponenten zusammen:
unsupported
supported
total
A230
= A230
+ A230
[GL 157]
unsupported
Hierin gibt A230
die Aktivität des überschüssigen Ioniums an, d.h. die nach GL 154
supported
berechnete Komponente, und A230
den Anteil, der in situ aus 234U entsteht. Die zweite
Komponente von GL 157 läßt sich aus einer vereinfachten Bateman-Gleichung für eine
„Dreierkette“ errechnen Aus der allgemeinen Formulierung der Bateman-Gleichungen GL
169, Seite 148 ergibt sich:
144
A. Radiogene Isotopensysteme
(
) (
N 230 = C238 e - l 238t + C234 e - l 234t + C230 e - l 230t + C234 e - l 234t + C230 e - l 230t
)
230
Th aus ursprünglich
Hierin beschreibt der erste Klammerausdruck die Bildung von
(t = 0) vorhandenem 238U und den Zerfall des daraus entstandenen 230Th (bis t = heute); der
zweite Klammerausdruck beschreibt dementsprechend die Bildung von 230 Th aus
ursprünglich vorhandenem 234U und den Zerfall des daraus gebildeten 230Th. Durch Einsetzen der Komponenten Ci ergibt sich:
0
0
é
l 238 l 234 N 238
l 238 l 234 N 238
N 230 = ê
e - l 238 t +
e - l 234 t
l
l
l
l
l
l
l
l
( 238 234 )( 230 234 )
238 )( 230
238 )
êë ( 234
0
0
ù é l N0
ù
l 238 l 234 N 238
l 234 N 234
+
e - l 230 tú + ê 234 234 e - l 234 t +
e - l 230 t ú
(l 238 - l 230 )(l 234 - l 230 )
(l 234 - l 230 )
úû êë (l 230 - l 234 )
úû
N ersetzt man hier durch A/l:
0
0
é
l 238 l 234 l 230 A238
l 238 l 234 l 230 A238
A230 = ê
e - l 238 t +
e - l 234 t
l
l
l
l
l
l
l
l
l
l
(
)
(
)
(
)
(
)
238
230
238
238
238
234
230
234
êë 238 234
0
0
0
ù
ù é l 234 l 230 A234
l 238 l 234 l 230 A238
l 234 l 230 A234
+
e - l 230 tú + ê
e - l 234 t +
e - l 230 t ú
l 238 (l 238 - l 230 )(l 234 - l 230 )
l 234 (l 234 - l 230 )
úû
úû êë l 234 (l 230 - l 234 )
l238 bzw. l234 lassen sich kürzen:
0
0
é
l 234 l 230 A238
l 234 l 230 A238
A230 = ê
e - l 238 t +
e - l 234 t
l
l
l
l
l
l
l
l
( 238 234 )( 230 234 )
238 )( 230
238 )
êë ( 234
0
0
0
ù
ù é l 230 A234
l 234 l 230 A238
l 230 A234
+
e - l 230 tú + ê
e - l 234 t +
e - l 230 t ú
(l 238 - l 230 )(l 234 - l 230 )
(l 234 - l 230 )
úû
úû êë (l 230 - l 234 )
Diese Gleichung läßt sich weiter vereinfachen, wenn man bedenkt, daß im Rahmen des
Anwendungsbereiches der Ungleichgewichtsmethoden l238 klein ist gegenüber l234 und
l230:
0
é l l A0
l 234 l 230 A238
A230 » ê 234 230 238 e - l 238 t +
e - l 234 t
l
l
l
l
l
(
)
234 230
234
230
234
êë
0
0
0
ù é l 230 A234
ù
l 234 l 230 A238
l 230 A234
e - l 230 tú + ê
e - l 234 t +
e - l 230 t ú
+
- l 230 (l 234 - l 230 )
(l 234 - l 230 )
úû êë (l 230 - l 234 )
úû
Daraus ergibt sich durch weiteres Kürzen und Ausklammern:
é -l t
ù
l 230
l 234
l 230
0
0
A230 » A238
e - l 234 t e - l 230 t ú + A234
e - l 234 t - e - l 230 t
êe 238 (l 230 - l 234 )
(l 234 - l 230 )
(l 230 - l 234 )
êë
úû
[
]
Da t klein ist gegen 1/l238, geht e - l 238 t gegen 0; außerdem bleibt die Aktivität von 238U konstant. Damit erhält man:
é
ù
l 230
l 234
l 230
0
A230 » A238 ê1 e - l 234 t +
e - l 230 t ú + A234
e - l 234 t - e - l 230 t
l
l
l
l
l
l
( 230 234 )
( 230 234 )
( 230 234 )
êë
úû
(
)
[GL 158]
Wenn man davon ausgeht, daß sich 234U und 238U im Meerwasser gleich verhalten und in
denselben Mengenverhältnissen in die Mineralneubildungen eingebaut werden bzw. an
Detritus adsorbiert werden, dann befindet sich 234U an oder in diesen Feststoffen im säku-
145
Die Ungleichgewichtsmethoden
laren Gleichgewicht mit
wesentlich:
238
0
U, d.h. A238 = A234
. Damit vereinfacht sich die Gleichung
é
ù
l 230
l 234
l 230
l 230
A230 » A238 ê1 e - l 234 t +
e - l 230 t +
e - l 234 t e - l 230 t ú
(l 230 - l 234 )
(l 230 - l 234 )
(l 230 - l 234 )
(l 230 - l 234 )
êë
úû
é
ù
l 234
l 230
A230 » A238 ê1 +
e - l 230 t e - l 230 t ú
(l 230 - l 234 )
(l 230 - l 234 )
êë
úû
é
ù
e - l 230 t
A230 » A238 ê1 +
l 234 - l 230 )ú
(
(l 230 - l 234 )
êë
úû
supported
A230
(
» A238 1 - e - l 230 t
)
[GL 159]
Dies, in GL 157 eingesetzt, ergibt:
unsupported
total
A230
» A230
(
)
+ A238 1 - e - l 230 t .
unsupported
Der Anteil A230
entspricht GL 154, und es resultiert:
total
A230
»
unsupported 0
A230 e - l 230 t
(
+ A238 1 - e - l 230 t
)
[GL 160]
und bei Normierung auf 232Th:
0
æ A230 ö
æA ö
æA ö
e - l 230t + ç 238 ÷ 1 - e - l 230t
» ç 230 ÷
ç
÷
è A232 ø total è A232 ø unsupported
è A232 ø
(
)
[GL 161]
Der erste Term in dieser Gleichung beschreibt das Abklingen des „überschüssigen“ Ioniums
im Sediment, der zweite das Anwachsen des Ioniums, das aus dem Zerfall von 234U bzw.
letztlich aus 238U resultiert. Je jünger das Sediment, desto größer ist der Beitrag des ersten
Terms zur Gesamtaktivität. Sedimente mit einem Alter bis zu einigen 105a lassen sich mit
dieser Methode datieren.
Die Ionium-Methode hat insbes. in den 60-er Jahren weite Verbreitung gefunden, um Sedimentationsraten in den Ozeanen zu bestimmen.
14.4
Die 234U/238U-Methode
238
U zerfällt über die beiden kurzlebigen Zwischenprodukte 234Th und 234Pa in 234U. Man
sollte erwarten, daß wegen der Kürze dieser Zeit keine Trennung der beiden U-Isotope
erfolgt, d.h. daß sie stets im säkularen Gleichgewicht vorliegen. Tatsächlich tritt im sedimentären Bildungsbereich häufig eine Trennung auf. Normalerweise ist das Verhältnis
A234/A238 von Süß- und Meerwasser sowie von sekundären U-haltigen Mineralen >1. Es
muß also bei der Verwitterung von Gesteinen Bedingungen geben, die in der Lage sind,
vorzugsweise 234U aus den primären (magmatischen oder metamorphen) Mineralen herauszulösen. Zur Erklärung dieses Phänomens gibt es drei durch Experimente erhärtete
Modelle, die in Abbildung 109 zusammengestellt sind (nach [164]). Das chemische Modell
geht davon aus, daß die primären Minerale Uran in seiner vierwertigen Form enthalten.
Beim a-Zerfall erleidet der 234Th-Kern einen Rückstoß, der zu einem teilweisen Abstreifen
der Elektronenhülle führt. Dadurch kann es zu einer Oxidation kommen, und nach dem
Zerfall von 234Pa liegt das Uran als 234U6+ vor, das durch Wasser bevorzugt aus dem Mineral
als Uranylion herausgelöst werden kann[176]. Nach einer zweiten Vorstellung wird das
234
Th durch den a-Rückstoß aus dem Kristall herausgeschossen und kann durch zirkulierende Wässer als 234Th, 234Pa oder 234U von den Mineraloberflächen gelöst werden[177]. Es
146
A. Radiogene Isotopensysteme
versteht sich von selbst, daß dieser Effekt auf Grund der geringen Reichweiten des Rückstoßes nur für Mineralpartien sehr nahe der Oberfläche Bedeutung haben kann und demnach
für Gesteine mit sehr geringen Korngrößen einen erheblich größeren Beitrag liefern kann
als für grobkörnige Gesteine. Das trifft analog für das dritte Modell zu. Danach können
durch einen a-Zerfall von 239Pu, das eine unwesentlich höhere Zerfallsenergie hat als 238U,
bis zu 104 Atome aus einem Kristallgitter „herausgesprengt“ und von zirkulierenden Wässern aufgenommen werden[178]. Eine Ätzung der a-Spuren durch Wasser[177] scheint dagegen keine Rolle zu spielen.
Als Konsequenz dieser Effekte gelangt also 234U bevorzugt über 238U ins Wasser der Flüsse
und Seen und dann letztlich in die Ozeane. Aus dem Meerwasser wird das Uran wesentlich
langsamer entfernt als das Th (siehe voriges Kapitel). Unter reduzierenden Bedingungen
wird es an Detritus adsorbiert und in neue Minerale – vor allem Karbonate – eingebaut. In
den Sedimenten klingt dann die überschüssige Aktivität des 234U mit seiner Halbwertszeit
von »2.48´105a ab, so daß sich bei der Alterung der Sedimente nach einigen 106a wieder
radioaktives Gleichgewicht einstellt.
„Rückstoßoxidation“
a-Rückstoß in die
wäßrige Phase
Lösung aus aRückstoßspuren
238U4+
a
ABBILDUNG 109
234U6+
Modelle zur Erklärung der Trennung von 234U und 238U
Das Verhältnis A234/A238 kann benutzt werden, um Karbonate zu datieren, vor allem
marine biogen gebildete. Die Gesamtaktivität des 234U eines solchen Karbonats setzt sich
aus zwei Komponenten zusammen:
supported
unsupported
total
A234
= A234
+ A234
supported
A234
[GL 162]
234
In dieser Gleichung steht
für die Aktivität des
U im säkularen Gleichgewicht
unsupported
238
mit U, und A234
ist der gemessene überschüssige Anteil, dessen Aktivität natürlich
nach dem einfachen Zerfallsgesetz
unsupported
A234
=
unsupported
0
A234
e - l 234t
abklingt. Die initiale Aktivität beim Einbau in das betrachtete Mineral
berechnet sich nach:
unsupported
0
A234
=
total
0
0
A234
- supported A234
[GL 163]
unsupported
0
A234
[GL 164]
wobei wegen der Voraussetzung des säkularen Gleichgewichtes
supported
supported
0
A234
= A234
= A238
[GL 165]
ist. Mit GL 165 in GL 164 eingesetzt, erhält man:
unsupported
0
A234
=
total
0
A234
- A238 ,
und dies in GL 163 eingesetzt ergibt:
unsupported
A234
=
(
total
)
0
A234
- A238 e - l 234t
[GL 166]
147
Die Ungleichgewichtsmethoden
Mit GL 165 und GL 166 in GL 162 eingesetzt ergibt sich schließlich:
total
A234
= A238 +
(
total
)
0
A234
- A238 e - l 234t
[GL 167]
Schließlich dividiert man beide Seiten noch durch A238 und erhält:
total
A234
= 1+
A238
bzw.
(
total
0
- A238
A234
A238
)e
- l 234t
total
0
æ total A234
ö
A234
= 1+ ç
- 1÷ e - l 234t
A238
è A238
ø
[GL 168]
Aus der Gleichung liest man ab, daß man zur Datierung nach dieser 234U/238U-Methode die
0
initiale totale Aktivität von 234U benötigt bzw. das Verhältnis total A234
A238 . Für Süßwasserkarbonate wird dieses Verhältnis i.a. nicht bekannt sein und lokal stark schwanken kön0
nen. Dagegen hat es sich das total A234
A238 des Meerwassers sowohl zeitlich als auch örtlich mit »1.15 als sehr konstant erwiesen und ermöglicht insbesondere für Korallen
verläßliche Datierungen bis herauf zu knapp 106a[179]. Dagegen sind Mollusken oft ungeeignete Datierungsobjekte, weil ihre Schalen nach der Sedimentation noch U aufzunehmen pflegen[180].
14.5
Die 230Th/234U- und 234U/238U-Methoden
Verläßlicher als die 234U/238U-Methode der Datierung ist die 230Th/234U-Methode. Die
Ionium-Methode gründet sich auf den Aktivitätsüberschuß von 230Th in detritischen Sedimenten und Mineralneubildungen wie Zeolithen oder Baryt am Meeresboden. Komplementär dazu findet man in marinen, aber auch vielen kontinentalen Kalken einen 230ThUnterschuß. Karbonate, die aus Wasser gefällt werden, sind bei ihrer Bildung oft praktisch
frei von 230Th, können jedoch einige ppm U enthalten. Bei ihrer Alterung baut sich dann
die Aktivität von 230Th auf, bis nach wenigen 106a das säkulare Gleichgewicht hergestellt
ist. Für Alter bis »106a lassen sich dann Karbonate nach der 230Th/234U-Methode datieren.
Die zur Altersbestimmung notwendigen Gleichungen lassen sich aus den Bateman-Gleichungen ableiten, die den radioaktiven Zerfall im Ungleichgewicht beschreiben. Die allgemeine Form der Bateman-Gleichung lautet:
N n = C1 e - l1t + C2 e - l 2t + ¼ + Cn e - lnt
mit C1 =
[GL 169]
l1 l2 ¼ ln -1 N10
l1 l2 ¼ ln -1 N10
und C2 =
(l2 - l1 )(l3 - l1 )¼(ln - l1 )
(l1 - l2 )(l3 - l2 )¼(ln - l2 )
usw. Hierin ist N10 die Zahl der Atome des Ausgangsnuklids der Zerfallskette (in unserem
Fall von 238U) zur Zeit der Bildung des Minerals oder Gesteins. Nn ist das letzte betrachtete
Nuklid der Zerfallskette (in unserem Fall 230Th) zur Zeit der Messung, die l’s sind die entsprechenden Zerfallskonstanten und t das Alter des Minerals oder Gesteins. Bei t = 0 sind
N 20 , N 30 , … N n0 = 0. Für die Zerfallskette von 238U Þ 234U Þ 230Th können die kurzlebigen
Zerfallsprodukte 234Th und 234Pa aus der Betrachtung herausgelassen werden, weil ihre
Aktivität stets im säkularen Gleichgewicht mit der von 238U steht.
Für die Zahl der zur betrachteten Zeit t vorhandenen Atome von 234U, die aus 238U seit der
Bildung des Minerals oder Gesteins entstanden sind, gilt dann:
234
und daraus:
148
U=
l 238 238 U 0 - l238t l 238 238 U 0 - l234t
e
+
e
l 234 - l 238
l 238 - l 234
[GL 170]
A. Radiogene Isotopensysteme
234
l 238 238 U 0 - l238t
e
- e - l234t
l 234 - l 238
(
U=
)
[GL 171]
War zur Bildungszeit (t =0) bereits „initiales“ 234U vorhanden, klingt dies nach der gewöhnlichen Zerfallsgleichung ab:
234
unsupported
Uinitial = 234 Uunsupported = 234 U 0
und die Gesamtzahl der Atome
beiden letzten Gleichungen:
234
234
Utotal =
(
234
234
´ e - l234t
[GL 172]
U zur Zeit der Messung ergibt sich aus der Summe der
Utotal = 234 Uunsupported + 234 U supported
unsupported
U0
é l 238 U 0 - l t
ù
´ e - l234t + ê 238
e 238 - e - l234t ú
ë l 234 - l 238
û
)
(
)
[GL 173]
Führt man Aktivitäten A = l N anstelle der Zahlen von Atomen ein, dann wird daraus:
Atotal æ
=ç
l 234
è
234
234
unsupported
A0
l 234
ö é 238 A0
ù
´ e - l234t ÷ + ê
e - l238t - e - l234t ú
ø ë l 234 - l 238
û
(
)
l238 ist klein gegenüber l234 und kann somit entfallen; im Zeitraum der Anwendbarkeit der
Methode (»106a) geht e - l 238t gegen e0=1 und 238A0 = 238A (konstant):
Atotal æ
ȍ
l 234
è
234
234
234
unsupported
A0
l 234
unsupported
Atotal » 234A0
ö é 238 A0
ù
´ e - l234t ÷ + ê
1 - e - l234t ú
ø ë l 234
û
(
(
´ e - l234t + 238A0 ´ 1 - e - l234t
)
)
[GL 174]
Aus GL 169 folgt für die Zahl der zur betrachteten Zeit t vorhandenen Atome von 230Th, die
aus 238U seit der Bildung des Minerals oder Gesteins entstanden sind:
230
Th(aus 238U ) =
l 238 l 234 238U 0
l 238 l 234 238U 0
e - l238t +
e - l234t
(l234 - l238 )(l230 - l238 )
(l238 - l234 )(l230 - l234 )
l 238 l 234 238U 0
e - l230t
+
(l238 - l230 )(l234 - l230 )
[GL 175]
daraus:
230
é
e - l238t
e - l234t
U0 ê
+
êë (l 234 - l 238 )(l 230 - l 238 ) (l 238 - l 234 )(l 230 - l 234 )
ù
e - l230t
+
(l238 - l230 )(l234 - l230 ) úúû
Th(aus 238U ) = l 238 l 234
238
[GL 176]
Lag zur Zeit der Bildung der Minerale oder Gesteine auch bereits 234U vor, so ergibt sich für
dessen Berechnung zur Zeit t eine GL 171 analoge Formel:
230
Th (aus
234
Uunsupported ) =
l 234 234 U 0 - l234t
e
- e - l230t
l 230 - l 234
(
)
[GL 177]
Lag auch noch eine Anfangsmenge an 230Th vor, so klingt diese nach einer GL 172 analogen Formel ab:
149
Die Ungleichgewichtsmethoden
Thunsupported =
230
230
unsupported
Th 0
´ e - l230t
Die Gesamtzahl der zur Meßzeit vorhandenen Atome von
Summation von GL 176, GL 177 und GL 178:
230
Thtotal =
230
Th(aus 238U ) +
230
Th(aus 234U ) +
[GL 178]
230
Th erhält man dann aus der
230
Thunsupported
[GL 179]
also:
é
e - l238t
e - l234t
U0 ê
+
êë (l 234 - l 238 )(l 230 - l 238 ) (l 238 - l 234 )(l 230 - l 234 )
ù l 234 234 U 0 - l t
e - l230t
unsupported
+
+
e 234 - e - l230t + 230 Th 0
´ e - l230t
(l238 - l230 )(l234 - l230 ) úúû l230 - l234
230
Thtotal = l 238 l 234
238
(
[GL 180]
)
Auch hier lassen sich wieder die Aktivitäten A = l N einführen:
é
e - l238t
e - l234t
A0 ê
+
êë (l 234 - l 238 )(l 230 - l 238 ) (l 238 - l 234 )(l 230 - l 234 )
234
230 unsupported
ù
e - l230t
A0
A0
+
e - l234t - e - l230t +
´ e - l230t
ú+
l 230
(l238 - l230 )(l234 - l230 ) úû l230 - l234
230
Atotal
= l 234
l 230
238
(
)
und durch Multiplikation mit l230:
é
e - l238t
e - l234t
A0 ê
+
êë (l 234 - l 238 )(l 230 - l 238 ) (l 238 - l 234 )(l 230 - l 234 )
.
ù l 230 234 A0 - l t
e - l230t
- l 230t
- l 230t
230 unsupported
234
+
+
e
-e
+
A0
´e
(l238 - l230 )(l234 - l230 ) úúû l230 - l234
230
Atotal = l 230l 234
238
(
)
Auch in diesem Fall lassen sich wieder Vereinfachungen vornehmen, weil l 238<<l 234, l 230
-l t
sowie e 238 »1:
230
é
ù
e - l234t
e - l230t
1
A0 ê
+
+
ú
êë l 234 l 230 ( -l 234 )(l 230 - l 234 ) ( -l 230 )(l 234 - l 230 ) úû
l 234 A0 - l234t
unsupported
e
´ e - l230t
+ 230
- e - l230t + 230A0
l 230 - l 234
Atotal » l 230l 234
238
(
)
und daraus durch weiteres Ausmultiplizieren:
230
Atotal »
é
l e - l234t
l e - l230t ù
A0 ê1 - 230
+ 234
(l230 - l234 ) (l230 - l234 ) úúû
êë
l 234 A0 - l234t
unsupported
´ e - l230t
+ 230
- e - l230t + 230A0
e
l 230 - l 234
238
(
[GL 181]
)
Im Fall der Datierung von Karbonaten ist der letzte Term dieser Gleichung oft vernachlässigbar klein (kein 230Th zur Zeit ihrer Bildung); damit erhält man vereinfacht:
230
Atotal »
é
l e - l234t
l e - l230t ù l 230 234 A0 - l234t
A0 ê1 - 230
+ 234
e
- e - l230t
ú+
l
l
l
l
l
l
( 230 234 ) ( 230 234 ) úû 230 234
êë
238
(
)
[GL 182]
Das 230Th/234U-Aktivitätsverhältnis ergibt sich aus der Division von GL 182 und GL 174:
150
A. Radiogene Isotopensysteme
238
230
Atotal
»
234 total
A
é
l e - l234t
l e - l230t ù l 230 234 A0 - l234t
A0 ê1 - 230
+ 234
+
e
- e - l230t
(l230 - l234 ) (l230 - l234 ) úúû l230 - l234
êë
234 unsupported
A0
´ e - l234t + 238A0 ´ 1 - e - l234t
(
(
)
)
Schließlich dividiert man noch Zähler und Nenner auf der rechten Seite der Gleichung
durch 238A0 º 238A:
234
A0
238
é
ù
l 230e
l e
A0 - l234t
+ 234
e
- e - l230t
ê1 ú+
l
l
l
l
l
l
(
)
(
)
ê
230
234
230
234
230
234 ú
û
» ë
234
A0
´ e - l234t + 1 - e - l234t
238
A0
- l 234t
230
Atotal
234 total
A
l 230
- l 230t
(
(
)
[GL 183]
)
Ein Spezialfall ergibt sich, wenn 234A0/238A0 = 1 ist:
230
Atotal
234 total
A
é
l 230e - l234t
l 234e - l230t ù
l 230
1
+
e - l234t - e - l230t
ê
ú+
l
l
l
l
l
l
(
)
(
)
ê
230
234
230
234
230
234 ú
û
» ë
- l 234t
- l 234t
+ 1- e
e
(
(
)
)
Atotal é
l 230e - l234t
l 234e - l230t ù æ l 230e - l234t
l 230e - l230t ö
»
1
+
+
ê
ú
ç
234 total
A
(l230 - l234 ) (l230 - l234 ) úû è l230 - l234 l230 - l234 ÷ø
êë
230
230
234
Atotal
l e - l230t
l e - l230t
» 1 + 234
- 230
total
l 230 - l 234 l 230 - l 234
A
Atotal
e - l230t
»
1
+
(l - l230 )
234 total
l 230 - l 234 234
A
230
230
Atotal
=
234 total
A
230
Atotal
» 1 - e - l230t
238 total
A
[GL 184]
Diese Gleichung entspricht GL 159, Seite 146 und gibt das Aktivitätsverhältnis von 230A/
238
A für den Fall an, daß 234U mit 238U zur Zeit des Einbaus in ein Mineral im säkularen
Gleichgewicht stand, während kein 230Th eingebaut wurde.
Die Auswertung von GL 183 erfolgt am einfachsten graphisch. In Abbildung 110 ist A230/
A234 gegen das Alter der betrachteten Probe für verschiedene initiale Verhältnisse 234A0/
238
A0 aufgetragen. In marinen und kontinentalen Karbonaten treten nur 234A0/238A0-Verhältnisse ³1 auf. Damit besteht bis zu einem Alter von »105a fast kein Unterschied zwischen den Kurven mit 234A0/238A0 = 1 – 3, und die Auswertung kann mit guter Näherung
nach GL 184 erfolgen. Die Altersbestimmung nach GL 183 erfordert zudem eine Abschätzung des 234A0/238A0-Verhältnisses. Dazu löst man GL 174, Seite 149 nach 234A0/238A auf
und setzt ein Alter ein, das man nach GL 184 berechnet. Damit läßt sich aus GL 184 ein
verbesserter Alterswert berechnen. Durch weitere Iteration erhält man bereits einen Alterswert mit einer Genauigkeit von ±1%, was wesentlich besser ist als die analytische Präzision[164].
Die Erfolge dieser 230Th/234U (und der hier nicht eigens behandelten 230Th/238U-Methode
liegen in Beiträgen zur Klimageschichte des Quartärs, abgeleitet aus marinen Karbonaten
(insbes. Korallen[161],[181],[182]) und terrestrischen Kalken (v.a. Sinter[164],[183]).
151
Die Ungleichgewichtsmethoden
1.2
3.0
2.0
1.0
1.0
1.5
0.
5
230Th/234U
0.8
0.6
0.4
Die Zahlen geben die
initialen Verhältnisse
234U/238U an.
0.2
0.0
4
10
2
3
4
5
6 7 8 9
5
10
2
3
4
5
6 7 8 9
6
10
t [a]
ABBILDUNG 110
14.6
Auftragung von GL 183 gegen die Zeit für verschiedene Verhältnisse von
234
U/238U
238
U–230Th-Ungleichgewichte in Vulkaniten
In der zweiten Hälfte der sechziger Jahre fand man heraus, daß in jungen Vulkaniten die
Zerfallsprodukte von 238U (ab 230Th) oft nicht im säkularen Gleichgewicht mit ihrem Mutternuklid stehen[184],[185]. Die Ursache dieser Ungleichgewichte ist jedoch Gegenstand kontroverser Diskussionen. Eine Schule schreibt sie Fraktionierungsprozessen bei der partiellen
Aufschmelzung zu, die auf einer unterschiedlichen Inkompatibilität von Th und U beruhen. Eine andere Schule sieht in den Ungleichgewichten vornehmlich Anzeichen sekundärer Veränderungen, z.B. durch Isotopenaustausch mit Seewasser oder durch Assimilation
von Fremdgestein bei der Magmenentwicklung. Junge Vulkanite weisen typischerweise Aktivitätsverhältnisse von 230Th/238U, 226Ra/238U oder sogar 210Pb/238U ³1 auf. Der Aktivitätsüberschuß an 210Pb scheint sich jedoch stets auf Aufnahme dieses kurzlebigen Isotops aus
See- oder Grundwasser zurückführen zu lassen[186]. Von besonderer Bedeutung ist das Aktivitätsverhältnis von 230Th zu 238U, das man versucht zu benutzen, um Prozesse der Bildung
und Entwicklung von sich aus dem Erdmantel ableitenden Magmen zu verfolgen. Außerdem eröffnet dieses Ungleichgewicht die Möglichkeit, junge Vulkanite zu datieren oder die
152
A. Radiogene Isotopensysteme
Zeit zwischen Magmenbildung und Extrusion zu ermitteln. Grundlage dafür ist Gleichung
GL 161, die bei der Besprechung der Ionium-Methode abgeleitet wurde:
0
æ A230 ö
æA ö
æA ö
» ç 230 ÷
e - l 230t + ç 238 ÷ 1 - e - l 230t
ç
÷
è A232 ø total è A232 ø unsupported
è A232 ø
Th / U:
4
)
[GL 161]
3
2
1.5
Gesamtgestein
1.5
Mineral 2
„E
q
(t® uil
in
¥ e“
)
2
230Th/232Th
Hierin beschreibt der
erste Term den Zerfall
des überschüssigen (=
bei t =0 vorhandenen) 230Th, der zweite
Term die Nachbildung von 230 Th aus
dem Zerfall von 238U.
(
Mineral 3
Mineral 1
Allègre[187] (1968) hat
darauf aufmerksam
t1
gemacht, daß diese
Gleichung analog der
tAnfang
initiales
Isochronenglei230Th/232Th
chung bei anderen
1
Isotopensystemen
„Equipoint“
benutzt
werden
kann, um das Alter
einer kogenetischen
Suite von Vulkaniten
0.5
oder durch eine
0.5
1
1.5
2
interne (= Mineral-)
238U/232Th
Isochrone das Eruptionsalter eines Vulkanits zu bestimmen, ABBILDUNG 111 Prinzip der Datierung junger Vulkanite nach der 238U–
wenn man A230/A232 230Th-Ungleichgewichtsmethode
(y) gegen A 238 /A 232
(x) aufträgt. Vorausgesetzt muß bei der Anwendung dieser Gleichung werden, daß bei t=0
die beiden Th-Isotope im Magma im chemischen Gleichgewicht gewesen sind, d.h. daß
alle Vulkanite einer Suite oder alle Minerale eines Vulkanits dasselbe initiale 230Th/232ThVerhältnis hatten. Außerdem muß bei t = 0 säkulares Gleichgewicht zwischen 234U und
238
U vorgelegen haben. Diese Voraussetzung läßt sich leicht durch Messung von A234/A238
überprüfen. Obwohl es als ziemlich wahrscheinlich gilt, daß bei der Magmenbildung die
beiden U-Isotope im säkularen Gleichgewicht vorlagen, findet man bei ozeanischen Basalten oft Werte von A234/A238 zwischen »1.00 und 1.15. Das gilt als Anzeichen für eine Reaktion dieser Basalte mit Seewasser, das ja global ein A234/A238 von »1.15 aufweist. Frische
Gläser ozeanischer Basalte zeigen dagegen keine Anzeichen sekundärer Veränderung und
eignen sich deshalb für A230/A238-Ungleichgewichtsuntersuchungen besonders gut. Über
den Zeitraum der Anwendbarkeit dieser Methode (einige 105a) können 238U und 232Th wieder als stabil betrachtet werden. Im A230/A232 – A238/A232-Isochronendiagramm hatten also
zur Zeit der Bildung (t = 0) eines Vulkanits alle seine Minerale dasselbe A230/A232, aber, als
Folge der geringfügig unterschiedlichen Geochemie, verschiedene U/Th-Verhältnisse
(siehe Abbildung 111[172]). Für t =0 wird e - l 230t = 1 und 1 - e - l 230t = 0, also
(
)
A230/A232 = (A230/A232)0.
153
Die Ungleichgewichtsmethoden
„E
qu
ili
ne
“
230Th/232Th
Bei der Alterung des Gesteins
ändern sich dann die A 230 /
2.0
Andesit CA2
Magnetit
A232-Verhältnisse seiner Kom(Costa
Rica)
ponenten; bei niedrigem U/
a
Th-Verhältnis überwiegt in GL
6K
1
161 die erste Komponente, also
0«
1.5
11
230
=
der Zerfall von
Th, als dest
sen Folge A230 /A232 sinkt; bei
Gesamtgestein
Komponenten mit hohen U/
Plagioklas
Th-Verhältnissen überwiegt die
1.0
Hypersthen
Nachbildung von 230 Th aus
238
Augit
U und führt zu einer Erhöhung des Verhältnisses A 230 /
A232. Mit zunehmendem Alter
0.5
rotiert die Isochrone dabei um
einen Punkt, den sogenannten
equipoint. Bei einem Alter des
Gesteins von »10 6 a hat die
0
0
0.5
1
1.5
2
2.5
Isochrone ihre Endposition
238U/232Th
erreicht mit einer Steigung von
1, d.h. 230Th und 238U sind wieder im säkularen Gleichge- ABBILDUNG 112 Beispiel einer Ungleichgewichtsdatierung
wicht. Für t³106a geht e - l 230t eines Vulkanits
gegen 0 bzw. 1 - e - l 230t gegen 1; damit ergibt sich:
(
)
A230/A232 = A238/A232 Þ A230 = A238.
230
238
1.4
MAR, 30°N
FAMOUS
1.2
Island
230Th/232Th
Diese Gerade für t®¥, auf der
also A230/A232 = A238/A232 ist,
nennt man equiline. Das
Gesamtgestein braucht keinesfalls mit dem equipoint
zusammenzufallen. Dieses Isochronensystem verhält sich
also völlig anders als Isochronen in anderen Isotopensystemen, in denen das auf der
Ordinate aufgetragene Verhältnis (z.B. 87Sr/86Sr) in allen
Komponenten des Gesteins
anwächst.
Afar
1.0
Réunion
0.8
Tristan da Cunha
Im Th/ U-System läßt sich
aus der Steigung der Isochronen das Alter des Gesteins
0.6
ebenso errechnen wie bei den
übrigen Systemen; die Steigung entspricht dem Ausdruck
0.703
0.704
0.705
1 - e - l 230t . Der Schnittpunkt
87Sr/86Sr
der Isochronen mit der Ordinate entspricht (A230/A232)0 ´
ABBILDUNG 113 Korrelation zwischen Th- und Sr-Isotopen in
e - l 230t . Nachdem t aus der
ozeanischen Basalten
Steigung errechnet wurde, läßt
(
154
)
A. Radiogene Isotopensysteme
sich daher das initiale A230/A232 errechnen. Abbildung 112 zeigt das Beispiel einer solchen
Isochrone für einen Andesitstrom und dessen Minerale aus Costa Rica, für den sich ein
Alter von 110Ka ergibt[188].
„E
qu
ili
ne
“
230Th/232Th
Wie bereits eingangs erwähnt,
1.6
findet das 230Th/238U-System,
bei 20°S
ähnlich wie z.B. Rb-Sr oder
Basalte vom East
20–23°N (Basaltgläser)
Sm-Nd, Anwendung als geoPacific Rise:
20–23°N (sonstige
1.5
chemischer Tracer zur VerfolBasalte)
gung der Magmenevolution.
So fanden Allègre und Mitar1.4
beiter Anhaltspunkte für eine
Korrelation zwischen A230/A232
und 87 Sr/ 86 Sr für ozeanische
1.3
und kontinentale Basalte (Abbildung 113, umgezeichnet
nach Daten in[172]), die unge1.2
fähr der zwischen den Nd- und
Sr-Isotopen entspricht. Hohes
A230/A232 ist dabei mit niedrigem 87 Sr/ 86 Sr gekoppelt. Die
1.1
wahrscheinlichste Erklärung
für diese Antikorrelation ist,
daß die Quellregionen der Ba1.0
salte im Erdmantel im radioak0.6
0.7
0.8
0.9
1
1.1
1.2
1.3
1.4
tiven Gleichgewicht sind, d.h.
238U/232Th
daß das Verhältnis A 230 /A 232
das Aktivitätsverhältnis 238U/
232
Th, also auch das Element- ABBILDUNG 114 Th-U-Isotopen(un)gleichgewichte in Basalverhältnis U/Th widerspiegelt. ten des East Pacific Rise
Daraus ergibt sich eine Verweilzeit der Magmen im flüssigen Zustand zwischen partieller Aufschmelzung und Extrusion, die klein ist gegen die Halbwertszeit von 230Th (maximal einige 103a). Damit folgt aus
der Antikorrelation zwischen Th- und Sr-Isotopen auch eine Antikorrelation von U/Th und
Rb/Sr in den Quellregionen. Nach kristallchemischen Erwägungen sollte Th4+ für Minerale
in basischen und ultrabasischen Gesteinen inkompatibler sein als U4+. Diese Überlegung
wird durch die Antikorrelation von Th- und Sr-Isotopen bestätigt. Wenn man in obigem
Diagramm den Schnittpunkt zwischen Korrelationslinie und bulk-earth-87Sr/86Sr auf die
Ordinate projiziert, ergibt sich ein A230/A232 von 0.86. Weil geschlossen wurde, daß im Erdmantel säkulares Gleichgewicht für die 238U-Zerfallskette herrscht, gilt
A230 = A238 Þ A230/A232 = A238/A232
A230 N 238 l238
=
´
A232 N 232 l232
N 232 A232 l238
=
´
N 238 A230 l232
N 232
1
1.55125 ´ 10 -10
=
´
= 3.65
N 238 0.86 4.9475 ´ 10 -11
Dies entspricht also einem Wert, den man auch für die Erde annimmt.
Die Analyse von Basalten aktiver Zentren ozeanischer Rücken (d.h. Basalte mit Alter t = 0)
hat z.T. ein 230Th/238U-Ungleichgewicht, z.T. aber auch ein Gleichgewicht ergeben und
damit für eine kontroverse Diskussion darüber gesorgt, wie sich solche Ungleichgewichte
155
Die Ungleichgewichtsmethoden
wohl erklären lassen. So haben Newman et al.[189] für frische Basaltgläser des East Pacific
Rise, von denen sie sekundäre Veränderungen glaubten, ausschließen zu können, Daten
erhalten, die links neben die equiline plotten, für die also A230/A238>1 ist (Abbildung 114).
Wenn dieses Ungleichgewicht nicht auf sekundäre Veränderungen der Basalte zurückzuführen ist und wenn im Erdmantel säkulares Gleichgewicht der 238U-Zerfallskette herrscht,
dann heißt das, daß sich bei der partiellen Aufschmelzung des Erdmantels Th inkompatibler verhielt als U, so daß 230Th über seine Gleichgewichtsaktivität mit 238U in die Schmelze
eintrat. Dies stimmt mit experimentellen Daten überein, wonach Ca-arme Klinopyroxene,
die nahe des Peridotitsolidus stabil sind, trotz niedriger Verteilungskoeffizienten für U und
Th tatsächlich A230/A238-Verhältnisse von bis ca. 1.35 erzeugen können[190], Werte, die mit
dem beobachteten maximalen 230Th-Überschuß von MORB gut übereinstimmen (Abbildung 115[191]). Durch ein Modell des dynamischen Aufschmelzens, bei dem die Aufschmelzung sich über einen beträchtlichen Tiefenbereich beim Aufstieg von Erdmantel vollzieht,
lassen sich diese Ungleichgewichte trotz großer Schmelzgrade modellieren, und der
gesamte Aufschmelzvorgang kann sich im Stabilitätsbereich von Spinellperidotit vollziehen[190]; Granat scheint nicht unbedingt notwendig zu sein, wie zunächst angenommen[191]. Bourdon et al. (1996)[191] beobachteten, daß der Überschuß an 230Th über die
Gleichgewichtsaktivität mit abnehmender Tiefe der mittelozeanischen Rücken sinkt
(Abbildung 115). Ein flach liegender Rücken bedeutet große Magmenproduktionsraten
und einen entsprechend heißen Mantel, so daß große 230Th-Überschüsse mit einem tiefen
Beginn der Aufschmelzung gekoppelt sind.
1.4
1.4
A230Th/238U
a
1.3
1.3
1.2
1.2
1.1
1.1
1.0
1.0
0.9
0.9
0
1000
2000
3000
axiale Tiefe [m]
ABBILDUNG 115
4000
AAD
EPR 9–10°N
MAR 37°–40°N
Gorda
Juan de Fuca
MAR bei 30°N
Tamayo-Rift
Tamayo-Swell
b
5000
a-spektrometrische Daten:
EPR
0
1000
2000
3000
axiale Tiefe [m]
4000
5000
N-MAR
Island
OsterinselMikroplatte
Aktivitätsverhältnisse 230Th/238U von ozeanischen Rückenbasalten[191], links
einzelne Daten, rechts über Rückensegmente gemittelt als Funktion der Tiefe der Rücken unter dem Meeresspiegel. Die Kurve in der rechten Abbildung
entspricht einem Modell aufsteigenden Mantels mit einer Aufstiegsgeschwindigkeit von 2cm/a, einer Matrixporosität von 0.1% und einer Aufschmelzrate von 0.9% pro kbar. Als Verteilungskoeffizienten Peridotit/
Schmelze wurden Werte von 2.6´10-3 und 1.4´10-3 für U und Th in Granatperidotit angenommen bzw. 1.0´10-4 und 1.5´10-4 für Spinellperidotit.
AAD = australisch–antarktische Diskordanz, EPR = ostpazifischer Rücken,
MAR = mittelatlantischer Rücken.
Während MOR-Basalte auf der linken Seite (oder oberhalb) der equiline liegen, fallen die
meisten Subduktionszonenbasalte rechts (oder unterhalb) der equiline (siehe Abbildung
116[145]). Das deutet darauf hin, daß bei ihrer Entstehung sich das U inkompatibler verhält
als Th. Residuale Minerale, die Th relativ zu U zurückhalten oder sechswertig vorliegendes
U mögen Gründe dafür sein.
156
A. Radiogene Isotopensysteme
2.5
1.5
e
alt
as
MORB
n
zo
1.5
s
ion
b
en
2.0
t
k
du
b
Su
2.5
3.0
1.0
Mantelquelle
230Th/232Th
230Th/232Th
2.0
3.5
4.0
Ozeaninselbasalte
0.5
1.5
2.0
238U/232Th
2.5
3.0
Th-U-Isotopien verschiedener Typen ozeanischer Basalte
Eine interessante Beobachtung
von Krishnaswami et al. [186]
bezieht sich schließlich auf die
Basalte des Mouna Loa auf
Hawaii, für die sie einen
Anstieg des A230/A232-Verhältnisses – aber 230Th/ 238UGleichgewicht – mit dem Eruptionsalter fanden (siehe Abbildung 117). Zur Erklärung
schlagen die Autoren vor, die
verschiedenen Basaltflüsse sollten aus verschiedenen Magmenkammern abzuleiten sein.
1.6
Basaltströme auf Hawaii
1.5
Mauna Loa
Kilauea
Th/232Th
ABBILDUNG 116
1.0
230
0.5
1.4
1.3
1.2
1.1
1.0
1850
1900
1950
2000
Eruptionsjahr
ABBILDUNG 117 Mouna Loa: Korrelation zwischen
230
Th/
232
Th und dem Eruptionsjahr
157
Kosmogene Radionuklide
15.0
Kosmogene Radionuklide
g
ahlun
t
ät
ivitä
tivit
a kt
nak
nen
nne
Son
So
le
ale
ma
ni
xim
Nuklid
10
Be
14
C
26
Al
36
Cl
e S tr
TABELLE 12:
isch
osm
ek
lar
Protonen/(cm23s3MeV)
so
Kosmogene Radionuklide entstehen durch
101
Wechselwirkung der kosmischen Strahlung mit
Materie. Die kosmische Strahlung setzt sich aus
2 Komponenten zusammen. Ihr Energiespek100
trum reicht von einigen MeV bis »10 15 MeV
(siehe Abbildung 118 [192] ). Der solare Anteil
10-1
besteht vorwiegend aus Protonen, daneben aus
geringen und wechselnden Mengen an a-Teil10-2
chen sowie wenigen schwereren Teilchen. Die
maximale Energie dieses Anteil liegt um 1GeV
m
i
pro Nukleon. Seine Intensität ist Schwankun10-3
gen unterworfen, d.h. von der Sonnenaktivität
ma
abhängig (z.B. dem »11jährigen Rhythmus, der
10-4
sich in der Zahl der Sonnenflecken äußert und
der damit verbundenen Änderung des Magnetgalaktische
10-5
feldes der Sonne). Der galaktische Anteil der koskosmische
mischen Strahlung besteht zu »90% aus ProtoStrahlung
nen, 9% a-Teilchen und »1% schwereren
10-6
Teilchen mit einer mittleren Energie von
»3GeV pro Nukleon. 80% dieses Anteil liegt
10-7
unter 4GeV/Nukleon; die wahrscheinlichste
101 102 103 104 105
Energie der galaktischen Strahlung liegt zwischen 400 und 600 MeV/Nukleon. Die IntensiProtonenenergie [MeV]
tät des galaktischen Anteils schwankt zeitlich
kaum, ist jedoch dem Modulationseffekt durch ABBILDUNG 118 Energieverteilung der kosdas Magnetfeld der Sonne unterworfen. Die mischen Strahlung im Erdabstand von der
durchschnittliche Intensität der kosmischen Sonne
Strahlung beträgt im Erdabstand von der Sonne
»1.7 Teilchen (bzw. 3.1 Nukleonen) pro cm2 und sec (4p-Geometrie).
kosmogene Radionuklide mit längeren Halbwertszeiten
t1/2 [a]
1.5´106
5730
0.716´106
0.308´106
l [a-1]
0.462´10-6
0.1209´10-3
0.968´10-6
2.25´10-6
Nuklid
53
Mn
59
Ni
81
Kr
t1/2 [a]
3.7´106
8´104
0.213´106
l [a-1]
0.187´10-6
0.86´10-5
3.25´10-6
Infolge der hohen Energie der kosmischen Strahlung treten bei ihrer Wechselwirkung mit
der irdischen Atmosphäre und natürlich auch mit fester Materie im All wie Meteoriten die
verschiedensten Spallationsreaktionen auf, d.h. die hochenergetischen Primärteilchen
übertragen einem getroffenen Targetkern soviel Energie, daß das Target – also O, N oder Ar
– zerstört wird. Die Targets verlieren dabei meist mehrere Nukleonen, wodurch Kerne niedrigeren Atomgewichts entstehen. Einige dieser Spallationsprodukte sind radioaktiv und
haben Halbwertszeiten in der Größenordnung von 100 bis >106a. Bei ihrer Entfernung aus
der Atmosphäre und Eintritt in den biologischen, hydrologischen oder Gesteinskreislauf
oder mit dem Fall eines Meteoriten auf die Erde endet die Produktion dieser Nuklide, und
ihre Aktivität klingt mit ihrer Halbwertszeit ab. Wenn man die Anfangsaktivität A0 kennt,
lassen sich „Alter“ von biologischen, geologischen oder Meteoritenproben bestimmen
oder auch geologische Prozesse verfolgen. Von den in Tabelle 12 aufgeführten Nukliden
hat 14C erhebliche Bedeutung für die Archäologie, während 53Mn und 59Ni nur für die
Meteoritik wichtig sind. Für die Geowissenschaften ist vor allen Dingen 10Be von Interesse.
158
A. Radiogene Isotopensysteme
Die 14C-Methode
Obwohl diese Methode für die Geowissenschaften bedeutungslos ist, soll sie kurz besprochen werden. Dies ist die einzige Datierungsmethode, für die ihrem Erfinder, W.F. Libby*,
ein Nobelpreis verliehen wurde (für Chemie, 1960). Trotz vieler Unzulänglichkeiten bietet
diese Methode den Archäologen die sicherste Absolutdatierungsmethode der Altersbestimmung für die Zeit vor der Erfindung der Schrift oder ohne bekannte Korrelation mit unserem Kalender.
14
C wird in der hohen Atmosphäre durch eine ganze Reihe von Reaktionen gebildet, von
denen die bei weitem wichtigste die Reaktion von Stickstoff mit sekundären langsamen
Neutronen ist, die bei Spallationsprozessen frei werden:
14
N(n,p)14C
(s = 1.81b).
14
C zerfällt dann wieder mit einer Halbwertszeit von 5730a unter b–-Emission in 14N. Die
b-Maximalenergie beträgt nur 156KeV, was die Messung der Strahlung nicht gerade vereinfacht. Die Messung wurde früher mit „Schirmgitterzählern“ (screen-wall counter) durchgeführt, die ähnlich aufgebaut sind wie Geiger-Müller-Zählrohre; hierbei wird die Probe (elementarer Kohlenstoff) auf der inneren Oberfläche eines Zylinders aufgetragen, der in das
Zählrohr geschoben wird[193]. Andere Gruppen benutzten Geiger-Müller- oder Proportionalzählrohre und zählten die Aktivität des Kohlenstoffs nach Überführen in Acetylen[194]
(Die Messung von CO2 hat sich als nicht sinnvoll erwiesen, weil es nicht genügend von
Fremdgasen zu reinigen ist, die als Löschgase in den Zählrohren wirken. Seit der zweiten
Hälfte der siebziger Jahre versucht man erfolgreich, 14C-Datierungen mit BeschleunigerMassenspektrometern durchzuführen[195], was den großen Vorteil hat, daß anstatt einiger
Gramm Kohlenstoff nur noch mg-Mengen erforderlich sind. Inzwischen gibt es mehrere
14
C-Labors, die kommerziell Analysen mittels Beschleuniger-Massenspektrometrie anbieten; in Deutschland das Leibniz-Labor der Universität Kiel in dieser Richtung aktiv (http:/
/www.uni-kiel.de/leibniz/).
Durch Reaktion mit Sauerstoff
18
oder Austauschreaktionen mit
CO2 tritt 14C in den CO2-Kreislauf der Natur ein. Die Durchmi16
15.3±0.3
schung der Atmosphäre ist sehr
rasch im Vergleich zur Halb14
wertszeit, so daß man global die14
selbe CO 2 -Konzentration in
der Atmosphäre findet. Durch
12
8S 60
40
20
0
20
40
60 8N
die Photosynthese (± durch Aufgeomagnetischer
Breitengrad
nahme über die Wurzeln) wird
14
C in Pflanzen eingebaut. Von
dort gelangt es direkt oder indi- ABBILDUNG 119 Messung der spezifischen Aktivität von
14
rekt in Tiere und den Menschen, C in heutigen Pflanzen als Funktion des geomagnetiwodurch sich in aller lebenden schen Breitengrades der Erde. Diese Daten wurden
Materie (fast) dieselbe 14C-Akti- ursprünglich benutzt, um die Konstanz der spezifischen
vität findet. Mit dem Tod des Aktivität zu belegen.
Organismus endet der 14C-Einbau jedoch, und das Nuklid klingt mit seiner Halbwertszeit ab. Man braucht daher „nur“
die 14C-Aktivität beim Absterben des Organismus zu kennen, dann läßt sich aus der heute
gemessenen Radioaktivität das 14C-Alter berechnen, also:
Zerfälle pro Minute
und Gramm C
15.1
* Willard Frank Libby (1908–1980), amerikanischer Chemiker an der University of Chicago und der
University of California in Berkeley; Libby und Mitarbeiter entwickelten 1947 die 14C-Methode.
159
Kosmogene Radionuklide
A = A0 e - lt Þ t = -
1 æ A ö 1 æ A0 ö
lnç
÷
÷ = lnç
l è A0 ø l è A ø
[GL 185]
Als bester Wert für die initiale oder Sättigungsaktivität A0 eines lebenden Organismus im
C-Austauschgleichgewicht mit der Atmosphäre gilt 13.56±0.07dpm/g C
Neutronenintensität
(Counts pro Minute)
Die Geschichte der 14C-Methode
30
10 km Höhe
beginnt 1946 mit der Abschät1000
zung von Libby, daß die 14C-ProHöhenabhängigkeit der Neutronenduktionsrate in der Atmosphäre
dichte in der freien Atmosphäre bei
hoch genug sein sollte, um es in
Princeton, N.J. (8. 1. 1949)
biologischen Proben nachzuwei100
sen. 1949 zeigten Arnold & Libby[196] durch Analyse archäologischer Proben bekannten Alters,
daß deren Datierung mit 1 4 C
10
möglich ist. 1951 wiesen Anderson & Libby[197] nach, daß die spezifische Aktivität von 14C in organischen Proben global nahezu
1
konstant ist (siehe Abbildung
10
20
30 40
50
60
70
119). Das führte zu der Ableitung
Druck (cm Hg-Säule)
eines globalen Wertes für A0 von
15.3±0.5 dpm/g C. Dieser Wert ABBILDUNG 120 Durch die Wechselwirkung der kosmiwurde dann im Verlauf der fol- schen Strahlung mit der Atmosphäre entstehen Neutrogenden »10a auf den oben ange- nen, deren Konzentration in der hohen Atmosphäre begebenen Wert herunterkorrigiert, sonders hoch ist.
z.T. zumindest als Folge einer besseren Abschirmung der Meßapparatur von Untergrundstrahlung.
Die Datierungsgrenze für die 14C-Methode liegt, optimistisch geschätzt, bei »105a, also ca.
17 Halbwertszeiten. Es lassen sich so unterschiedliche Materialien wie Holz und Holzkohle,
Saatgut, Papier, Tuch, Knochen, Geweih, Karbonatschalen und -skelette von Organismen
oder auch Töpferwaren datieren.
Neutronenintensität
(Counts pro Minute)
Im Verlauf der fünfziger Jahre
1000
wurden aber auch die Tücken
Neutronenintensität in Abhängigkeit
des Verfahrens klar und die
von der geomagnetischen Breite
800
in 10 km Höhe
anfänglichen Annahmen eines global und zeitlich konstanten A0 mußten z.T. modi600
fi z i e r t
werden.
Die
Produktionsrate von 14C
400
hängt i.w. von dem durch die
kosmische Strahlung erzeugten Neutronenfluß ab. Dieser
200
ändert sich natürlich mit der
Höhe (siehe Abbildung 120)
0
10
20
30
40
50
60
70
Grad geomagnetische Breite
und erreicht ein Maximum
zwischen »12 und 15km über
Meeresspiegel. Außerdem ist ABBILDUNG 121 Infolge variabler Abschirmung der Erde
er an Nord- und Südpol we- durch das ihr Magnetfeld ist die Menge an produzierten Neugen der dort fehlenden bzw. tronen von der Breite abhängig.
stark verringerten Abschirmung durch das irdische Magnetfeld »4-mal so hoch wie am Äquator (siehe Abbildung
121, beide Diagramme aus [193]). Infolge der raschen Durchmischung der Atmosphäre
160
A. Radiogene Isotopensysteme
Zuweilen aber erregen 14C-Datierungen auch heute noch Aufsehen der
Öffentlichkeit, so z.B. im Oktober
1988, als das Turiner Grabtuch Christi von drei 14C-Laboratorien unabhängig voneinander als mittelalterliche Fälschung angesprochen
wurde.
15.2
Das 10Be
erforderliche Alterskorrektur [a]
gleichen sich die als Konsequenz des unterschiedlichen Neutronenflusses produzierten unterschiedlichen 14C-Mengen global rasch aus. Andererseits ändert sich der lokale Neutronenfluß infolge von Schwankungen in der solaren Komponente der kosmischen Strahlung
und von Änderungen der Intensität des Magnetfeldes der Erde. Das findet seine Entsprechung natürlich in einer zeitlichen Variation der 14C-Produktion. Darüber hinaus war es
Mitte der fünfziger Jahre Suess* klar, daß A0 von Holz von im 20. Jahrhundert gewachsenen
Bäumen um »2% niedriger ist als das Holz früherer Zeiten, was er auf den Ausstoß von fossilem CO 2 durch die Verfeuerung fossiler Brennstoffe in den letzten »100a zurückführte[198]. In den 1950-er und 1960-er Jahren wurden dann aber erhebliche 14C-Mengen
durch die Kernwaffenexplosionen in der Atmosphäre erzeugt. de Vries[199] beobachtete andererseits, daß A0 um 1500 und um 1700 »2% über dem „Normalwert“ (den man für ca.
1850 definiert) lag – eine Beobachtung, deren Ursache unerklärlich blieb. Als Folge all dieser Unwägbarkeiten hat man seit den 1960-er Jahren die 14C-Skala mit Hilfe der Dendrochronologie im Südwesten der USA geeicht und für die letzten »8000a Korrekturen der 14CAlter eingeführt, die bis zu 10% ausmachen (siehe Abbildung 122). Korrekturfaktoren für
höhere Alter sind naturgemäß nicht bekannt. Nicht korrigierbar sind auch probenspezifische Probleme, wie Verunreinigung von Holzkohle mit jungem Pflanzenmaterial oder CAustausch nach dem Absterben des Organismus durch Huminsäureinfiltration.
800
600
400
200
Natürliches Be besteht als einzig stabiles Isotop aus 9Be. Daneben kom0
men darin noch winzige Mengen
der beiden Radioisotope 7 Be und
10
-200
B e v o r, d i e b e i d e d u r c h
2000 1000
0
1000 2000 3000 4000
Spallationsprozesse aus Stickstoff
14 C-Alter von Hölzern
(heute)
und Sauerstoff in der hohen Atmosphäre gebildet werden. 7Be zerfällt
unter Elektroneneinfang mit einer ABBILDUNG 122 Durch den Vergleich mit Ergebnissen
Halbwertszeit von »53 Tagen in 7Li. der Dendrochronologie im Südwesten der U.S.A. hat
Auf Grund der geringen Halbwerts- man festgestellt, daß gewisse Korrekturen an 14C-Dazeit ist es allenfalls für die Meteoro- ten anzubringen sind, die wohl Schwankungen im atlogie interessant. 10Be macht einen mosphärischen Gehalt an Radiokohlenstoff zuzuschreib – -Zerfall mit einer Halbwertszeit ben sind.
von 1.5Ma nach 10B und eignet sich
daher prinzipiell sowohl zur Datierung als auch als Tracer über den Zeitraum Jungtertiär bis
rezent. Seine globale Produktionsrate liegt wahrscheinlich zwischen »0.015 und 0.03 Atomen 10Be pro cm2 und sec[200]. Meist vernachlässigbar geringe Mengen werden zusätzlich
noch in U-reichen Gesteinen gebildet durch Reaktionen wie 7Li(a,p)10Be, 9Be(n,g)10Be oder
10
B(n,p)10Be[201]. Aus der Atmosphäre wird das kosmogene 10Be rasch entfernt und gelangt
über den Niederschlag auf die feste Erdoberfläche oder in die Gewässer. In wäßriger Lösung
verhält sich Be chemisch bekanntlich ähnlich wie Al (26Al wird auf dieselbe Weise gebildet
* Hans E. Suess (1909–1993), österreichisch-amerikanischer Kosmo- und Geochemiker, Enkel des Alpengeologen Eduard Suess; H. Suess hat auch wichtige Arbeiten zum Schalenmodell des Atomkerns und zur Häufigkeit der Elemente im Sonnensystem verfaßt.
161
Kosmogene Radionuklide
– allerdings in noch niedrigeren Konzentrationen – und wird dann zusammen mit 10Be
ausgeschieden.). Seine Residenzzeit in Seewasser beträgt einige 100a [202], und es gelangt
schließlich durch Adsorption und Einbau in anorganische und organische Partikel in die
Sedimente am Meeresboden, in denen es mit seiner Halbwertszeit abklingt. Seine Konzentration in jungen marinen Sedimenten kann dann dazu benutzt werden, die zeitliche und
örtliche Variation seiner Produktionsrate zu bestimmen oder das Alter von Sedimenten zu
berechnen.
Peters[203] schloß Mitte der 1950-er Jahre auf Grund von theoretischen Überlegungen, daß
sich 10Be in der Natur finden müsse, und er sowie Arnold[204] erkannten, daß mit Hilfe von
10
Be marine Sedimente datierbar sein müßten. Versuche damit begannen bereits 1957[205].
In der einfachsten Form lassen sich Sedimentationsraten mit dieser Methode analog zur
Ionium-Methode bestimmen:
ln 10 Be = ln 10 Be 0 -
lh
a
[GL 186]
wobei a = h/t die Sedimentationsrate ist (h = Tiefe des Sediments unter Meeresboden).
Wegen der niedrigen 10Be-Konzentrationen blieben solche Versuche jedoch spärlich und
auf Materialien mit relativ hohen Be-Konzentrationen beschränkt. Selbst das Wachstum
von Mn-Knollen hat man versucht, durch 10Be zu datieren, z.B. wie Abbildung 123 zeigt,
auch durch eine Kombination von 10Be mit 26Al[206] nach der Gleichung:
26
Al æ 26Al ö - (lAl - lBe )t
=ç
÷ e
10
Be è 10 Be ø 0
[GL 187]
l Al - l Be = 0.968 ´ 10 -6 - 0.462 ´ 10 -6 = 0.506 ´ 10 -6
Al æ 26Al ö -0.506´10-6 t
=ç
÷ e
10
Be è 10 Be ø 0
4
-4
10Be
2
ln(26Al/10Be)
ln(d.p.m. pro kg Mn-Knolle)
26
0
-2
26Al
-6
-8
-10
-4
0
5
10
15
20
25
Tiefe in mm
-6
0
5
10
15
20
25
Tiefe in mm
ABBILDUNG 123
Linkes Diagramm: Zerfallsrate von kosmogenem 10Be und 26Al in einer Manganknolle aus dem Tuamotu-Archipel im Pazifik. Aus den Steigungen der
Abklingkurven errechnen sich Wachstumsgeschwindigkeiten von
2.8±0.6mm/Ma (10Be) bzw. 2.3±1.0mm/Ma (26Al). Rechtes Diagramm:
Hypothetische Abklingkurve für das Verhältnis 10Be/26Al in derselben Manganknolle. Aus der Steigung errechnet sich eine Wachstumsrate von »2mm
pro Ma
Diese Kopplung zweier kosmogener Radionuklide hat den Vorteil, daß Fluktuationen ihrer
Produktionsraten – die einander parallel verlaufen sollten – dabei herausgemittelt werden.
162
A. Radiogene Isotopensysteme
Führt man in dieser Gleichung wieder die Beziehung a = h/t ein und logarithmiert, dann
ergibt sich:
æ 26Al ö
æ 26Al ö
0.506 ´ 10 -6 ´ h
lnç 10 ÷ = lnç 10 ÷ a
è Be ø
è Be ø 0
[GL 188]
Aus der Steigung läßt sich dann eine Wachstumsrate von »2mm/Ma errechnen mit einem
initialen (26Al/10Be)0-Verhältnis von 0.0115, während die Einzelauswertungen Wachstumsraten von »2.8±0.6 (10Be) bzw. 2.3±1.0 (26Al) mm pro Ma ergaben.
In der zweiten Hälfte der 1970-er Jahre wurde die Methode der Beschleuniger-Massenspektrometrie entwickelt (z.B. Review[207]), mit der inzwischen noch Mengen von 106 Atomen
10
Be bei Verhältnissen von 10Be/9Be»10-14 gemessen werden können[201]. Allerdings hält
diese Methode in Bezug auf ihre Genauigkeit keinen Vergleich mit konventioneller
Massenspektrometrie aus (mit der man 10Be/9Be-Verhältnisse jedoch gar nicht messen
könnte). Bei den niedrigen 10Be-Gehalten von Vulkaniten sind allenfalls Werte zu erhalten,
die auf ±10% genau sind.
Subduktionszonen
ohne 10Be
Halmahera
Marianen
Sunda
0
1
2
3
310 6 Atome 10 Be
pro g Gestein
ABBILDUNG 124
diverse Basalte
ohne 10Be
MORB
Ozeaninselbasalte
Flutbasalte
(Columbia River)
0
1
2
3
310 6 Atome 10 Be
pro g Gestein
Subduktionszonenvulkanite und verschiedene Basalttypen ohne 10Be
163
Kosmogene Radionuklide
Mit Hilfe dieser Technik sind seit den achtziger Jahren Sedimente und Magmatite intensiv
analysiert worden. Tiefseesedimente scheinen nach diesen Untersuchungen mittlere 10BeKonzentrationen von (5.7±3.2)´109 Atomen pro Gramm Gestein aufzuweisen[208], etwa
eine Zehnerpotenz mehr als fluviatile Sedimente oder Böden, was sicherlich auf die langsame Sedimentationsgeschwindigkeit in der Tiefsee zurückzuführen ist und damit die
Möglichkeit, 10Be aus dem Seewasser zu extrahieren und adsorbieren oder einzubauen.
Basaltgläsern mittelozeanischer Rücken fehlen signifikante Mengen an 10Be; dadurch kann
ausgeschlossen werden, daß die Basaltschmelzen bei ihrer Extrusion am Meeresboden größere Mengen an Sedimenten assimiliert haben[209].
Alëuten
Subduktionszonen mit
Mittelamerika
10Be
Japan
Peru
0
5
10
310 6 Atome
ABBILDUNG 125
10 Be
15
23
25
pro g Gestein
Subduktionszonenvulkanite mit 10Be
10 Be
(10 6 Atome pro g Gestein)
Aufsehen erregt haben seit den frühen
24
achtziger Jahren
Be in Laven von Bogoslof (Alëuten)
10
Be-Untersuchun20
gen von Vulkaniten
Eruption von 1796
in Subduktionszonen. In Abbildungen
Eruption von 1927
16
124 und 125 sind die
Ergebnisse solcher
Untersuchungen an
12
Vulkaniten unterschiedlicher geotektonischer Stellung in
8
Histogrammform
aufgetragen[201]. Da4
nach ergibt sich, daß
Basalte der mittelozeanischen Rücken,
0
Ozeaninseln und
0
1
2
3
9
kontinentale FlutbaBe [ppm]
10
salte Be-Konzentrationen von <106 AtoABBILDUNG 126 Korrelation zwischen natürlichem Be und kosmogemen/g
Gestein
nem 10Be in Laven der Alëuteninsel Bogoslof
aufweisen. Ähnlich
164
A. Radiogene Isotopensysteme
niedrige Gehalte wurden auch in Subduktionszonenbasalten hinter dem Sunda-Graben
oder Marianengraben gemessen. Andererseits gibt es in den Alëuten und in Mittelamerika
zahlreiche Basalte und Andesite mit 10Be-Gehalten, die um eine Größenordnung oder
mehr darüber liegen. – Woran liegt das? Eine in-situ-Produktion von 10Be durch freie Neutronen oder a-Partikel durch Reaktionen wie einleitend erwähnt, ist sicherlich auszuschließen. Auch Abhängigkeiten vom Alterationsgrad der Vulkanite, die durch Aufnahme von
10
Be aus Seewasser oder Regen hätten erklärt werden können, waren nicht zu erkennen.
Daher bleibt nur eine Möglichkeit übrig, um das 10Be zu beziehen, nämlich marine Sedimente, da nur sie dieses Nuklid in ausreichend hohen Konzentrationen enthalten. Fraglich
ist allerdings der Zeitpunkt der Inkorporation von Sediment; zum einen könnten Sedimente in den Subduktionsprozeß mit einbezogen werden, zum anderen Sedimente beim
Aufstieg der Magmen in die Magmenkammern geraten und aufgeschmolzen werden. Aus
Subduktionszonenvulkaniten analysierte Einsprenglinge wiesen ebensolche Überschüsse
an 10Be auf wie die Vulkanite selbst[201]; wenn 10Be während des Magmenaufstiegs in die
Magmenkammern geraten ist, muß dies während eines Stadiums vor der Kristallisation der
Einsprenglinge geschehen sein, was zwar nicht auszuschließen ist, andererseits aber auch
nicht übermäßig plausibel erscheint. Außerdem wurde in einem detailliert analysierten
Vulkanit gefunden, daß in Gesamtgestein und Einsprenglingen eine gute Korrelation zwischen 10Be und 9Be besteht, was anzeigt, daß beide Isotope gut durchmischt sind, so daß
das 10Be nicht erst nach der Kristallisation der Einsprenglinge in das Magma geraten sein
kann[210] (siehe Abbildung 126). Die bevorzugte Vorstellung ist daher die, daß das 10Be aus
subduzierten Sedimenten stammt, auch wenn Assimilation von Sedimenten in Magmenkammern nicht mit letzter Sicherheit ausgeschlossen werden kann. Diese Erkenntnis hat
den Streit (fast) entschieden, ob Sedimente subduzierbar sind oder nicht (Abbildung
127[211]). Auf Grund ihrer geringen Dichte schien das nicht wahrscheinlich, zumal nicht
für die oberste Schicht, die auf Grund ihres jungen Alters als 10Be-Quelle erforderlich ist,
sondern es schien wahrscheinlicher, daß sie von der subduzierten Platte „abgekratzt“ wird.
Andererseits haben Subduktionszonenvulkanite oft einige Charakteristika, die sich ohne
Sedimentbeimischung nur schlecht erklären lassen; dazu gehören vor allem hohe Ba/LaVerhältnisse und radiogene Pb- und Sr-Isotopenzusammensetzungen; sie sind jedoch in
verschiedenen Subduktionszonen unterschiedlich ausgeprägt.
Alëutengraben
6.5 cm/a
Bogoslof
260
km
Lithosphäre
100km
1.5–3 cm/a
Asthenosphäre
200km
Eklogit
Asthenosphäre
300km
ABBILDUNG 127
Die pazifische Platte wird unter den Alëutenbogen subduziert. Dabei werden Sedimente in die Subduktion mit einbezogen.
165
Kosmogene Radionuklide
Wenn das 10Be tatsächlich aus subduzierten Sedimenten stammt, dann ergeben sich wichtige Implikationen nicht nur für die geochemische Entwicklung von Kruste und Erdmantel, sondern auch für die Dynamik der Subduktion. Marine Sedimente haben 10Be-Gehalte
»103-mal so hoch wie Subduktionszonenmagmen der Alëuten oder Zentralamerikas. Wenn
man einen Sedimentkomponente von <10% in den Basalten und Andesiten annimmt,
dann verbleibt als Zeitspanne zwischen Subduktion und Magmenförderung ein Zeitraum
von nicht mehr als »107a. Realistische Modellrechnungen haben gezeigt, daß der Sedimentanteil in Vulkaniten der Alëuten sehr gering sein kann (<1%), um die gemessenen
Konzentrationen an 10Be zu erklären[212]. Dabei hat sich auch – überraschenderweise –
gezeigt, daß Be sich bei Prozessen der partiellen Aufschmelzung von Erdmantel und der
Fraktionierung basischer Schmelzen als inkompatibles Element verhält, das stark dem Verhalten des Nd ähnelt.
kosmischer Staub
3.6´10-4m/a
in-situ P:
3.6´10-3m/a
3.0´10-6m/a
P: 3.5m/a
Troposphäre: 0.7m; 0.1a
1.
2.
9m
/a
Stratosphäre: 6.3m; 0.9a
Böden und jungSeen,
tertiäre Sedimente:
Flüsse:
1.3´106m;
0.5m; 3.4a
4.7´105a
gelöst:
0.1m/a
„mixed layer“:
81m; 6.7a
m
/a
Eis:
2.9´103m;
1.6´104a
3.7´10-5m/a
V
V
4m
/a
6.
V
Subduktion,
Akkretion:
Tiefsee:
2.9´103m; 285a
1.3´10-3m/a
2.0m/a 1.8m/a
Schmelzwasser:
g
ge elö
bu st
nd un
en d b
: 8 io
.4 ge
m n
/a
1.5m/a
V
ABBILDUNG 128
1
0.18m/a
terrestr.
Sedim.:
6.4m/a
Sedimente auf den
Kontinentalhängen:
1.4´107m; 2.2´106a
in-situ P:
1.2´10-3m/a
3´
10 -
nmu
trö /a
ufs
m
in A n: 2.4
ge
0.6m/a
V
in Suspension und als
kontinentale Schelfsedimente:
4.3´106m; 2.2´106a
V
in-situ P:
6.6´10-4m/a
Staub: 0.3m/a
Sedimentfracht: 1.9m/a
2.0m/a
7.5m/a
P: 7.0m/a
V1.3´10 m/a
-3
in Mn-Knollen:
3.4´10-3m/a
Tiefseesedimente:
3.4´106m; 2.2´106a
V
1.5m/a
0.03m/a
Modell des Kreislaufs von 10Be in der Natur.„P“ steht für Produktionsrate;
Boxen repräsentieren Reservoire; gekrümmte Pfeile stehen für Zerfall von
10
Be, und die übrigen Pfeile geben den Austausch von 10Be zwischen Reservoiren oder die Flüsse in ein Reservoir hinein an.
Abbildung 128 zeigt schließlich noch den Versuch einer quantitativen Abschätzung des
Be-Kreislaufs in der Natur mit Produktionsraten und Transportmengen[213]. Infolge der
kurzen Halbwertszeit von 10Be entspricht die Zerfallsrate (mit Schlangenlinien gekennzeichnet) der Produktionsrate. Mit „mixed layer“ wird die obere Schicht der Ozeane (»100
– 200m) bezeichnet, in der durch den Wind eine rasche Durchmischung erfolgt. Die Produktionsraten sind in Mol pro Jahr angegeben, die Mengen in den einzelnen Reservoiren
in Mol; der Zahlenwert dahinter steht für die Residenzzeit in Jahren.
10
166
A. Radiogene Isotopensysteme
15.3
Kosmogene Radionuklide in der Kosmochemie
Die Hauptanwendung der kosmogenen Radionuklide in der Kosmochemie ist die der
Bestimmung von „Bestrahlungsaltern“ von Meteoriten (oder der Mondoberfläche). Die
Meteorite werden als Bruchstücke größerer Körper interpretiert, insbes. der Asteroide im
Asteroidengürtel unseres Sonnensystems. Einige Meteorite stammen sehr wahrscheinlich
vom Mond; für andere (die SNC-Meteorite) wird sogar eine Herkunft vom Mars diskutiert.
Bevor die Meteoroide als Meteorite auf die Erde fielen, waren sie unterschiedlich lange Zeiten dem ungeschützten Bombardement durch die kosmische Strahlung ausgesetzt, weil sie
ja weder über eine abschirmende Atmosphäre noch über ein Magnetfeld verfügen. Beim
Durchfallen der Atmosphäre können die Meteorite durch Ablation einen wesentlichen Teil
ihrer Masse einbüßen – mehrere dm große Körper typischerweise einige cm. Die kosmogenen Radionuklide, die man in dem auf die Erdoberfläche auftreffenden Körper, also dem
Meteoriten, findet, stammen daher aus dem Innern des Meteoroiden und sind vor allem
durch den hochenergetischen Teil der kosmischen Strahlung, also die galaktische Komponente, erzeugt worden. Als grobes Maß für die Eindringtiefe der kosmischen Strahlung in
einen Meteoroiden kann man sich 1 – 2m merken.
Durch Messung der Gehalte an kosmogenen Radionukliden lassen sich zwei Arten von
Altern bestimmen, nämlich das Bestrahlungsalter, also die Zeit zwischen der Loslösung der
Meteoroide von ihrem Mutterkörper und dem Fall auf die Erde, sowie das terrestrische
Alter, also die Zeit zwischen ihrem Fall und dem Fund bzw. der Analyse.
Die Produktionsrate Ps eines Spallationsnuklids läßt sich unter Annahme einer kugelförmigen Gestalt des Meteoriten aus der Aktivierungsgleichung errechnen (übernommen aus
[214]):
Ps ( R, d ) = å å ò
i
mit
j
¥
E =0
N i s ij ( E) F j ( E, R, d )dE
[GL 189]
i = Targetnuklid
j = Teilchenart
Ni = Anzahl der Targetnuklide
sij = Wirkungsquerschnitt der Reaktion
Fj = Teilchenfluß am Probenort
E = Teilchenenergie
R = Radius des Meteoriten
d = Abschirmtiefe (unter Meteoritenoberfläche) des Targetnuklids.
Die Summierung über i erfolgt, weil ein Radionuklid aus mehreren Targetkernen entstehen
kann, und die Summierung über j, weil mehrere Teilchenarten das Radionuklid produzieren können. Aus dieser Formel geht hervor, daß die Produktionsraten von einer Reihe von
Faktoren abhängen, z.B. von der Art und Energieverteilung des erzeugenden Teilchens der
kosmischen Strahlung, der Zusammensetzung des Meteoriten, von der Intensität der kosmischen Strahlung am Ort der Meteoroidenflugbahn oder der Bestrahlungsgeometrie.
Die Intensität der kosmischen Strahlung scheint in den letzten »109a innerhalb eines Faktors 2 konstant gewesen zu sein (zitiert bei [192]). Die Bestrahlungsalter der Meteorite
machen jedoch nur einen Bruchteil dieser Zeitspanne aus. Nimmt man daher konstante
Bestrahlungsbedingungen für die Meteoroide an, dann läßt sich die induzierte Aktivität
At rad eines kosmogenen Radionuklids berechnen nach
(
At rad ( R, d ) = Asat ( R, d ) ´ 1 - e - lt rad
)
[GL 190]
167
Kosmogene Radionuklide
wobei trad das Bestrahlungsalter ist und Asat die Sättigungsaktivität, die sich einstellt, wenn
der Meteoroid einige Halbwertszeiten des betrachteten kosmogenen Radionuklids lang der
kosmischen Strahlung ausgesetzt war. In diesem letzt genannten Fall läßt sich natürlich
kein Bestrahlungsalter mehr berechnen. Prinzipiell ist Asat bei bekannter Produktionsrate
zu errechnen. Wenn das Bestrahlungsalter in der Größenordnung der Halbwertszeit des
kosmogenen Radionuklids liegt, läßt es sich aus der obigen Gleichung leicht ermitteln zu
t rad = -
At ö
1 æ
lnç 1 - rad ÷
l è
Asat ø
Die Bestrahlungsalter werden in der Regel mit Hilfe langlebiger kosmogener Radionuklide
errechnet, z.B. 10Be, 26Al oder 53Mn. Auch die Kombination von 2 Radionukliden, z.B. 53Mn
und 26Al ist vorteilhaft anwendbar. Dafür ergibt sich die Bestimmungsgleichung:
Mn æ 53 Mn ö
1 - e - l53 trad
=
´
ç 26 ÷
26
-l t
Al
è Al ø sat 1 - e 26 rad
53
[GL 191]
ein Quadrat
repräsentiert
jeweils einen
Meteoriten
0
250
53Mn-Sättigungsaktivität
ABBILDUNG 129
500
750
[dpm/kg Fe] von Steinmeteoriten
Die 53Mn-Sättigungsaktivitäten von Steinmeteoriten geben Hinweise auf ihr
Bestrahlungsalter.
Da hier das Verhältnis zweier kosmogener Radionuklide eingeht, ist diese Gleichung nur
wenig empfindlich gegenüber tiefenabhängigen Variationen der Produktionsraten. 53Mn
wird fast ausschließlich durch Spallation von Fe gebildet, 26Al aus Al und Si[214] und 10Be
aus O und/ oder Mg und/oder Si[214]. Da verschiedene Meteorite aus ein- und derselben
Klasse sich in ihrem Chemismus meist nur wenig unterscheiden, hat man für diese Klassen
Sättigungsaktivitäten für einige kosmogene Radionuklide ableiten können. Abbildung 129
zeigt 53Mn-Sättigungsaktivitäten für eine ganze Reihe von Steinmeteoriten (zusammengestellt von [214]). Selbst innerhalb dieser diversen Gruppe schwanken die Asat-Werte nur
relativ wenig; und selbst ohne weitere Aufgliederung in Klassen sollte man mit Hilfe eines
168
A. Radiogene Isotopensysteme
aus dem Histogramm abgeleiteten Mittelwertes das 53Mn-Bestrahlungsalter auf einen Faktor »2 genau bestimmen können. Unwägbarkeiten der Bestimmung ergeben sich aus der
Variation der solaren Komponente der kosmischen Strahlung entlang der Umlaufbahn des
Meteoroiden. Von ihr hängen die Produktionsraten der kosmischen Radionuklide zum
Glück nicht entscheidend ab, weil ihre Eindringtiefe in den Körper infolge ihrer vergleichsweise niedrigen Energie gering ist.
1.0
1 – e-ltrad
A/Asat
0.8
0.6
0.4
e-ltter
0.2
0
0
2
4
6
8
10
trad/t1/2 bzw. tter/t1/2
Exponentialfunktionen zur Beschreibung des Anstiegs der Aktivität mit der
Bestrahlungszeit und ihres Abklingens mit der Verweilzeit auf der Erde
30
[dpm/kg]
Daneben gibt es auch die Möglichkeit, Bestrahlungsalter mittels stabiler kosmogen entstandener Nuklide zu ermitteln.
Wichtig dabei ist, daß es sich
dabei um Nuklide von
Elementen (mit mehreren stabilen Isotopen) handelt, die in
den Meteoriten nur in sehr
niedrigen
10Be-Produktionsrate
ABBILDUNG 130
20
10
Korrelation zwischen
Produktionsraten und
21Ne- Bestrahlungsaltern
für L- und H-Chondrite
10Be-
Konzentrationen vorliegen, so
daß sich massenspektrome10
20
30
40
50
trisch große Verschiebungen
21Ne-Bestrahlungsalter [106a]
der Isotopenzusammensetzung
messen lassen. Solche Elemente sind vor allen Dingen ABBILDUNG 131 Da die Bestrahlungsalter der meisten Medie Edelgase mit den Nukliden teorite einige Millionen Jahre betragen, liegt die Aktivität von
3
He (natürliche Häufigkeit 10Be in der Sättigungsaktivität.
0.000137%), 21 Ne (0.257%)
und 38Ar (0.063%). Die Konzentration c solcher stabiler kosmogener Nuklide steigt in den
Meteoroiden linear mit der Bestrahlungsdauer an:
c = Ps ´ trad
[GL 192]
169
Kosmogene Radionuklide
40
Anzahl
30
H-Chondrite
20
10
0
0
10
20
30
40
50
60
Bestrahlungsalter [Ma]
Verteilung der Bestrahlungsalter (vorwiegend 22Ne/21Ne) von H-Chondriten
t ter
=
1 æ Asat ö
ln
l çè At ter ÷ø
Anzahl
L-Chondrite
5
0
0
Anzahl
At ter = Asat ´ e - lt ter Þ
12
10
4
Anzahl
Mit dem Fall des Meteoriten
auf die Erde endet die Produktion, und die Isotopenverhältnisse von z.B. 22Ne/
21
Ne ändern sich nicht
mehr. Demgegenüber klingt
die induzierte Aktivität der
kosmogenen Radionuklide
aber nach dem Fall der
Meteorite ab. Die terrestrischen Alter tter der Meteorite
lassen sich daher prinzipiell
ebenfalls errechnen, und
zwar als:
6
20
30
40
0
10
20
30
40
C-Chondrite
0
0
[GL 193]
10
LL-Chondrite
0
10
20
30
40
10
Anzahl
ABBILDUNG 132
Achondrite
Zu ihrer Berechnung eignen
sich auch kurzlebige kosmo0
gene Radionuklide wie 14 C
oder 59Ni, da in den meisten
0
25
50
75
100
Fällen die terrestrischen
Bestrahlungsalter [Ma]
Alter der Meteorite klein
sind gegenüber ihren
133 Verteilung von Bestrahlungsaltern (vorwieBestrahlungsaltern. In Abbil- ABBILDUNG
22
21
gend
Ne/
Ne) von anderen Chondrittypen sowie von
d u n g 1 3 0 s i n d At rad Asat
Achondriten
u n d At ter Asat g e g e n d e n
170
A. Radiogene Isotopensysteme
Faktor t/t1/2 aufgetragen. Bei der Bestrahlung ist die Sättigungsaktivität bereits nach »5
Halbwertszeiten erreicht. Abbildung 131 zeigt die Ergebnisse einer Korrelation von 10BeProduktionsraten mit 21Ne-Bestrahlungsaltern[215]. Wie sich erkennen läßt – und wie wohl
auch zu erwarten war, liegt in Meteoriten mit Ne-Bestrahlungsaltern >10 Ma das 10Be in der
Sättigungsaktivität vor.
Abbildung 132 und Abbildung 133 zeigen Bestrahlungsalter von Edelgasen, vorwiegend
auf der Basis von 22Ne/21Ne berechnet (nach Angaben in[192]). Auffallend ist das Maximum
für die H-Chondrite, eine Klasse reduzierter (hohes Fe0/åFe) Chondrite, bei »5 Ma, was als
Auseinanderbrechen ihres Mutterkörpers zu jener Zeit interpretiert wird. Die übrigen
Typen zeigen nur schwach ausgebildete oder gar keine Maxima.
Die terrestrischen Alter können z.T. recht hoch sein in Klimaten, in denen die Verwitterungsvorgänge langsam ablaufen. Z.B. können sie in den antarktischen Eisfeldern einige
105a betragen, während Steinmeteorite in unserem Klima bereits nach »102 – 103a zerfallen und dann nicht mehr als Meteorite zu erkennen sein werden. Eisenmeteorite halten
sich auch in unserem Klima länger, da sie an der Oberfläche eine Art Passivierungsschicht
ausbilden.
10 Be-Produktionsrate
[dpm/kg]
Ein etwas überraschen30
der Befund ergibt sich,
wenn man Tiefenprofile
der
kosmogenen
28
Nuklide mißt, d.h. ihre
Produktionsraten in
Abhängigkeit von der
Position im Meteoriten.
26
Ein Beispiel dafür ist in
Abbildung 134 gegeben
für 10Be im L5-Chondriten Knyahinya[215].
24
Danach steigt die 10 BeProduktion von der
Oberfläche des Meteori22
ten bis »30cm tief ins
Innere hin an, obwohl
die Intensität der kosmischen Strahlung in die20
ser Richtung infolge
Tiefenprofil für 10 Be im
zunehmender AbschirL5-Chondriten Knyahinya
mung natürlich stark
18
sinkt. Die Ursache dieses
Anstiegs ist darin zu
0
10
20
30
40
suchen, daß in den oberAbstand vom Zentrum des Meteoriten [cm]
sten Schichten eines
Meteoroiden die ProdukABBILDUNG 134 Vielfältig sind die Effekte, die zu den Tiefenprofilen
tion an energiereichen
der Produktionsraten von kosmogenen Radionukliden in MeteoriSekundärteilchen durch
ten beitragen.
die kosmische Strahlung
zunimmt und deren Abfall überkompensiert und in einer Tiefe von »30 – 40cm in Steinmeteoriten ein Maximum erreicht. Da diese Sekundärteilchen aber auch zur Bildung der kosmogenen Radionuklide beitragen, beobachtet man von der Oberfläche bis in Tiefen von
30 – 40 cm charakteristischerweise einen Anstieg der Produktionsraten und erst anschließend ein Abfallen. Theoretische Modelle vermögen die Tiefenprofile jedoch bislang nicht
quantitativ zu beschreiben.
171
Kosmogene Radionuklide
15.4
Die Beschleuniger-Massenspektrometrie
Wegen der Bedeutung der Beschleuniger-Massenspektrometrie für die Analyse der kosmogenen Radionuklide sei sie hier abschließend kurz skizziert (nach Angaben in [214],[216]; für
einen ausführlichen Review siehe[217]). Abbildung 135 zeigt die Anordnung an der Rutgers
University/New Brunswick (New Jersey). Ein Strahl positiv geladener Ionen (insbes. von
Cs+) erzeugt durch Oberflächenzerstäubung („sputtering“) negative Ionen, z.B. von BeO–
oder von Al–. Diese werden mittels einer Zugspannung (z.B. 30 – 50KeV) aus der Ionenquelle extrahiert und auf einen ersten Elektromagneten fokussiert, der die Ionen so
ablenkt, daß nur noch die gewünschten Spezies in den Tandem van de Graaff-Beschleuniger gelangen. Dort werden die Ionen zunächst auf das in der Mitte des Tanks gelegene „Terminal“ hin beschleunigt, das z.B. für BeO–-Messungen auf +4 –+6MV geladen ist. Hier
befindet sich ein sogenannter „stripper“ – entweder eine gasgefüllte Zelle oder eine wenige
µm dünne C-Folie. Dieser dient dazu, von den mit hoher Energie anfliegenden Ionen (+4–
6MeV) Elektronen abzustreifen und sie zu positiven Ionen umzuladen. Die positiven Ionen
werden dann auf das auf Erdpotential liegende Ende des Tandems beschleunigt, wobei sie
je nach Ladungszustand Energien bis zu 30MeV erreichen können (z.B. 22MeV im Fall von
Be3+). Anschließend selektiert ein elektrostatischer Analysator Ionen des gewünschten
Ladungs- und Energiezustandes. Die Ionen werden dann im Feld eines zweiten Elektromagneten mit einer Auflösung von M/DM»500 nach ihren Massen getrennt und noch störende Ionen durch Aufprallen auf Schlitze herausgefiltert. Ein „post stripper“ wandelt den
größten Teil der Be3+-Ionen in Be4+-Ionen um, aber nur einen kleinen Teil des mit 10Be isobaren 10B3+. Dadurch kann anschließend das störende B abgetrennt werden. In einem
abschließenden Detektorsystem werden die Ionen des Radionuklids in einem Teilchendetektor nachgewiesen, der den linearen Energieverlust DE und die Restenergie E der eintretenden Ionen mißt. Die im Vergleich dazu hohen Ströme der stabilen Isotope werden mit
einem gewöhnlichen Faraday-Auffänger gemessen.
Tandem van de Graaff
Inflection
Magnet (20°)
O2 gas stripper
Wien
Filter
Magnetic
Spectrograph
Analyzing
Magnet (90°)
Mylar Foil
–
BeO
Negative
Ion Source
Slits
Carbon foil post-stripper
Removable slant Au foil
Switching
Magnet (65°)
ABBILDUNG 135
172
Be 3+
Detector
DE–E–xE
Detector
Be 4+
Switching
Magnet (55°)
Skizze der Funktionsweise eines Beschleuniger-Massenspektrometers
A. Radiogene Isotopensysteme
16.0
Edelgase und abgeklungene Radionuklide
Die Edelgase beziehen ihre Bedeutung aus ihrer geringen Häufigkeit in der Erde und ihrem
inerten Charakter. Da verschiedene Isotope der Edelgase verschiedenen nuklearen
Ursprungs sind, lassen sich mit ihrer Hilfe sowohl Prozesse im frühen Sonnensystem verfolgen als auch z.B. die Entgasungsgeschichte der Erde einschließlich der Bildung der
Atmosphäre. Abgeklungene Radionuklide sind solche, die im frühen Sonnensystem vorhanden waren, aber infolge ihrer kurzen Halbwertszeiten längst vollständig zerfallen sind.
Hinweise auf ihre frühere Existenz liefern Isotopenanomalien des Elementes, dem das
Tochternuklid angehört. Ursprünglich eventuell vorhandene Isotopenanomalien sind auf
der Erde infolge ihrer komplexen thermischen Geschichte längst verschwunden mit der
möglichen Ausnahme der Xe-Isotope, so daß die Beschäftigung mit abgeklungenen Radionukliden weitgehend eine Domäne der Kosmochemiker ist, während alle Edelgase sowohl
geo- als auch kosmochemisch von Interesse sind.
3
He/4He
primordiales He
Die terrestrische Variation
10-4
des Verhältnisses der beiden
verarmter Mantel
stabilen He-Isotope 3He und
4
He macht gut 4 ZehnerpoMORB
10-5
tenzen aus und liegt zwi-9
schen »10 in U-Mineralen
und 5´10 -5 in Basaltlaven
von Hot Spots. Das niedrige
10-6
Verhältnis im erstgenannten Fall ist auf den a-Zerfall
des Urans zurückzuführen.
10-7
Läßt man solche Uranminerale fort, dann macht die
Variation aber immer noch
3 Größenordnungen aus
10-8
Gesteinsarten:
und kann dann, mit wenisaure
g e n A u s n a h m e n , d u rc h
intermediäre
Mischung von 3 Endkom-9
basische
10
ponenten erklärt werden,
Li-Minerale
nämlich von atmosphäri3
4
U-Minerale
schem He mit He/ He
»1.4´10 - 6 , radiogenem He
10-10
(»10 -7 ) und Erdmantel-He
10-10
10-9
10-8
10-7
10-6
10-5
(»10-5). Die Isotopenfraktio3
4
( He/ He)berechnet
nierung infolge von thermischer Diffusion sollte bei
beiden Isotopen naturge- ABBILDUNG 136 Variation der He-Isotopien in Gesteinen und
mäß hoch sein; sie sinkt Mineralen
jedoch mit steigender Temperatur und spielt bei Tieftemperaturprozessen sicherlich eine Rolle. Zur Erklärung der terrestrischen He-Isotopenvariation reichen solche Effekte aber nicht aus.
(3He/4He)gemessen
16.1
In der Erdatmosphäre ist He mit einer Häufigkeit von 5.24 Vol.ppm vorhanden bei einem
3
He/4He-Verhältnis von (1.39±0.01) ´10-6. Als Folge der raschen Durchmischung der Atmosphäre (»10a) ist dieses Isotopenverhältnis global recht konstant, und die Atmosphäre wird
daher als bequemer He-Isotopenstandard verwandt und mit RA bezeichnet. Die Residenzzeit des He in der Erdatmosphäre liegt bei »106a, d.h. ein He-Atom entweicht innerhalb
dieser Zeit im Durchschnitt in den Weltraum, 3He erheblich rascher als 4He.
173
Edelgase und abgeklungene Radionuklide
Die radiogene Komponente hat ihren Ursprung in U-und Th-reicher Umgebung, d.h. vor
allen Dingen in der kontinentalen Erdkruste. Typische R/RA-Verhältnisse liegen bei 0.1 –
0.01 (R = 3He/4He im betrachteten Reservoir). Das 3He dieser Komponente wird auf die
Kernreaktion 6Li(n,a)3H®3He zurückgeführt. R/RA-Verhältnisse bis zu »9 sind in Spodumen gefunden worden und Verhältnisse um 10-3 in U-Mineralen. In Abbildung 136 sind
berechnete gegen gemessene 3He/4He-Verhältnisse aufgetragen. Die Gerade mit positiver
Steigung verbindet 3He/4He-Verhältnisse von U-reichen Mineralen mit Li-reichen[218]
(etwas U muß natürlich zur Produktion von Neutronen vorhanden sein) Mineralen.
Helium mit R/RA>1 (bis >30) findet sich in Basaltgläsern verschiedener geotektonischer
Umgebung (MORB, Subduktionszonen, Ozeaninseln) und auch in geothermisch aktiven
Gebieten oder kontinentalen Hot Spots. Hohes R/RA scheint daher eine Signatur des Erdmantels zu sein, der arm an den a-Strahlern U und Th ist. Das 3He dieser Komponente wird
meist als primordiale Komponente angesehen, welche bei der Akkretion der Erde eingebaut
wurde. Alternativ könnte es sich um alte (archaische) subduzierte Ozeankruste handeln,
deren hohes 3He/4He geringen U- und Th-Gehalten zuzuschreiben ist, durch welche die
He-Isotope nahezu eingefroren bleibt[219].
10-3
Hot Spots
101
10-5
MORB
Luft
100
1
10-6
Kruste
0.1
10-1
10-7
0.01
10-2
10-8
10-7
10-6
10-5
10-4
10-3
3He/4He
3He/4He
103
102
Mischungslinien
zwischen Luft und
Komponenten mit
R/RA = 10
10-4
Sonnenwind
(relativ zum atmosphärischen Verhältnis)
primordiale
Verhältnisse aus
Meteoriten
10-2
10-1
100
3He/Ne
ABBILDUNG 137
He-Isotope und 3He/Ne-Verhältnisse terrestrischer und anderer Materialien
Wie Abbildung 137 zeigt[220], haben MORB ein ziemlich konstantes R/RA von »8 – 9 (bei
weiter 3He/Ne-Variation), während ozeanische Hot Spots wie Hawaii ein noch höheres R/
RA aufweisen (aber auch eine größere Variation, die in der Skizze nicht voll erfaßt ist), was
damit erklärt wird, daß sie tiefere Mantelniveaus beproben als MORB. Island, das auf dem
Mittelatlantischen Rücken und zugleich über einem Hotspot sitzt, zeigt in seinen Basalten
R/RA-Werte, die von MORB-Verhältnissen bis zu typischen Plume-Werten von »30 reichen[221]. Reines primordiales He mag durch den Sonnenwind oder die primordialen Edelgase in Meteoriten gegeben sein. Das zeigt an, daß auch der Erdmantel nur noch eine
geringe primordiale He-Signatur aufweist.
Die Konzentration der beiden He-Isotope in der Atmosphäre wird durch eine dynamische
Balance zwischen Gewinn durch Diffusion aus der festen Erde plus kosmische Strahlung
einerseits und Verlust in den Weltraum andererseits eingestellt. Da die diversen He-Quellen
174
A. Radiogene Isotopensysteme
unterschiedliche Isotopenzusammensetzungen haben und beim Diffusionsverlust in den
Weltraum das 3He bevorzugt wird, ist damit zu rechnen, daß im Lauf der geologischen
Geschichte die atmosphärische He-Zusammensetzung nicht konstant war. Tabelle 13 vermittelt einen ungefähren Überblick über die irdische Gewinn- und Verlustrechnung für die
beiden He-Isotope.
TABELLE 13:
Abschätzungen der irdischen He-Bilanz (nach J.E. Lupton)
Quellen:
Sonnenwind
interstellares Gas
primordialer Fluß (Ozeane)
primordialer Fluß (Land)
galaktische Strahlung
kosmischer Staub + Meteorite
Wechselwirkung der galaktischen
Strahlung mit Materie
radiogen: kontinentale Kruste
radiogen: ozeanische Kruste
å
Verluste:
thermisches Entweichen
nicht-thermisches Entweichen
å
3
He-Fluß
(Atome/(cm2 s1)
4
»5
»5
4–5
1 – 10?
»1
<1
»0.6
– (?)
–
–
–
–
–
–
»0.1
–
16?
3
»0.3
»3
6
1
7
0.1?
2–8
2–8
He-Fluß
(106 Atome/(cm2 s1)
Die Erkenntnis, daß R/RA
Oahu
von aus dem Erdmantel
stammenden Gesteinen
Maui
wesentlich höher als das
Salt Lake
Haleakala:
der Atmosphäre ist, hat
Crater:
17–37
seit Mitte der siebziger
7.5–8.1
Jahre zu einer intensiven
Hawaii
Untersuchung solcher
Hualalai:
Gesteine und der Fahn9–13
8.2; 10.6
dung nach primordialem
Helium in der Erde
Kilauea:
14–18
[3He/4He]Probe/[3He/4He]Luftgeführt (z.B. [222]). Der
Verhältnisse für Proben der
Befund, daß MORB ein
Hawaii-Inseln und des LoihiLoihi Searelativ konstantes R/R A
mount: 20–32
Seamounts
um 8 – 9 haben, war überraschend, und er wurde
dahingehend interpretiert, daß das He im Erd- ABBILDUNG 138 He-Isotopien verschiedener Basalte auf Hawaii
mantel gut durchmischt
ist, während andere Isotopensysteme das Gegenteil anzeigen. Es kommt noch hinzu, daß
3
He im Mantel primordial, 4He aber größtenteils aus Th und U entstanden ist, so daß die
Konstanz der He-Isotopenzusammensetzung letztlich ein ziemlich konstantes (Th+U)/He
des Mantels nahelegt.
175
Edelgase und abgeklungene Radionuklide
Helium mit Mantelisotopie findet man nur in Basaltgläsern, also den abgeschreckten Rändern von Pillows, während deren Inneres infolge von Diffusion entlang Korngrenzen die
He-Isotopie des Meerwassers angenommen hat, woraus sich auch schließen läßt, daß die
kristallinen Phasen bei der Kristallisation ihr He weitgehend verlieren. Andererseits wird
auch argumentiert, daß Olivine He-reiche Gasblasen bei raschem Wachstum umschließen[223] und daß solche Olivine wegen des niedrigen (U+Th)/He der Gasblasen die Heimat
einer Komponente mit hohem R/RA sind, während außerhalb der Olivine in den Basalten
hohe (U+Th)/He-Verhältnisse vorliegen, die rasch ein niedriges R/RA entwickeln[224].
Anders als die He-Isotopie variieren die He-Gehalte in ozeanischen Basaltgläsern erheblich
um mehr als das 100-fache. Inwieweit He im Lauf der Zeit durch Diffusion aus den Gläsern
verloren geht, ist unklar. Wenn es das tut, wird man einen bevorzugten Verlust des leichten
Isotops erwarten. Werte von R/RA bis herab »3, kombiniert mit niedrigen He-Konzentrationen sind in 4 – 10 Ma alten Basaltgläsern gemessen worden[222],[225], was für einen Diffusionsverlust spricht.
Unter den Hot Spots ist Hawaii der best untersuchte und auch der, der das höchste gesicherte terrestrische R/RA geliefert hat. Abbildung 138 zeigt einige dieser Meßwerte. Der
höchste Wert wurde auf der Insel Maui gemessen. Der Hot Spot sollte sich heute ungefähr
unter dem Loihi-Seamount befinden, dem südöstlichsten aktiven Vulkan der HawaiiEmperor-Kette. Warum auf der Hauptinsel Hawaii niedrigere R/RA-Werte gefunden werden
als auf Maui nordwestlich und Loihi südöstlich, ist unbekannt.
Maui
relativ zum atmosphärischen Verhältnis
3He/4He
30
Loihi
Seamount
Island
20
10
B
MOR
Sa
mo
Kilauea
ReykjanesRücken
Réunion
Macdonald
Seamount
Guadalupe
Tahiti
Jan Mayen
Azoren
MAR 33-358N
Osterinsel
0
0.702
a
0.703
Gough
Tristan da Cunha
0.704
0.705
0.706
87Sr/86Sr
ABBILDUNG 139
Variation von He- und Sr-Isotopen in Ozeaninselbasalten und in MORB
Kontinentale Hot Spots haben niedrigere R/RA-Verhältnisse, wohl weil das He hier in der
kontinentalen Kruste kontaminiert wird. Vulkanite der Subduktionszonen haben niedrigere R/RA-Werte als MORB, was anzeigt, daß Anteile aus einer subduzierten Komponente
stammen können. Zum Beispiel variiert R/RA in Olivinen von Vulkaniten auf den Antillen
zwischen 8.4 – 6.8 auf den nördlichen Inseln (Saba bis Dominica) und 7.6 – 3.6 im Süden
(Martinique bis Grenada)[226]. Das stimmt mit den Ergebnissen der Pb-Isotopien überein,
176
A. Radiogene Isotopensysteme
die dahingehend interpretiert wurden, daß im Süden des Antillenbogens subduzierte Sedimente in der Magmenquellregion vorhanden sind, im Norden dagegen nicht[147].
Zwar nicht mit Hilfe der He-Isotopie allein, aber unter Hinzunahme der Sr-Isotope läßt sich
noch eine weitere Mantelkomponente abtrennen, die als die Tristan-Komponente bezeichnet und auf Inseln des Südatlantiks gefunden wird; sie hat R/RA»6 – 7 und 87Sr/86Sr»0.704
– 0.705 und könnte Mantel mit einer subduzierten zugemischten Komponente sein. In
einem He-Sr-Diagramm (Abbildung 139) unten sind diese Komponenten mit Ausnahme
der Subduktionszonenvulkanite dargestellt (Endglieder: MORB – Hawaii – Tristan da
Cunha / Gough).
Eine interessante Ergänzung zum 3He/4He stellt das Verhältnis 40Ar/36Ar dar. 40Ar entsteht
durch radioaktiven Zerfall von 40K, während 36Ar nur sehr untergeordnet durch Kernprozesse gebildet werden kann und daher weitgehend primordialen Ursprungs ist (Hier
zeigt sich auch die Inkonsequenz der Isotopengeochemiker, da im einen Fall das primordiale Nuklid im Zähler steht [3He], das andere mal im Nenner [36Ar]). Wie Abbildung 140
erkennen läßt, kann die wesentliche Variation der He- und Ar-Isotope in MORB und
Ozeaninselbasalten als Mischung zwischen 3 Endgliedern interpretiert werden, von denen
das eine verarmter Erdmantel ist (D: R/RA» 9, 40Ar/36Ar »16000), dessen Isotopien von den
MOR-Basalten nicht ganz erreicht wird, ferner eine Plume-Komponente, die durch
Ozeaninseln am besten repräsentiert wird (primitiver Mantel mit R/RA»40, 40Ar/36Ar »400)
sowie die Atmosphäre mit R/RA=1 und 40Ar/36Ar =295.5).
100
10-4
primitiver Mantel
10
3 He/ 4 He
eld
10-5
Luft
Hawaii-Basalte
Peridotitxenolithe,
Hawaii
Diamanten
Peridotitxenolithe,
Südafrika
10-7
102
103
104
1
3 He/ 4 He
verarmter
Mantel
MORB-F
relativ zum atmosphärischen Verhältnis
10-6
0.1
105
40Ar/36Ar
ABBILDUNG 140
Relation zwischen He- und Ar-Isotopen für Erdmantelproben[220]. Die Pfeile
stellen Obergrenzen der He-Isotopie dar.
Ein Modell zur Erklärung dieser Systematik wurde von Hart et al.[227] (1985) entwickelt und
ist in Form eines „Kastenmodells“ in Abbildung 141 dargestellt. Die Autoren stellen sich
vor, daß der tiefe Mantel (>670km) separat vom oberen Mantel konvektiert. Ein Materialkreislauf zwischen tiefem und oberem Mantel findet nicht statt. Daher hat der tiefe Mantel
seine primordiale He- und Ar-Isotopenintegrität behalten. Aufstieg von Plumes vom tiefen
in den oberen Erdmantel ist jedoch in dem Modell erlaubt und ist auch mit Daten anderer
Isotopensysteme kompatibel. Der obere Mantel bildet zusammen mit Erdkruste und Atmosphäre ein weitgehend geschlossenes System. Der Gehalt an 36Ar von oberem Erdmantel +
177
Edelgase und abgeklungene Radionuklide
Erdkruste ist klein gegen den atmosphärischen 36Ar-Gehalt. Der Unterschied im 40Ar/ 36Ar
zwischen oberem Mantel und Atmosphäre ist daher durch den unterschiedlichen 40ArGehalt bestimmt, das in den Gesteinen der Kruste und des oberen Mantels durch 40K fortwährend nachgebildet wird. Das hat außerdem zur Folge, daß 40Ar/36Ar im tiefen Mantel
und der Atmosphäre nahezu identisch sind (40Ar/36Ar von oberem Erdmantel, Kruste und
Atmosphäre sollten identisch mit 40Ar/36Ar des tiefen Mantels sein). 3He/4He ist im unteren
Erdmantel am höchsten und in der Atmosphäre am niedrigsten, weil He infolge seines
niedrigen Atomgewichts – im Gegensatz zum Ar – in den Weltraum diffundiert, und zwar
3
He erheblich rascher als 4He. Inwieweit die Vorstellung, daß der tiefe Mantel ein geschlossenes System ist, richtig ist, ist schwer zu beurteilen. Eine Reihe von Geophysikern und
Petrologen geht davon aus, daß in steil stehenden Subduktionszonen Material in diesen
tiefen Mantel gelangt. Ob das die Massenbilanz der Edelgase stört, hängt vor allem davon
ab, bis in welche Tiefe in Subduktionszonen Minerale stabil sind, die K sowie U und Th einzubauen vermögen.
Die He-Entgasung der ozeanischen
Kruste und des darunterliegenden
Mantels ist durch Untersuchungen
der He-Gehalte der Ozeane ziemlich genau bekannt. So hat man
festgestellt, daß über aktiven Teilen
der mittelozeanischen Rücken
regelrechte He-Plumes bestehen,
wie z.B. in Abbildung 142 dargestellt. Da Seewasser einen erheblichen Teil an atmosphärischem He
enthält, sind die Effekte relativ
klein und werden daher meist als
prozentuale Abweichung d angegeben, die definiert ist als
(
)
d 3 He = 100( R RA - 1)
He-Verlust
Atmosphäre
oberer
Mantel
40Ar/36Ar
» 295
3He/4He » 1.4´10-6
Ar, He
40Ar/36Ar
» 24500
3He/4He » 12.6´10-6
Kruste
K, U
Plume
unterer Mantel
40Ar/36Ar
3He/4He
» 400
» 52´10-6
[GL 194]
Anreicherung von d (3He) bis »50% ABBILDUNG 141 Modell zur Erklärung der He- und Arüber den normalen Seewasserwert Isotopensystematik in verschiedenen Materialien der
sind z.B. über dem East Pacific Rise Erde
bei 15°S gemessen worden.
Die Isotope 238U, 235U, 232Th und 40K sind nicht nur die Tochternuklide von radiogenem He
bzw. Ar, sondern auch die Hauptproduzenten der radiogenen Wärme in der Erde. Als Konsequenz dessen sind Edelgasproduktion und Wärmeproduktion in der Erde räumlich und
zeitlich miteinander gekoppelt. Gegenwärtig werden » 1012 Atome 4He und 2´1011 Atome
40
Ar je Joule Wärme gebildet bei „bulk-earth“ K/U- und Th/U-Verhältnissen von 1.3´104
bzw. 3.8. Da die kontinentale Kruste ähnliche Elementverhältnisse hat, sollte obiges Produktionsverhältnis auch für die Kruste gelten. Im oberen Mantel wird dieses Produktionsverhältnis etwas niedriger sein, da das Th/U-Verhältnis hier wohl bei nur »2.5±0.2 liegt.
Wie bereits eingangs erwähnt, wird ein Teil des 3He durch eine (n,a)-Reaktion aus 6Li gebildet, wobei die Neutronen aus dem Zerfall von U und Th stammen. Für typische Erdmantelund Erdkrustenzusammensetzungen dürfte das radiogene Produktionsverhältnis 3He/4He £
5´10-8 betragen[228]. Eine Bildung von 3He durch Zerfall von Tritium, das durch die atmosphärischen Kernwaffenexplosionen in den 1950-er und 1960-er Jahren produziert wurde,
wirkt sich zwar in der Atmosphäre und den Ozeanen noch aus, kann aber im folgenden
vernachlässigt werden.
178
A. Radiogene Isotopensysteme
He-Isotopenanomalien im Ozeanwasser entlang des EPR bei 158S
5
20
25
Tiefe [km]
10
15
1
30
2
35
40
30
3
Die Zahlen geben Konturen
von d3He (%) an.
45
25
20
4
East Pacific Rise
5
1000km
130°
120°
0
110°
1000km
100°
90°
westliche Länge
Konturen von d3He über und um den East Pacific Rise. Ein riesiger He-Plume
markiert die Rückenachse infolge der Entgasung von Basalt und breitet sich
mit den Strömungen in mittleren Wassertiefen nach Westen aus.
ABBILDUNG 142
r
rds e eg a b e
No
n
sy
Mantelhelium vorhanden
nur radiogenes Helium
em
st
er en
Eg rab
g
Pannonisches
Rheingraben
Becken
Massif
Central
ABBILDUNG 143
(3He/4He)Probe /(3He/4He)Luft -Verhältnisse in der Kruste Mitteleuropas. Thermalwässer mit R/RA > 0.08 werden als Mantelhelium enthaltend angesehen.
Es ist naheliegend, daß eine Mantelkomponente vor allem dort zu identifizieren ist, wo es jungen Vulkanismus gibt.
179
Edelgase und abgeklungene Radionuklide
Bis zu 50% des Urans und Thoriums der
3He/4He
Erde finden sich in der kontinentalen Kru10-8 10-7 10-6 10-5
ste. Nimmt man an, daß im Schnitt dieselbe Menge an He aus der Kruste in die
Ozeanrücken
Atmosphäre entgast wie in der Kruste
durch Zerfallsprozesse entsteht, dann entSizilien
spricht dies einem Gleichgewichtsfluß
von 2.8´1010 Atomen/(m2´s)[229]. Nimmt
Egergraben
man darüber hinaus einen He-Fluß vom
Massif Central
Erdmantel in die kontinentale Kruste an,
der genauso groß ist wie der unter den
Oberpfalz
Ozeanen, nämlich 5´109 Atome/(m2 ´ s)
Pannonisches Becken
bei einem Verhältnis R/RA = 8, dann sollte
das Misch-He, das auf den Kontinenten
Larderello
entgast, ein mittleres 3He/4He-Verhältnis
Rheingraben
von 1.8´10 -6 aufweisen. Da der Unterschied zwischen primordialem und radioGriechenland
genem 3He/4He rund 4 Größenordnungen
beträgt, lassen sich noch Beimischungen
Molassebecken
von weniger als 1% primordialem in
Großbritannien
radiogenem He erkennen. Abweichungen
primorwerden in beide Richtungen beobachtet.
radiogen
dial
Abbildung 143 und Abbildung 144 zeigen
die Ergebnisse von He-Messungen in
0.01
1
10
0.1
Europa. Auf den Britischen Inseln werden
3
4
R/R
A
ziemlich einheitliche He/ He-Verhältnisse beobachtet, die um den Wert des
berechneten krustalen Produktionsver- ABBILDUNG 144 Variation der He-Isotopien in eihältnisses schwanken (Mantel-He £0.5% nigen Vulkangebieten in Europa
des totalen He). Im Pannonischen Becken,
Im Egergraben, im Rheintalgraben und im Massif Central werden wesentlich höhere Verhältnisse gemessen, die z.T. typische Mantelheliumwerte erreichen. Generell läßt sich
sagen, daß eine Mantel-He-Komponente überall dort vorhanden ist, in der es junge vulkanische Aktivität gibt bzw. in Gegenden mit Krustenextension. Für unerwartet niedrige 3He/
4
He-Verhältnisse, die man vielerorts in Europa findet, gibt es mehrere Erklärungsmöglichkeiten. Z.B. könnte der aus dem Mantel kommende He-Fluß unter den Kontinenten eine
oder zwei Größenordnungen unter dem ozeanischen Mantel-He-Fluß liegen; daneben
könnte die krustale Radioaktivität in diesen Gebieten wesentlich höher sein als erwartet;
schließlich könnten auch Abweichungen vom Gleichgewichtszustand zwischen krustaler
He-Produktion und Entgasung extrem groß sein. Das könnte aber für hohe 3He/4He-Verhältnisse umgekehrt auch heißen, daß die krustale Radioaktivität in solchen Gebieten anomal niedrig ist oder daß der He-Fluß aus dem Mantel höher ist als erwartet.
Der Fluß von He und Wärme aus dem Erdmantel ist für den ozeanischen Bereich ziemlich
gut bekannt. Der Wärmefluß liegt bei »100mW/m2 und der 4He-Fluß ist wahrscheinlich
kaum höher als 4´109 Atome/(m2´s). Mit diesen Werten haben O’Nions & Oxburgh errechnet, daß aus den Mengen an U, Th und K (errechnet aus K/U»10000), die erforderlich sind,
um die radiogene Komponente des Mantel-He-Flusses zu erklären, nur ein kleiner Teil des
beobachteten Wärmeflusses stammen kann. Das beobachtete Verhältnis von 4 He zu
Wärme liegt bei 4´1010 Atomen pro Joule, das erwartete Verhältnis bei »1012, wie bereits
früher erwähnt. Der gemessene He-Fluß des Mantels erklärt also paradoxerweise nur knapp
5% des Wärmeflusses. Auch wenn Wärmefluß und He-Entgasung keine Schlüsse über die
Verteilung von U und Th im Mantel erlauben, läßt sich abschätzen, daß dieses He aus einer
Konzentration von »5ppb U und einer äquivalenten Menge Th im oberen Erdmantel stammen kann (Ähnliche Überlegungen sollten sich auch mittels 40Ar anstellen lassen; genaue
Messungen des Ar-Flusses sind jedoch sehr schwierig wegen seiner hohen Konzentration in
180
A. Radiogene Isotopensysteme
der Luft). Diese Überlegungen werden auch durch neuere Abschätzungen bestätigt, die für
Mantel + Kruste zu einem U-Gehalt von »20ppb gelangen, woraus man errechnen kann,
daß der gemessene He-Fluß aus dem Mantel lediglich »10% des produzierten He entspricht. Mit anderen Worten: Es kommt erheblich weniger He aus dem Erdmantel als dort
durch den Zerfall von U und Th gebildet werden sollte. Dieses Paradox läßt sich auflösen,
wenn es irgendwo im Mantel eine Grenze gibt, über die hinweg der Transport von Wärme
größer ist als die Diffusion des He. Andernfalls sind die Modelle, welche die chemische und
thermische Entwicklung unseres Planeten beschreiben sollen, grundlegend falsch.
log(3He/4He)3106
Für die Kontinente ist ein Ver3.5
1
2
3
18
gleich von He- und Wärmefluß erheblich schwieriger als
2
2
8
14
3.0
für die Ozeane, weil sich der
2
2
3
5
3
1
kontinentale He-Fluß kaum
messen läßt. Sowohl für konti2
1
5
6
6
21
2.5
nentales als auch für ozeani1
1
5
5
4
5
sches Milieu glauben Polyak &
2.0
Tolstikhin eine in erster Nähe2
1
2
4
7
8
rung lineare Beziehung zwi4
3
5
3
1
6
6
schen der He-Isotopie und
1.5
dem Wärmefluß q (in HFU, 1
3
4
4
2
2
7
HFU = 10-6cal s-1 cm-2 =
5
2
7
7
9
14
1.0
41.868mW/m 2 ) beobachten
zu können. Ihr Plot ist in
3
1
7
12
17
16
Abbildung 145 wiedergege0.5
10
6
6
11
19
ben. Ein Trend ist zwar nicht
5
3
4
zu leugnen; bei gegebenem q
11
0.0
kann das beobachtete 3He/4He
6
jedoch bis zu mehr als eine
Zehnerpotenz von der Korrela2.0
1.0
1.5
2.5
q [HFU]
tionsgeraden abweichen, was
diese Datenauftragung im einzelnen nicht sehr nützlich ABBILDUNG 145 „Korrelation“ zwischen He-Isotopie und
erscheinen läßt. So variiert q Wärmefluß. Die Regressionsgerade ist als durchgezogene Liz.B. auf den Britischen Inseln nie dargestellt. Die Zahlen in den Quadraten entsprechen der
bei ziemlich konstanter He- jeweiligen Anzahl von Meßdaten[218]
Isotopie von 5´10 -8 um das
Zweieinhalbfache von »50 – 125mW/m2, eine Variation, die im Diagramm einer Änderung
von 3He/4He um zwei Zehnerpotenzen entsprechen sollte.
Nach einem von dem Geophysiker BIRCH gefundenen empirischen Zusammenhang
besteht für die kontinentale Kruste der folgende Zusammenhang zwischen Wärmefluß q
und Wärmeproduktion A (mW/cm3):
q = qm + Ah ( = qm + qc )
[GL 195]
Dieser Zusammenhang nimmt an, daß die Wärme produzierenden Elemente U, Th und K
in der obersten Hälfte der Kruste erheblich angereichert sind, so daß A die Wärmeproduktion nur dieser Schicht ergibt; h ist dann die Mächtigkeit dieser Schicht. Der Achsenabschnitt qm („reduzierter Wärmefluß“) ist der Wärmefluß, der aus größerer Tiefe kommt.
Meist wird unterstellt, daß dies der aus dem Mantel stammende Wärmefluß ist, Ah also der
aus der Kruste kommende Wärmefluß (qc). Nimmt man an, daß der He-Fluß ebenfalls aus
2 Komponenten zusammengesetzt ist, einen Teil jm aus dem Mantel und einen Fluß jc aus
der kontinentalen Kruste und beide Teile mit verschiedener Isotopie, dann wird das an der
Erdoberfläche gemessene 3He/4He bei festem qm und jm/qm mit wachsendem q (wachsendem Anteil der krustalen Wärmeproduktion) sinken. Umgekehrt wird 3He/4He mit zunehmendem q steigen, wenn jm ansteigt bei festem jm/qm und Ah (wachsender Anteil des
181
Edelgase und abgeklungene Radionuklide
Wärmeflusses aus dem Mantel). Es scheint plausibel, daß beide Fälle in der Natur auftreten,
und deswegen ist eine strenge Linearität zwischen q und 3He/4He nicht zu erwarten.
Das Verhältnis jm/qm, das für die Ozeangebiete bei »4´1010 Atomen He pro Joule liegt, ist
unter alten Kratonen wohl £5´109 Atome/Joule. Andererseits ist im südlichen Rheingraben
jm/qm mindestens eine Größenordnung höher als in den Kratonen, obwohl qm wahrscheinlich kaum mehr als 50% über den Werten für Kratone liegt. Alles in allem scheint es daher,
als wären He- und Wärmefluß in der kontinentalen Lithosphäre, abhängig von ihrem
jeweiligen Transportmechanismus, allenfalls locker aneinander gekoppelt. In den kühlen
Kratongebieten der Erde, in denen die Wärme sich nur durch Strahlung ausbreitet und das
He durch Diffusion, muß das thermische Diffusionsvermögen (Wärme) größer sein als das
chemische Diffusionsvermögen (He). Die primordiale He-Komponente in jungen tektonisch aktiven kontinentalen Gebieten zeigt dagegen einen anderen Transportmechanismus für das He an, wahrscheinlich durch Aufdringen von Mantelschmelzen in die tiefe
Kruste (crustal underplating) und deren Entgasung, während wohl auch hier Strahlung
weiterhin der Haupttransportmechanismus der Wärme bleibt.
16.2
Xenon
Xenon hat 9 stabile Isotope mit Massenzahlen zwischen 124 und 136. In extraterrestrischen Proben können die Häufigkeiten der Xe-Isotope mit den Massenzahlen 129, 131,
132, 134 und 136 als Folge von Zerfallsprozessen variieren. Für die 4 schwersten Xe-Isotope
kommen zwei Quellen in Frage, die nach der Nukleosynthese zur Bildung der Isotope
131
Xe, 132Xe, 134Xe und 136Xe beitragen konnten, nämlich die Spontanspaltung von 238U
und von 244Pu (Abbildung 146). 244Pu hat eine Halbwertszeit von nur 82Ma und kann
daher heute nicht mehr in den Natur auftreten. Es muß jedoch in der Frühzeit der
Entwicklung des Planetensystems vorhanden gewesen sein, denn allein durch die Spontanspaltung von 238U lassen sich die Xe-Isotopenanomalien mancher Meteorite nicht erklären. 129Xe-Anomalien werden auf den Zerfall von 129I zurückgeführt, das eine Halbwertszeit von »17Ma hat und ebenfalls nur in der Frühzeit des Sonnensystems vorhanden war.
Insbesondere mit 129I/129Xe-Methode haben Kosmochemiker versucht, frühe Prozesse in
der Entwicklung der Meteorite bzw. damit unseres Sonnensystems zu datieren[230].
längst zerfallene 129
I
Radionuklide:
124
126
128 129 130 131
noch vorhandenes Radionuklid:
ABBILDUNG 146
244Pu
132
134
136
238U
Fünf der neun Xe-Isotope können Beiträge von kurz- und langlebigen Radionukliden enthalten.
Auf der Erde wird man heute Xe-Isotopenvariationen durch Zerfall der kurzlebigen Nuklide
I und 244Pu nicht unbedingt erwarten, da ursprünglich vorhandene Anomalien durch
tektonische Prozesse auf der Erde in den uns zugänglichen Gesteinen homogenisiert werden sollten. Staudacher & Allègre[231] haben dennoch versucht, terrestrische Xe-Variationen in Materialien des Erdmantels und der Erdkruste aufzuspüren. Die Ergebnisse sind in
Abbildung 147 und Abbildung 148 aufgeführt. Als Referenzen dienen die Isotopien des
Sonnenwindes und der kohligen Chondrite sowie der irdischen Atmosphäre. Alle terrestrischen Proben weisen 134Xe/ 130Xe-Verhältnisse (und ebenso 131Xe/130Xe, 132Xe/130Xe und
136
Xe/ 130Xe) auf, die größer sind als die der Chondrite oder des Sonnenwindes, während
129
Xe/130Xe höher sein kann, aber nicht sein muß. MORB-Gläser zeichnen sich jedoch
129
182
A. Radiogene Isotopensysteme
dadurch aus, daß ihr 129Xe/130Xe höher ist als das der Atmosphäre, während ihr 134Xe/130Xe
nur unwesentlich das der Atmosphäre übersteigt. Die einzige Möglichkeit, das erhöhte
129
Xe/130Xe zu erklären, ist durch Zerfall von 129I in der Frühzeit der Entwicklung der Erde.
Es ist daher auch plausibel, das erhöhte 134Xe/130Xe der MORB zumindest teilweise dem
Zerfall von 244Pu zuzuschreiben.
134Xe/130Xe
Entwicklungslinie der kontinentalen Kruste
Phanerozoische
krustale
3.8
Gesteine (Granitoide) zeigen
demgegenüber dasselbe 129 Xe/
130
Xe-Verhältnis wie die Atmosphäre, aber ein höheres und
sehr variables 134Xe/130Xe. Da es
MORB
sich hierbei um junge, zumin3.4
OIB
dest überwiegend durch innerDazite
krustales Schmelzen gebildete
Gesteine handelt, darf man
Granitoide
davon ausgehen, daß diese
Karbonatite
Variationen auf der Spontanspaltung von 238 U beruhen, zumal
3.0
solche Gesteine sich durch ein
hohes U/Xe-Verhältnis auszeichnen. Lediglich der proterozoische Granitoid des Pikes Peak in
Colorado zeigt auch Anzeichen
eines erhöhten 129Xe/130Xe, das
MORB
2.6
wieder 129 I zugeschrieben werAtmosphäre
den muß. Zwischen der Entwicklungslinie der kontinentalen
kohlige Chondrite
Kruste und der des MORB-Mantels oder des hypothetischen tieSonnenwind
fen Mantels sind alle Mischisoto2.2
pien denkbar. In diesem Sinn
6.2
6.4
6.6
6.8
kann die Isotopie des Pikes-Peak
129Xe/130Xe
Batholiths als die eines krustalen
Gesteins mit einer beträchtlichen aus dem Erdmantel abge- ABBILDUNG 147 Variation der Xe-Isotope auf der Erde
leiteten Komponente erklärt
werden.
7
Die Bedeutung der 238U-Spontanspaltung auf die Entwicklung der Xe-Isotope in verschiedenen Reservoirs der Erdkruste kann man mit Hilfe der Zerfallsgleichung abzuschätzen:
134
Xe æ 134 Xe ö
=ç
÷ +
130
Xe è 130 Xe ø 0
238
130
U lf
´
´ j ´ e la t - 1
Xe la
(
)
[GL 196]
mit lf = Zerfallskonstante für Spontanspaltung des 238U = 8.46´10-17a-1, la = 1.55125
´10-10a-1, j = Isobarenausbeute für Masse 134 bei der 238U-Spaltung = 0.0552. Die mittlere
U-Konzentration in Granitoiden liegt bei 3.7ppm, das sind
3.7 ´ 10 -6 [g / g]
´ 0.9927 = 1.543 ´ 10 -8 [mol
238.03 [g / mol]
238
U / g Gestein]
Typische Gehalte an 130Xe liegen bei 10-11 – 10-12 cm3/g, also z.B. für 10-11cm3/g:
10 -11 [cm3 / g]
= 4.464 ´ 10 -16 [mol / g Gestein] ,
3
22400 [cm / mol]
183
Edelgase und abgeklungene Radionuklide
und daraus: 238U/130Xe = 3.46´107.
Für ein Gesteins- oder Reservoiralter von t = 2 Ga erhält man für den zweiten Summanden
der rechten Seite von GL 196:
é 8.46 ´ 10 -17
ù
-10
9
´ 0.0552 ´ e1.55125´10 ´ 2´10 - 1 ú
3.46 ´ 107 ´ ê
-10
ë1.55125 ´ 10
û
(
(
)
)
= 3.46 ´ 107 ´ 1.095 ´ 10 -8 = 0.379
Bezogen auf einen Wert von 134Xe/130Xe » 2.55 für die Atmosphäre oder den oberen Erdmantel entspricht das einer Änderung auf 134Xe/130Xe = 2.93 oder (0.379/2.55) ´100 =
14.8%. D.h. die beobachteten krustalen Variationen des 134Xe/130Xe-Verhältnisses lassen
sich leicht als Folge des in-situ-Zerfalls (Spaltung) von 238U erklären.
Entwicklun
gslinie der
kontinentale
n Kruste
3
isc
hu
ng
str
en
d
e
2.6
M
är
ph
os
m
134Xe/130Xe
3.4
unterer Mantel?
3.8
At
Analog ergibt sich für den Erdmantel eine Abschätzung unter
Annahme eines U-Gehaltes von
6ppb Þ (6´10-9/238.03)´0.9927 =
2.50´10-11 mol/g und eines 130XeGehaltes von 1.5´10 -12 cm 3 /g Þ
1.5´10-12/22400 = 6.70´10-17 mol/g
ein 238U/130Xe = 3.74´105. Das entspricht innerhalb von 2 Ga einem
Wachstum des 134Xe/130Xe von nur
3.74´10 5 ´ 1.095´10 -8 = 0.0041
oder (0.0041/2.55)´100 = 0.16%,
also rund 2 Zehnerpotenzen weniger als in Graniten. Ein derartiger
Wert ist erheblich zu niedrig, um
meßbare Variationen im 134 Xe/
130
Xe des Mantels zu verursachen.
MORB
kohlige Chondrite
2.2
Schließlich läßt sich für die „bulk6.2
6.4
6.6
6.8
7
earth“ bei einem U-Gehalt von
129Xe/130Xe
»20ppb und unter der (falschen)
Annahme, das gesamte terrestrische Xe befinde sich in der Atmo- ABBILDUNG 148 Die Xe-Isotopensystematik irdischer
sphäre, ein minimales 238 U/ 130 Xe Gesteine kann erklärt werden durch Prozesse in der früvon »5.4´10 5 abschätzen, also hen Geschichte des Sonnensystems (Variation im 129Xe/
kaum höher als für den MORB- 130Xe, möglicherweise auch ein Beitrag zur Variation von
Mantel. Das heißt, daß die hohen 134Xe/130Xe), durch den Zerfall von U über den Lauf der
134
Xe/ 130 Xe-Verhältnisse sowohl Erdgeschichte (134Xe/130Xe) und durch Mischungsprovon MORB als auch der Atmo- zesse zwischen verschiedenen Reservoiren.
sphäre gegenüber dem Wert für
Chondrite nicht oder zumindest überwiegend nicht auf dem 238U-Zerfall beruhen können,
sondern eher der Spontanspaltung von 244Pu zugeschrieben werden müssen.
Staudacher & Allègre erklären die 129Xe- und 134Xe-Überschüsse des Erdmantels gegenüber
der Atmosphäre mit dem Modell eines sehr frühen Entgasens der Erde, während der das Xe
in die Atmosphäre gelangte, wohingegen I und Pu in der festen oder flüssigen Erde verblieben. Der vollständige Zerfall von 129I und 244Pu erzeugte dann die Xe-Isotopenanomalien
im Erdmantel. Für den unteren Erdmantel nehmen Staudacher & Allègre ein höheres
134
Xe/130Xe an als für den oberen Erdmantel (Siehe Abbildung 147, Abbildung 148), weil in
den oberen Erdmantel durch Subduktion von Sedimenten atmosphärisches Xe gelangt,
184
A. Radiogene Isotopensysteme
während die ursprüngliche Xe-Isotopie der festen Erde im tiefen Mantel wohl weitgehend
konserviert wurde.
Aus dem 129Xe-Überschuß der Atmosphäre über den Wert von Chondriten schätzten Staudacher & Allègre ein Bildungs- (Entgasungs-)Alter der Atmosphäre von »25 – 10Ma nach
der Bildung der Erde ab und aus den Daten für die Gesamterde eine Bildung der Erde (was
auch immer „Bildung“ hier bedeutet) von »50 – 70Ma nach den Meteoriten. Wenn man als
Bildungsalter der Meteorite »4.55 Ga annimmt, läge demnach das Bildungsalter der Erde
bei »4.48 – 4.50 Ga; die Entgasung der primitiven Erde hätte nochmals 10 – 25 Ma später
stattgefunden.
Abbildung 149[232] zeigt modellhaft die Entgasungsgeschichte des Erdmantels und die Entwicklung der Atmosphäre für die Isotopenverhältnisse 4He/3He (also nicht aufgetragen als
3
He/4He), 40Ar/36Ar und 129Xe/130Xe. Infolge der kurzen Halbwertszeiten von 129I (und
244
Pu) steigt die Xe-Isotopie nur während »10 Halbwertszeiten dieser Nuklide an und wird
im Mantel seitdem als konstant angenommen. Im Gegensatz dazu werden 4He und 40Ar
durch den Zerfall von U, Th und K fortwährend nachgebildet, so daß sich kein Endwert für
die Isotopenverhältnisse von 4He/3He und 40Ar/36Ar einstellen konnte. Die He-Isotopie der
Atmosphäre ist gerechnet für einen Fall ohne He-Diffusion in den interplanetaren Raum,
was in einem gut 6-mal höheren Wert resultiert als es dem gemessenen entspricht.
11000
4He/3He
507000
407000
10000
307000
9000
7100
207000
8000
107000
7000
4.55 4.50 4.45 Ga
7000
7000
4
3
2
1
0 Ga
4
3
2
1
0 Ga
40Ar/36Ar
300
10
20000
200
5
10000
100
0
0
129Xe/130Xe
4
3
2
1
0 Ga
6.75
3
2
1
0 Ga
1
0 Ga
6.40
in der
Atmosphäre
im Erdmantel
6.34
6.34
4
ABBILDUNG 149
4
6.45
7.00
6.50
0
4.55 4.50 4.45 Ga
3
2
1
0 Ga
4
3
2
Modell der Entwicklung der Isotopien der Edelgase über den Verlauf der Erdgeschichte
185
Edelgase und abgeklungene Radionuklide
16.3
Hf-W-Chronometer
Mit kurzlebigen bei der Nukleosynthese (siehe Kapitel 2.4, Seite 9) gebildeten Radionukliden einiger Elemente lassen sich Differentiationsprozesse in kleinen und großen Körpern
des Sonnensystems verfolgen. Über die Zeit der Nukleosynthese steigt die Konzentration
solcher Nuklide langsam (s-Prozeß) oder sehr rasch (r-Prozeß) an. Wenn ein (dem heutigen
Sonnensystem) naher Stern, der in einer Supernova-Explosion geendet ist, für die Entstehung aller radioaktiven r- und p-Prozeß-Nuklide verantwortlich ist, ist die Zeit dieser
Nukleosynthese extrem kurz. Nach deren Ende zerfallen die Radionuklide mit ihrer charakteristischen Halbwertszeit. Dies ist in Abbildung 150 für einige wichtige kurzlebige Nuklide
dargestellt. Es ist offensichtlich, daß mit solchen Nukliden nur Prozesse verfolgt werden
können, die in der frühesten Geschichte des Sonnensystems abliefen, und nur in Körpern,
die früh erkaltet sind.
238U
1.0
40K
235U
0.6
Elementbildung
Elementzerfall
0.4
182Hf, 53Mn,
U,
235
238
n
0.0
53 M
26Al
U,
2 Hf
0.2
18
26Al
40K
relative Häufigkeit
0.8
keine Zeitskala
0.00
0.05
0.10
0.15
Zeit seit Ende der Nukleosynthese [Ga]
ABBILDUNG 150
186
Schematische Darstellung von Bildung und Zerfall nukleosynthetisch gebildeter Radionuklide. Bei t = 0 endet die Nukleosynthese. Wichtige kurzlebige
Radionuklide wie 182Hf oder 53Mn sind nach 50 Ma oder rascher weitgehend
zerfallen. Der Zerfall der langlebigen U-Isotope und des 40K über 150 Ma
sind zum Vergleich dargestellt. 26Al und 53Mn mögen in der Frühzeit des
Sonnensystems in solch hohen Gehalten vorhanden gewesen sein, daß sie
eine erhebliche Wärmequelle in den inneren Planeten darstellten. Möglicherweise können kurzlebige neutronenarme radioaktive Nuklide wie 26Al,
41
Ca und 53Mn auch in der T Tauri-Phase der Sonne durch Spallationsreaktionen mit hoch energetischen Protonen gebildet worden sein[ 2 3 4 ] , [ 2 3 5 ] ;
das ist die Phase, in der ein sehr junger Stern – noch vor Zünden der Kernfusion in seinem Innern – durch einen intensiven solaren Wind die Reste der
Staubwolke „wegbläst“, aus der er gebildet wurde – eventuell der Beginn
der Entstehung von Planeten. Hoch energetische Protonen werden heute in
der Sonne bei relativ seltenen starken magnetischen Ausbrüchen beobach-
A. Radiogene Isotopensysteme
tet. Solche Ausbrüche sind in den jungen Sternen, die rezent im Orion-Nebel gebildet werden, um zwei Zehnerpotenzen häufiger und um denselben
Faktor stärker.10Be, dessen Existenz in Ca–Al-reichen Einschlüssen des Chondriten Allende durch Isotopenvariationen des Elementes B belegt ist, wird
nicht bei der Nukleosynthese in Sternen gebildet; für seine Bildung werden
Spallationsreaktionen im frühen Sonnensystem verantwortlich gemacht[236].
182
Hf ist ein neutronenreiches Nuklid, für welches das Modell der Bildung im
frühen Sonnensystem jedoch nicht anwendbar ist. Andererseits stammt es
wegen seiner relativ großen Halbwertszeit vielleicht nicht unbedingt aus einer Supernova, sondern mag wie die heute noch auf der Erde vorhandenen
radioaktiven Isotope schwerer Elemente in der Galaxis durch eine Reihe von
Supernovae einen Gleichgewichtswert erreicht haben[237].
Stellvertretend für die abgeklungenen Radionuklide soll hier das Hf-W-Chronometer
besprochen werden. Das r-Prozeß-Nuklid 182Hf zerfällt mit einer Halbwertszeit von »9 Ma
in 182W und kann folglich Isotopenanomalien in Wolfram erzeugt haben. Als sehr schwer
flüchtiges Element läßt sich W nur schwierig mittels Thermionenmassenspektrometrie
bestimmen (negativ geladene Ionen), und es ist erst der Entwicklung von doppelfokussierenden ICP-Massenspektrometern mit Multikollektoren als Auffänger zu verdanken, daß
sich die Isotopenzusammensetzung von W inzwischen präzise bestimmen läßt[20]. Hf verhält sich lithophil, W dagegen mäßig siderophil. Daher wird bei Silikat–Metall-Segregationen eine starke Fraktionierung dieser Elemente erwartet. In der Metallphase wird sich die
Isotopenzusammensetzung von W infolge eines sehr kleinen Hf/W-Verhältnisses im Vergleich zur Silikatphase nicht oder kaum noch verändert haben.
Ein Isotopensystem mit einem abgeklungenen Radionuklid muß anders als ein konventionelles Mutter–Tochtersystem mit noch vorhandenem radioaktivem Mutternuklid beschrieben werden. Für das Hf–W-System ergibt sich die Anzahl an heute vorhandenen Atomen
182
W als Summe der zur Zeit t=0 (Ende der Nukleosynthese oder Alter des Sonnensystems)
vorhandenen Atome 182W0 plus dem Anteil, der durch den vollständigen Zerfall von
ursprünglich vorhandenem 182Hf dazugekommen ist, also:
182
W = 182W0 + 182Hf
Diese Gleichung wird auf das Isotop
nachgebildet wurde:
[GL 197]
184
Hf normiert, das nicht durch einen Zerfallsprozeß
182
W æ 182W ö
=ç
÷ +
184
W è 184 W ø 0
182
184
Hf
W
Das Verhältnis auf der linken Seite dieser Gleichung kann man an einer Probe messen; die
beiden Verhältnisse auf der rechten Seite sind dagegen unbekannt. Multipliziert man das
zweite Verhältnis auf der rechten Seite mit dem Verhältnis eines stabilen Hf-Isotops, z.B.
180
Hf/180Hf, dann ergibt sich:
182
184
W æ 182W ö
=ç
÷ +
W è 184 W ø 0
182
180
Hf
´
Hf
180
184
Hf
W
[GL 198]
Der letzte Term auf der rechten Seite ist ebenfalls an einer Probe meßbar; er ist proportional
dem Hf/W-Verhältnis. Dies ist für eine kogenetische Serie von Proben, insbesondere Minerale aus Meteoriten, eine Geradengleichung in den Koordinaten von 182W/184W (y) und
180
Hf/184W (x). Der Achsenabschnitt entspricht dem initialen 182W/184W und die Steigung
dem initialen 182Hf/180Hf. Im Gegensatz zu einer gewöhnlichen Isochronengleichung ist
ein Alter aus dieser Beziehung aber nicht ableitbar. Im Gegensatz zu anderen Chronometern wie dem 53Mn–53Cr-Chronometer[233] konnten für das 182Hf–182W-System bislang
keine initialen Werte auf diese ideale Weise gewonnen werden. Die W-Isotopenvariation
187
Edelgase und abgeklungene Radionuklide
von Meteoriten ist in Abbildung 151 dargestellt[238],[239],[240]. Die niedrigsten 182W/184WVerhältnisse haben demnach die Eisenmeteorite, gefolgt von den gewöhnlichen Chondriten. Es existiert eine Diskrepanz zwischen den frühen Daten[238],[239] und neueren Daten für
die kohligen Chondrite[240],[241],[242], über deren Ursache nur spekuliert werden kann[242]
(nicht korrekt korrigierte Masseninterferenzen, Kontamination durch irdisches W, unvollständige Auflösung der Proben bei der Erzeugung der älteren Daten). Im Vergleich zu den
neuen Chondritdaten weist die Silikatfraktion der Erde – der Erdkern ist naturgemäß nicht
zugänglich – höhere W-Isotopien auf. Noch höhere Werte zeigen die SNC-Meteorite, die
wohl vom Mars stammen, und insbesondere die beiden Eukrite Juvinas und ALHA78132.
Die negativen eW-Werte der Eisenmeteorite relativ zu den kohligen Chondriten zeigen an,
daß die Eisenmeteorite aus Mutterkörpern stammen, die sehr früh im Sonnensystem differenziert sind zu einer Zeit, als noch 182Hf existierte. Ihre 182W/184W-Isotopien stellen eine
gute Näherung an den Initialwert des Sonnensystems dar, der aber immer noch eine Obergrenze sein muß. Auch der Mutterkörper der Eukrite, Mars und Erde haben eine Metall/Silikat-Fraktionierung erfahren, als noch eine beträchtliche Menge an 182Hf vorhanden war.
32
28
24
20
12
Erde
C1-Chondrite
gewöhnliche Chondrite
Eisenmeteorite
SNC-Meteorite
Eukrite
10
«W
8
6
4
2
0
Erde
-2
-4
-6
ABBILDUNG 151
188
W-Isotopenvariation in verschiedenen Typen von Meteoriten (gefüllte Symbole: [238], [239]; offene Symbole: [240]). Der e-Wert (Erläuterung auf
Seite 57) ist relativ zu Proben der silikatischen Erde definiert, die als in dieser
Hinsicht homogen gilt. Da verschiedene Laboratorien trotz fast gleicher
Normierung zu verschiedenen Werten für das 182W/184W der irdischen Proben kommen (0.86500[238], 0.864696[240], 0.864778[242]), wurde auf die
A. Radiogene Isotopensysteme
Angabe der Absolutwerte verzichtet. Die Daten für die gewöhnlichen Chondrite beziehen sich auf Konzentrate von Metallphasen. Eine lunare Probe
(hier nicht dargestellt, hat ein 182W/184W, das von dem der Erde nicht unterscheidbar ist[243]. Die alten Daten für die C-Chondrite[238] sollten als inkorrekt angesehen werden.
Die unterschiedlichen W-Isotopien verschiedener Typen von Meteoriten bergen grobe
Informationen über das Alter der Differenzierung relativ zum Alter der Eisenmeteorite oder
relativ zu den ältesten Objekten des Sonnensystems. Die Anzahl an Atomen des zu einer
bestimmten Zeit t nach der Bildung der ältesten Objekte noch vorhandenen 182Hf ergibt
sich aus der Differenz der zur Zeit t = 0 vorhandenen Menge und des radiogen entstandenen 182W:
182
Hft = 182Hf0 – 182Wrad
Ersetzt man 182Hft durch die Definition der Zerfallsgleichung, wird daraus:
Hf0 ´ e-lt = 182Hf0 – 182Wrad
182
Umgeformt und normiert auf 184W erhält man:
æ 182W ö
æ 182Hf ö
- lt
=
ç 184 ÷
ç
÷ ´ 1- e
è W ø rad è 184 W ø 0
(
)
und für das gesamte 182W/184W:
æ 182 W ö
æ 182 W ö
æ 182W ö
= ç 184 ÷ + ç 184 ÷
ç 184 ÷
è W ø gesamt è W ø 0 è W ø rad
æ 182Hf ö
æ 182 W ö
æ 182W ö
= ç 184 ÷ + ç 184 ÷ ´ 1 - e - lt
ç 184 ÷
Wø0
è W ø gesamt è W ø 0 è
(
)
und schließlich durch Multiplizieren von (182Hf/184W)0 mit 180Hf/180Hf:
æ 182W ö
æ 182 W ö
æ 182Hf ö
= ç 184 ÷ + ç 180 ÷ ´
ç 184 ÷
è W ø gesamt è W ø 0 è Hf ø 0
180
184
Hf
´ 1 - e - lt
W
(
)
[GL 199]
Für im Vergleich zur Halbwertszeit große Zeiten t entspricht diese Gleichung der GL 198.
189
Edelgase und abgeklungene Radionuklide
182W/ 184W
Interne Hf–W-Isochronen mit präzise
bestimmten BilH-Chondrit Ste. Marguerite
dungsaltern bieten
0.8655
sich an, um das
NM–1
initiale 182 Hf/180 Hf
des Sonnensystems
NM–2
abzuschätzen.
Kleine et al.[240]
0.8650
wählten dazu zwei
H-Chondrite. Für
NM–3
einen davon sind
die Daten in Abbildung 152 reproduziert. Die Daten für
0.8645
eine magnetische
M
und drei verschiedene nicht magneM = magnetische Fraktion
NM = nicht magnetische Fraktion
tische Fraktionen
liegen auf einer
0.8640
Geraden, deren
0
2
4
6
8
10
12
14
Steigung direkt dem
180Hf/ 184W
182
Hf/180Hf-Verhältnis zur Zeit der
[240]
. Die
Schließung dieses ABBILDUNG 152 Interne Hf–W-Isochrone eines H-Chondrits
-4
Steigung
entspricht
nach
GL
198
einem
Wert
von
(0.85±0.05)´10
.
Systems entspricht.
Das Alter des HChondrits ist auf Grund von hoch präzisen U–Pb-Datierungen an Phosphaten mit
4.5627±0.0006 Ga bekannt[244]. Da die Mutterkörper der Meteorite vergleichweise rasch
abgekühlt sind, wird man dieses Alter auch für dasjenige der Schließung des Hf–W-Systems
ansetzen dürfen. Für das Alter des Sonnensystems setzen Kleine et al.[240] dasjenige der CaAl-reichen Einschlüsse (CAIs) in Chondriten an, das zu 4.566±0.002 Ga bestimmt
wurde[245]; die CAIs gelten als älteste Aggregate des Sonnensystems. Damit ergibt sich für
die initiale Hf-Isotopie
æ 182 Hf ö
æ 182 Hf ö
9
= ç 180 ÷
´ e l Dt = 0.85 ´ 10 -4 ´ e l ( 4.566 - 4.5627)´ 10 = 1.09 ´ 10 -4
ç 180 ÷
Hf ø 4.566 Ga è
Hf ø 4.5627 Ga
è
mit einem Fehler von ±0.09´10-4. Cameron glaubt dagegen, daß die CAIs älter sind als das
Sonnensystem und bereits in der Explosionshülle einer Supernova entstanden[246]; damit
wäre der obige Wert für das Sonnensystem zu hoch angesetzt.
Für differenzierte Körper des Sonnensystems mit hohem Hf/W-Verhältnis läßt sich aus den
Hf–W-Isotopien die Zeit ihrer Differenzierung relativ zum „Bildungsalter des Sonnen–
systems“ vor 4.566 Ga abschätzen[240]. Eukrite sind basaltische (also differenzierte) Meteorite, deren Mutterkörper der Asteroid Vesta sein könnte. Eine interne Hf–W-Isochrone[247]
lieferte ein initiales 182Hf/180Hf von »8´10-5. Daraus läßt sich ein Alter von
æ 182 Hf ö
æ 182 Hf ö
1
- lt
Þ t = ln
ç 180 ÷ = ç 180 ÷ ´ e
l
Hf ø t è
Hf ø 0
è
190
(
(
182
182
Hf
180
Hf
180
)
Hf )
Hf
0
t
=
æ 1.09 ´ 10 -4 ö
1
ln
ç
÷ » 4 Ma
7.7 ´ 10 -8 è 8 ´ 10 -5 ø
A. Radiogene Isotopensysteme
40
30
«'W (relativ zu « bei t=0)
nach dem Bildungsalter des
Sonnensystems
vor 4.566 Ga für
die Bildung der
Eukrite errechnen [240] , d.h. für
die Differenzierung ihres Mutterkörpers in einen
silikatischen und
einen metallischen Teil – in guter Übereinstimmung mit der
Chronologie, wie
sie sich aus den
Chronometern
53
Mn– 5 3 Cr- und
60
Fe–60Ni
ergibt[248],[249].
C-Chondrite
Eukrite
Mars (Silikatanteil)
Erde (Silikatanteil)
20
Beginn des Sonnensystems (t=0): 4566 Ma
«W zu Beginn des Sonnensystems = 0
10
0
0
20
40
60
80
Ma nach Beginn des Sonnensystems
GL 199 eignet
sich ebenfalls für ABBILDUNG 153 Abschätzung der Zeit der Differenzierung der Erde, des
A b s c h ä t z u n g e n Mars und des Mutterkörpers der Eukrite in metallischen Kern und silikatides Differenzie- schen Mantel. Der Einfachheit halber ist eW = 0 als Wert zur Zeit der Entsterungsalters[240]. In hung des Sonnensystems definiert (entsprechend 182W/184W » 0.86436).
Abbildung 153 ist Nach ca. 10 Halbwertszeiten (90 Ma) ist praktisch alles 182Hf zerfallen.
dazu der radiogen
entstandene Teil des 182W/184W [= (182W/184W)gesamt – (182W/184W)0] als eW aufgetragen. Im
Gegensatz zur üblichen Definition des e-Wertes (Seite 57) wird hier der Einfachheit halber
nur der Initialwert des Sonnensystems als 0 definiert (entsprechend (182 W/ 184 W) 0 »
0.86436). Der heutige Unterschied von ca. 37eW-Einheiten der Eukrite über die Chondrite
läßt sich bei einem Hf/W-Verhältnis der Eukrite von »35 (entsprechend 180Hf/184W = Hf/
W´1.18 »41) und einem Hf/W der C-Chondrite von 1.33 erklären, wenn die Differenzierung des Mutterkörpers der Eukrite in einen metallischen Mantel und einen silikatischen
Kern 4 Ma nach dem Beginn des Sonnensystems stattgefunden hat, in exzellenter Übereinstimmung mit dem Wert, der aus der internen Hf–W-Isochrone erhalten wurde[247]. Bei
einem Hf/W-Verhältnis von 17.7 für den primitiven Erdmantel ergibt sich der heutige
Unterschied von knapp 2eW zwischen Chondriten und Erde, wenn die Differenzierung der
Erde in metallischen Kern und silikatischen Mantel ca. 34 Ma nach dem Beginn des Sonnensystems stattfand – sofern dies ein Ereignis und kein kontinuierlicher Vorgang in der
Frühgeschichte der Erde gewesen ist. Für den Mars erhält man mit Hf/W = 5.1 für den Silikatanteil und einem Unterschied von knapp 2.5eW zu den C-Chondriten ein Kern–MantelDifferenzierungsalter von rund 14 Ma nach dem Beginn des Sonnensystems.
Voraussetzung dafür, daß diese Abschätzungen sinnvoll sind, sind homogene W-Isotopenzusammensetzungen der Silikatanteile dieser Körper. Yin et al.[242] sind unabhängig von
Kleine et al.[240] zu einer sehr ähnlichen Hf–W-Chronologie des Sonnensystems gelangt.
191
Edelgase und abgeklungene Radionuklide
Überraschenderweise sind für ca. 3.8 Ga alte
+1
archaische Sedimente
archaische Metasedimente variable und z.T.
Ø Enstatitchondrite
negative e W-Werte um -1 gefunden wor0
CV3-Chondrit Allende
[241]
den
. Diese Daten werden im Sinn eines
Ø Eisenmeteorite
-1
späten intensiven Bombardements der Erde
durch Meteorite interpretiert, wie es auch aus «W
-2
der Kratergeschichte des Mondes bekannt ist.
Die W-Isotopien scheinen eine Mischungs-3
linie hin zu Meteoriten zu bilden (Abbildung
154), wobei aber nicht zwischen verschiede-4
0.001
0.01
0.1
1
10
100
nen Typen von Chondriten und EisenmeteoCr/Ti
riten unterschieden werden kann. Es wird
vorgeschlagen, daß die Sedimente in Wasser
abgelagert wurden, wobei sowohl terrestri- ABBILDUNG 154 W-Isotopie von archaischen
sche Gesteine als auch meteoritisches Mate- Metasedimenten aus Isua (Westgrönland) und
für
rial das Liefergebiet der Sedimente bildeten. Labrador (Kanada) im Vergleich zu Daten
[241]
.
Ge8 verschiedene Typen von Meteoriten
Unter der Annahme einer Zeitdauer von 10 a
für das intensive Bombardement hätte je strichelt eingezeichnet ist eine RegressionsgeQuadratmeter Erdoberfläche im Durch- rade durch die Daten der Metasedimente.
schnitt eine Menge in der Größenordnung von 102 Tonnen niedergehen können, entsprechend einer mehrere Zehner Meter hohen Schicht. Es ist dann anzunehmen, daß sich dieser späte meteoritische Eintrag auch in erhöhten Gehalten der Elemente der Platingruppe
niedergeschlagen hat, wofür es vage Hinweise in den Gesteinen von Isua gibt.
Es sei noch erwähnt, daß sich durch abgeklungene Radionuklide erzeugte Isotopenanomalien auch zu anderen Zwecken eignen: Shukolyukov und Lugmair[115] haben in Proben von
der Kreide/Tertiär-Grenze in Dänemark und in Spanien eine kleine negative Anomalie im
53
Cr/52Cr relativ zur Erde von ca. -0.3 bis -0.4e-Einheiten festgestellt. Ein geringer Teil des
heutigen 53Cr ist durch Zerfall von 53Mn im frühen Sonnensystem entstanden. Auf der
Erde sind die Cr-Isotopien in allen Gesteinen identisch, während verschiedene Meteorite
unterschiedlich große Anomalien konserviert haben. Die Cr-Anomalie an der K/T-Grenze
läßt sich durch den Einschlag eines kohligen Chondriten deuten. Noch wesentlich größere
Cr-Isotopenanomalien, entsprechend einem höheren Anteil an chondritischem meteoritischem Material, wurden in archaischen Gesteinen aus dem Barberton Mountain Greenstone-Gürtel Südafrikas gefunden[116].
192
B. Stabile Isotope
17.0
Stabile Isotope • Allgemeines
In der Geochemie der stabilen Isotope untersucht man Variationen in den Häufigkeitsverhältnissen der leichten und/oder flüchtigen Elemente; das sind vor allem H, Li (für dieses Element siehe z.B. [250], [251]), B, C, N, O, (Si), S, Ca und Se (z.B. [252], [253]). Mit fortschreitender Verbesserung der Präzision von massenspektrometrischen Analysen und
Entwicklung neuer Meßtechniken – namentlich der ICP-MS-Technik (siehe Seite 27) – wurden weitere Elemente dieser Liste zugefügt, insbesondere Übergangsmetalle wie Fe (z.B.
[254], [255]), Cu (z.B. [256]) und Zn[257], Mo[258],[259],[260] und sogar Tl[68]. Die relativen Massenunterschiede zwischen dem schwersten und dem leichtesten Isotop sind bei den leichten Elementen groß, z.B. 1.125 für 18O/16O, während der Unterschied für 205Tl/203Tl nur
noch 1.010 beträgt. Am höchsten ist die Variation beim Wasserstoff mit »2, und daher
beobachtet man für dieses Element Isotopenfraktionierungen, also selektive Anreicherungen des schweren Isotops Deuterium (2H oder D) oder leichten Isotops 1H, die um ca. eine
Zehnerpotenz höher sind als die der übrigen Elemente. Viele der hier relevanten Elemente
kommen in mehreren Oxidationsstufen vor; einige Elemente gehen in der Natur zudem
Verbindungen ein, in denen sie fest, flüssig oder gasförmig vorliegen. Im Fall des Bors spielt
die stark pH-abhängige Koordination in Komplexen eine Rolle. Gemeinsam ist vielen Elemente zudem, daß ihre chemischen Bindungen einen beträchtlichen kovalentem Anteil
haben. Obwohl die Ca- und Mg-Isotope große Massenunterschiede aufweisen (1.20 für
48
Ca/40Ca oder 1.083 für 26Mg/24Mg), fand man bei diesen Elementen in der Natur nur eine
recht geringe Variation der Isotopenverhältnisse. Diese Elemente weisen in ihren Bindungen überwiegend Ionencharakter auf und/oder kommen in ihren Mineralen meist gebunden an Sauerstoff vor, Mg z.B. in der Regel mit oktaedrischer Umgebung, so daß bei ihnen
auch Gitterplatzwechsel keine Triebfeder einer Isotopenfraktionierung sein kann. Aber
auch hier beginnt sich die Situation zu ändern. So fand man in Tropfsteinen weltweiter
Vorkommen Variationen im 26Mg/24Mg von insgesamt gut 4‰, wobei die Unterschiede
sowohl auf Variationen zwischen den Wässern als auch auf den Ausfällungsprozeß des Karbonats zurückzuführen sind[261]. Bei den schweren Elementen Fe, Cu und Zn wird die Fraktionierung sowohl biologischen als auch abiogenen Prozessen zugeschrieben, wobei die
Mechanismen im einzelnen jedoch längst nicht vollständig gedeutet werden können. Für
Cr, Fe, Cu und Zn liegen die Isotopenvariationen – unabhängig von der Ursache – immerhin noch in der Größenordnung eines Promilles pro Masseneinheit. Überraschend große
Isotopenvariationen wurden selbst bei Tl gefunden. Die 205Tl/203Tl-Verhältnisse im marinen Milieu streuen um mehr als 2‰, wobei besonders große Unterschiede zwischen Meerwasser und bei niedriger Temperatur entstandenen hydrogenetischen Fe–Mn-Krusten
gemessen wurden (bis +14e gegenüber -8e für Meerwasser)[68]. Es wird vermutet, daß der
Adsorptionsprozeß diese Isotopenfraktionierung verursacht hat, zumal die Unterschiede
zwischen Meerwasser und diagenetisch gebildeten Krusten (kleineres H 2O-Reservoir in
Form von Porenwasser) bzw. hydrothermalen Ablagerungen (höhere Bildungstemperatur)
geringer sind. Die Isotopenunterschiede können bei den Schwermetallen mit der ICP–MSTechnik am besten aufgelöst werden, weil bei der Thermionenmassenspektrometrie die
geräteinterne Massenfraktionierung nur mit hohem Aufwand zu korrigieren ist (siehe auch
Kapitel 7.0 auf S. 75).
Die Isotopenvariationen hängen sowohl vom Massenunterschied als auch von der Masse
selbst ab. Für ein Element, z.B. den Sauerstoff, bedeutet dies, daß die Fraktionierung zwischen 17O und 16O oder zwischen 18O und 17O (fast genau) halb so groß ist die zwischen
18
O und 16O. Mit steigender Masse der Elemente sinkt der relative Massenunterschied Dm/
m, und die Fraktionierung pro Masseneinheit wird geringer, wenn man sich chemisch ähnlich verhaltende Elemente miteinander vergleicht. Abweichungen von dieser massenab-
193
Stabile Isotope • Allgemeines
hängigen Fraktionierung sind auf der Erde selten, aber z.B. aus Sulfatablagerungen
bekannt[262]. Die Anomalien werden dabei der Oxidation von Schwefel in der Atmosphäre
zugeschrieben, wobei der genaue Mechanismus allerdings erst noch aufzuklären ist.
Die Geochemie der stabilen Isotope befaßt sich mit den Isotopenvariationen oder Isotopieeffekten (letztere sind die Unterschiede in den physikalischen und chemischen Eigenschaften verschiedener Isotope eines Elementes, die auf deren unterschiedlicher Masse beruhen), die entweder durch Isotopenaustauschreaktionen verursacht werden oder denen
massenabhängige Fraktionierungen bei physikalischen und chemischen Vorgängen in der
Natur zugrunde liegen. Die Ursachen der Isotopieeffekte liegen in der Quantenmechanik,
sie lassen sich aber durch die Gesetze von Kinetik und Thermodynamik quantitativ
beschreiben.
Unterschieden werden kann zwischen kinetischen und Gleichgewichtsisotopieeffekten.
Kinetische Isotopieeffekte treten neben den Gleichgewichtseffekten auf und können sogar
größer sein als jene. Die kinetischen Isotopieeffekte lassen sich als Ungleichgewichtsreaktionen charakterisieren. Sie stehen meist im Zusammenhang mit schnellen, unvollständigen, in eine Richtung verlaufenden Vorgängen wie Verdampfung, Diffusion, Dissoziation.
Die Effekte im Zusammenhang mit Diffusion und Verdampfung kann man durch die
unterschiedlichen Translationsgeschwindigkeiten der verschiedenen Moleküle in einer
Phase oder über eine Phasengrenze hinweg erklären. Bei gegebener Temperatur ist die kinetische Energie Ekin in idealen Gasen je Molekül gleich. Z.B. gilt für 12C16O und 12C18O:
Ekin = 1 2 m1 v12 = 1 2 m2 v 22
[GL 200]
v1 v 2 = m2 m1 = 30 28 = 1.035
d.h. daß die durchschnittliche Geschwindigkeit von 12C16O »3.5% größer ist als die von
12 18
C O in demselben System. Daher können leichte Moleküle z.B. rascher aus einem
System herausdiffundieren als schwere oder rascher aus einer flüssigen in die gasförmige
Phase übertreten. Infolge eines solchen kinetischen Effekts liegt d18O (Definition siehe
Seite 202) von Wasserdampf über den Ozeanen bei » -13‰, während der Gleichgewichtswert bei nur -9‰ liegen sollte. Mit – nicht verwirklichter – Annäherung des Wasserdampfdruckes der Atmosphäre an seinen Gleichgewichtswert ginge der kinetische Anteil gegen
Null, und der Gleichgewichtseffekt würde das d18O im Wasserdampf zu -9‰ bestimmen.
Im Gegensatz dazu läßt sich die Kondensation in den Wolken zu Regen weitgehend als
Gleichgewichtseffekt beschreiben (siehe Kapitel 18.1 auf S. 205).
Moleküle, die das schwere Isotop eines Elementes enthalten, sind stabiler und haben
höhere Dissoziationsenergien als diejenigen, die das leichte Isotop desselben Elementes
enthalten (siehe nächster Abschnitt). Daher brechen z.B. Bindungen wie 12C–H oder 32S–O
leichter als 13C–H oder 34S–O. Kinetische Isotopieeffekte, die auf solchen Unterschieden in
den Dissoziationsenergien beruhen, können vor allem bei biologischen – inklusive bakteriellen – Reaktionen in der Natur außerordentlich groß sein, weil dabei die Reaktionsprodukte kontinuierlich durch den Metabolismus der Lebewesen aus der Reaktionskette
entfernt werden. So erzeugt z.B. die Photosynthese der sogenannten C3-Pflanzen (zu denen
ca. 90% der Landpflanzen und alle marinen Pflanzen gehören) eine Verarmung des schweren Kohlenstoffs 13C relativ zum leichten Isotop 12C in den Pflanzen gegenüber dem anorganischen CO2 oder HCO3- der Luft oder des Wassers von 20 bis 30‰, die der C4-Pflanzen*
* Die Namen C3 und C4 beziehen sich auf die Anzahl von C-Atomen in den beiden Kohlenhydraten,
die bei der Photosynthese in diesen Pflanzen im ersten Schritt der C-Fixierung nach Reduktion von
CO2 entstehen. Bei einer kleinen Gruppe von Pflanzen (CAM-Pflanzen (Crassulacean acid metabolism: Ananas, Kakteen und andere Sukkulenten) gleicht die chemische Reaktion derjenigen der C4Pflanzen, Licht- und Dunkelreaktion sind jedoch nicht räumlich, sondern zeitlich getrennt; CAMPflanzen halten tagsüber die Spaltöffnungen geschlossen, um den H20-Verlust zu minimieren.
194
B. Stabile Isotope
(Mais, Zuckerrohr) von 13‰ – jeweils kinetische und Gleichgewichtsfraktionierung insgesamt, wovon der letztere Anteil nur rund 5‰ bei den C3-Pflanzen ausmachen sollte. Generell werden bei biologischen Prozessen die leichten Isotope eines Elementes im Organismus
angereichert.
dissoziierte Atome
0
potentielle Energie [kcal/mol]
Kinetische Isotopieeffekte
sind vornehmlich bei Reaktionen bei niedrigen Temperaturen (also an oder nahe
d e r E r d o b e r fl ä c h e ) v o n
Bedeutung. Sie werden in
der Geochemie der stabilen
Isotope von metamorphen
oder magmatischen Prozessen daher meist nur am
Rande behandelt. Hier
beschäftigt man sich vornehmlich mit Gleichgew i c h t s i s o t o p i e e f f e k t e n.
Diese haben ihre Ursache in
der Abhängigkeit der Bindungsenergie von der
Atommasse. Wenn in einem
Molekül ein leichtes Isotop
durch ein schwereres ersetzt
wird, bleiben Kernladung
und Elektronenverteilung
und ebenso die Kurve des
Potentialenergieverlaufs
unverändert. Da schwerere
Isotope jedoch niedrigere
Schwingungsenergieniveaus besetzen als leichte,
ist ihre Bindungsenergie in
einem Molekül etwas größer
als die des Moleküls mit
dem leichten Isotop. Das ist
für den Fall des Wasserstoffmoleküls in Abbildung 155
dargestellt [263] . Beschreibt
man ein zweiatomiges
Molekül als harmonischen
Oszillator, dann berechnen
sich die Schwingungsenergieniveaus zu
104.0
109.4
103.2
105.3
harmonischer
Oszillator
H-H
H-D
D-D
Nullpunktsenergie (4.1)
interatomarer Abstand
ABBILDUNG 155 Schematisches Diagramm der potentiellen Energie des Wasserstoffmoleküls für die drei verschiedenen Spezies. Dargestellt sind die Schwingungsenergieniveaus für n = 0.
Die wichtigen Schwingungsfrequenzen liegen bei 4405 Wellenzahlen [cm-1] für H2, 3817 Wellenzahlen für HD und 3119 Wellenzahlen für D 2 . Mit steigender Temperatur werden die
Schwingungen aller Moleküle zunehmend unharmonisch und
die Unterschiede zwischen den einzelnen (hier nicht gezeigten)
Energieniveaus kleiner und kleiner, bis die Moleküle schließlich
dissoziieren. Alle Spezies des Wasserstoffs haben dieselbe spektroskopische Dissoziationsenergie [109.4 kcal/mol]; aber die
chemischen Dissoziationsenergien und die Nullpunktsenergien
unterscheiden sich um bis zu 2 kcal/mol. Die Moleküle mit dem
schwereren Isotop haben höhere Dissoziationsenergien und
sind somit stabiler als die mit dem leichten Isotop. Die Isotopenfraktionierung zwischen den Molekülen läßt sich durch Unterschiede in ihren Nullpunktsenergien erklären.
Evibr = (n + 1/2) hn
[GL 201]
mit n = 0, 1, 2, …
h = Plancksches Wirkungsquantum (6.626´10-27 erg´sec = 6.626´10-34 J´sec)
n = Schwingungsfrequenz (s-1).
Am absoluten Nullpunkt (T = -273.15°C) ist n = 0, und damit ergibt sich die Energie des
Grundschwingungszustands zu E = 1/2 hn. Die Schwingungsfrequenz berechnet sich für den
idealen harmonischen Oszillator zu
195
Stabile Isotope • Allgemeines
n=
1
2p
é
ê
ê N m =
ê kg
ê
ë
k
m
[GL 202]
ù
kg m s 2
ú
m
-1 ú
=s
ú
kg
ú
û
Darin stehen k für die Kraftkonstante und µ für die sogenannte reduzierte Masse, die sich
für ein zweiatomiges Molekül berechnet zu (m1, m2 = Massen der Moleküle M1 und M2):
m1 m2
m1 + m2
1
=
1
1
+
m2 m1
m=
[GL 203]
Aus dieser Gleichung erkennt man, daß µ mit steigender Masse m steigt und n folglich
sinkt. Damit besetzt beispielsweise das Molekül D–D niedrigere Schwingungszustände als
1
H–D oder gar 1H–1H. Die relativen Unterschiede der reduzierten Massen für verschiedene
Moleküle sind bei schweren Elementen kleiner als bei den leichten, so daß die Energieniveaus verschiedener Moleküle bei schwereren Elementen relativ näher beieinander liegen; die Fraktionierung der Isotope ist damit bei schwereren Elementen in der Natur kleiner als bei leichten.
Die Grundschwingungszustände sind in Abbildung 155 für die Moleküle D2, DH und H2
schematisch angegeben. Das Molekül des schweren Wasserstoffs besitzt demnach eine
Nullpunktsenergie, die um knapp 2 kcal/mol niedriger ist als die von H2. Bei T>>0 K werden die Molekülschwingungen zunehmend unharmonisch und die Abstände zwischen
den einzelnen Schwingungsenergieniveaus kleiner und kleiner, bis das Molekül schließlich
dissoziiert. Die Dissoziationsenergie für D2 liegt um denselben Betrag von knapp 2 kcal/
mol über der für H2, d.h. die Bindung von D2 ist etwas stärker als die von HD oder H2.
Die freie Energie, die bei Isotopenaustauschreaktionen in Erscheinung tritt, ist um Größenordnungen niedriger als Bindungsenergien oder Reaktionswärmen. Sie ergibt sich für
T = 0 K z.B. als Differenz der Nullpunktsenergien zwischen den beiden betrachteten
Molekülarten, sonst als Differenz der entsprechenden Energieniveaus für T. So ist z.B. mit
dem Isotopenaustausch
/2C16O2 + H218O
1
º 1/2 C18O2 + H216O,
der bei 25°C eine Gleichgewichtskonstante von 1.0412 aufweist, nur eine Änderung der
freien Energie
RT ln K = -23.9 cal/mol
verbunden, eine Energie, die viel zu klein ist, um chemische Reaktionen in Gang zu setzen.
Andererseits wird man davon ausgehen dürfen, daß p,T-Bedingungen, die geeignet sind,
Bindungen wie Si–O oder Al–O in Mineralen aufzubrechen und umzubauen – also Isotopengleichgewicht herzustellen – auch ausreichen werden, um in einem System chemisches
Gleichgewicht herzustellen. Mit anderen Worten: Wenn in einem System die Minerale im
stabilen Isotopengleichgewicht stehen, besteht eine große Wahrscheinlichkeit dafür, daß
das Gestein auch im chemischen Gleichgewicht steht.
Eine der wichtigsten Definitionen in der Geochemie stabiler Isotope ist die des Fraktionierungsfaktors a zwischen 2 Substanzen A und B:
196
B. Stabile Isotope
aA-B = RA/RB
[GL 204]
wobei RA,B die Verhältnisse des schweren zum leichten Isotop sind, also z.B. D/H, 13C/12C,
18
O/16O. Wenn die Isotope statistisch auf alle in Frage kommenden Positionen des betrachteten Moleküls oder der Verbindung verteilt sind, besteht zwischen a und der Gleichgewichtskonstanten K die Beziehung
a = K1/n
[GL 205]
wobei n die Anzahl der in der betrachteten Reaktion ausgetauschten Atome ist. Man kann
sich a als eine Art Verteilungskoeffizient vorstellen, der oft auch in der Form lna, 103 lna,
K, lnK, e º D = (RProbe /RStandard – 1)´103 [‰] angegeben wird. Die Gleichgewichtskonstante K
ergibt sich für eine Reaktion wie
H218O + 1/3CaC16O3
º H216O + 1/3CaC18O3
nach dem Massenwirkungsgesetz zu:
[H
K=
[H
16
2
18
2
] [
O] ´ [CaC
16
13
]
O ]
O ´ CaC 18 O3
13
3
[H
[H
13
æé
CaC 18 O3 ù
= çê
ú
ç êë CaC 16 O3 úû
è
]
]
Oö
÷
16
÷
2 O ø
18
2
Man setzt hierin Konzentrationen anstatt von Aktivitäten oder Fugazitäten ein, weil die
Verhältnisse von Aktivitätskoeffizienten für Moleküle mit verschiedenen Isotopen 1 sind.
Wie alle Gleichgewichtskonstanten, so ist auch K temperaturabhängig. Das bildet die Basis
für die Benutzung von Isotopenaustauschgleichgewichten als Geothermometer.
Aus obiger Gleichung für K kann man a berechnen. In der Reaktion wird ein Sauerstoff ausgetauscht bzw. 1 mol mit 1/3 mol CaCO3 umgesetzt; n ist daher 1 für H2O und 1/3 für
CaCO3:
13
a=K
1n
é CaC 18 O3 ù 1 3
=ê
ú
16
êë CaC O3 úû
[H
[H
18
2
16
2
] = ( O O)
O]
( O O)
O
18
16
CaCO3
18
16
H2O
Die Gleichgewichtskonstante K kann mit der sogenannten Verteilungsfunktion Q in Beziehung gesetzt werden, einer Funktion, die aus der statistischen Mechanik stammt. Die Verteilungsfunktionen enthalten alle Informationen über den Energieinhalt eines Moleküls.
Die innere Energie Eintern eines Moleküls kann als Summe aller Energieformen beschrieben
werden, nämlich einem Translationsanteil, einem Rotationsanteil, einem Schwingungsanteil, einem elektronischen sowie einem Kernspinanteil:
Eintern = Etrans + Erot + Evibr + Eel + Espin
[GL 206]
Die beiden letzten Terme sind dabei vernachlässigbar klein. Zu jedem betrachteten Zeitpunkt können Eintern und ihre Verteilung auf die verschiedenen Energieformen variieren.
Im Gleichgewicht bei gegebener Temperatur T beträgt der Anteil der Moleküle nE/n0, die
den Energieinhalt Eintern aufweisen
n E n0 = g i e - Ei
kT
[GL 207]
mit nE = Anzahl Moleküle mit Energieinhalt Eintern,
n0 = Anzahl Moleküle mit Nullpunktsenergie,
gi = statistischer Gewichtsfaktor („Entartung“ von Eintern),
k = Boltzmann-Konstante (1.3807´10-23 J/K).
Es kann sein, daß es mehr als einen Zustand mit demselben Energieniveau Ei gibt; ein solcher Zustand heißt „degeneriert“ oder „entartet“ und muß mit dem Wichtungsfaktor gi
197
Stabile Isotope • Allgemeines
versehen werden, welcher der Anzahl der einzelnen Zustände mit Ei entspricht. Durch
Summierung der Gleichung über i, d.h. alle erlaubten Energieniveaus der Moleküle, erhält
man Q:
Q = å g i e - Ei
kT
[GL 208]
i
Q wird auch als „Zustandssumme“ oder „statistische Summe“ bezeichnet. Die mittlere
Energie des betrachteten Systems von Molekülen ist dann das, was man gewöhnlich als
innere Energie bezeichnet. Wenn die erlaubten Energien des gesamten Systems von Molekülen E1, E2, … Ei, berechnet sich die mittlere Energie zu:
å ni Ei = å g i Ei e - E kT
å ni
å g i e - E kT
i
E=
= kT 2
i
¶ ln Q
¶T
[GL 209]
Für einen Isotopenaustausch, bei dem a Moleküle A, die das leichte Isotop l enthalten, mit
b Molekülen B, die das schwere Isotop s enthalten, umgesetzt werden, also
aAl + bBs
º aAs + bBl
berechnet sich die Gleichgewichtskonstante K zu
a
b
(Q ) (Q ) = (Q
K=
(Q ) (Q ) (Q
As
Bl
a
Al
a
s
Ql ) A
s
Ql )B
b
b
Bs
[GL 210]
Ähnlich wie die einzelnen Energieformen kann auch die Verteilungsfunktion eines Moleküls in die einzelnen Anteile zerlegt werden:
Qs æ Qs ö
=ç ÷
Q l è Q l ø trans
æ Qs ö
ç ÷
è Q l ø rot
æ Qs ö
ç ÷
è Q l ø vibr
[GL 211]
Die Unterschiede zwischen dem translationalen und rotationalen Anteil sind zwischen
den einzelnen Komponenten auf der rechten und linken Seite der Isotopenaustauschgleichung ähnlich groß (mit Ausnahme des Wasserstoffs), so daß im wesentlichen unterschiedliche Schwingungsenergien als Ursache der Isotopieeffekte übrig bleiben.
In die Exponentialfunktion von Q und damit auch in Q und a oder K geht die Temperatur
ein. Darauf beruht die Möglichkeit, Isotopenaustauschgleichgewichte für die Zwecke der
Geothermometrie zu nutzen. Die Druckabhängigkeit ist dagegen – zumindest für Festkörper und freie Moleküle so klein, daß sie unter den Drücken der Erdkruste vernachlässigt
werden kann. Ausnahmen sind D–H-Austauschreaktionen, an denen Wasser beteiligt
ist[264]. Die Verteilungsfunktionen sind nur für ideale Gase einfach zu berechnen, und bei
der Übertragung auf flüssige und feste Stoffe muß man eine Anzahl von mehr oder weniger
gesicherten Annahmen machen. Theoretische Berechnungen[265] haben ergeben, daß für
die Isotopenfraktionierung zwischen H2O-freien Mineralpaaren bei Temperaturen >500 °C
einfache Beziehungen des Typs
1000 ln a = A/T2
[GL 212]
2
gelten sollten (a @ 1/T ) und für die Fraktionierung zwischen Mineralen und Fluiden bei
T<500 °C Beziehungen vom Typ
1000 ln a = A/T2 + B.
[GL 213]
Petrologische Thermometer, die auf dem chemischen Austausch zwischen Phasen beruhen, zeigen demgegenüber meist eine Variation mit 1/T. Dennoch sollten die Gleichungen
nicht weit über den Bereich extrapoliert werden, für den einigermaßen gesicherte Daten
198
B. Stabile Isotope
vorliegen. Neben der Temperaturabhängigkeit zeigen a bzw. K natürlich auch eine starke
Abhängigkeit von Chemismus und Art der chemischen Bindung.
Zur Ermittlung der Gleichgewichtskonstanten für die Isotopenaustauschreaktionen bieten
sich 3 Methoden an, nämlich (a) die theoretische Berechnung, (b) die experimentelle
Bestimmung und (c) die empirische Eichung. Methode (b) ist bislang nur auf Mineral/
Fluid- und Schmelze/Fluidsysteme angewandt worden, und ist sicherlich die zu diesem
Zweck best geeignete. Sie folgt den Prinzipien der experimentellen Petrologie, wonach das
Gleichgewicht von beiden Seiten her kommend eingestellt werden muß.
e
nd
1000 ln aMineral–H2O
t
le
b
rn
Ho
vi
ko
us
M
Abbildung 156 zeigt die
°C
650
450
350
250
200
150
Temperaturabhängigkeit
des WasserstoffisotopenausFraktionierung der Wasser20
tausches einiger Mineral/
stoffisotope zwischen
H 2 O-Gleichgewichte für
Mineralen und H2O
den Wasserstoffisotopen0
austausch [263] . Insbesontin
pen
r
e
dere die FraktionierungsS
kurve für Kaolinit– H 2 O
verhält sich danach merknit
-20
oli
Ka
würdig und zeigt nicht die
Chlorit
Proportionalität mit 1/T 2 .
Bi
Nach Driesner[264] liegt die
Klinozoisit
ot
it
-40
Ursache für diese und viele
ähnliche scheinbar sonderbare D/H-Fraktionierungen
Zo
in einer nicht korrigierten
-60
isi
t
Druckabhängigkeit. Seine
Berechnungen zeigen, daß
der Druckeffekt besonders
-80
groß ist im Bereich um die
Temperatur des kritischen
Punktes von Wasser bei
1
2
3
4
5
6
Drücken zwischen ca. 22
106/T2
und 200 MPa (0.22 – 2 kbar)
und darüber, unter Bedingungen also, die für hydro- ABBILDUNG 156 Tatsächliche oder vermeintliche Temperaturthermale Austauschreaktio- abhängigkeit des Austauschs der Wasserstoffisotope D und H für
nen in der Natur relevant verschiedene Mineral/H2O-Gleichgewichte
sind (Abbildung 157-oben). Weiterhin weist er darauf hin, daß z.B. experimentelle Daten
für die D/H-Fraktionierung zwischen Epidot und H2O eine erhebliche Druckabhängigkeit
zeigen, wenn man notwendige Korrekturen an den Daten für die Struktur der Dampfphase
(polymere H2O-Cluster, deren Anteil in der Dampfphase oberhalb von 200 °C stark ansteigt, fraktionieren D und H anders als einzelne Moleküle) und den Druckeffekt der flüssigen Phase vornimmt (Abbildung 157-unten). Es ist dann zu sehen, daß oberhalb von ca.
300 °C die Temperaturabhängigkeit der D/H-Fraktionierung abnimmt, so daß diese sich
möglicherweise gar als Geobarometer eignet.
Für die Abhängigkeit von a und K vom Chemismus und der Art der chemischen Bindung
lassen sich einige systematische Charakteristika herausstellen: Bindungen an Ionen mit
hohem Verhältnis von Ladung zu Ionenradius und niedrigem Atomgewicht zeichnen sich
durch hohe Schwingungsfrequenzen aus und haben eine Tendenz, das schwere Isotop
anzureichern, um die freie Energie des Systems zu erniedrigen. So weist z.B. Quarz eine Bindung des hoch geladenen und kleinen Si4+ an Sauerstoff auf, während der Sauerstoff im
Magnetit an das relativ große, weniger hoch geladene Fe2+ und Fe3+ gebunden ist. Tatsächlich ist Quarz unter den gesteinsbildenden Mineralen – betrachtet bei gleicher Temperatur
– dasjenige mit der höchsten 18O-Anreicherung und Magnetit das 18O-ärmste.
199
Stabile Isotope • Allgemeines
200
20‰
100
50
10‰
15‰
Druck [MPa]
150
5‰
1‰
22.1MPa
s.v.p.
100
200
kritischer Punkt
300
400
500
600
Temperatur [8C]
650 550 450
1000ln aEpidot–Wasser
H 2 O scheint sich in dieses
Schema nicht einzupassen. Es
hat wesentlich höhere
Schwingungsfrequenzen
(zwischen 1600 und 3900
cm-1) als die meisten Minerale
(<1000 cm-1) und sollte von
daher 18O-reich sein. Tatsächlich ist die Fraktionierung
Mineral/Wasser bei Temperaturen unterhalb von ca. 400 –
500 °C derart, daß sich 18O in
den meisten Mineralen anreichern wird. Das liegt daran,
daß neben hoher Schwingungsfrequenz noch eine
zweite Komponente wichtig
ist, nämlich die Änderung der
Schwingungsfrequenz bei der
Isotopensubstitution; und die
ist für O–H (»1%) viel niedriger als für O–Si, O–Al oder O–
Fe (»7 – 8%). Bei tiefen Temperaturen ist dann der Effekt
der Frequenzänderung dominierend, bei hoher Temperatur die Höhe der Schwingungsfrequenz.
350 300
250
200
8C
-20
-40
400
200
100
50
Nach Quarz sind Feldspäte
s.v.p.
-60
die Minerale mit dem nächst
höheren 18 O-Gehalt. Es ist
einleuchtend, daß d18O von
-80
Feldspäten niedriger als das
0.1MPa
von Quarz ist, weil Al3+ ein
niedrigeres Verhältnis von
-100
Ladung zu Radius hat als Si4+.
1.0
2.0
3.0
4.0
5.0
Demgegenüber ist der Einfluß
106/T2 [T in K]
der übrigen Kationen der
Feldspatstruktur (Alkalien,
Ca) klein oder gar vernach- ABBILDUNG 157 Oben: berechnete Druckabhängigkeit der
D/H-Fraktionierung in H2O, dargestellt in einem p–T-Dialässigbar.
gramm. Die angegebenen Werte sind
Unter den Granaten Grossu- unterhalb des kritischen Punktes relativ zur Fraktionierung
lar und Andradit reichert der entlang der Siedekurve (s.v.p. = saturated vapor pressure) anerstere 18O relativ an, was i.w. gegeben, rechts davon relativ zur Fraktionierung beim Druck
der geringen Atommasse des des kritischen Punktes (22.1 MPa). Unten: D/H-FraktionieAl gegenüber Fe3+ zuzuschrei- rung zwischen Epidot und H O als Funktion von p und T, kor2
ben ist. ZnS reichert 34S relativ rigiert von [264] nach Literaturdaten.
zu PbS an, auch hier erklärbar
durch die geringere Masse des Zn.
Karbonate sind im Vergleich zu anderen Mineralgruppen reich an 18O, was der Bindung des
Sauerstoffs an das kleine und hoch geladene C4+ zuzuschreiben ist sowie – im Fall sedimentärer Karbonate – der niedrigen Bildungstemperatur. Innerhalb der Gruppe der Karbonate
hat MgCO3 die höchste relative Anreicherung an 18O, wenn die Karbonate mit Wasser im
Isotopenaustauschgleichgewicht stehen, erklärbar durch den kleinen Ionenradius von Mg.
200
B. Stabile Isotope
18
O/16O-Fraktionierung zwischen MCO3 und H2O
TABELLE 14:
M
Mg
Ca (Aragonit)
Ca (Calcit)
Mn
Sr
Cd
Ba
Pb
D18O (25°C)a
31.2
28.7
28.0
–
26.8
26.1
24.5
–
D18O (240°C)
–
–
7.2
6.8
6.2
6.0
4.7
4.5
Radius (M2+)
0.72
1.18
1.00
0.83
1.16
0.95
1.36
1.18
Atomgewicht (M)
24.3
40.1
40.1
54.9
87.6
112.4
137.4
207.2
a. D18O = 1000 ln a(MCO3 – H2O)
Cd2+ und Ca2+ haben denselben Radius. Das niedrigere D18O von CdCO3 unterstreicht
deutlich die Rolle der Atommasse für das Gleichgewicht. Tabelle 14[263] gibt eine Aufstellung von D18O-Werten für den Sauerstoffaustausch zwischen Karbonaten und Wasser.
Tabelle 15 schließlich gibt hypothetische Werte für die zu erwartende Abfolge der O-Isotopien für eine Reihe von Mineralen in Metapeliten an[266].
TABELLE 15:
Hypothetische Abfolge der d18O-Werte koexistierender Minerale aus
pelitischen Schiefern bei niedrig-bis mittelgradiger Metamorphose
Mineral
Quarz
Dolomit
K-Feldspat, Albit
Calcit
Anorthit
Muskovit, Paragonit
Augit, Diopsid
Orthopyroxen
d18O
+15.0
+14.2
+13.0
+12.8
+11.5
+11.3
+10.5
+10.5
Mineral
Hornblende
Titanit
Olivin, Granat
Zirkon
Biotit
Chlorit
Ilmenit
Magnetit
d18O
+10.0
+10.0
+9.5
+9.5
+8.5
+8.0
+5.5
+4.5
Anders als bei den radiogenen Isotopen werden die Isotopenverhältnisse der stabilen Isotope stets relativ zu Standardmaterialien angegeben. Herstellung und Verteilung dieser
Standards ist vor einigen Jahren der internationalen Atomenergiebehörde (IAEA) in Wien
übertragen worden[269]. Zur Angabe der Isotopien von Wasserstoff und Sauerstoff wird vornehmlich „standard mean ocean water“ (VSMOW „V“ für „Vienna“) benutzt, das von R.
Weiss und H. Craig* für die IAEA hergestellt wurde.
Bei den Kohlenstoffisotopen ist der Vorrat des ursprünglichen Standards PDB (Peedee
Belemnite aus South Carolina) längst erschöpft. Dies war der Standard, der an der University of Chicago im Anschluß an eine theoretische Arbeit von Urey† bei der Entwicklung der
* Harmon Craig (1926–2003), amerikanischer Geochemiker an der Scripps Institution of Oceanography in La Jolla; als Schüler von H.C. Urey beschäftigte sich Craig zuerst mit C- und O-Isotopen von
Meteoriten, bevor er sich der Geochemie der Ozeane im weitesten Sinn zuwandte.
† Harold C. Urey (1893–1981) amerikanischer Chemiker, Nobelpreis für Chemie 1934 für die Entdeckung des Deuteriums. Später arbeitete Urey vor allem an grundlegenden Fragen der Kosmo- und
Geochemie. Er schlug auch die Methoden der Paläotemperaturbestimmung mittels mariner Karbonate vor (siehe Seite 209).
201
Stabile Isotope • Allgemeines
Paläotemperaturbestimmung der Ozeane über das Verhältnis 18 O/ 16 O verwendet
wurde[273]. Mit Hilfe von sekundären, an PDB geeichten Standards wird aber auch heute
noch die C-Isotopenzusammensetzung relativ zu PDB angegeben (als VPDB), desgleichen
die O-Isotopenzusammensetzung bei der Paläotemperaturbestimmung der Ozeane. Der
neuere Karbonatstandard NBS 19 mit d13CNBS19/PDB = 1.95, scheint geeignet, die übrigen
Sekundärstandards zu ersetzen.
Bei der Messung der N-Isotope wird Luftstickstoff als bequemer Standard verwendet, dessen Isotopenzusammensetzung weltweit konstant ist. S-Isotopenzusammensetzungen
werden relativ zu der von Troilit aus dem Eisenmeteorit Canyon Diablo angegeben (in Rußland Troilit aus dem Meteoriten Sikhote Alin); auch hier werden zahlreiche Sekundärstandards verwendet.
Tabelle 16 zeigt eine Übersicht über die Isotopenzusammensetzungen der wichtigsten der
aufgezählten Standards[266].
TABELLE 16:
Isotopenverhältnisse einiger internationaler Standards
Standard
SMOW
Verhältnis
D/H
18
O/16O
akzeptiertes Verhältnis
0.00015576±10
0.00200520±43
17
O/16O
13
C/12C
18
O/16O
17
O/16O
15
N/14N
34 32
S/ S
PDB
Luftstickstoff
Canyon Diablo-Troilit
0.000373±15
0.0112372±29
0.0020671±21
0.000379±15
0.0036765±81
0.0450045±93
Die Fehler entsprechen 95% Vertrauensintervall (2s) und beziehen sich auf die jeweils letzten Stellen.
Mit Hilfe solcher Standards werden die Zusammensetzungen der stabilen Isotope in der dFormulierung angegeben (ähnlich wie bei einigen radiogenen Isotopensystemen in der
e-Formulierung):
æ R
ö
d [ ‰] = ç Pr - 1÷ ´ 103
è RStd
ø
[GL 214]
z.B. für Sauerstoff:
é
d [ ‰] = ê
ê
êë
(
(
18
18
)
O)
O
16
O
16
O
Pr
Std
ù
- 1ú ´ 103
ú
ûú
wobei Pr für Probe, Std für Standard steht. Sind verschiedene Standards in Gebrauch, dann
lassen sich die d-Werte der Proben leicht auf die verschiedenen Standards umrechnen, vorausgesetzt der Umrechnungsfaktor der beiden Standards untereinander ist bekannt:
202
(i)
æR
ö
d Std 2/Std1 = ç Std 2 - 1÷ ´ 103 Þ RStd 2 = 10 -3 d Std 2/Std1 + 1 ´ RStd1
è RStd1
ø
(ii)
ù
é
æ R
ö
RPr
ú ´ 103
d Pr / Std2 = ç Pr - 1÷ ´ 103 = ê
1
ú
ê 10 -3 d Std 2/Std1 + 1 ´ RStd1
è RStd 2
ø
û
ë
(
(
)
)
B. Stabile Isotope
(
)(
)
Þ RPr = 10 -3 d Pr / Std2 + 1 10 -3 d Std2 / Std1 + 1 RStd1
(iii)
(
)(
)
-3
ù
é 10 -3 d
æ R
ö
Pr / Std2 + 1 10 d Std2 / Std1 + 1 RStd1
d Pr / Std1 = ç Pr - 1÷ ´ 103 = ê
- 1ú ´ 103
ú
ê
RStd1
è RStd1
ø
û
ë
æ R
ö
d Pr / Std1 = ç Pr - 1÷ ´ 103 = 10 -3 d Pr / Std2 + 1 10 -3 d Std2 / Std1 + 1 - 1 ´ 103
R
è Std1
ø
[(
) ]
)(
[GL 215]
d und a können ebenfalls leicht ineinander umgerechnet werden. Gegeben seien die
d-Werte für zwei Phasen A und B (z.B. verschiedene Minerale oder verschiedene Aggregatzustände derselben Komponente):
æ RA
ö
d A/SMOW = ç
- 1÷ ´ 103 Þ RA = 10 -3 d A/SMOW + 1 RSMOW
è RSMOW
ø
(
)
æ RB
ö
d B/SMOW = ç
- 1÷ ´ 103 Þ RB = 10 -3 d B/SMOW + 1 RSMOW
R
è SMOW
ø
(
(
(
)
)
)
10 -3 d A/SMOW + 1
RA
a=
=
RB
10 -3 d B/SMOW + 1
[GL 216]
Mit Hilfe von GL 215 lassen sich die Umrechnungen vornehmen, die erforderlich sind, um
die auf frühere Standards bezogenen Analysen von D/H, 13C/12C und 18O/16O zu korrigieren. Verbindlich sind derzeit[270]:
•
•
•
D/H-Verhältnisse werden relativ zu VSMOW angegeben, derart, daß dDSLAP/VSMOW =
-428‰ ist.
13
C/12C-Verhältnisse werden relativ zu VPDB angegeben, so daß d 13CNBS19/VPDB =
+1.95‰.
18
O/16O wird entweder relativ zu VSMOW oder zu VPDB angegeben, dergestalt daß
18
d OSLAP/VSMOW = -55.5‰.
203
Wasserstoff und Sauerstoff
18.0
Wasserstoff und Sauerstoff
Wasserstoff und Sauerstoff werden gemeinsam behandelt wegen der engen Vergesellschaftung der beiden Elemente in der Natur.
Wasserstoff besteht
vorzugsweise Verlust von
aus den beiden stabi1H aus der Atmosphäre
len Isotopen H und
D. In SMOW liegt die
Häufigkeit des Deutemeteorisches Wasser
riums bei 155.8 ppm.
Wegen des großen
Meerwasser
Isotopieeffekts als
Folge des großen
Sedimente
Massenunterschieds
zwischen H und D
Magmatite und Metamorphite
zeigt Wasserstoff eine
riesige Isotopenfrakjuvenile Wässer?, OH-Minerale aus
dem Mantel?
tionierung in der
Natur, die >50% auf
der Erde ausmacht
-300
-200
-100
0
( s i e h e A b b i l d u n g -400
[266]
158)
.
dD [‰]
Sauerstoff besteht aus
drei stabilen Isotopen
mit den Massenzahlen 16, 17 und 18,
deren natürliche
H ä u fi g k e i t e n b e i
»99.63%, 0.0375%
bzw. 0.1995% liegen.
Das Verhältnis 18 O/
16
O variiert auf der
Erde um »10% als
Folge sowohl von
Gleichgewichts- als
auch von kinetischen -60
Prozessen (Abbildung
158[263]
100
meteorisches Wasser
Meerwasser
Sedimente
Metamorphite
granitische Gesteine
basaltische Gesteine
-40
-20
0
20
40
d18O[‰]
Die massenspektro18
16
metrische Messung ABBILDUNG 158 Variation der Verhältnisse D/H [oben] und O/ O
erfolgt in Form von [unten] in Gesteinen und Wässern
Gasen – H2 und CO2. Silikate werden meist mit BrF5 aufgeschlossen, seltener mit ClF3 oder
F2. Bei Karbonaten genügt die Umsetzung mit H3PO4, bei H2O die Äquilibrierung mit CO2.
Größtes Gewicht ist auf Vollständigkeit der chemischen Reaktion zu legen (Aufschluß)
bzw. auf Einhaltung konstanter Bedingungen zur Erzielung der Gleichgewichtseinstellung
bei Reaktionen mit bekanntem K (Äquilibrierung). Bei unvollständiger Reaktion kann
nicht erwartet werden, daß Reaktionsprodukt und ungelöster Rest eine identische Isotopenzusammensetzung haben. Die Reproduzierbarkeit guter massenspektrometrischer Analysen liegt für Sauerstoff bei »±0.02‰. Wesentlich größere Fehler resultieren jedoch aus
der Aufbereitung der Proben, so daß für den Gesamtfehler einer O-Messung »±0.1‰, für
Wasserstoff von »±0.5 – 2‰ angenommen werden kann. Inzwischen erzielt man gute
Ergebnisse mit der Laserfluorierung, bei der ein kleines Volumen eines Minerals durch
einen Laserstrahl verdampft und mit F2-Gas fluoriert wird; es ist zu erwarten, daß dieses
204
B. Stabile Isotope
Verfahren für viele Anwendungen die konventionellen Aufschlußmethoden bald weitgehend verdrängen wird. Bei der Analyse irdischer Proben beschränkt man sich in der
Regel auf die beiden Sauerstoffisotope 16O und 18O. Dabei wird unterstellt, daß durch
natürlich ablaufende Prozesse auf der Erde die Sauerstoffisotope massenabhängig fraktioniert werden, d.h. d17O = 0.52 d18O (der Faktor ist nicht exakt 0.5, weil der relative Massenunterschied Dm/m zwischen 16O und 17O etwas größer ist als halbe Massenunterschied zwischen 16O und 18O). Auf die Meteorite trifft das jedoch nicht zu (hier spielen Effekte der
Elemententstehung und -fraktionierung im solaren Nebel eine Rolle), und daher werden in
der Kosmochemie sowohl 18O/16O als auch 17O/16O gemessen, was wegen der geringen
Häufigkeit von 17O zudem größeren analytischen Aufwand erfordert.
18.1
Sauerstoff und Wasserstoff in Hydro- und Atmosphäre
In der Geochemie der stabilen Isotope wird zwischen Ozeanwasser und meteorischem Wasser unterschieden. Als meteorisch wird Wasser bezeichnet, das den meteorologischen
Zyklus durchlaufen hat, also Verdampfung (über den Ozeanen), Kondensation, Niederschlag. Das Wasser auf den Landoberflächen fällt damit auch unter diese Kategorie, d.h. das
Wasser der Flüsse und Seen sowie der Gletscher.
1.14
1.014
Fraktionierungsfaktoren:
a18O =
aD =
1.010
1.12
1.10
a18O
aD
1.008
1.08
1.006
1.06
1.004
1.04
1.002
-50
Fraktionierungsfaktor, D
Fraktionierungsfaktor, 18O
1.012
(18O/16O)H2O-flüssig
(18O/16O)H2O-Dampf
(D/H)H2O-flüssig
(D/H)H2O-Dampf
1.02
0
50
100
150
T [8C]
ABBILDUNG 159
Temperaturabhängigkeit der Isotopenfraktionierung bei der Verdampfung
von Wasser
Wenn das Wasser an der Oberfläche der Ozeane verdampft, ist die Dampfphase am schweren 18O und an D relativ verarmt, weil H216O den höchsten Dampfdruck aller denkbaren
Wassermoleküle hat. dD und d18O des Wassers in der Atmosphäre haben daher negative
dSMOW-Werte. Abbildung 159[16] zeigt die experimentell bestimmten Fraktionierungskurven
für Gleichgewichtsverdampfung von H2O für a18O und aD in Abhängigkeit von der Temperatur. Tatsächlich hat das atmosphärische H2O im Nordpazifik und Nordatlantik aber ein
deutlich negativeres d18O (um »4‰) als es dieser Gleichgewichtskurve entspricht, was
kinetischen Effekten zugeschrieben wird.
205
Wasserstoff und Sauerstoff
Wenn das atmosphärische Wasser zu
Schematische Darstellung der
Regen kondensiert, reichern sich die
Sauerstoffisotopenfraktionierung
im
schweren Isotope im Regen an, und
atmosphärischen Wasserkreislauf
-17‰
der in der Gasphase verbleibende
Rest wird daher isotopisch immer
-15‰
-5‰
leichter, wie es in Abbildung 160[266]
(Regen)
schematisch gezeigt ist. Dieser
-3‰
Zusammenhang hat sich als nützlich
Dampf
(Regen)
erwiesen, um die Heimat von „Ötzi“ d18O=-13‰
im heutigen Südtirol zu lokalisieren,
das seinen Niederschlag vorzugsOzean
weise vom Mittelmeer erhält, und
Kontinent
d18O=0‰
nicht im Gebiet nördlich der Wasserscheide, das im Einzugsgebiet des
wesentlich weiter entfernten Atlan- ABBILDUNG 160 Das Ausregnen von Wolken bewirkt
tiks liegt[267].
als Funktion der Entfernung vom Entstehungsort der
Die Kondensation des Wasserdamp- Wolken (Ozeane) eine Isotopenfraktionierung des
fes zu (Regen)Wasser unter Gleichge- H2O, das isotopisch ständig leichter wird.
V
V
V
È
wichtsbedingungen kann durch das
Rayleighsche Destillationsgesetz beschrieben werden:
R R0 = f (
a -1)
[GL 217]
0
ABBILDUNG 161 Fraktionierung der Sauerstoffi-
-5
fl
sig
-10
da
-15
m
pf
fö
r
m
ig
d18O[‰]
üs
sotope bei der Kondensation von Wasser aus der
Dampfphase nach dem Rayleighschen Destillationsgesetz (a = 1.0092). Das initiale d18O des
Wasserdampfes wurde zu -9.2‰ angenommen.
Das erste Kondensat dieses Dampfes hat dann
ein d18O von 0. Durch Entfernung jedes Inkrements von kondensiertem Wasser aus der Wolke
wird das d18O des Dampfes sinken, und damit
sinkt auch d18O des folgenden Kondensats ständig.
-20
-25
-30
1.0
0.8
0.6
0.4
0.2
0.0
Anteil des verbleibenden Dampfes
wobei R das 18O/16O- oder D/H-Verhältnis des verbleibenden Wasserdampfes ist, R0 das
initiale 18O/16O- oder D/H-Verhältnis des Wasserdampfes vor Beginn der Kondensation
und f der Bruchteil des noch verbleibenden Wasserdampfes. Durch Einsetzen von [GL 216]
erhält man daraus für die Sauerstoffisotope:
10 -3 d 18O + 1
R
a -1
=f( ) =
R0
10 -3 d 18O + 1
(
)
[GL 218]
0
oder
[
(
d 18O = ìíf (a -1) 10 -3 d 18O
î
206
)
0
]
[(
a -1
+ 1 - 1üý ´ 103 = f ( ) d 18O
þ
)
0
]
+ 103 - 103
[GL 219]
B. Stabile Isotope
wobei d18O der Wert des verbleibenden Wasserdampfes ist. In Abbildung 161[16] ist d18O
von Wasserdampf und Kondensat gegen f aufgetragen für T = 25°C und a = 1.0092 sowie
(d18O)0 = -9.2‰. Der darin aufgetragene d18O-Wert des Kondensats im Gleichgewicht mit
Wasserdampf läßt sich berechnen durch Auflösen von [GL 216], wenn A = Wasser und B =
Wasserdampf gesetzt wird:
[(
) ]
d L/SMOW = a 10 -3 dV /SMOW + 1 - 1 ´ 103
(
)
d L/SMOW = a dV /SMOW + 103 - 103
Da die Fraktionierung
bei der Kondensation
von Wasserdampf für
beide Isotopensysteme
gleichsinnig verläuft,
verwundert es nicht,
daß es hier eine Korrelation gibt, die sich mit
dD = ad18O + b
[GL 221]
beschreiben läßt und
als meteoric water line
bekannt ist.
100
0
schwerster
Niederschlag
„Meteoric Water Line“
dD = 8´d18O + 10
ten
dD [‰]
rei
nie
-200
he
ho
-40
abgeschlossene
Becken
Steigung der Trajektorien
der Verdampfung »5
en
-400
-50
B
ige
dr
-100
-300
it
Bre
-30
-20
-10
0
10
d18O [‰]
0
-10
d18O [‰]
Aus Abbildung 161
geht hervor, daß d 18 O
von Wasserdampf und
Wasser mit zunehmender Kondensation 18Oärmer werden. Darin
liegt die Ursache, daß
das Süßwasser auf den
Kontinenten niedrigere D/H- und 18O/16OVerhältnisse hat als
Ozeanwasser. Ausnahmen sind Gewässer in
Gebieten mit exzessiver
Verdunstung.
[GL 220]
-20
-30
d18O = 0.695´T – 13.6
-40
-40
-30
-20
-10
0
10
20
Die Werte von a und b
Jahresdurchschnittstemperatur der Luft [8C]
sind innerhalb gewisser
Grenzen variabel, weil
ABBILDUNG 162 Oberes Diagramm: „meteoric water line“. Die Isoabhängig von den
topie von Wasser und Schnee zeigen eine ausgeprägte Abhängigkeit
Bedingungen der Vervom der geographischen Breite und damit der Temperatur der Kondampfung und des Niedensation. Wässer abgeschnürter Becken und einiger Seen und Flüsderschlags sowie dem
se im nordöstlichen Afrika mit extremer Verdampfungsrate zeigen
Transport des Wassers
eine Abweichung von der sonst gültigen Beziehung mit einer Steiin der Gasphase.
gung um 5. Das untere Diagramm zeigt den Zusammenhang zwiTypisch sind Werte von
schen dem Jahresmittel von d18O des Niederschlags und der Lufta » 8 und b » 5 – 10.
temperatur
Diese Gleichung ist in
[16]
der Abbildung 162
schematisch dargestellt. Die Gleichgewichtsfraktionierung stabiler
Isotope verläuft proportional 1/T2; daher findet man die größte Fraktionierung (d.h. die
niedrigsten Werte von dD und d18O in den Niederschlägen der Polarregionen, während
207
Wasserstoff und Sauerstoff
Niederschläge in den Äquatorgebieten Werte bis zu d18O, dD » 0 annehmen können. Die
inverse Kopplung der Fraktionierung mit der Temperatur ist aus dem unteren Teil der
Abbildung 162 abzulesen, in der das mittlere jährliche d18O des lokalen Niederschlags
gegen die mittlere jährliche Temperatur aufgetragen ist. Bei hohen Temperaturen nähert
sich d18O dem Wert der Ozeane an als Ausdruck der Tatsache, daß die Fraktionierung mit
steigender Temperatur kleiner wird.
d18O [‰]
d18O [‰]
Die d18O- und dD5
Werte von Seewasser
schwanken nur wenig
43°N
um 0‰ SMOW. Die
35°N
NADW
0
Schwankung
der
Norweg. See
Golf von Maine
Werte für ozeanisches
Oberflächenwasser ist
Ostküste Grönland
vor allem auf die
-5
Effekte der Verdampfung zurückzuführen,
wobei die leichten Iso-10
tope bevorzugt in die
nahe Grönland
Dampfphase eintreten. Parallel zur
zunehmenden Ver-15
10
20
30
40
dampfung geht eine
Salinität [‰]
Dichteerhöhung des
Meerwassers. Das ver0.50
dampfte
Wa s s e r
gelangt über isoto0.25
nordatlantisches
pisch leichten NiederTiefenwasser
schlag, z.T. über salz0.00
arme Flüsse vom
nordatlantische
pazifisches
Oberflächenwässer
Festland, wieder in die
Tiefenwasser
-0.25
Ozeane zurück und
vermischt sich mit
Wasser des
Weddell-Meeres
antarktisches
dem Oberflächenwas-0.50
Bodenwasser
ser. Es ist daher nicht
verwunderlich, daß
-0.75
für das Oberflächenwasser eine lineare
-1.00
Beziehung zwischen
33
34
35
36
d18O und der Salinität
Salinität [‰]
besteht, die z.B. für
den Nordatlantik in
die Formel
ABBILDUNG 163 oberes Diagramm: Beziehung zwischen Salinität
und d18O [‰] für den Nordatlantik; unteres Diagramm: Beziehung
d18O = -21.2 + 0.61 ´ zwischen Salinität und d18O [‰] für verschiedene OzeanwasserSalinität (‰) [GL 222] massen
gekleidet werden kann[271] und in Abbildung 163 dargestellt ist[266]. Auf dieser Mischungslinie liegt auch das nordatlantische Tiefenwasser (NADW), das sich durch Vermischung
von wärmerem, höher salinarem Wasser des Golfstroms mit kaltem, niedriger salinarem
arktischem Wasser bildet und infolge seiner höheren Dichte auf den Grund des Nordatlantiks sinkt und nach Süden strömt, wo es ungefähr ab 20°N von noch dichterem antarktischem Tiefenwasser der Gegenströmung unterschichtet wird[272] und schließlich mit dem
antarktischen Zirkumpolarstrom auch in Indik und Pazifik verfrachtet wird, wobei es allmählich seine Identität verliert. Dieses antarktische Tiefenwasser liegt nicht auf der
Mischungslinie für das nordatlantische Oberflächenwasser, weil es auf andere Weise ent-
208
B. Stabile Isotope
steht: Im antarktischen Winter kühlt sich das Wasser des Weddell-Meeres soweit ab, daß
sich nahezu salzfreies Treibeis auf seiner Oberfläche bildet. Der Fraktionierungsfaktor a für
diesen Prozeß beträgt für Sauerstoff nur 1.002, d.h. das Eis hat ein d18O um 2‰ höher als
das Oberflächenwasser, was in der Massenbilanz für das Oberflächenwasser vernachlässigbar gering ist. Das zurückbleibende kalte, hochsalinare Wasser sinkt auf den Meeresboden
ab und vermischt sich dabei mit weniger salinarem, eher etwas wärmerem Wasser. Das so
entstandene Wasser hat die höchste Dichte des Ozeanwassers überhaupt und strömt auf
dem Meeresboden nach Norden, wobei es sich natürlich langsam weiter vermischt und
seine Identität verliert. Infolge seines Bildungsmechanismus hat dieses Tiefenwasser vor
der Antarktis ein d18O wie das Oberflächenwasser, aber eine höhere Dichte (die sich als
Effekte der niedrigen Temperatur und hohen Salinität ergibt), was im unteren Teil von
Abbildung 163 dargestellt ist[266]. Bei seiner Strömung im Pazifik und Indik mischt es sich
mit dem nordatlantischen Tiefenwasser. Daß das pazifische Tiefenwasser (PDW) nicht
genau auf einer Mischungslinie zwischen antarktischem und arktischem Tiefenwasser
liegt, wird auf die Gegenwart zusätzlicher Komponenten zurückgeführt.
Eine der frühesten Anwendungen der Geochemie stabiler Isotope (O, C), die auch heute
noch in der Geologie erhebliche Bedeutung hat, ist die Paläotemperaturbestimmung, die
auf eine grundlegende thermodynamische Arbeit von H. Urey zurückgeht[273]. Er schlug
darin vor, es sei prinzipiell möglich, durch die Analyse der Sauerstoffisotopenzusammensetzung der Karbonatschalen fossiler mariner Organismen auf die Temperatur der Paläoozeane zurückzuschließen. Grundlage dafür ist das Isotopenaustauschgleichgewicht
/3 CaC16O3 + H218O
1
º 1/3 CaC18O3 + H216O
mit der Gleichgewichtskonstanten
([CaC
K=
18
[H
und
K1 n =
([
][
O] [H
CaC 18 O3
CaC 16 O3
[H
16
18
2
2
O
]
18
2
])
13
] [CaC O ])
O] [H O]
16
O3
3
16
[GL 223]
2
13
13
=
RCaCO3
RH2O
=a
Dieses Austauschgleichgewicht ist temperaturabhängig. Die nötigen experimentellen
Eichungen wurden bereits Anfang der 1950-er Jahre von Mitarbeitern Ureys an der University of Chicago gemacht und in Gleichungen gekleidet. Später stellte sich heraus, daß die
Fraktionierung zwischen Calcit und Wasser anders ist als die zwischen Aragonit und Wasser. Diese Fraktionierungen werden durch die beiden folgenden Gleichungen beschrieben[274]:
Calcit – Wasser: (°C) = 13.85 – 4.54 D Cc -H2O + 0.04 D2Cc -H2O
[GL 224]
Aragonit – Wasser: (°C) = 17.04 – 4.34 D Arg -H2O + 0.16 D2Arg -H2O
[GL 225]
Darin ist D = dCc, Arg – d H2O die ‰-Differenz zwischen CO2, das aus dem Calcit bzw. Aragonit durch Reaktion mit H3PO4 bei 25°C freigesetzt wurde, und CO2, das bei 25°C mit dem
Meerwasser äquilibriert wurde, aus dem sich das Karbonat ausgeschieden hat. Die beiden
Fraktionierungskurven sind in Abbildung 164 dargestellt. Man erkennt daraus, daß die DWerte für relevante Temperaturen nur zwischen » -2 und +4‰ liegen und die beiden Fraktionierungskurven fast parallel verlaufen, d.h. D Cc -H2O » D Arg -H2O .
Schon bald nachdem die Methode geeicht war, zeigten sich jedoch die Grenzen der Paläotemperaturbestimmung der Ozeane, und man benutzt die Methode heute lieber allgemein,
um (relative) Änderungen der Temperatur der Ozeane aufzuzeigen, d.h. als Indikator für
209
Wasserstoff und Sauerstoff
das Paläoklima. Ein Beispiel dafür ist in Abbildung 165 angegeben für d18OPDB von Foraminiferen aus der Karibik über die letzten » 700 Ka[275]. Das d18O des Meerwassers ist, wie im
folgenden Abschnitt angeführt, in Warmzeiten niedriger als in Kaltzeiten; außerdem wird
die Fraktionierung zwischen CaCO3 und Wasser mit zunehmender Temperatur geringer
(bzw. D wechselt das Vorzeichen). Daraus folgt, daß die d18O-Werte der Karbonate in Warmzeiten niedriger sind als in Kaltzeiten.
–H
O
H2
it
on
–
lcit
Ca
g
Ara
Das Problem der Ableitung einer exakten
24
Temperatur aus der Sauerstoffisotopie von
organogen gebildetem Karbonat liegt in 8C
20
der Zweideutigkeit, die das d18O anzeigt. In
GL 224 und GL 225 stehen mit T und d H2O
16
2 Unbekannte. d H2O ist aber, wie bereits
gesagt, örtlich nicht konstant – und auch
12
nicht zeitlich. Örtlich besteht eine Abhängigkeit von der Salinität. In den Kaltzeiten
8
ist ein nicht vernachlässigbarer Teil des
Wassers über Verdampfung und Nieder4
schlag als (isotopisch leichtes) Gletschereis
auf den Kontinenten gebunden; als Folge
0
müssen die Ozeane global ein höheres
-6 -4 -2
0
2
4
6
d18O gehabt haben als heute, so daß Karbod
nat, das aus Meerwasser mit derselben
Karbonat – H2O
Temperatur ausgeschieden wird, in Kaltzeiten ein höheres d18O hat als in WarmzeiABBILDUNG 164 Paläotemperaturberechnung
ten. Das kalte Bodenwasser der Ozeane
auf der Basis des Isotopenaustauschs zwischen
wird von den Temperaturschwankungen
Calcit und Wasser bzw. Aragonit und Wasser
nicht oder kaum beeinflußt. Sein d18O ist
daher nur vom globalen d18O-Wert der Ozeane und damit dem Globalklima abhängig.
Wenn man daher benthonische Foraminiferen analysiert, wird deren d18O nur Ausdruck
des Globalklimas sein, während gleichzeitig damit lebende planktonische Foraminiferen
ein d18O haben, das sowohl vom Globalklima bzw. globalen d18O der Ozeane abhängig ist
als auch von der lokalen Temperatur des oberflächennahen Meerwassers.
d18O [‰]
O
2
Ein weiteres Problem
besteht darin, daß manche
marine Organismen Karbonat nicht im Gleichgewicht
mit dem Ozeanwasser ausscheiden (z.B. Crinoiden,
Echinodermen, Asteroideen). Und schließlich ist
zu beachten, daß Isotopenaustauschreaktionen auch
bei der diagenetischen
Rekristallisation stattgefunden haben können oder daß
Aragonit in Calcit umgewandelt werden kann.
-2
-1
0
0
100
200
300
400
500
600
700
Alter [Ka]
ABBILDUNG 165 d18O-Fluktuationen in den Schalen der Fora-
miniferen Globigerina sacculifer in Kernbohrungen der Karibik
im Verlauf des Quartärs. Die Minima (niedrige Werte) und Maxima spiegeln Warm- bzw. Kaltzeiten wider.
Trotz dieser Probleme bestätigt das d18O von Foraminiferen für das Pleistozän sehr gut die
globale Klimaentwicklung. Für ältere Proben werden Temperaturableitungen dagegen
zunehmend problematischer infolge von zunehmenden Problemen mit diagenetischer
Rekristallisation und schlechterer Kenntnis von d H2O .
210
B. Stabile Isotope
18.2
Sauerstoff und Wasserstoff in der Lithosphäre
Bereits im vorigen Kapitel war angeführt, daß für die Isotopenfraktionierung zwischen zwei
Phasen und T einfache Beziehungen der Form
1000 lna = A/T 2 + B
[GL 213]
bestehen, wobei B für die meisten Austauschgleichgewichte zwischen Mineralen = 0 ist.
Nach [GL 216] gilt außerdem:
a12 =
R1 10 -3 d1 + 1
=
(1,2 = Komponenten).
R2 10 -3 d 2 + 1
Logarithmiert wird daraus:
(
)
(
)
ln a12 = ln 10 -3 d1 + 1 - ln 10 -3 d 2 + 1
Für Reaktionen in natürlichen Gesteinssystemen liegen die d-Werte für Sauerstoff bei maximal einigen 10‰. Man darf deshalb in guter Näherung schreiben:
(
)
ln 10 -3 d + 1 » 10 -3 d
-3
z.B. für d = 10‰: ln (10 ´10 + 1) = ln (1.010) = 0.00995 » 0.010.
Damit ergibt sich: ln a12 » 10 -3 (d1 - d 2 )
oder D12 º d1 - d 2 » 1000 ln a12 =
bzw. nach T aufgelöst: T »
A
+B
T2
[GL 226]
A ( D12 - B) (T in Kelvin).
Wenn 2 Minerale (1 und 2) Sauerstoff mit einem Reservoir (z.B. einem Magma) äquilibriert
haben, dann ist die Differenz ihrer individuellen d18O-Werte also eine Funktion der Temperatur. Bei experimentell oder empirisch bekannter Temperaturabhängigkeit von a12
kann man daher T durch Messung von d1 und d2 einfach berechnen. Infolge experimenteller Schwierigkeiten (niedrige Reaktionsgeschwindigkeit) sind die Fraktionierungsfaktoren
a12 zwischen verschiedenen Mineralen leider weitgehend unbekannt und müssen über die
Fraktionierungsfaktoren Mineral/H20 abgeleitet werden, was die Verläßlichkeit der Bestimmungsgleichungen nicht gerade erhöht. a Min- H2O -Werte sind für viele gesteinsbildende
Minerale, wie Quarz, Feldspäte, Magnetit, Glimmer, Rutil oder Karbonate für Temperaturen
bis »800°C recht gut bekannt. So lauten die Temperaturbestimmungsgleichungen für den
Sauerstoffisotopenaustausch zwischen Quarz und H20 bzw. zwischen Magnetit und H20:
d Qtz - d H2O » 1000 ln a Qtz - H2O = 4.10 ´ 10
6
T2
6
und d Mag - d H2O » 1000 ln a Mag - H2O = -1.47 ´ 10
- 370
T2
- 370
[GL 227]
[GL 228]
Durch Subtraktion beider Gleichungen erhält man den Fraktionierungsfaktor zwischen
Quarz und Magnetit:
(d
Qtz
) (
)
- d H 2O - d Mag - d H 2O » 1000 ln a Qtz - H 2O - 1000 ln a Mag - H 2O
6
6
= æ 4.10 ´ 10 2 - 370ö - æ -1.47 ´ 10 2 - 370ö
è
ø
è
ø
T
T
Wegen a12 = R1/R2 wird daraus:
211
Wasserstoff und Sauerstoff
[(
) (
)]
d Qtz - d Mag » 1000 ln RQtz - ln RH2O - ln RMag - ln RH2O = 5.57 ´ 10
DQtz-Mag= dQtz – dMag » 1000 ln aQtz-Mag = 5.57´106/T2
6
T2
[GL 229]
Diese Gleichungen sind insofern recht typisch, als daß im allgemeinen für Mineral-H20Austauschreaktionen B ¹ 0 und für Mineral-Mineral-Gleichgewichte B » 0 ist.
Durch derartige Kombination ist eine ganze Reihe thermometrischer Gleichungen abgeleitet worden, von denen einige wichtige in Tabelle 17 zusammengestellt (Koeffizienten A
und B der Temperaturgleichung) und in Abbildung 166 aufgetragen sind.
Wenn man von ³3 Mineralen das d18O bestimmt hat, ist es im Prinzip möglich, T aus ³3
Gleichungen zu berechnen (für D12, D13, D23). Erhält man annähernd dieselben Temperaturen, spricht einiges dafür, daß man die Temperatur eines geologisch relevanten Prozesses
erhalten hat. Konkordante Temperaturen geben v.a. Quarz, Magnetit, Feldspäte, Muskovit
und Calcit. Man sollte sich jedoch stets vergegenwärtigen, daß in langsam abkühlenden
Gesteinen (Plutonite, Metamorphite) nicht erwartet werden kann, daß alle Mineralpaare
bei derselben Temperatur aufhören, Sauerstoffisotope miteinander auszutauschen. Vorsicht ist daher geboten, die aus der Sauerstoffisotopenfraktionierung koexistierender Minerale berechneten Temperaturen als die der Kristallisation eines Plutons oder die Maximalbedingungen der Metamorphose anzusehen.
TABELLE 17:
Geothermometrische Gleichungen basierend auf dem
Sauerstoffisotopenaustausch zwischen koexistierenden Mineralena
Mineral
Quarz – Albit
Quarz – Anorthit
Quarz – Plagioklas
Quarz – Jadeit
Quarz – Diopsid
Quarz – Magnetit
Quarz – Zoisit
Quarz – Muskovit
Albit – Diopsid
Albit – Magnetit
Anorthit – Diopsid
Anorthit – Magnetit
Plagioklas – Amphibol
Plagioklas – Biotit
Pyroxen – Olivin
Pyroxen – Granat
A
0.50
1.59
0.46 + 0.55bb
1.09
2.08
6.1±0.2
1.56
2.20
1.58
5.61
0.49
4.52
2.178 – 1.04b
2.27 – 1.04b
1.24
0.21
B
0
0
(0.02 – 0.85b)
0
0
0
0
-0.60
0
0
0
0
-0.30
-0.60
0
0
a. Tabelle nach der Zusammenstellung in [16]
b. b = Molenbruch der Anorthitkomponente im Plagioklas
212
DT [°C]
400 – 800
400 – 800
500 – 800
400 – 800
400 – 800
800
500 – 700
>500
400 – 800
400 – 800
400 – 800
400 – 800
>500
>500
>500
>500
B. Stabile Isotope
An
or
th
it–
M
ag
ne
tit
arz
–M
ag
ne
tit
etit
it–M
agn
Qu
Al b
D18O [‰]
Voraussetzung für die Anwend8C 1000 800
600
500
400
barkeit solcher Isotopen7
thermometer ist natürlich die
Einstellung eines Isotopen6
gleichgewichts zwischen den
analysierten Mineralen eines
Gesteins, d.h. das System muß
5
sich langsamer Temperaturänderung jeweils angepaßt
haben, und der Isotopenaus4
tausch muß sich im geschlossenen System vollzogen haben.
Diese Bedingungen sind
3
jedoch in höchstens der Hälfte
der untersuchten Fälle erfüllt,
2
vor allen Dingen, weil die
Minerale metamorpher und
lcit
magmatischer Gesteine mit
z–Ca
1
Quar
fluiden Phasen reagieren, die
dem System zugeführt oder
von ihm weggeführt werden.
0
Wie lassen sich aber Gleichge0
0.5
1.0
1.5
2.0
2.5
3.0
wichte von Ungleichgewich6
2
-2
10 /T [K ]
ten in einem Datensatz unterscheiden? – Aus der Identität
ABBILDUNG 166 Variation von D18O mit der Temperatur.
von
D18O ist die Differenz zwischen den individuellen d18O-Werten der koexistierenden, äquilibrierten Minerale.
d1 – d2 º D12
folgt trivialerweise
d1 = d2 + D12
[GL 229]
Das heißt nichts anderes, als daß im geschlossenen System bei gegebener Temperatur (d.h.
bei konstantem D12) das Gleichgewicht zwischen zwei Phasen in Gesteinen mit unterschiedlicher Pauschalzusammensetzung eingestellt ist, wenn die Phasen in einem Plot von
d1 gegen d2 auf eine Gerade mit der Steigung 1 und Achsenabschnitt D12 fallen. Als Folge
lokal unterschiedlicher Pauschalzusammensetzung verschiedener Teile eines Gesteinskomplexes können die Mineralpaare, die auf eine konstante Temperatur äquilibriert sind, überhaupt erst unterschiedliche d18O-Werte entwickeln. Man denke z.B. an einen Granit, bei
dem das Mineral Quarz in allen Bereichen des Plutons ursprünglich (so halbwegs) dasselbe
d18O bei der Erstarrung des Komplexes hatte, desgleichen Feldspat. Infolge variabler Mengenverhältnisse beider Minerale, also lokal heterogener Pauschalzusammensetzung,
kommt es im Zuge einer Metamorphose zur Einstellung auf eine neue Temperatur, wobei
der Isotopenaustausch jedoch auf den Nahbereich beschränkt ist, so daß Quarz und
Feldspat aus verschiedenen Teilen des Komplexes zwar dasselbe D12, aber variable Werte
von d1 und d2 ausbilden. In Abbildung 167 ist das Prinzip dieser Reäquilibrierung in einem
d1-d2-Diagramm für ein Zweikomponentensystem skizziert[276]. Für T ® ¥ wird D12 = 0, d.h.
die Gerade geht durch den Koordinatenursprung. Zu niedrigeren Temperaturen hin wird
der Achsenabschnitt je nach Vorzeichen der Fraktionierung D12 positiv oder negativ. Für
Mineralpaare mit vergleichbaren Strukturen, z.B. Pyroxene und Olivin, sollte sich D12
monoton ändern, ohne aber die Gerade für T ® ¥ zu kreuzen, während im Fall sehr unterschiedlicher Strukturen oder bei Mineral-H20-Gleichgewichten die Fraktionierung diese
Gerade durchaus queren kann, d.h. das Vorzeichen der Fraktionierung ändert sich („crossover“), wie bereits im vorigen Kapitel gezeigt.
Um die Bedingung des geschlossenen Systems zu erfüllen, dürfen sich seine Masse und sein
d-Wert bei der Anpassung an die neue Temperatur nicht ändern, d.h.
213
Wasserstoff und Sauerstoff
dSystem = åxi di
[GL 230]
wobei xi die Molenbrüche der verschiedenen Phasen für das interessierende Element (z.B.
O, H) sind. Für ein Zweikomponentensystem mit den Komponenten 1 und 2 würde die
Gleichung daher lauten:
d System = x1d1 + x2d 2
oder, nach d1 aufgelöst
d1 =
d System - x2d 2
x1
=-
d System
x2
d2 +
x1
x1
[GL 231]
=
D
D
=
0
1
(T
(A
®
nf
¥
)
an
gs
te
m
pe
ra
tu
r)
D
=
2
D
=
—
3
D
=
—
4
d1
D
—
=
5
Dies ist die Gleichung einer
Geraden in den Koordinaten
d1 und d2 mit negativer Steigung. Wie ändern sich nun
x2 ® 1
die Verhältnisse der stabilen
Isotope der beiden Minerale
dieses ursprünglich homogex1 = x2
nen Zweikomponentensystems bei Temperaturänderung? Im d 1 –d 2 -Diagramm
von Abbildung 167 werden
x1 ® 1
die Minerale 1 und 2 zu
x1 = x2
Beginn durch einen Punkt
repräsentiert, der durch d10 D12
und d 20 gegeben ist, und der
wegen der Steigung 1 auf
einer genau definierten Geraden mit dem Achsenabschnitt D02 liegt. Wenn die
Minerale bei einer neuen 0
d2
Temperatur reäquilibrieren, D12
wird ein neues D 12 eingestellt; bei Temperaturerniedrigung wird sich D12 i.a. wei- ABBILDUNG 167 Änderung der d-Werte in einem geschlosseter von 0 fortbewegen, bei nen System mit zwei Phasen als Funktion der Temperatur
Temperaturerhöhung auf 0
zubewegen. Die Isotopie der beiden Minerale des Zweikomponentensystems wandert
daher vom Punkt ( d10 , d 20 ) auf die neue Gerade mit dem der neuen Temperatur entsprechenden D12 und bildet den Punkt (d1,d2). Für die Lage dieses neuen Punktes auf der Geraden mit Achsenabschnitt D 12 gibt es 2 Grenzfälle: Geht x 1 ®1 (º x 2 ®0), dann geht
d1®dSystem , d.h. die Steigung der Geraden [GL 231] wird 0, und die Minerale reäquilibrieren
auf einer Linie, die parallel zur d2-Achse verläuft. Umgekehrt, wenn x1 ®0 (º x2®1), geht
die Steigung der Geraden ®¥, d.h. die Minerale reäquilibrieren auf einer Geraden parallel
der d1-Achse, bis der Schnittpunkt mit der Geraden mit dem neuen D12 erreicht ist. Je nachdem, welche Pauschalzusammensetzung das Zweikomponentensystem vor der Reäquilibrierung hatte, dürfen die neuen Werte (d1,d2) der Phasen nur innerhalb eines rechtwinkligen Dreiecks liegen (in Abbildung 167 farbig markiert), das durch die Schnittpunkte der
Geraden für das neue D12 (= Isotherme) mit den beiden Linien der Grenzfälle der Reäquilibrierung für x1®1 und x1®0 gebildet wird. Dies ist ein Dreieck im linken oberen Quadranten (Temperaturerniedrigung) bzw. rechten unteren Quadranten (Temperaturerhöhung) in
einem Koordinatensystem mit Ursprung ( d10 , d 20 )*.
Ein Zweikomponentensystem stellt natürlich nur eine grobe Vereinfachung eines natürlichen Gesteins dar; immerhin lassen sich aber so wichtige Gesteine wie Granite (Quarz,
214
B. Stabile Isotope
Feldspat), Gabbros (Feldspat, Pyroxen), Eklogite (Pyroxen, Granat) oder Peridotit (Olivin, 2
Pyroxene) als Zweikomponentensystem annähern. Die Beschreibung von Systemen mit
mehr als 2 Komponenten ist in der Darstellung zwar schwieriger, kann jedoch auf ähnliche
Weise erfolgen. Dabei ist aber zu beachten, daß die Reäquilibrierung innerhalb eines rechtwinkligen Dreiecks nur für die beiden Endglieder mit dmin und dmax erfolgt; in den übrigen
Plots sind die Dreiecke schiefwinklig, die sich durch Projektion eines Dreiecks im d1–d2–d3Raum auf eine Ebene ergeben. Für ein Dreikomponentensystem ist dies im d–d Diagramm
in Abbildung 168 dargestellt [276] . Die initialen d -Werte dieser Phasen, die einer
Anfangstemperatur entsprechen, bei der die Minerale zuletzt äquilibriert sind, seien +6, +2
bzw. +1. Im Plot von d1 gegen d2 liegt der Anfangswert demnach auf einer Geraden mit dem
Achsenabschnitt D12 = +4, im Plot von d1 gegen d3 auf einer Geraden mit Achsenabschnitt
D13 = +5 und im Plot von d2 gegen d3 auf einer Geraden mit Achsenabschnitt D23 = +1. Nach
der Massenbilanzgleichung [GL 230] läßt sich der d-Wert des Systems ermitteln, wenn die
Proportionen der einzelnen Minerale im Gestein bekannt sind. Wird dieses System aufgeheizt auf T® ¥, dann werden die drei Minerale nach Reäquilibrierung denselben d-Wert
aufweisen (keine Fraktionierung bei hoher Temperatur), der dem des Systems entspricht.
Auch hier lassen sich wieder Grenzfälle unterscheiden: In der Auftragung von d3 gegen d1
wird für x1 ® 1 der Vektor des Isotopenaustauschs parallel der d3-Achse verlaufen, bis sich
in Mineral a und den infinitesimal kleinen Mengen der Minerale b und c der Endwert
von d = +6 einstellt. Geht x3 ® 1, dann verläuft der Isotopenaustausch entlang eines Vektors parallel der d1-Achse bis zum Endwert d = +1. Diese beiden Austauschvektoren spannen
mit der Geraden für DT®¥ ein rechtwinkliges Dreieck auf, innerhalb dessen sich der Isotopenaustausch für alle denkbaren Proportionen der drei Phasen vollziehen muß. Der Austauschvektor für x1 = x2 = x3 = 1/3 wird dann per Massenbilanz bei d = +3 enden (1/3 ´ 6 + 1/
1
3 ´ 2 + /3 ´ 1). Wenn in dem System x2 gegen 1 geht, endet der Austauschvektor bei d = +2,
also auch innerhalb des von den Trajektorien für d3 und d1 aufgespannten Dreiecks. Bei
Auftragung von d1 gegen d2 oder von d2 gegen d3 ergeben sich schiefwinklige Dreiecke, auf
die der Isotopenaustausch beschränkt ist.
8
d2
6
d1
g
d1
7
a
®
D
D
4
fü
fü
rT
rT
5
a
¥
-A
nf
an
a
3
x1 = x2 = x3 = 1/3
2
x1 = x2 = x3 = 1/3
b
1
b
c
1
2
ABBILDUNG 168
3
4
5
6
7
b
c
d2
0
0
x1 = x2 = x3 = 1/3
0
1
2
c
d3
3
4
5
6
7
0
1
d3
2
3
4
5
6
7
8
Isotopenaustausch in einem System mit den Phasen a, b und c. Die initialen d-Werte der Phasen seien +6, +2 bzw. +1, entsprechend der Äquilibrierung auf eine Anfangstemperatur. Durch Erhitzung des Systems auf T ® ¥
stellen sich nach Reäquilibrierung in allen drei Phasen identische d-Werte
ein.
* Genaugenommen dürfen die Minerale bei vollständiger Einstellung auf die neue Temperatur nur
auf der neuen Isothermen liegen; eine Streuung der Datenpunkte innerhalb eines Dreiecks charakterisiert die Einstellung auf Temperaturen irgendwo zwischen To und T1.
215
Wasserstoff und Sauerstoff
Aus
folgt
6
6008C
5
DPlag-Magnetit [‰]
Für Systeme mit ³3 Komponenten
werden in der Literatur oft D-D-Diagramme benutzt, um eine Gleichgewichtsisotopeneinstellung zu beweisen. Ein Beispiel dafür ist in
Abbildung 169 angeführt[16]. Gleichgewicht gilt als vorhanden, wenn die
D-D-Werte der Minerale aus einem
Gesteinskomplex auf eine Gerade fallen, die durch den Koordinatenursprung geht. In dem dargestellten
Fall kann die Mineral-Mineral-Fraktionierung der Sauerstoffisotope zur
Abschätzung ihrer Kristallisationstemperaturen benutzt werden. Tatsächlich ist dies zwar eine notwendige, aber keine hinreichende
Bedingung, wie aus der folgenden
Betrachtung zu erkennen ist:
700
4
800
3
1000
2
1200
Minerale aus:
Vulkaniten
Plutoniten
1
D » A/T 2 + B
1
D - B12 D 23 - B23
= 12
=
A12
A23
T2
0
0
0.5
Nach D12 aufgelöst, ergibt das
D12 =
A12 ( D 23 - B23 )
A23
+ B12
D12 =
1
DPlag–Cpx [‰]
1.5
2
ABBILDUNG 169 Mit einem D–D-Diagramm dieser
Art kann Gleichgewicht nicht nachgewiesen werden.
æ
ö
A12
A
D 23 + ç B12 - 12 B23 ÷
A23
A23
è
ø
[GL 232]
Da die Koeffizienten A und B dieser Temperaturgleichung Konstanten sind, ist dies die
Gleichung einer Geraden in Koordinaten von D12 und D23, die für D23 = 0 nur durch den
Koordinatenursprung geht, wenn der Klammerausdruck auf der rechten Seite der Gleichung ebenfalls 0 wird. In Abbildung 170 ist ein Beispiel für ein D–D-Diagramm angegeben[277]. Fall III mit den Gleichungen d1 = 2d2 + 1 und d2 = 3d3 + 0.5 verläuft nicht durch
den Ursprung und ist daher einfach als Ungleichgewicht zu identifizieren. In Koordinaten
des d–d-Diagramms repräsentiert aber auch Fall II mit den Gleichungen d1 = 2d2 + 1 und d2
= 1.5d3 + 0.5 ein Ungleichgewicht, da die Steigung der Geraden ¹ 1 ist. Im D-D-Diagramm
transformiert sich eine Reihe von Ungleichgewichtsgleichungen in Geraden durch den
Ursprung, was wie folgt nachgewiesen werden kann:
Ausgehend von den Gleichungen
D12 - b2
(1)
a2 - 1
= d 2 - d 3 Þ d 2 = a3 (d 2 - D 23 ) + b3
d1 = a2d 2 + b2 und D12 = d1 - d 2 Þ d 2 =
sowie
d 2 = a3d 3 + b3 und D 23
Þ d 2 = a3d 2 - a3 D 23 + b3
a3 D 23 = d 2 (a3 - 1) + b3 (2),
darin (1) eingesetzt: a3 D 23 =
216
a3 - 1
(D12 - b2 ) + b3
a2 - 1
B. Stabile Isotope
éa -1
ù 1
a -1
b2 + b3 ú ´
D 23 = ê 3
D12 - 3
a
a
1
1
2
ë 2
û a3
é a -1
a3 - 1
b ù
D 23 = ê 3
D12 b2 + 3 ú
a3 (a2 - 1)
a3 úû
êë a3 (a2 - 1)
35
50
D12
I
30
II
III
I
II
III
D13
40
25
30
20
15
10
I Gleichgewicht:
Startpunkt (6,2,1) und
Endpunkt (3,3,3)
0
15
20
25 0
D23
5
10
15
0
20
D23
Beispiel I repräsentiert den Fall eines Gleichgewichts (analog dem Beispiel in
Abbildung 168 für xi = 1/3); die beiden übrigen Beispiele stellen Ungleichgewichte dar.
k1/k2 < 1
geschlossenes
System
x1
=
1
1
=
2
5
0.
k
=
0
fe
ne
s
x2
=
1/
=
x1
st
em
x1
ABBILDUNG 171 Unterscheidung zwischen
Gleichgewichts- und Ungleichgewichtsbedingungen im d-d-Diagramm für zwei Minerale 1
und 2 mit den Molenbrüchen x1 und x2. Wenn
beide Minerale gleich schnell mit der externen
fluiden Phase reagieren, vollzieht sich die Änderung ihrer d18O-Werte entlang einer Geraden, bei unterschiedlicher Reaktionsgeschwindigkeit entlang einer Kurve.
k
10
10
of
ABBILDUNG 170
5
d18O1
0
Sy
5
20
II und III Ungleichgewichte:
II: d1 = 2d2 + 1
d2 = 1.5d3 + 0.5
III: d1 = 2d2 + 1
d2 = 3d3 + 0.5
k1/k2 > 1
d18O2
217
Wasserstoff und Sauerstoff
Dies ist wieder eine Geradengleichung im D-D-Plot. Wenn die Gerade durch den Ursprung
gehen soll, werden D12 und D23 = 0, also
0=-
a3 - 1
b
b2 + 3
a3 (a2 - 1)
a3
b2 (a3 - 1) = b3 (a2 - 1)
Falls diese Gleichung erfüllt ist, geht die Gerade im D–D-Diagramm tatsächlich durch den
Ursprung, obwohl kein Gleichgewicht vorliegt.
12
-1
Ida
0
-2
=
0‰
P–
F
=
D
D
P–
F
Om
Ga an:
bb
ros
Ska
er
Fe- gaar
d
rei
ch :
Elba
Bat
ho
2
hol
Q
–F
ith
=
4
8
6
4
Skaergaard
:
Haupttren
d
–F
Q
1.
5‰
6
D
d18OFeldspat [‰]
8
10
2
0
-2
Skye:
Gabbros
-4
-4
4
ABBILDUNG 172
d18OFeldspat [‰]
D
10
=
Oman:
Plagiogranit
‰
0‰
12
6
8
18
d O
10
12
Quarz
[‰]
14
0
2
4
6
8
d18OPyroxen [‰]
10
Beispiele für Ungleichgewichtsbeziehungen für Granitoide (links) und gabbroide Gesteine (rechts). Die Fraktionierung der Sauerstoffisotope dieser Minerale weist deutlich auf Reaktion mit hydrothermalen Lösungen hin.
Wie Abbildung 171 zeigt, wieder für ein Zweikomponentensystem, ist das Ungleichgewicht, also Reaktionen im offenen System, im d–d-Diagramm leicht zu erkennen[277]. Die
Reaktionen im geschlossenen System sind durch die gepunkteten Dreiecke dargestellt, die
vom Punkt ( d10 , d 20 ) ausgehen. Wenn die beiden Minerale dieses Systems mit einer externen fluiden Phase mit identischer Reaktionsgeschwindigkeit reagieren (k1/k2 =1), ändert
sich das d18O der beiden Phasen gleich schnell, d.h. die Gerade, entlang der sich die Isotopie ändert, hat die Steigung 1. Wenn die Reaktionsgeschwindigkeit von Mineral 1 mit der
fluiden Phase größer ist als die des Minerals 2, ändert sich zunächst die Isotopie von Mineral 1 rascher als die von Mineral 2. Im Diagramm äußert sich dies in einer starken positiven
Steigung. Sobald aber sich die Reaktion zwischen Mineral 1 und der fluiden Phase dem
Gleichgewicht nähert, flacht die Steigung der Kurve im d–d-Diagramm ab, weil sich jetzt
nur noch der d-Wert der Phase 2 infolge der Reaktion mit der fluiden Phase ändert. Das
Endstadium ist erreicht, wenn die beiden Minerale d-Werte erreicht haben, die auf der
Geraden mit k1/k2 =1 liegt. Verdächtige Hinweise dafür, daß ein Gestein mit einer externen
fluiden Phase reagiert hat, sind also Trends mit positiver Steigung im d–d-Diagramm, welche die Isothermen (Linien mit Steigung 1) mit großen Winkeln schneiden. Besonders verdächtig wird es, wenn diese Trends die Isotherme für T®¥ schneiden, d.h. wenn sich das
218
B. Stabile Isotope
Vorzeichen der Fraktionierung ändert, was bei strukturell ähnlichen Mineralen nicht zu
erwarten ist.
d18OQuarz [‰]
Beispiele für die Inter16
Chlorit
pretation von Trends
Granat Olivin
mit positiver Steigung
Klino- Amphifür d18O, die als Konse14
bol
pyroxen
quenz von Reaktionen
mit externen Fluiden
Plagio12
interpretiert worden
klas
sind, sind in den
Abbildungen 172 und
10
in 173 angegeben, und
zwar für Granitoide
und
gabbroide
8
Gesteine
einerMORB
Quarz
seits[276],* und für „kru6
stale“ Eklogite (Quarz
– Klinopyroxen) und
Blauschieferfaziesge4
Eklogite und
steine (Amphibol –
Blauschiefer:
Klinopyroxen) ande[277]
Klinopyroxen
2
rerseits
. We n n
man
MORB
als
Amphibol
Ausgangsmaterial der
0
Eklogite und Blau0
2
4
6
8
10
12
schiefergesteine
18
annimmt, lassen sich
d OCpx oder Amph [‰]
die d18O-Daten der
Minerale aus diesen
Gesteinen nicht erklä- ABBILDUNG 173 Sauerstoffisotopenfraktionierung zwischen Quarz
ren durch Reaktion in und Klinopyroxen bzw. Amphibol aus Hochdruckgesteinen. Das gröeinem geschlossenen ßere hellere Doppeldreieck stellt die zu erwartende Fraktionierung im
System (stärker schraf- geschlossenen System dar, wenn man ein MORB-Gestein als Ausfi e r t e s F e l d : d 1 8 O - gangsmaterial wählt und man als Mineralzusammensetzung im ExDaten typischer Eklo- tremfall 100% Plagioklas bzw. 100% Chlorit zuläßt. Das kleinere Dopgite mit Klinopyroxen peldreieck gibt die zu erwartende Isotopenvariation wieder, wenn nur
und Granat als Haupt- Klinopyroxen und Granat stabile Phasen und das System geschlossen
[278],[279]
.
minerale). Läßt man gewesen wäre
als mögliche Isotopenaustauschpartner noch Plagioklas, Olivin und Chlorit zu, erhält man für den Fall des
geschlossenen Systems das leicht gepunktete Feld, in dem jedoch nur wenige Quarz-Klinopyroxen-Paare aus Eklogiten und Blauschiefern liegen. Zur Erklärung dieser Daten muß ein
18
O-Austausch mit krustalem Sauerstoff gefordert werden, für die Minerale mit d18O<5.5
auch eine Reaktion mit hydrothermalen Lösungen bei hohen Temperatur (z.B. Meerwasser).
Die d 18 O-Variationen terrestrischer Magmen reichen von mindestens -2 bis +16‰.
Wesentlich schlechter bekannt sind ihre dD-Variationen, die von vielleicht -200 bis -30‰
gehen. Als Ursachen der Variationen können angeführt werden:
•
Variationen in den Isotopenzusammensetzungen bei der Kondensation der Erde,
* Die Temperaturen der Plutonite in diesem Diagramm sind Subsolidustemperaturen, während die
der Vulkanite wohl infolge von deren rascher Abkühlung die Bedingungen der magmatischen Kristallisation widerspiegeln.
219
Wasserstoff und Sauerstoff
•
•
•
•
•
Effekte der magmatischen Kristallisation im geschlossenen System,
Effekte der magmatischen Kristallisation im offenen System,
Auswirkungen der partiellen Aufschmelzung und von Heterogenitäten der Quellregionen der Magmen hinsichtlich ihrer Isotopien,
Ungleichgewichtseffekte und Magmenmischung, sowie
Effekte fluider Phasen.
Abbildung 174 und Abbildung 175[280] illustrieren für wichtige Gesteinstypen des magmatischen Bildungsbereichs die dD- und d18O-Zusammensetzungen und -Variationen. Es zeigt
sich dabei, daß die meisten Magmatite auf der Erde nur relativ geringe Schwankungsbereiche in der Zusammensetzung ihrer stabilen Isotope haben, nämlich zwischen » -50 bis -100
im dD und zwischen » +5.5 und +11 im d18O. Gesteine außerhalb dieser Bereiche haben
sich i.a. unter außergewöhnlichen Bedingungen gebildet oder haben sekundäre Veränderungen erfahren.
Metamorphite
Marine Sedimente
und Tonalite
diverse Granite, Granitoide,
Granitoide
Schottische Hebriden
Sierra Nevada Batholith, CA
San Juan Mts., CO
Boulder Batholith, CO
Cascades, WA
Skaergaard
Basalte, Gabbros
Ultramafite
-180
-160
-140
-120
-100
-80
-60
-40
-20
0
dD [‰]
ABBILDUNG 174
Wasserstoffisotopenzusammensetzungen verschiedener Gesteinstypen. Die
dD-Werte der meisten Gesteine liegen zwischen ca. -55 und -85‰. Die meisten Gesteine mit negativeren Werten haben vermutlich mit (meteorischem)
Wasser in Hydrothermalsystemen reagiert.
Mondgesteine zeigen nur eine enge Streubreite ihrer d18O-Werte. Das wird der Abwesenheit
von H20 auf dem Mond zugeschrieben und der infolgedessen fehlenden hydrothermalen
Überprägung. Mond und Erde folgen demselben Fraktionierungstrend bezüglich 17O/16O
und 18O/16O, und man kann vielleicht gleiche mittlere 18O/16O-Werte annehmen. Unwägbarkeiten in dieser Annahme bestehen darin, daß gegenwärtig die Hypothese am wahrscheinlichsten gilt, wonach der Mond durch Kollision der frühen Erde mit einem Körper
von ungefähr der Masse des Mars entstanden ist, wobei der Mond dann in wesentlichem
Maße die Zusammensetzung dieses Körpers repräsentierte[281], die nicht identisch derjenigen der Erde sein muß. Diesem primordialen Verhältnis nahe kommen frische MORBasalte, die mit 5.7 ±0.3‰ ein sehr uniformes d18O aufweisen, das zudem über die geolo220
B. Stabile Isotope
gische Geschichte hindurch konstant geblieben zu sein scheint, denn archaische Komatiite
zeigen d18O-Werte um 6‰. Dieser Schluß ergibt sich auch aus der Untersuchung von
Mineralen aus Peridotitxenolithen, wonach Olivineinschlüsse aus Diamanten, für die
archaische Alter abgeschätzt wurden, identische d18O-Werte haben wie Olivine aus rezenten Peridotiten[282]. Diese Arbeit hat zudem gezeigt, daß Olivine uniforme d18O-Werte von
5.2±0.3‰ aufweisen; koexistierende Pyroxene haben – bei Temperaturen um 1000 °C im
Erdmantel – ca. 0.4‰ (Cpx) bzw. 0.5‰ (Opx) höhere Verhältnisse. Die Gesteine der kontinentalen Erdkruste sind im Vergleich zum Erdmantel an 18O angereichert; ihr mittleres
d18O dürfte höher sein als ca. 7.5‰.
Syenite, Trachyte
Granitoide
Rhyolithe, Dazite
Schottische Hebriden
San Juan Mts., CO
Boulder Batholith, CO
Skaergaard
Cascades, WA
Vulkanite, Island
Anorthosite
Eklogite
Andesite
Basalte, Gabbros
Ultramafite
Mondgesteine
Meteorite
-10
ABBILDUNG 175
-5
0
5
d18O [‰]
10
15
Sauerstoffisotopenvariation von Meteoriten, lunaren Gesteinen und einer
Reihe von terrestrischen Gesteinen. Gesteine mit d18O-Werten <5.5 dürften
mit Wasser bei hohen Temperaturen reagiert haben.
Das primordiale D/H-Verhältnis der Erde ist unbekannt und kann auch nicht aus Meteoritendaten abgeleitet werden, die einen riesigen Bereich zwischen » -500 und +9000‰ zeigen[283]. Wasserstoffisotopendaten lunarer Gesteine sind nicht hilfreich, weil der Mond
seine flüchtigen Komponenten sehr früh in seiner Geschichte verloren hat, so daß der Wasserstoff, der heute vorhanden ist, zum großen Teil aus dem Deuterium-freien Sonnenwind
stammt. Das mittlere dD der irdischen Hydrosphäre dürfte bei » -10‰ liegen. Der größte
restliche Teil des Wasserstoffs auf der Erde liegt wohl gebunden in OH-haltigen Silikaten
vor, die relativ zum Ozeanwasser an Deuterium verarmt sind. (dD » -40 bis -90‰). Ähnliche Werte zeichnet auch das magmatische H2O aus. Das mittlere terrestrische dD könnte
heute bei vielleicht -15 bis -20‰ liegen. Bei einer Abschätzung des primordialen dD ist zu
bedenken, daß 1H im Lauf der Erdgeschichte über 2H aus der Atmosphäre in den interplanetaren Raum diffundiert ist. Aber auch bei den Wasserstoffisotopen gibt es keine Hinweise
auf eine systematische Änderung der dD-Werte der Gesteine im Verlauf der geologischen
221
Wasserstoff und Sauerstoff
Geschichte. Praktisch alle Gesteine (Magmatite, Metamorphite und Sedimente), die nicht
hydrothermal überprägt wurden, haben dD-Werte zwischen » -40 und -95‰, d.h. es lassen
sich nicht, wie bei den Sauerstoffisotopen, Mantel- von krustalen D/H-Verhältnissen unterscheiden. Als Grund dafür wird angeführt, daß durch die Prozesse der Subduktion Wasser
aus der Hydrosphäre in den oberen Mantel gelangt. Da diese geotektonischen Vorgänge
wahrscheinlich seit mehreren 109a ablaufen, ist im oberen Mantel ein ursprünglich primordiales dD längst durch die Werte der Erdkruste überprägt und nicht mehr davon unterscheidbar. Aus der Isotopengeochemie der Edelgase weiß man, daß es in Basalten noch primordiale Komponenten bezüglich des He und des Xe gibt, deren Reservoir im unteren
Erdmantel vermutet wird. Daß es dort auch noch ein ähnliches Reservoir für die Wasserstoffisotope gibt, kann nur vermutet, aber nicht belegt werden. Die frischesten MORB mit
d18O-Werten um 5.7‰ weisen dD-Verhältnisse um -80‰ auf, was wohl am besten der
Wasserstoffisotopie des primitiven oberen Erdmantels entspricht.
Die Effekte der magmatischen Kristallisation im geschlossenen System sind nur schwer
quantitativ zu fassen, weil sich einerseits in-situ-Messungen an Einsprenglingen und
Matrix in der Natur schwierig gestalten und es andererseits nur wenige magmatische Komplexe gibt, die frei von sekundären Alterationsprozessen sind. Seit der klassischen Arbeit
von Wager & Deer[284] wurde die Skaergaard-Intrusion in Ostgrönland lange als ein klassischer Fall der fraktionierten Kristallisation eines tholeiitischen Ausgangsmagmas betrachtet. Frühe Analysen der Sauerstoffisotopenverhältnisse bestätigten diese Meinung, indem
relative d18O-Verarmungen um 3 – 4‰ in den späten Differentiaten durch eine Fraktionierung nach dem Rayleighschen Gesetz erklärt wurden[285]. Erst einige Jahre später äußerte
Taylor[286] auf Grund von O-Isotopenuntersuchungen die Ansicht, daß der gesamte Komplex durch Reaktion mit hydrothermalen Fluiden umgewandelt ist.
Als geeignete Gesteinssequenzen, die nur die Rolle der Fraktionierung widerspiegeln, gelten die Alkalibasalt- und Tholeiitkomplexe von Ascension (Südatlantik), der Osterinsel,
von Kiglapait (Grönland) und Apollo 12, die d18O-Trends aufweisen, die innerhalb von
»1‰ übereinstimmen. Danach ändert sich die Sauerstoffisotopie während der ersten »70
– 95% Kristallisation des Ausgangsmagmas nur um wenige Zehntel ‰. Größere Effekte
kann man nur für das Endstadium der Differentiation erwarten und/oder wo die Kristallisation von Quarz, Biotit oder Magnetit bedeutsam wird. Daraus und aus der Analyse von
Einsprenglingen und Matrix aus Rhyolith- und Dazittuffen ist zu entnehmen, daß Fraktionierungen zwischen Kristallen und Schmelze für d18O kleiner als ±2‰ für die wichtigsten
gesteinsbildenden Minerale (Quarz, Feldspat, Pyroxene, Olivin, Hornblende, Biotit etc.)
sein sollten. Die Kristallisation von Quarz wird dabei eine 18O-Verarmung der Restschmelze
bewirken und die von Magnetit, Ilmenit, Hornblende, Biotit, Pyroxen und Olivin zu einer
Erhöhung führen. Die Richtung, in der sich das d18O des Magmas entwickeln wird, hängt
daher meist von DFeldspat-Schmelze ab. In der Theorie sollte bei Kristallisation eines basischen
Magmas das d18O der Restschmelze leicht ansteigen, jedoch wohl um nicht mehr als 1‰
bei der Fraktionierung von Basalt zu Rhyolith.
Man kann daher das d18O eines Gesteins, ähnlich wie die Sr- oder die Nd-Isotopie, als Tracer benutzen, um etwas über die Herkunft von Magmen oder/und die Wege ihrer sekundären Veränderung zu erfahren, speziell über den Anteil von krustalen und Mantelkomponenten. Besonders nützlich zu diesem Zweck ist die Kombination von Sauerstoffisotopen
und radiogenen Isotopen, z.B. 87Sr/86Sr. Positive Korrelationen zwischen d18O und 87Sr/86Sr
sind in einer Reihe von Magmenprovinzen beobachtet worden. Ein gutes Beispiel dafür
sind die Plutonite (Granitoide, Gabbros) im Westen der USA (siehe Abbildung 176[287]).
Danach sind niedrige d18O-Werte bis herab zu +6‰ mit Sr-Isotopien um 0.703 verknüpft,
beides Isotopensignaturen, die man mit Gesteinen des Erdmantels in Beziehung bringt.
Die Korrelation beider Isotopensysteme wird von Taylor[288] im Sinn eines „AFC-Modells“
gedeutet, bei dem ein Magma aus dem Erdmantel in relativ seichtem Krustenniveau Krustenmaterial mit hohem d18O und 87Sr/86Sr assimiliert und parallel dazu eine fraktionierte
Kristallisation erfährt. Bei der Bildung von Kumulaten wird Kristallisationswärme frei, die
zur Assimilation von Nebengestein verwendet werden kann. Die Masse der Kumulate bei
222
B. Stabile Isotope
einem solchen Prozeß wird immer wesentlich größer sein als die Masse der assimilierten
Gesteine, da der gegenteilige Fall nicht nur aus thermischen Gründen kaum vorstellbar ist,
sondern auch eine Volumenvergrößerung des Magmas zur Folge hätte. Granitoide mit
d18O<6 sind offensichtlich sekundär hydrothermal überprägt.
0.709
0.708
initiales 87Sr/86Sr
Granitoide
Gabbros
0.707
S-Typ
San Jacinto + Santa Rosa
Block (Granitoide)
0.706
hydrothermal
alteriert bei
³4008C
0.705
0.704
Baj
aC
Baja
California
0.703
alif
orn
I-Typ
ia
0.702
3
ABBILDUNG 176
5
7
d18O
9
11
13
[‰]
O-Sr-Isotopenbeziehungen für Gesteine aus den Batholithen der Sierra Nevada und der Peninsular Range (Kalifornien und Niederkalifornien)
Auf Grund der 18O/16O-Verhältnisse hat Taylor[289] die Granitoide in drei Gruppen unterschieden, nämlich die der normalen Granitoide (6 £d18O £10‰), Granitoide mit hohem
d18O (>10‰) sowie eine Gruppe mit Werten <6‰. Obwohl diese Einteilung etwas künstlich wirkt, weil die beiden ersten Hauptgruppen eine kontinuierliche Abfolge bilden können, hat sie sich bewährt. Die erste Gruppe ist identisch mit derjenigen der I(gneous)-Typ
Granitoide, die zweite mit derjenigen der S(edimentary)-Typ Granitoide. Reine I-Typ Granitoide kommen insbesondere in Inselbögen vor, in denen kontinentale Kruste nicht vorhanden ist, aber auch unmittelbar hinter Subduktionszonen, wo die abtauchende Platte
noch nicht von dicker kontinentaler Kruste überlagert ist. So weisen an der Westküste der
USA die küstennahen Granitoide die niedrigsten Werte von d18O und 87Sr/86Sr auf und die
höchsten Werte von 143Nd/144Nd, die denen des Erdmantels nahe kommen. Granitoide mit
d18O>10‰ müssen im wesentlichen durch Assimilation von (Meta-)Sedimenten entstanden sein. Dazu gehören z.B. die meisten der herzynischen Granite in Mitteleuropa
(Schwarzwald, Fichtelgebirge). Unter den Granitoiden mit d18O-Werten unter 6‰ gibt es
neben einer Gruppe, die unter Subsolidusbedingungen mit meteorischen Hydrothermalwässern äquilibriert ist, auch einige Körper, in denen das niedrige d18O bereits im magmatischen Zustand erworben wurde. Beispiele dafür sind bekannt aus Island[290] oder aus dem
Yellowstone[291]. Diese Magmen haben offensichtlich Nebengestein mit niedrigem 18O/16O
assimiliert, das durch die Reaktion mit großen Mengen von hydrothermalen Fluiden entstanden ist.[288]
223
Wasserstoff und Sauerstoff
Bei der Kontamination von basischen Schmelzen mit Krustenmaterial erhöht sich das d18O
der Restschmelze mit zunehmendem Assimilationsgrad mehr oder weniger empfindlich, je
nachdem wie groß der Unterschied in der Sauerstoffisotopie zwischen den beiden Endgliedern der Mischung ist. Nach Taylor & Sheppard[280] läßt sich ein AFC-Modell mit Hilfe der
folgenden Gleichungen quantifizieren:
c
cm
1 - f -z
= f - z + 0a ´
0
cm 1 - j (1 - b )
cm
und
[GL 233]
0
Rm - Rm0
cm
1
=
f -z
cm
Ra - Rm0
[GL 234]
wobei z = 1 - jb (j - 1) ,
b = Verteilungskoeffizient å Minerale/Schmelze,
j = Verhältnis Kumulate/assimiliertes Material,
c = Konzentration des betrachteten Elementes,
R = Isotopenverhältnis (z.B. 87Sr/86Sr, eNd, d18O),
m = Schmelze, 0 = initiale Schmelze, a = assimiliertes Material,
f = Anteil der noch verbleibenden Schmelze (0 – 1).
0.80
w=
w 10
=
7.
5
kristallisierter Magmenanteil
1.00
0.60
w
=
5
0.40
0.20
0.00
5
ABBILDUNG 177
7
18
d OMagma
»
9
18
d O
11
Kumulate
13
[‰]
Illustration eines AFC- Vorgangs für verschiedene j (= Verhältnis Kumulate
zu assimiliertem Nebengestein); Endglieder der Rechnung sind MORB
(5.7‰) und krustales Nebengestein (19‰).
Im Fall der Sauerstoffisotope kann man – im Gegensatz zu den radiogenen Isotopen – vereinfacht davon ausgehen, daß Schmelze, Kumulate und assimiliertes Material dieselbe Sau-
224
B. Stabile Isotope
erstoffkonzentration haben und daß der Verteilungskoeffizient b zwischen Kumulatmineralen und Schmelze 1 beträgt. Damit vereinfacht sich [GL 234] zu:
é
j
éj
ù
ù
é j
j -1 ù
ê j -1 -1ú
ê
ú
1 - ê1- (j -1)úû
Rm - Rm0
1 j -1
( ) û
= 1- f ë
= 1- f ë
= 1 - f ë j -1 j -1 û = 1 - f ( )
0
1
Ra - Rm
(
)[
]
1 j -1
Rm = Ra - Rm0 1 - f ( ) + Rm0
[GL 235]
Diese Gleichung ist gültig mit der Einschränkung, daß die Kumulate dieselbe Isotopenzusammensetzung haben müssen wie die Schmelze, aus der sie ausgeschieden werden. Das ist
bei den radiogenen Isotopen wie 87Sr/86Sr, 143Nd/144Nd oder den Pb-Isotopen wegen der
geringen Massendifferenz immer der Fall (Solche potentiellen Effekte werden jedoch durch
die Massenfraktionierungskorrektur mit korrigiert.), in guter Näherung auch für das 18O/
16
O. Abbildung 177[280] zeigt die Änderung des d18O eines Magmas mit initialem d18O =
5.7‰ und d18O des assimilierten Materials = 19‰ für verschiedene Verhältnisse j von
Kumulat zu assimiliertem Material in Abhängigkeit von (1 – f).
he
iolit
Oph
d18O [‰]
In Abbildung 178
30
sind schematisch
Kieselschiefer
Sedimente und
die Sauerstoffund Kalke
Metasedimente
und Sr-Isotopen25
Mergel
zusammensetzungen von Magmatiten und von
20
sandige und
Sedimenten getonige Sedimente
zeigt. Auffallend
ist der enge Be15
Arkosen
reich frischer
Grauwacken
ozeanischer und
kontinentaler Ba10
Granitoide
salte und das riesige Feld, das von
5
Sedimenten einverwitterte Basalte
meteorisch und hydrothermal
genommen wird.
frische
überprägte Gesteine
Die höchsten
Basalte
18
d O-Werte (bis zu
0.710 0.715 0.720 0.725 0.730 0.735 0.740
0.700 0.705
35‰) zeigen Se87Sr/86Sr
dimente, die entweder einen hoh e n b i o g e n e n ABBILDUNG 178 Sr- und O-Isotopenvariationen in Gesteinen der kontiAnteil
h a b e n nentalen und der ozeanischen Kruste
(Kalk- oder Silikatskelette) oder die im Meer authigen gebildet werden (großer Fraktionierungsfaktor bei
niedrigen Temperaturen). Die Sedimente mit dem niedrigsten d18O sind Sedimente, die
durch die Abtragung von Magmatiten entstanden sind und daher direkt deren Sauerstoffisotopie reflektieren. Metamorphite werden i.w. denselben Bereich in diesem Diagramm
einnehmen wie die Gesteine, aus denen sie entstanden sind, wobei natürlich zu berücksichtigen ist, daß das 87Sr/86Sr eine Funktion des Rb/Sr-Verhältnisses sowie des Alters des
Gesteins ist.
Seit Mitte der sechziger Jahre sind die Prozesse, die zur Alteration der Ozeankruste führen,
Gegenstand intensiver und systematischer Untersuchung. Die Temperaturen, bei denen
diese Prozesse stattfinden, reichen von 0 bis vielleicht 450°C und werden im Deutschen
unter dem Sammelbegriff „Spilitisierung“ zusammengefaßt. Die Tieftemperaturalteration
wird auch als „subozeanische Verwitterung“ bezeichnet, die Hochtemperaturprozesse
225
Wasserstoff und Sauerstoff
nennt man auch „hydrothermale Alteration“. Ursache dieser Prozesse ist in beiden Fällen
die Instabilität der Ozeankruste gegenüber Seewasser. Die an den mittelozeanischen
Rücken gebildete Kruste weist eine hohe Permeabilität auf. Seewasser dringt in Kluftsysteme ein, kühlt die ursprünglich warme Kruste ab und tritt in Gestalt heißer Quellen mit
hohen Schwermetall- und Sulfidgehalten, den „Black Smokers“ wieder an anderer Stelle
der Rücken aus. Bei hohen Temperaturen sind Plagioklas, Pyroxen, Magnetit und basaltisches Glas instabil und reagieren zu Albit, Chlorit, Epidot, Aktinolith, Quarz, Hämatit und
Zeolithen, während bei tiefen Temperaturen v.a. smektitische Tonminerale und Calcit neu
gebildet werden.
Hoch- und Tieftemperaturalteration führen zu völlig verschiedenen O-Isotopien. Bei niedrigen Temperaturen sind die Fraktionierungsfaktoren hoch, und das d18O der Ozeankruste
wird von Werten zwischen »5.5 und 6‰ für frische MORB erhöht bis zu Werten um 25‰,
wobei z.T. eine positive Korrelation zwischen d18O und dem H2O-Gehalt zu beobachten ist.
Mit zunehmender Temperatur werden die Fraktionierungsfaktoren kleiner und können bei
einigen 100°C ihre Vorzeichen umkehren, d.h. d18O der Silikate nimmt ab. Typischerweise
sind daher die d18O-Werte der Ozeankruste direkt am Meeresboden am höchsten (Tieftemperaturverwitterung) und nehmen mit der Tiefe zu ab. Das ist in Abbildung 179 für einen
Bohrkern aus dem Costa Rica-Rift schematisch gezeigt. Charakteristisch für die submarine
Verwitterung sind hohe Verhältnisse von H2O zu Basalt (>>1), während niedrige Verhältnisse die Hochtemperaturalteration kennzeichnen (»1).
m
DSDP Hole 504B (Costa Rica Rift, Pazifik)
0
Blöcke
frische Basalte
200
T = 0 – 1508C
submarine
Verwitterung
400
Pillows
T < 1508C
reduzierend
600
Übergangszone
Metamorphose
unter
hydrothermalen
Bedingungen
(100 – 4008C)
800
Dikes
1000
3
4
5
18
d O
6
Basalt
ABBILDUNG 179
226
7
8
9
[‰]
Variation der Sauerstoffisotope in einem Bohrkern des Deep Sea Drilling-Projektes im Costa Rica-Rift
B. Stabile Isotope
Am detailliertesten lassen sich die Alterationsprozesse in obduzierter Ozeankruste studieren, den Ophiolithen. Man muß sich dabei allerdings im klaren sein, daß Ophiolithe nicht
unbedingt an mittelozeanischen Rücken produzierte Kruste sein muß (z.B. wird für Troodos auf Zypern ein Inselbogenursprung) diskutiert und daß während und nach der Obduktion Prozesse abgelaufen sein können, welche die Verteilung der stabilen Isotope verändert
haben. Abbildung 180[292] zeigt ein vollständiges Profil durch einen Ophiolithkomplex am
Beispiel des Macquarie-Ophioliths (zwischen Australien und der Antarktis), in dem die
Sequenz von den d18O-reichen Pillowlaven bis zu den hydrothermal überprägten Gabbros
und serpentinisierten Harzburgiten erhalten ist.
Das Seewasser, das mit der ozeanischen Kruste reagiert, erfährt natürlich eine gegensinnige
Veränderung seines d18O. Modellrechnungen legen jedoch den Schluß nahe, daß sich die
Effekte von Hoch- und Tieftemperaturalteration gegenseitig kompensieren, so daß das
Wasser der Ozeane unter dem Strich keine Änderung seines d18O von 0‰ erfährt. Alte
Ophiolithe wie der kambrische Bay of Islands-Komplex auf Neufundland und archaische
Greenstone-Belts in Kanada und Südafrika zeigen eine analoge Variation ihres d18O von
Werten >6‰ in den Laven und <6‰ in den plutonischen Teilen wie moderne Ozeankruste, so daß es von daher keinen Grund gibt, eine Änderung des 18O/16O der Ozeane im Verlauf der geologischen Geschichte anzunehmen. Andererseits wurden aus der Analyse alter
mariner Sedimente auf d18O-Werte bis zu -18‰ für die Ozeane im Archaikum abgeleitet.
Diese Kontroverse um die Sauerstoffisotopie der frühen Ozeane ist bislang nicht entschieden, auch wenn mehr für die Konstanz des d18O zu sprechen scheint.
m
Profil durch den Macquarie-Ophiolith
0
1000
Pillowlaven,
massive
Laven
Verwitterung
durch Seewasser
Zeolithfazies
untere Grünschieferfazies
2000
Sheeted
Dykes
3000
massive
Gabbros
4000
obere Grünschieferfazies
lagige
Gabbros
rekristall.
Gabbros
5000
Harzburgit
Serpentinit
6000
3
4
5
6
d18O
ABBILDUNG 180
7
8
9
10
[‰]
Variation der Sauerstoffisotope im Macquarie-Ophiolith im Südozean südlich von Australien
227
Kohlenstoff
19.0
Kohlenstoff
Kohlenstoff ist nach Wasserstoff,
organisches sedimentäres
Helium und Sauerstoff zwar das
Material, Kohle, Öl
vierthäufigste Element des SonnenOrganismen
systems, aber auf der Erde nur mit »
200 – 350ppm vertreten. C spielt
SüßwasserKarbonate
eine herausragende Rolle in der Biomarine Karbonate
sphäre, hauptsächlich in reduzierter
Luft-CO2
Form, während anorganischer Kohlenstoff meist oxidiert in Form von
Karbonatite,
Diamanten
Karbonaten vorliegt. Auf Grund der
Vielzahl von Oxidations- und Bin40 30 20 10
0 -10 -20 -30 -40 -50
dungszuständen, in denen C vorlied13C [‰] relativ zum Standard PDB
gen kann, sind die Voraussetzungen
für seine Isotopenfraktionierung in
der Natur ideal, zumal viele der Ver- ABBILDUNG 181 Variation der Kohlenstoffisotope in
bindungen in der Natur gasförmig der Natur
oder flüssig vorkommen.
8C
0
20
40
Ca
10
lci
60
t–
80
CO
2 -G
as
–
6
–
CO
as
-G
2
1000 ln a
g)
un
ös
(L
3
8
CO
H
Kohlenstoff hat 2 stabile Isotope mit den
Massenzahlen 12 (Häufigkeit 98.89%), das
als Referenz der Atomgewichtsskala dient,
und 13 (1.11%). Die massenspektrometrische Messung des 13 C/ 12 C-Verhältnisses
erfolgt an CO 2 -Gas, das aus Karbonaten
durch Reaktion mit H3PO4 oder thermische
Zersetzung freigesetzt wird und aus organischen Komponenten und Silikaten durch
Erhitzen auf ³ »1000°C und eventuelle Oxidation im O2-Strom oder mit CuO ausgetrieben wird. Die C-Isotopenzusammensetzung
wird auch heute noch auf den Standard PDB
bezogen, obwohl dessen Vorrat längst
erschöpft ist, so daß die Messung gegen
sekundäre, an (V)PDB geeichte Standards
erfolgen muß.
4
ng)
H
– (Lösu
CO 3
it –
Die natürlichen Isotopenvariationen des
Calc
2
Kohlenstoffs machen mehr als 10% aus und
reichen im d13C von »+20‰ („schwere“ Karbonate) bis -90‰ (CH4-Gas). Die d13C-Werte
0
wichtiger Kohlenstoffreservoirs sind in
3.6
3.4
3.2
3.0
[266]
Abbildung 181
angegeben. Die höchsten
1000/T
[K]
d 13 C-Werte zeigen marine Karbonate, in
denen sich 13C infolge des AustauschgleichABBILDUNG 182 C-Isotopenfraktionierung im
gewichts
System CO 2 (Gas) – HC O3– (in Lösung) –
CaCO3 (fest) als Funktion der reziproken TemH12 CO3- + 13CO2 º 12CO2 + H13 CO3peratur
im in Wasser gelösten Bikarbonat gegenüber
dem Kohlendioxid der Atmosphäre anreichert (Abbildung 182[16]). In Calcit im Gleichgewicht mit H CO3- steigt d13C mit zunehmender Temperatur zwar an; da der Austausch zwischen H CO3- und CO2 aber eine starke negative Temperaturabhängigkeit zeigt und H CO3im Wasser im Gleichgewicht mit CO2 steht, ist zu erwarten, daß d13C des Calcits per Saldo
mit abnehmender Temperatur ansteigt, ähnlich wie d18O in Karbonaten.
228
B. Stabile Isotope
Bei der Photosynthese der grünen Pflanzen wird das leichte Isotop 12C infolge eines kinetischen Effekts in der organischen Materie angereichert und damit über die Nahrungskette
auch in der Tierwelt. Organische Moleküle wie CH4 können zudem auf anorganischem
Wege gebildet werden durch Reaktionen wie CO2 + 4H2 º CH4 + 2 H2O, wobei sich das
leichte Isotop im CH4 anreichert.
1000 ln a
CO
2
–
CO
2
CH
4
–C
H
4
(C
ra
ig
,1
95
3)
In Abbildung 183[293] sind die
600
400
300
200
150
8C
Fraktionierungsfaktoren
1000lna (» dA – dB) für einige
35
wichtige Reaktionen auf der
Grundlage thermodynamischer Berechnungen angegeben. Danach reichert sich
30
d 13 C z.B. in CO 2 gegenüber
Diamant und Calcit (im letzteren Fall nur bei T > 200°C)
an oder in Calcit gegenüber
25
Graphit. Die hohe Reaktionsfähigkeit des Kohlenstoffs und
die Vielzahl möglicher Isoto20
penaustauschreaktionen in
der Natur führen dazu, daß
t
die Gesteine von Erdkruste
phi
Gra
–
und -mantel nicht so leicht
15
cit
Cal
durch ihr 13C/12C-Verhältnis
zu unterscheiden sind wie
CO2 – Dia
mant
durch ihre Sauerstoffisotopie.
10
Es kommt noch hinzu, daß
Kohlenstoff – im Gegensatz
zum Sauerstoff – kein unerschöpfliches Reservoir im Erd5
phit
mantel bildet. Außerdem sind
t – Gra
n
a
m
ia
CO2 – Calcit
D
organische Kohlenstoffverbindungen in der Biosphäre
0
allgegenwärtig und werden
1
2
3
4
5
6
mehr oder weniger fest an
6/T2 [K2]
10
anorganische Materialien
adsorbiert, so daß in Gesteinen oft eine Überlagerung ABBILDUNG 183 Berechnete Isotopenfraktionierungsfaktoren
verschiedener C-Isotopensi- für Kohlenstoff in den Systemen Calcit – CO – Diamant – Gra2
gnaturen zu finden ist. So phit – CH
4
zeigt aus MORB extrahierter
Kohlenstoff eine Variation im d13C, die von » 0 bis -35‰ reicht[294]. Dabei wird bei Temperaturen unter » 600°C eine Komponente aus den Basalten freigesetzt mit d13C um -30 bis
-20‰, während die bei höheren Temperaturen entgaste Komponente d13C um -5‰ aufweist. Ebenfalls um -5‰ liegen die d13C-Werte von CO2 in Fluideinschlüssen ozeanischer
Basalte, was darauf hindeutet, daß dies die C-Isotopie vieler solcher Magmen ist. Aber
schon der Grund für die niedrigen 13C/12C-Verhältnisse des bei tiefer Temperatur abgegebenen Kohlenstoffs ist umstritten. Nach einer Vorstellung handelt es sich dabei um residualen Kohlenstoff nach einer vielstufigen CO2-Entgasung der basaltischen Magmen während ihres Aufstiegs[295]. Geht man dabei von ursprünglichen Werten um -5‰ aus und
bedenkt, daß selbst bei Temperaturen zwischen »1100 und 1300°C CO2-Gas noch um »
4‰ gegenüber dem im Magma gelösten C angereichert ist[296], dann ist es nicht schwierig,
über eine Rayleigh-Destillation zu Werten von -30‰ zu gelangen. Als Hinweis darauf, daß
dieser Prozeß auftritt, wurden positive Korrelationen zwischen d13C und dem C-Gehalt
gewertet, die in einigen kogenetischen Suiten ozeanischer Basalte beobachtet wurden.
229
Kohlenstoff
Allerdings erfordert dieses Modell sehr hohe initiale C-Konzentrationen von >2000ppm
anstelle der » 200ppm, die man typischerweise in MORB-Gläsern findet, und damit auch
hohe Gehalte im Erdmantel. Nach einem anderen Modell handelt es sich bei dem unterhalb von 600°C abgegebenen C um Kontaminationen, die an der Erdoberfläche erworben
wurden[297]. Bei Inselbogenbasalten kann auch die Hochtemperaturphase ein deutlich
niedrigeres d13C als -5 aufweisen, was als Mischung zwischen Mantel- und subduziertem
Kohlenstoff gedeutet wird.
Anzahl der Proben
Immerhin scheint
CO2-Einschlüsse in MORB
Einigkeit insofern zu
1
bestehen, daß weite
Teile des subozeani10
Kimberlite
schen und des subkontinentalen Erdmantels
20
d 1 3 C - We r t e u m - 5
Karbonatite
10
haben. Dafür sprechen
die Daten der Hochtem100
peraturentgasung von
MOR-Basalten, Daten
60
Diamanten
für Kimberlite und Karbonatite und Daten für
20
Diamanten, wie Abbildung 184 erkennen
0
-5
-10
-15
-20
-25
-30
läßt [266] . Insbesondere
13
d C
die Diamanten zeigen
aber eine sehr weite
Va r i a t i o n d e r d 1 3 C - ABBILDUNG 184 Variation der Kohlenstoffisotope in Materialien des
Werte bis hin zu sehr Erdmantels
leichten Isotopien. Besonders leichte C-Isotopien sind dabei in Diamanten zu finden, die
aus Eklogiten stammen. Möglicherweise spielen bei der Diamantentstehung variable Sauerstoffugazitäten eine Rolle und damit das Vorliegen von C-haltigen reduzierten (CH4) und
oxidierten Gasen (CO2), also Reaktionspartner mit großem Fraktionierungsfaktor. Darüber
hinaus ist sogar der Vorschlag geäußert worden, es könne sich bei Diamanten mit besonders niedrigen d 13 C-Werten um subduzierten Kohlenstoff mit ehemals organischem
Ursprung handeln[268].
Größere Bedeutung als bei den Magmatiten kommt den Kohlenstoffisotopen bei den Metamorphiten zu. Das liegt daran, daß bei der Metamorphose fluide Phasen eine wichtige
Rolle spielen können, und zwar bei Entwässerungs- und Dekarbonatisierungsreaktionen,
vor allem bei der prograden Metamorphose von Sedimenten[298]. Diese Reaktionen werden
in der Regel mit großen positiven Volumenänderungen verbunden sein, wobei der größte
Teil der Fluide aus dem System nach oben hin entweicht, in geringen Tiefen in Verbindung
mit Kluftsystemen aber auch zur Seite oder gar abwärts. Die Änderung der stabilen Isotopenverhältnisse der residualen Gesteine als Folge eines derartigen Prozesses läßt sich mit
Hilfe von 2 extremen Modellen beschreiben, nämlich dem Gleichgewichtsmodell und dem
Modell der Rayleigh-Fraktionierung. Beim Gleichgewichtsmodell wird angenommen, daß
die entwickelte fluide Phase (zunächst) im System verbleibt und mit dem residualen
Gestein reäquilibriert. Für die Isotopenverhältnisse gilt dabei eine einfache Massenbilanzgleichung:
d0 = f ´ d + (1 – f) ´ dfluid ,
[GL 236]
wobei d0 die Isotopie des Gesteins vor Beginn der Reaktion ist, d seine Isotopie zum Zeitpunkt, zu dem der Anteil des Kohlenstoffs mit dem Molenbruch f (oder des Sauerstoffs,
etc.) noch nicht reagiert hat und dfluid die Isotopie der fluiden Phase beim Reaktionsgrad (1
– f ). In der Regel wird sich das schwere Isotop 13C (aber auch 18O) in der fluiden Phase
anreichern ( a CO2 -CaCO3 >1, siehe Abbildung 183). Wegen
230
B. Stabile Isotope
1000 lna » dfluid – d
wird daraus: d 0 » f ´ d + (1 - f ) ´ (d + 1000 ln a )
d 0 » f ´ d + d - f ´ d - f ´ 1000 ln a + 1000 ln a = d + 1000 ln a - f ´ 1000 ln a
d » d 0 - 1000 ln a (1 - f )
[GL 237]
Mit dieser Gleichung erhält man einen minimalen Wert für die Änderung des Isotopenverhältnisses eines Gesteins infolge der Fluidentwicklung. Die maximale Änderung wird
durch das Rayleighsche Gesetz beschrieben, das im Kapitel „H und O in der Hydro- und
Atmosphäre“ eingeführt wurde (GL 218):
d + 1000
R
a -1
=f( ) =
R0
d 0 + 1000
[GL 238]
und daraus d = f (a -1) (d 0 + 1000) - 1000
[GL 239]
da (a – 1) sehr klein ist, geht f (a – 1) gegen 1, und es gilt näherungsweise:
f (a – 1) ´ d0 » d0
(
)
d = d 0 + 1000 f (a -1) - 1
[GL 240]
Zu Beginn der Reaktion (große Werte von f) werden die nach beiden Methoden berechneten d-Werte nur wenig voneinander abweichen. Erst wenn die Reaktion weit fortgeschritten ist, wird das Modell der Rayleigh-Fraktionierung zu einem großen Isotopieeffekt und
großen Unterschied zum Gleichgewichtsmodell führen. Dekarbonatisierungsreaktionen
wirken sich sowohl auf das 13C/12C- als auch das 18O/16O-Verhältnis des Gesteins aus. Da
die Fraktionierung beider Isotopenverhältnisse dasselbe Vorzeichen hat, sollten d13C und
d18O für derart betroffene Gesteine miteinander korreliert sein. Abbildung 185[298] zeigt die
nach beiden Modellen zu erwartenden Fraktionierungen in einem d13C-d18O-Diagramm
für verschiedene Werte von fKohlenstoff. Die beiden Geraden sind nach dem Gleichgewichtsmodell berechnet, die beiden Kurven modellieren das Rayleighsche Gesetz. Das Modell
entspricht den typischen Dekarbonatisierungsreaktionen
CaCO3 + SiO2
º CaSiO3 + CO2 und
CaMg(CO3)2 + 2 SiO2
º CaMgSi2O6 + 2 CO2.
Die C-Isotopie ändert sich in erheblich stärkerem Maße als die O-Isotopie, weil, den Reaktionen entsprechend, das Sauerstoffreservoir des Gesteins viel größer ist als das Kohlenstoffreservoir, so daß noch 60Mol% Sauerstoff verbleiben, wenn der gesamte Kohlenstoff
bereits entgast ist. Die durch das freiwerdende CO2 verursachte Volumenvergrößerung
beträgt bei beiden Reaktionen »40%; und von daher ist es klar, daß der größte Teil der
Fluide aus dem System entweichen wird. Der rechte Teil von Abbildung 185[298],[299] zeigt
ein Beispiel der Änderung des d13C mit f CO2 in Tonsteinen im Kontakt zu Granodiorit,
wobei eine Situation zwischen „Batch-“ und Rayleigh-Fraktionierung vorgelegen hat.
Generell scheint der Dekarbonatisierungstrend von typischen Werten sedimentärer Karbonate (d18O » 20 – 25, d13C » -2 bis +5) zu Werten für magmatische Karbonatite hin zu gehen
(d18O » 6 – 10, d13C » -4 bis -8), wenn f gegen 0 geht.
Die fluiden Phasen, die infolge von Dehydratation und Dekarbonatisierung aus einem
Gesteinskomplex auswandern, werden andere Gesteine infiltrieren und mit ihnen reagieren. Die Isotopenverschiebungen, die das infiltrierte Gestein dabei erleidet, sind natürlich
umso größer, je höher das Verhältnis Fluide/Gestein ist, je größer die Isotopenunterschiede
zwischen den Reaktionspartnern sind und je höher die Permeabilität des Gesteins ist. Die
Permeabilität wird von Größe, Anzahl, Verteilung und Orientierung von Brüchen abhän231
Kohlenstoff
gen, von der Porosität des Gesteins, dem Streß und dem Fluiddruck. Generell sollte die Permeabilität mit zunehmender Tiefe in der Kruste abnehmen. In seichtem, hoch permeablem Niveau wird P H2O ungefähr dem hydrostatischen Druck einer hypothetischen
überlagernden Wassersäule entsprechen. Mit der Tiefe und mit zunehmender Temperatur
wird die Duktilität der Gesteine zunehmen, und die Fluide werden auf den lithostatischen
Druck komprimiert, der wegen des Dichteunterschieds » dreimal so hoch ist wie der hydrostatische Druck. Infiltration von Oberflächenfluiden (meteorische Wässer, Seewasser) wird
auf relativ seichte Krustenniveaus beschränkt sein, in dem die Fluiddrücke £ dem hydrostatischen Druck sind. Unter den Ozeanen wurde Eindringen von Seewasser bis in » 6km Tiefe
nachgewiesen und Eindringen von meteorischen Wässern in die kontinentale Kruste bis in
Tiefen von gut 10km.
d13C
-2
-20
%
f = 0.75
-10%
-40
%
f = 0.5
-20%
f = 0.25
-30%
-4
f = 0.125
-35%
-6
-8
-10
ABBILDUNG 185
18
20
d18O
-4
-6
Ra
yle
ig
h
-8
-10
D13CCO2 – Calcit = 4.5
0.9
f = 0.025
16
„Gle
ichge
wich
t“
0
-2
d13C
0
0.7
0.5
ƒCO2
0.3
0.1
22
links: Auftragung der gekoppelten O-C-Isotopentrends, die für Gleichgewichts- („Batch“, gerade Linien) und Rayleigh-Verdampfung (Kurven) errechnet wurden unter Annahme normaler Dekarbonatisierung[298]. Die
gewählten Fraktionierungsfaktoren sind realistisch für metamorphe Temperaturen: a13C (CO2 – Gestein) = 1.0022 und a18O (CO2 – Gestein) = 1.006
und 1.012 (Die größeren Verschiebungen im d18O ergeben sich für a =
1.012). Die Werte für fC und die ungefähre Verringerung des Gesteinsvolumens (%) sind ebenfalls angegeben. Die resultierende Variation im d18O ist
wenig abhängig von der Wahl des Gleichgewichts- oder des Rayleigh-Modells, da das System selbst bei vollständiger Dekarbonatisierung noch den
größten Teil des Sauerstoffs behält.
rechts: Auftragung des gemessenen d13C gegen den Anteil des noch nicht
dekarbonatisierten Gesteins (gefüllte Quadrate) für Tonsteine aus der
Kontaktzone zum Notch Peak Stock in Utah[299]. Die beiden Kurven entsprechen den theoretischen d13C-Verarmungen, die nach dem totalen
Gleichgewichts- („Batch“) und dem Rayleigh-Modell zu erwarten wären.
Die Meßwerte legen daher nahe, daß eine Situation zwischen diesen beiden extremen Modellen verwirklicht war.
Die Menge an Fluiden, die ein Gestein infiltriert und mit ihm ausgetauscht hat, kann über
eine isotopische Massenbilanzgleichung errechnet werden. Wenn es sich dabei um eine
Gleichgewichtsreaktion handelt, bei der die gesamte Fluidmasse mit einem Gestein reagiert, dann gilt nach Taylor[289]:
0
d
- d Gestein
æ Fö
,
= 0 Gestein
ç ÷
è R ø closed system d Fluide - d Gestein + D
232
[GL 241]
B. Stabile Isotope
wobei F und R die Atomprozente des interessierenden Elementes in der fluiden Phase und
im Gestein sind (F + R = 100%) und D = dGestein – dFluide ; d 0 sind die Initialwerte und die nicht
0
mit „0“ indizierten d’s die Werte nach Beendigung der Reaktion. d Gestein
kann man oft an
einer Partie messen, die der Fluidinfiltration entgangen ist. dGestein läßt sich an den reagier0
ten Gesteinen messen, d Fluide
kann abgeschätzt werden, wenn die Quelle der Fluide
bekannt ist. D läßt sich abschätzen, wenn man die Temperatur der Äquilibrierung kennt.
Geschieht die Fluidinfiltration dagegen im offenen System, wobei ein Inkrement der fluiden Phase mit dem Gestein reagiert und dann das System verläßt, dann gilt eine andere
Gleichung:
ù
éæ F ö
æ Fö
= ln êç ÷
+ 1ú ,
ç ÷
è R ø opensystem
êëè R ø closed system úû
[GL 242]
wobei (F/R)closed system das aus GL 241 errechnete Verhältnis ist. Zu den Prozessen, die sich
durch derartige Fluidinfiltrationen beschreiben lassen, gehören z.B. die Bildung von Skarnen oder generell Kontaktmetamorphosen um fluidreiche granitische Plutone.
Eines der größeren Probleme in der Geochemie und Petrologie der Metamorphite ist die
Granulitisierung. Granulite sind Gesteine, die sich unter Druckbedingungen der Unterkruste bei niedrigen Wasseraktivitäten aus Sedimenten und Magmatiten bilden.Eine zeitweilig
populäre Theorie, welche die niedrigen H2O-Aktivitäten erklärt, ist die, daß CO2-Fluide aus
dem Erdmantel strömen und in der Unterkruste Dehydratationen bewirken, wobei der
größte Teil des Wassers in seichtere Krustenniveaus auswandert[300]. Diese Theorie bezieht
ihre Nahrung aus der Beobachtung, daß die Fluideinschlüsse in Mineralen aus Granuliten
meist reines CO2 sind und damit den Fluideinschlüssen der Erdmantelperidotite ähneln,
aber nicht denen anderer Krustengesteine. Dieses Strömungsmodell erfordert jedoch Mengenverhältnisse für Fluid (CO2)/Gestein von »0.1 – 0.3[301] und sollte damit erhebliche Auswirkungen auf die d13C- und d18O-Werte der Granulite haben. Tatsächlich scheint das aber
nicht der Fall zu sein, wenn man Granulite und amphibolitfazielle Gesteine vergleicht, die
dieselben Edukte haben, was der Infiltrationstheorie klar widerspricht. Die Tendenz geht
daher heute dahin, das CO2 der Fluideinschlüsse in Metasedimenten aus dem Abbau von
Karbonaten abzuleiten, während es in den Metamagmatiten ein magmatisches Relikt sein
könnte. Metamagmatite könnten zudem primär „trockene“ Gesteine sein, so daß die H2OArmut der aus ihnen hervorgegangenen Granulite eine zwanglose Erklärung hat.
233
Stickstoff
20.0
Stickstoff
Stickstoff besteht aus zwei stabilen Isotopen mit den Massenzahlen 14 (natürliche Häufigkeit 99.64%) und 15 (0.36%). Das größte irdische Stickstoffreservoir ist wahrscheinlich die
Atmosphäre, in der 15N mit einer Häufigkeit von 0.3663% (relativ zum Gesamtstickstoff)
vertreten ist. Da das 15N/14N-Verhältnis der Atmosphäre weltweit konstant ist, wird es
bequemerweise als Referenzwert für die Angabe des d15N beliebiger Proben verwendet.
Neben der elementaren Form kommt Stickstoff auf der Erde als Nitrat vor in seltenen Mineralen wie a-KNO3 oder NaNO3, daneben aber auch als Ammonium-Ion in seltenen Phosphaten oder auch als Ammoniak. In der Ammonium-Form scheint er auch – neben der elementaren Form – in den meisten Magmatiten aufzutreten, in denen NH4+ auf Grund seines
identischen Ionenradius K+ zu ersetzen vermag. Stickstoff ist allgegenwärtig in der Biosphäre, wo es essentieller Baustein von Aminosäuren und Proteinen ist. Der N-Gehalt von
Magmatiten liegt meist in der Größenordnung 10 – 100ppm; in Sedimenten ist er höher
und kann in Tonen bis zu einigen 1000ppm betragen, liegt jedoch meist zwischen »100
und 1000ppm.
Isotopenfraktionierungen treten beim Stickstoff einerseits infolge von kinetischen Prozessen bei der bakteriellen Nitrifizierung und Denitrifizierung auf; ihrer Größe nach sind dies
die bedeutendsten Effekte. In der anorganischen Welt spielt vor allem die Reaktion
NH4+
º NH3(Gas)
eine Rolle, für die bei 25°C ein Fraktionierungsfaktor a von 1.034 berechnet wurde[266].
Die IsotopengeocheErdgas
mie des Stickstoffs
erfreut sich, mit AusÖl
nahme der Bio- und
Umweltgeochemie,
Landlebewesen
keiner besonderen
marine Organismen
Beachtung, einerseits,
weil man sich von der
N2
NH3
Analyse der N-Isotope
Meerwasser
keine wesentlichen
Atmosphäre
Informationen verspricht, die nicht mit
Magmatite
Hilfe anderer Isotopensysteme besser gewonDiamanten
nen werden können;
zum anderen ist die -20
-10
0
10
20
Gefahr der sekundären
15
d N
Verunreinigung von
Gesteinen und Mineralen nicht zu vernach- ABBILDUNG 186 Variation der Stickstoffisotope in der Natur
lässigen, und außerdem weiß man vergleichsweise wenig über die Wege der Stickstofffraktionierung in der
festen Erde. Der in Gesteinen elementar vorliegende Stickstoff (Fluideinschlüsse in Mineralen aus Metasedimenten enthalten in der Regel erhebliche Stickstoffmengen.) wird sich als
inertes N2-Molekül bei den meisten geochemischen Prozessen relativ inaktiv verhalten und
nur durch Diffusion fraktionieren können. Man wird daher erwarten, daß die N-Isotopenzusammensetzung der Atmosphäre nicht sehr verschieden ist von dem Reservoir des Erdmantels, aus dem die Atmosphäre letztlich entgast ist[294].
Abbildung 186[266] gibt eine Übersicht über die d15N-Werte verschiedener wichtiger terrestrischer Stickstoffreservoirs. Magmatite können demnach eine sehr weite Variation ihrer
234
B. Stabile Isotope
Stickstoffisotopie zeigen. Die N-Analyse von submarinen Basalten hat gezeigt, daß mittels
verschiedener (Extraktions-) Techniken verschiedene Ergebnisse erhalten werden; daher
hängen die d15N-Werte vielfach davon ab, in welchem Labor die Analysen durchgeführt
wurden. Typischerweise findet man durch Schmelzextraktion des Stickstoffs in MORB
Gehalte um 1ppm, während Methoden der instrumentellen Neutronenaktivierungsanalyse eine Größenordnung höhere Gehalte liefern; allerdings ist mit dieser Methode keine
Isotopenanalyse möglich. Die Angaben für d15N von MORB schwanken zwischen »+17[302]
und » 0[303], wobei den niedrigeren Werten die größere Glaubwürdigkeit beigemessen wird,
da andernfalls die Stickstoffisotope während der Bildung der Atmosphäre erheblich fraktioniert worden wären, wofür es keinen plausiblen Mechanismus gibt.
Hohe Stickstoffgehalte von 100 – 2100ppm und Isotopenvariationen zwischen -11.2 und
+6.0 wurden in Diamanten gefunden[304], wobei Konzentrationen und Isotopien positiv
miteinander korreliert waren. Die niedrigen d15N-Werte, die vornehmlich in Diamanten
der peridotitischen Suite gefunden werden, wurden dabei als Hinweis auf eine heterogene
Akkretion der Erde gedeutet, weil diese Isotopenverhältnisse niedriger sind als die in
MORB. Diese Interpretation wird allerdings nicht uneingeschränkt akzeptiert, weil die
Stickstoffisotopie z.B. nicht mit der He-Isotopie von Diamanten parallel läuft. Hohe d15NWerte in Diamanten korrelieren mit niedrigen d13C-Werten und unterstützen damit die
Hypothese, daß die Kohlenstoffquelle solcher Diamanten subduzierter Kohlenstoff biogenen Ursprungs sein kann. Diese Interpretation wird allerdings dadurch erschwert, daß
individuelle Diamanten Wachstumszonierungen zeigen können, mit denen beträchtliche
Isotopenvariationen verbunden sind, z.B. mehr als 10‰ für d13C und mehr als 20‰ für
d15N[305].
235
Schwefel
21.0
Schwefel
Schwefel besteht aus den 4 stabilen Isotopen 32S (Häufigkeit 95.02%), 33S (0.75%), 34S
(4.21%) und 36S (0.02%). Die S-Isotopie wird konventionell als das Verhältnis 34S/32S angegeben und als d34S relativ zum 34S/32S-Verhältnis des Troilits aus dem Canyon DiabloMeteorit ausgedrückt.
Im Massenspektrometer wird Schwefel vorzugsweise als SO2 gemessen, wobei der Schwefel
in Sulfiden oder elementarer S zu SO2 oxidiert und Sulfate mittels H3PO2 und/oder HJ reduziert werden. Nach einer anderen Methode wird ein Gemisch aus Sulfid- und Sulfatschwefel bei 280°C im Vakuum mit H2O-freier Phosphorsäure, die Sn-Ionen enthält, umgesetzt.
H2S und SO2 werden dadurch freigesetzt und können auf geeignetem Wege voneinander
getrennt und gemessen werden.
Schwefel ist ein allgeEvaporite
genwärtiges Element,
sowohl in Gesteinen
Meerwasser
des magmatischen und
metamorphen BilSedimente
dungsbereichs (hier vor
allem in Form von SulMetamorphite
fiden, selten als elementarer S) als auch in
Granitoide
Sedimenten (als Sulfate
und Sulfide). Er kommt
Basalte
gelöst als Sulfat im
Meerwasser vor (» 900
-30
-20
-10
0
10
20
30
40
50
p p m S [ 4 1 ] ) , i n d e r -40
34
Atmosphäre als SO 2
d S
und in der Biosphäre in
einer Vielzahl von Ver- ABBILDUNG 187 Variationsbereich der Schwefelisotope in Materialibindungen und Oxida- en der Erde
tionsstufen. Die natürliche d34S-Variation macht » 150‰ aus. Die Isotopie wichtiger geochemischer Reservoirs
ist in Abbildung 187 dargestellt[266]. Die isotopisch schwersten Sulfate haben ein d34S um
+90‰ und die leichtesten Sulfide von -65‰. Für diese große Variation sind zwei Effekte
verantwortlich:
a) verschiedene chemische Austauschreaktionen zwischen Sulfaten und Sulfiden; begünstigt werden die Isotopieeffekte dabei durch unterschiedlichen Bindungscharakter und
Aggregatzustände (fest-flüssig-gasförmig); die schweren S-Isotope werden in der weniger
flüchtigen Phase – in der Regel den Sulfaten – konzentriert;
b) infolge eines kinetischen Effektes werden die leichten S-Isotope bei der bakteriellen
Reduktion von Sulfaten zu Sulfiden angereichert; dieser Prozeß ist für den weitaus größten
Isotopieeffekt verantwortlich. Die beiden wichtigsten Arten der sulfatreduzierenden Bakterien sind Desulfovibrio desulfuricans und Desulfatomaculum. Sie beziehen die Energie ihres
Wachstums und der Reduktion der Sulfate aus der anaerobischen Oxidation von H2 und
organischer Materie, wozu sie den Sauerstoff des Sulfats verwenden. Die Bakterien gedeihen bei Temperaturen zwischen 0 und 100°C in Süßwasser und Salzwasser mit bis zu 30%
NaCl bei Drücken bis zu 1kbar, bei pH-Werten zwischen 4.2 und 10.4 und EH-Werten zwischen +350 und -500mV. Im Labor lassen sich mit solchen Bakterienkulturen S-Isotopenfraktionierungen bis zu 5% erzielen. Die Größe der Isotopenfraktionierung und die Menge
des entwickelten H2S hängen vom Sulfatgehalt, der Größe der Bakterienkolonien, der Verfügbarkeit von Nährstoffen, der Sedimentationsrate, der Salinität und der Temperatur ab.
Auch die Isotope des Selens – eines Elementes, das sich geochemisch ähnlich verhält wie
236
B. Stabile Isotope
Schwefel – werden durch manche Mikroorganismen fraktioniert, insbesondere einige Salmonellenarten, die 76Se um einige 10‰ über das 82Se anzureichern vermögen. Auf Grund
der S-Isotopenvariation mariner Sulfide schließt man auf die Existenz solcher Sulfat-reduzierender Bakterien seit mindestens 2.3Ga. Die marinen Sulfide des Archaikums weisen
dagegen durchweg d34S-Werte um 0 auf.
noch vorhandenes Sulfat [%]
Besonders große Isotopenva1
riationen sind in der Natur
unter Bedingungen des offenen Systems zu erwarten, aus
Sul
fat
Sul
dem das produzierte H2S konfid
tinuierlich entfernt wird (Rayleigh-Fraktionierung), z.B.
0.1
durch Entgasung oder durch
Ausfällung von FeS2. Die
RayleighReaktion wird dann fortFraktionierung
schreiten, bis entweder das
Sulfat verbraucht ist oder
keine Nahrung mehr für die
0.01
B a k t e r i e n z u r Ve r f ü g u n g
steht. Da der Schwefel im H2S
Mittelwert für das bis
leichter ist als im Sulfat, wird
zu diesem f-Wert
das residuale Sulfat und damit
entwickelte Sulfid
auch das später gebildete Sulfid mit abnehmender Sulfat0.001
menge schwerer. Das ist sche-20
0
20
40
60
matisch in Abbildung 188
34S [‰]
[266]
d
. Im Gegensatz
dargestellt
dazu wird unter anaeroben
Bedingungen wie im Schwar- ABBILDUNG 188 Variation von d34S von Sulfid und residualem
zen Meer nur ein geringer Teil Sulfat durch Rayleigh-Fraktionierung, ausgehend von Sulfat
des zur Verfügung stehenden mit d34S = 10‰ zu Beginn und unter Annahme eines FraktioSulfats verbraucht, weil das nierungsfaktors a = 1.025.
Reservoir sehr groß ist. Das
gebildete, isotopisch leichte H2S bleibt im System (H2O) und führt zu dessen Vergiftung, so
daß die Meeresorganismen, die nach ihrem Tod die Nahrung der sulfatreduzierenden Bakterien darstellen, absterben. Und damit kommt schließlich auch das Wachstum der Bakterien selbst zum Stillstand.
Bei Temperaturen unter »50°C scheint die bakterielle Aktivität die einzige Möglichkeit der
Sulfatreduktion zu sein. Bei Temperaturen oberhalb »250°C spielt auch die Reduktion
durch Fe2+ eine Rolle. Einen großen Isotopieeffekt hat potentiell die Reaktion
32
SO 24- + H234S
º
34
SO 24- + H232S,
für die ein Fraktionierungsfaktor a von 1.075 bei 25°C berechnet wurde. Es ist jedoch kein
Mechanismus bekannt, der die Reaktion bei so niedriger Temperatur ablaufen läßt.
Der Erdmantel scheint in Bezug auf seine Schwefelisotopenzusammensetzung ein relativ
homogenes Reservoir darzustellen, dessen d34S-Werte nur wenig über dem des Canyon Diablo-Troilits liegen[294] (siehe Abbildung 189). Sulfide wie Pyrrhotin und Pentlandit, die man
gelegentlich in Xenolithen (Granatperidotite, Eklogite) in Kimberliten findet, weisen d34S
zwischen etwa 0 und +2 auf, was wahrscheinlich den Verhältnissen im Erdmantel am
besten entspricht. Basaltische Gesteine zeigen eine höhere Variation. Aus subaerisch ausgeflossenen Basalten kann der Schwefel zum Teil entgasen, wobei eine geringe Fraktionierung
auftritt. Bei Basalten aus Hawaii hat man d34S-Werte bis » -5‰ beobachtet, gekoppelt an
niedrige S-Gehalte. Man muß daraus folgern, daß die entgaste Komponente oxidiert ist
237
Schwefel
Norilsk
5
Muscox
SO42- aus submarinen Basalten
Tholeiite
d34S [‰]
10
Alkalibasalte
Hawaii
submarine OIB
MORB
Peridotitxenolithe
Karbonatite
(SO2). Als wichtige Komponenten magmatischer Fluide sind neben SO2 und SO3 auch reduzierte Spezies wie S und H2S bekannt. Bei hohen Temperaturen ist SO2 jedoch die dominierende Phase. Große basische Intrusionen in die kontinentale Kruste können erhebliche SKontaminationen erfahren (z.B. Muskox, Norilsk), so daß ihre S-Isotopien keine Rückschlüsse auf die des Erdmantels erlauben.
0
-5
0
400
800
1200
1600
ppm S
ABBILDUNG 189
links: d34S-Werte und Schwefelgehalte ozeanischer Basalte und von
Peridotitxenolithen. Die subaerischen Ozeaninselbasalte (OIB) aus Hawaii
haben niedrigere Schwefelgehalte und d34S-Werte als submarine OIB und
MOR-Basalte. Verlust von 34S und Gesamtschwefel scheinen daher einander
bei der Entgasung von Magmen parallel zu verlaufen. Der Sulfatschwefel
ozeanischer Basalte hat ein höheres d34S als der Gesamtschwefel.
rechts: zum Vergleich sind die S-Isotopien für kontinentale Tholeiite und
Alkalibasalte aus Europa, Karbonatite aus Afrika und von zwei basischen
Intrusionen eingetragen.
Ein wichtiges Reservoir im S-Zyklus der Erde sind die Ozeane, die » 10% des Schwefels des
Systems Kruste + Ozeane enthalten[307]. Der Schwefel liegt in den Ozeanen fast ausschließlich als Sulfat vor mit einem mittleren d34S von heute » +20‰. Das Sulfat hat eine mittlere
Residenzzeit von » 7.9Ma und wird als Sulfid (sedimentäre oder organisch gebundene Sulfide) oder Sulfat (Gips) in einem Mengenverhältnis von etwa 1:2 ausgefällt, der wesentliche
Teil davon durch bakterielle Reduktion. So gilt z.B. der mitteleuropäische Kupferschiefer als
das Produkt bakterieller Tätigkeit[308]. Der durchschnittliche S-Gehalt von Sedimenten liegt
um 5000ppm, der von Magmatiten und hochmetamorphen Gesteinen bei nur 200 ppm.
Der Schwefel in Sedimenten macht ca. 60% des S im System Kruste + Ozeane aus. Bedenkt
man, daß dieser Schwefel über den sedimentären Kreislauf auch mit dem Ozeanschwefel
austauscht, dann wird klar, daß direkt oder indirekt der Schwefel des Seewassers eine wichtige Rolle bei der Entstehung vieler Sulfidlagerstätten spielen muß.
238
B. Stabile Isotope
Alter [Ma]
Aus der Analyse von Evaporiten ist
0
bekannt, daß das 34S/32S-Verhältnis T
im Lauf der Erdgeschichte in den K
100
Ozeanen stark geschwankt hat,
[266]
(siehe Abbildung 190
). Ein Maxi- J
200
mum ist im Kambrium zu verzeich- Tr
34
nen mit d S von gut +30, ein Mini- P
C
300
m u m i m P e r m m i t c a . 1 0 ‰ . C21
Obwohl die Gründe für diese D
400
Schwankungen weit davon entfernt S
sind, klar zu sein, hat die Vorstellung O
500
einiges für sich, daß sie letztlich den
Zustrom von S durch Abtragung der C
Kontinente widerspiegeln[309],
600
gekoppelt mit vermehrter oder verminderter Bildung von Evaporiten.
700
In Zeiten vermehrter Evaporitbil- p
dung wie im Perm werden erhebli- C
800
che Teile des S dem Meerwasser entzogen, so daß das d34S empfindlicher
900
auf die Zumischung von bezüglich
der Isotopie andersartigem Schwefel
aus Magmatiten reagiert. In Zeiten, 5
35
10
25
15
20
30
in denen keine Evaporite gebildet
d34S [‰]
werden, z.B. im Kambrium, wirkt
sich der Zustrom von S mit negativerem d34S dagegen nicht aus. Um die ABBILDUNG 190 Variation der Schwefelisotope im
S-Isotopenunterschiede des Meer- Meerwasser im Verlauf der letzten » 1Ga. Die Striche
wassers zwischen dem Kambrium stellen die zu einer bestimmten Zeit beobachtete Geund dem Perm von »20‰ zu erklä- samtvariation dar, das breite Band Mittelwerte über
ren, wäre eine Variation des in Sedi- den Verlauf der Zeit.
menten und den Ozeanen festgelegten Schwefels um ±30% erforderlich[311].
Stabile Isotope bieten die besten geochemischen Möglichkeiten, um die Herkunft erzführender Fluide aufzudecken und die Bildungstemperaturen von Lagerstätten abzuschätzen.
Da zahlreiche wichtige Lagerstätten Sufide sind oder enthalten, ist es nicht verwunderlich,
daß die Geochemie der S-Isotope weite Anwendung in der Lagerstättenkunde findet. Zwei
wesentliche Faktoren kontrollieren die S-Isotopenzusammensetzung hydrothermaler
Lagerstätten:
•
Aus der Fraktionierung D zwischen verschiedenen S-haltigen Mineralen lassen sich
Rückschlüsse auf die Bildungstemperatur der Lagerstätte gewinnen. Abbildung 191
zeigt Gleichgewichtsfraktionierungskurven zwischen H2S und verschiedenen Sulfiden
und Sulfat, aus deren Kombination sich Sulfid-Sulfid-Thermometer ableiten lassen.
Eine hohe Fraktionierung weist das Zinkblende-Bleiglanz-Thermometer auf, daß sich
besonders weiter Verbreitung erfreut, weil beide Sulfide praktisch immer miteinander
vergesellschaftet vorkommen. Für dieses Thermometer gilt die folgende Gleichung:
T=
(0.85 ± 0.03) ´ 103
D ZnS-PbS
[GL 243]
Obwohl einige dieser Sulfidthermometer experimentell kalibriert sind, sind die Übereinstimmungen der Eichungen verschiedener Arbeitsgruppen nicht sonderlich befriedigend. Die Fraktionierungskurven für das ZnS–PbS- und zwei weitere Thermometer
sind in Abbildung 192 dargestellt[16].
239
Schwefel
Die Isotopie des Gesamt800 400 300 200
100
50 8C
schwefels gibt Hinweise auf
30
seinen Ursprung. Da die SIsotope zwischen den Fluiden und Sulfidmineralen
25
fraktionieren, muß man
eine gute Kenntnis der Iso20
topie des gesamten an der
Bildung des Vorkommens
teilhabenden Schwefels ha15
ben. Auf Grund der d 34 SWerte des Gesamtschwefels
10
lassen sich drei Quellen der
SO2 – H2S
Erzlösungen unterscheiden: Werte um 0 weisen auf
5
magmatische Quellen hin,
S
FeS2 – H2
während Werte um 20‰
ZnS – H2S
(je nach Alter der Lagerstät0
te auch andere Werte, siehe
HS– – H2S
Abbildung 190) Seewasser
PbS – H
-5
als Quelle des Schwefels an2S
zeigen. Intermediäre Werte
zwischen »5 und 15‰ kön-10
nen auf krustale Gesteine
0
1
2
3
4
5
6
7
8
9 10
verschiedenster Art hinwei6
2
2
10 /T [K ]
sen oder auf Mischungen
der beiden ersten Quellen
(Sulfide der mittelozean- ABBILDUNG 191 Experimentell bestimmte Gleichgewichtsischen Rücken ohne Sedi- fraktionierungsfaktoren a zwischen diversen S-Verbindunmentauflage zeigen d 34 S- gen einerseits und H S andererseits. Gepunktete Kurventeile
2
Variationen zwischen ca. 0 stellen Extrapolationen dar.
und 5‰; bei Gegenwart
von Sedimenten, z.B. im Roten Meer, sind die Variationen größer und gehen bis ca.
15‰ hinauf[306]). Abbildung 193, Seite 242 zeigt die Schwefelisotopien mariner Sulfide
und Sulfate und massiver Sulfiderze über die geologische Zeit[307]. Es ist daraus zu erkennen, daß archaische Sulfide und Sulfate d34S-Werte haben, die nahe 0 liegen und
damit eine Erdmantelabkunft nahelegen. Größere Abweichungen in beide Richtungen
sind erst seit gut 2Ga zu verzeichnen, wobei Abweichungen zu negativen 34S/32S-Verhältnissen als Anzeichen der Tätigkeit sulfatreduzierender Bakterien gedeutet werden
können. Besonders bemerkenswert ist die sehr weite Variation des d34S im Kupferschiefer. Solche großen Variationen, zumal dann, wenn sie im Sediment über den cm-Bereich beobachtet werden können, gelten als sehr starke Indizien für eine bakterielle
Entstehung. Es ist jedoch zu betonen, daß es, im Gegensatz zu früheren Lehrmeinungen, Lagerstätten, die allein bakteriell entstanden sind, nicht zu geben scheint. Auch
Lagerstätten, die ihre Entstehung ausschließlich magmatischen Prozessen verdanken,
scheint es eher nicht zu geben[307]. Durch Subduktionsprozesse kann mariner Sulfidund Sulfatschwefel in den Mantel transportiert werden, wo er erneut für die Bildung
von Fluiden zur Verfügung steht und eine wichtige Schwefelquelle in Lagerstätten über
Subduktionszonen werden kann.
1000 ln a
4
SO 2
-
–H
2S
•
240
B. Stabile Isotope
800
400
200
100
50
8C
16
14
Bl
ei
gl
an
z
12
it
–
10
8
6
de
en
l
b
nk
Zi
z
an
Py
r
D34S [‰]
Da Schwefel ein Bestandteil
aller organischer Materie ist, ist
er elementar oder in Form verschiedenster Verbindungen
auch in fossilen Brennstoffen
enthalten. Bei der Verbrennung
von Öl und Kohle geraten große
Mengen an aggressivem SO2 in
die Umwelt, wo sie ein nicht
unbeträchtliches Gefährdungspotential darstellen. Gewaltige
Mengen an SO2 können bei Vulkaneruptionen freigesetzt werden. Beim Ausbruch der LakiSpalte auf Island in den Jahren
1783 und 1784 sollen ca. 120
Millionen Tonnen SO 2 in die
Atmosphäre gelangt sein [310] .
Zusammen mit anderen Gasen
(Halogene) verursachten sie ein
großes Viehsterben auf der
Insel.
l
ig
le
–B
lende
nkb
i
Z
t–
4
i
Pyr
2
0
Ein erheblicher Teil des SO 2
0
2
4
6
8
10
12
kann bei heftigen Explosionen
6
2
2
auch in die Stratosphäre gelan10 /T [K ]
gen, wo es mit photochemisch
freigesetzten OH-Radikalen zu
H 2 SO 4 reagiert. Die Schwefel- ABBILDUNG 192 Fraktionierung der Schwefelisotope zwisäure verbindet sich im Verlauf schen kogenetischen Sulfiden als Funktion der Temperatur.
von Wochen bis Monaten mit Die Daten basieren auf berechneten GleichgewichtskonStaubpartikeln zu Aerosolen stanten.
(typischer Durchmesser 0.5µm)
und wird erst innerhalb einiger Jahre aus der Stratosphäre entfernt. Diese Aerosolwolken
vermindern die Sonneneinstrahlung auf der Erde und bewirken somit eine Abkühlung. Die
durch den Ausbruch des El Chichón in Mexico 1982 in die Stratosphäre gelangte Menge
SO2 entsprach » (10 – 20)´106 Tonnen H2SO4 bei nur » 0.5 km3 ausgeworfenen Aschen[312].
Nach dem Ausbruch des Pinatubo auf den Phillipinen Anfang der 1990-er Jahre konnte
man vor allem in den Äquatorialgebieten für einige Monate eine Temperaturerniedrigung
nachweisen.
241
Schwefel
0.0
Kuroko
Zypern
marine Sulfate und Sulfide
Besshi
Kupferschiefer
Sulitjelma
Meguma
0.5
0.0
Raul
0.5
Notre Dame
New Brunswick
1.0
White Pine
Adirondacks
1.5
McArthur Basin
Skellefteå
Anderson
Skellefteå
Onwatin
Outokumpu
2.0
2.0
t [Ga]
t [Ga]
1.5
1.0
Roseberry
Pine Creek
2.5
Hamersley
Zimbabwe
Yilgarn
3.0
3.5
3.0
Aldan
Fig Tree
Warrawoona
Onverwacht
Barberton
North Pole
Big Stubby
4.0
-40
-20
d34S
ABBILDUNG 193
242
3.5
Sulfidlagerstätten
Isua
4.0
-60
2.5
Geco
Noranda
South Bay
Birch-Uchi
Michipicoten
0
[‰]
20
40 -10
0
10
d34S
20
30
40
[‰]
Schwefelisotopie mariner Sulfate und Sulfide (links) und massiver Sulfidlagerstätten (rechts). Dicke Linien stellen die Hauptvariation dar. Hellblaue
Linien stehen für Sulfatschwefel, dunkelblaue Linien für Sulfidschwefel.
B. Stabile Isotope
22.0
Calcium
Die technische Weiterentwicklung der Massenspektrometrie von den Geräten mit einem
Faraday-Auffänger zu solchen mit Multikollektoren hat dazu geführt, daß man heute kleinere Isotopenunterschiede auflösen kann, als dies noch um 1980 der Fall war. Damit ist
auch das Ca über seine Anwendung in der Geochronologie von Gesteinen mit hohen K/
Ca-Verhältnissen hinaus interessant geworden. Die Ca-Isotope erfahren in der Natur eine
Fraktionierung sowohl bei biologischen als auch bei chemisch-physikalischen Prozessen.
Die wenigen Laboratorien, die sich mit der Isotopengeochemie von Ca beschäftigen, geben
die Isotopenverhältnisse als
d
44
é
Ca [‰] = ê
ê
êë
(
(
44
44
Ca
Ca
40
40
Ca
Ca
)
)
Probe
Standard
ù
- 1ú ´ 1000
ú
úû
[GL 244]
40
an. Diese Angabe relativ zu Ca hat natürlich den Nachteil, daß nicht zwischen einer Isotopenfraktionierung und einer radiogenen Quelle (übernormale Häufigkeit von 40Ca aus
dem Zerfall von 40K) unterschieden werden kann. Zhu & Macdougall (1998)[313] schlagen
auf Grund ihrer Analysen von Meerwasser verschiedener Ozeane und Tiefen vor, als Standard Meerwasser zu verwenden, weil dies auf Grund seiner hohen Residenzzeit (ca. 1 Ma)
eine homogene Zusammensetzung von 44Ca/40Ca = 0.0217470±13 aufweist. Leider verwenden verschiedene Laboratorien verschiedene Standards und benutzen außerdem verschiedene Fraktionierungskorrekturen bei ihren Messungen, so daß auch die d44Ca-Werte
nicht miteinander direkt vergleichbar sind.
0.5
C. kullenbergi
N. pachyderma
G. sacculifer
Atlantik, Kokkolithenschlamm
Atlantik, Kokkolithenschlamm
tropische Koralle
MORB, Südatlantik
Pazifik, Kokkolithenschlamm
MORB, EPR
MORB, Südatlantik
Aldan
Yana
Kolyma
Lena
Ganges-Nebenfluß
-2.5
Ganges-Nebenfluß
-2.0
Orinoco
Orinoco
-1.5
Amazonas
dCa
-1.0
Ganges-Nebenfluß
Ganges-Nebenfluß
Yangtze
-0.5
Atlantik, Karbonatschlamm
Karibik, Kokkolithenschlamm
Meerwasser
0.0
Atlantik, Karbonatschlamm
Flußwässer
MORB
Karbonatschlämme
Foraminiferen
-3.0
ABBILDUNG 194
Ca-Isotopenvariation in Flußwässern, MORB, holozänen Karbonaten der
Meeresböden und einzelnen Foraminiferen. Unter den drei Spezies von
Foraminiferen wurde jeweils eine aus wärmerem und/oder flacherem und
eine aus tieferem und/oder kälterem Wasser analysiert. Die Foraminiferen
aus dem tieferen oder kälteren Wasser haben jeweils das niedrigere d44Ca.
243
Calcium
2
Tümmler
Tümmler
Tümmler
Seeotter
Schnecke
Sardelle
Seestern
Napfschnecke
-2
Foraminifere
-1
Foraminifere
0
Meerwasser
dCa
1
-3
ABBILDUNG 195
Variation von d44Ca in marinen Organismen[314]. Es ist zu beachten, daß die
d44Ca-Werte nicht unmittelbar mit denen in Abbildung 194 vergleichbar
sind, wie an dem positiven d44Ca-Wert des Meerwassers erkennbar ist.
Wenn man das d44Ca des Meerwassers mit demjenigen von Flußwässern, marinen Hydrothermalquellen (MORB als Vertreter für das d44Ca solcher Wässer) und rezenten marinen
Karbonatsedimenten vergleicht, stellt man fest, daß das Meerwasser unter allen diesen
Materialien das höchste d44Ca aufweist (Abbildung 194[313]). Unter den Flußwässern haben
die Nebenflüsse des Ganges besonders niedrige d44Ca-Werte, verbunden mit extrem hohen
87
Sr/86Sr-Verhältnissen (0.76 – 0.80) und geringen Ca-Gehalten aufweisen. Dies deutet auf
eine Herkunft aus Granitoiden im Himalaya hin, bei denen infolge des hohen K/Ca-Verhältnisses nicht auszuschließen ist, daß das niedrige d44Ca zumindest teilweise radiogenen
Ursprungs ist. Inwieweit der Unterschied zwischen dem d44Ca des in die Weltmeere eingetragenen Ca und den aus dem Meerwasser ausgeschiedenen biogenen Sedimenten signifikant ist, ist nicht vollends klar. Wenn er signifikant ist, müßte das dahingehend gedeutet
werden, daß Zufluß und Austrag nicht im Gleichgewicht stehen. Immerhin scheinen die
Karbonatschalen mariner Organismen (und auch anorganisch ausgefällte Karbonate) eine
Anreicherung des leichteren Isotops 40Ca gegenüber dem Meerwasser aufzuweisen. Als
Grund mag angeführt werden, daß die Fraktionierung kinetischer Natur ist, wobei das
leichteste Ca-Isotope am raschesten aus dem Meerwasser ausgefällt wird[313]. Skulan et al.
(1997)[314] haben zudem die Beobachtung gemacht, daß sich in der marinen Nahrungskette das leichtere Isotope 40Ca anreichert (Abbildung 195). Beim Vergleich der d44CaWerte der Schalen von Foraminiferen schließlich zeigt sich, daß Exemplare aus tieferem
und/oder kälterem Wasser negativere d44Ca-Werte aufweisen als solche aus flacherem und/
oder wärmerem Wasser, daß die Fraktionierung also – erwartungsgemäß – mit sinkender
Temperatur größer wird[313],[315]. Die Ca-Isotopenfraktionierung kann dabei für verschiedene Foraminiferen eine sehr unterschiedliche Temperaturabhängigkeit von mehr als einer
Größenordnung aufweisen[315], die bislang nicht genügend verstanden sind, um die CaIsotope zur Paläotemperaturbestimmung zu verwenden. Es ist zudem noch darauf hinzuweisen, daß die Fraktionierung der Ca-Isotope bei der Ausscheidung von Karbonaten aus
Wasser umgekehrt verläuft wie diejenige der Sauerstoffisotope, d.h. je niedriger die Temperatur, desto leichter die Ca-Isotope und desto schwerer die O-Isotope. Gussone et al.[315]
schlagen dafür ein Modell vor, wonach die Ca-Isotopenfraktionierung allein durch kinetische Effekte bestimmt ist, diejenige der Sauerstoffisotope aber sowohl durch kinetische als
auch durch Gleichgewichtseffekte.
244
B. Stabile Isotope
23.0
Eisen und andere schwere Elemente
Mit der Etablierung von ICP-MS-Geräten, die mit mehreren Faraday-Kollektoren ausgestattet sind, ist es einfacher geworden, natürliche Isotopenvariationen schwerer Elemente zu
dokumentieren als mit der Thermionenmassenspektrometrie, bei der die Massenfraktionierung während der Messung schwer zu kontrollieren ist (vergleiche Seite 75 und folgende
oder [316] für die Fe-Isotopenanalyse unter Verwendung eines Doppelspikes). Damit ist die
Erfassung der massenabhängigen Isotopenfraktionierung der schwereren Elemente und
Klärung ihrer Ursachen seit dem Ende der 1990-er Jahre zum Gegenstand intensiver Forschung innerhalb der Isotopengeochemie geworden. Übergangsmetalle wie Cr, Fe, Ni, Cu
oder Zn bieten sich besonders an, weil sie in der Natur relativ häufig vorkommen und
zudem biologisch von Bedeutung sind. Die Darstellungsweise der Isotopenvariationen ist
für diese Elemente nicht einheitlich, weil sowohl die Angabe der d-Abweichung (‰) als
auch die der e-Abweichung (1/10000) verwendet werden, so daß beim Vergleich von Daten
verschiedener Quellen entsprechende Aufmerksamkeit anzuraten ist.
Unter den vier Fe-Isotopen mit den Massenzahlen 54, 56, 57 und 58 hat das letztere nur
eine natürliche Häufigkeit von ca. 0.28%; es wird in der Regel in Veröffentlichungen nicht
aufgeführt. Die Fe-Isotopien werden meist als Abweichung des 56Fe/54Fe-Verhältnisses von
einem Standard angegeben, seltener als Abweichung des 57Fe/54Fe. Als Standards sind
sowohl künstliche („IRMM–14“ Metallstandard des europäischen Institute for Reference
Materials and Measurement, http://www.irmm.jrc.be/[255]) als auch natürliche (Basalte BCR2[317], BIR[318]; Eisenmeteorit Canyon Diablo[317]) in Gebrauch, deren Fe-Isotopie sich voneinander nur sehr wenig unterscheidet.
Als Element mit ungerader Ordnungszahl wird Cu nur aus den beiden Isotopen mit den
Massenzahlen 63 und 65 aufgebaut; infolgedessen wird das Isotopenverhältnis 65Cu/63Cu
in der e- oder d-Form angegeben. Als Standard dient NIST 976 des National Institute of Standards, http://ts.nist.gov/srm[256]. Zn verfügt über fünf stabile Isotope (Massenzahlen 64, 66,
67, 68, 70), unter denen die beiden erstgenannten die häufigsten sind. Angegeben wird die
Abweichung des 66Zn/64Zn von einem Standard der Firma Johnson & Matthey[257]. Cr setzt
sich aus den Isotopen mit den Massenzahlen 50, 52, 53 und 54 zusammen, unter denen
52
Cr mit einer Häufigkeit von 83.8% dominant ist. Das Verhältnis 53Cr/52Cr wird relativ zu
NIST 979 angegeben[319].
7
2.5
2.0
Romil Cu-Lösung
(Zn-dotiert)
1.5
5
0.5
«65Cu
«65Cu
1.0
0.0
-0.5
-1.0
3
1
-2.0
0
2
4
6
8
Analyse Nr.
ABBILDUNG 196
4
2
-1.5
-2.5
Romil Cu-Lösung
relativ zu NIST 976
Ø = 3.43±0.56 (2s)
6
10
12
14
0
0
2
4
6
8
10
12
14
Analyse Nr.
Illustration der Korrektur der meßtechnischen Massenfraktionierung am Beispiel von Cu[256]. Links: Durch Zugabe von Zn als innerer Standard. Das gemessene 68 Zn/ 66 Zn wird benutzt, um einen Korrekturfaktor für das
gemessene 65Cu/63Cu zu ermitteln. Rechts: Durch das „Klammerverfahren“,
bei dem vor und nach jeder Probe ein Standard mit bekannter Isotopenzusammensetzung analysiert wird. Die Cu-Isotopie der Probe ist relativ zur interpolierten Isotopie des NIST-Standards angegeben.
245
Eisen und andere schwere Elemente
Zur Eliminierung der ICP–MS-internen Massenfraktionierung werden zwei Verfahren eingesetzt, die in Abbildung 196 erläutert sind. Zum einen kann man, ähnlich wie auf Seite 81
beschrieben, der Analysenlösung eine Menge eines im Periodensystem benachbarten Elementes mit bekannter Isotopenzusammensetzung als innerer Standard zusetzen, z.B. Zn
bei einer Cu-Analyse. Aus der Abweichung des Isotopenverhältnisses dieses inneren Standards von seinem Sollwert läßt sich für das Element von Interesse ein Korrekturfaktor mit
genügender Genauigkeit abschätzen. Bei der Thermionenmassenspektrometrie müssen
demgegenüber Isotope des zu analysierenden Elementes zugesetzt werden, im Idealfall
radioaktive Isotope mit langer Halbwertszeit, die in der natürlichen Probe nicht vorhanden
sind. Das zweite in der ICP–MS-Analytik eingesetzte Verfahren ist weniger zeitaufwendig.
Hierbei wird vor und nach jeder Probe ein Standard mit bekannter Isotopenzusammensetzung analysiert und daraus sein Verhältnis für den Zeitpunkt der Analyse der Probe interpoliert. Der Meßwert der Probe kann damit unmittelbar mit dem für den Standard interpolierten Wert in Beziehung gesetzt werden und zur Errechnung des e- oder d-Wertes dienen.
Die ersten hoch präzisen Fe-Isotopenanalysen ergaben identische Fe-Isotopien für irdische
und lunare Magmatite[316], aber davon abweichende Isotopien für Mn-Knollen und BIFProben (banded iron formation). Diese Beobachtung führte die Autoren zu dem voreiligen
Schluß, daß die Fraktionierung der Fe-Isotope auf der Erde im wesentlichen biologischen
Prozessen zuzuschreiben ist. Inzwischen ist in der Tat gut dokumentiert, daß biologische
Proben weite Variationen der Fe- und Cu-Isotope aufweisen. So zeigen menschliches
Blut[320] und Hämoglobin von Säugetieren[321] e56Fe-Werte von -20 bis unter -30 (wesentlich niedriger als pflanzliches Material, das als Nahrung dienen kann), und Cu-haltige Proteine von Hefen erreichen in Laborversuchen e65Cu-Werte bis -20[321]. Fe aus Komplexbildnern bakteriellen Ursprungs hatte ein um bis zu 8e-Einheiten niedrigeres e 56 Fe als
anorganisch gebundenes Fe aus Böden, aus denen die Bakterien das Fe bezogen[322]. In
allen diesen Beispielen wiesen die biologischen Proben also kleinere Fe- bzw. Cu-Isotopenverhältnisse auf als die Ausgangsprodukte. Dies stimmt mit der Erwartung überein,
wonach kinetische Effekte dazu führen, daß Bindungen des leichteren Isotops eines Elementes leichter gebrochen, diese Isotope mithin leichter von Organismen genutzt werden
können als schwere. Nicht ganz so eindeutig sind Zn-Isotopenuntersuchungen an marinen
Schwebstoffen aus dem Atlantik vor Mauretanien zu interpretieren, für die eine saisonale
Variation beobachtet wurde[257]. Für Fe-Mn-Knollen wurden in derselben Arbeit d66ZnWerte gefunden, die bis zu 1‰ über denjenigen von marinen tonigen Sedimenten liegen;
auch dieser Unterschied wird biologischer Tätigkeit im oberen Teil der Wassersäule zugeschrieben.
Inzwischen ist klar, daß beträchtliche Fraktionierungen der Isotope der schwereren Elemente auch durch abiogene Prozesse hervorgerufen werden können. Bereits im Jahr 2000
wurde berichtet, daß für die Fe-Isotope in Fe-Mn-Krusten aus dem Nordatlantik eine Korrelation mit der (durch radioaktiven Zerfall bestimmten) Pb-Isotopie besteht, was für eine FeZufuhr von Land als Ursache spricht und nicht für biologische Aktivität in der Wassersäule[255]. Im selben Jahr veröffentlichte dieselbe Arbeitsgruppe eine Studie über die Cu-Isotopenvariation in Erzmineralen aus Lagerstätten und gewöhnlichen Gesteinen[256] .
Danach weist Chalkopyrit aus magmatischen Gesteinen weltweit die geringste Variation,
während Minerale, die sich unter Beteiligung wäßriger Lösungen bei niedrigeren Temperaturen gebildet haben (z.B. Sulfide aus Black Smoker-Kaminen), eine beträchtlich größere
e65Cu-Streuung zeigen. Eine Temperaturabhängigkeit der Fraktionierung der Cu- und FeIsotope wurde inzwischen auch für eine proterozoische Lagerstätte aus Australien gefunden (Abbildung 197[323]). Dort steigen e65Cu und e57Fe in den Sulfiden mit fallender Temperatur an (Richtung der Pfeile). Dieser Befund wird so gedeutet, daß sich aus den heißen
Lösungen Pyrit und Chalkopyrit mit niedrigeren e65Cu- und e57Fe-Werten ausgeschieden
haben; dadurch wurden die Restlösungen ständig isotopisch schwerer, so daß sich aus den
kühleren Lösungen zunehmend isotopisch schwerere Sulfide ausscheiden mußten. Als
Ursache für die große isotopische Streuung der Niedrigtemperatursulfide wird bakterielle
Sulfatreduktion geltend gemacht. In hydrothermalen Lösungen von Quellen auf dem Mee-
246
B. Stabile Isotope
resboden entlang des Juan de Fuca-Rückens wurden Fe-Isotopien mit negativen e56Fe-Verhältnissen gemessen [317] . Auch dafür werden nicht biogene Prozesse verantwortlich
gemacht, ohne daß jedoch eine exakte Beschreibung der Ursache der Fraktionierung derzeit möglich ist. Für südafrikanische BIFs wurden e56Fe-Variationen zwischen -25 und +10
gefunden[324]; dabei weisen die Autoren darauf hin, daß Isotopenfraktionierungen auf chemische Sedimente beschränkt zu sein scheinen. Die Ursachen sehen die Autoren in einer
Kombination aus mineralspezifischen Gleichgewichtsfraktionierungen, Isotopenvariationen der Fluide oder Lösungen, aus denen die Minerale ausgeschieden wurden und auch in
bakterieller Tätigkeit. Besonders hoch ist e56Fe in Magnetit, besonders niedrig in Pyrit.
Pyrit «57/54Fe
heiße Lösungen
(»150°C)
3000
Position in der Lagerstätte [m]
Chalkopyrit «Cu
TSR
TSR
2500
2000
BSR
BSR
BSR
BSR
TSR
TSR
kalte Lösungen
(<100°C)
-5
0
5
10
15
20
-30
-20
«Cu [65Cu/63Cu]
0
10
20
«Fe [57Fe/54Fe]
Cu- und Fe-Isotopenvariation in Pyrit und Chalkopyrit in einem Profil der
sedimentären Pb–Zn–Ag-Lagerstätte McArthur River im Northern Territory
von Australien[323]. Entlang der vertikalen Achse nimmt die Bildungstemperatur der Minerale nach unten ab. TSR steht für thermochemische Sulfatreduktion, BSR für bakterielle Sulfatreduktion.
Analog zum Verhalten der O-Isotope wird man
erwarten, daß bei magmatischen Temperaturen
nur noch eine minimale Fraktionierung bei Elementen wie Fe oder Cu auftritt. Analysen an
Mineralen aus Peridotitxenolithen und aus Pallasiten zeigen selbst für Temperaturen um 1000
°C noch geringe Unterschiede zwischen Olivin
einerseits und Pyroxenen bzw. Metallphase
andererseits um 1e pro Masseneinheit (Abbildung 198). Dieser Unterschied ist vergleichbar
demjenigen, der für die Sauerstoffisotope in
Peridotiten zwischen denselben Mineralen
gefunden wurde (ca. 0.25‰ je Masseneinheit[282] (siehe auch Seite 221), wenn man den
unterschiedlichen Verhältnissen Dm/m zwischen 18O/16O (2/16) und 57Fe/54Fe (3/54) Rechnung trägt, und der im Einklang mit theoretischen Berechnungen steht, wonach die
Fraktionierung bei 1000K um ca. eine Größenordnung unterhalb derjenigen bei Raumtemperatur liegen sollte[327].
6
Amp
Peridotite
4
«57Fe
ABBILDUNG 197
-10
1500
2
0
-2
Pallasite
Metall
Opx
Cpx
Ol
Opx
Cpx
Metall
Ol
Ol
Ol
Ol
-4
TKN31F
JL1(BC)
BD3855 Eagle Station Imilac
ABBILDUNG 198 Fe-Isotopenverhältnisse in
Mineralen aus Peridotitxenolithen aus dem
Erdmantel und aus Pallasiten (Steineisenmeteorite)[321]. Die Bildung von Amphibol
in Peridotit BD3855 wird einem metasomatischen Prozeß zugeschrieben; er mag daher mit den übrigen Mineralen nicht im
Isotopengleichgewicht stehen.
247
Eisen und andere schwere Elemente
Erhebliche Isotopenfraktionierungen lassen sich im Labor durch chromatographische Prozesse erzielen. In einem einfachen Versuch wurde eine wäßrige Cu-Chloridlösung auf eine
Anionenaustauschersäule geladen und das Eluat in kleinen Portionen analysiert (Abbil63
265
2dung 199). CuCl 4 wird dabei stärker an das Austauscherharz gebunden als CuCl 4 , so
daß das 65Cu/63Cu über den Verlauf des Auswaschens von der Säule kontinuierlich sinkt.
Die Größe der Fraktionierung hängt von der „Anzahl an theoretischen Böden“ des Harzes
ab (Art des Harzes, Vernetzungsgrad, Körnung, Länge der Säule).
Als weiterer wichtiger Parameter, der bestimmend für die Fraktionierung der Isotope
schwererer Elemente ist, wurden Redoxprozesse erkannt. In einem Laborversuch wurde
CuI aus einer wäßrigen Cu(NO 3 ) 2 -Lösung
durch Zugabe von KI ausgefällt (Abbildung
200). Das leichtere Cu-Isotop reagierte dabei
bevorzugt, so daß der e-Wert des reduzierten
Cu um ca. 40 Einheiten unter dem des Cu in
der Lösung lag. Aus der Konstanz dieser Differenz bei variablen Versuchsparametern
(Verhältnis von Cu(NO3)2 zu KI) wurde abgeleitet, daß bei dem Redoxprozeß Isotopengleichgewicht erreicht war.
15
«65Cu
«65Cu
40
% Cu
10
0
5
-40
-80
0
5
10
15
20
-0
30
25
eluiertes Volumen [ml]
40
20
«65Cu
der Cu-Isotope in einer wäßrigen Chloridlösung auf einer Anionenaustauschersäule[321].
Chromatographische Säulen werden in der
Geochemie der radiogenen Isotope zur Trennung z.B. von Rb und Sr oder Sm und Nd verwandt. Die dabei auftretende Fraktionierung
wird, zusammen mit derjenigen im Massenspektrometer, korrigiert (Kapitel 7.0 auf S. 75),
ohne daß zwischen beiden unterschieden werden kann und muß.
80
Cu eluiert (% je ml Eluat)
ABBILDUNG 199 Gleichgewichtsfraktionierung
0
Cu2+
-20
Cu+
-40
-60
0
1
2
3
4
5
Cu(NO3)2/KI (molar)
ABBILDUNG 200 Fraktionierung der Cu-IsotoBei Laborversuchen mit der Reduktion von
pe
bei 20 °C in wäßriger Lösung zwischen
stark toxischem Cr 6+ zu wenig toxischem
2+
Cu
(gelöst) und Cu + (als CuI-NiederCr3+ durch Suspensionen von Magnetit und
schlag)[321]. Die aufgetragenen e65Cu-Werte
Ästuarsedimenten (reich an Bakterien)
sind relativ zur vorgegebenen Cu-Lösung
wurde ein noch etwas größerer Effekt erzielt 65
(e Cu = 0) errechnet.
als beim Cu: Das reduzierte Cr hatte ein um
ca. 34 e-Einheiten kleineres 53Cr/52Cr als das vorgegebene Chromat, und die beobachtete
Fraktionierung war unabhängig von der Art des eingesetzten Reduktionsmittels[319]. Die
Cr-Isotopie könnte damit – obwohl analytisch aufwendig – hilfreich in der Abschätzung
des Anteils an toxischem Cr6+ in Gewässern sein.
Fe-Fraktionierungen treten auch bei der Verlagerung von Eisen in Böden auf[325]. Dabei
erweisen sich die leichteren Isotope als mobiler, indem sie sich in die Tiefe anreichern. In
einem komplexen System wie einem Boden ist es außerordentlich schwierig, die Mechanismen der Fraktionierung zu klären. Es ist jedoch wahrscheinlich, daß sowohl abiogene
(Redoxprozesse, Komplexbildung und chromatographische Effekte) als auch biogene Prozesse (bakterielle Eisenreduktion) dabei eine Rolle spielen.
An einem Bach mit durch vulkanische Einflüsse geprägtem Wasser auf der Nordinsel von
Neuseeland wurde der Einfluß der Oxidation des zunächst zweiwertigen Eisens und der
anschließenden Ausfällung als Ferrihydrit über eine Distanz von ca. 1.6 km studiert (Abbildung 201). Das ausgefällte Eisen erwies sich dabei als isotopisch deutlich schwerer als das
248
B. Stabile Isotope
Weitere theoretische und vor allem
praktische Arbeiten sind nötig, um die
Mechanismen der Fraktionierung stabiler Isotope der schwereren Elemente
unter unterschiedlichen Bedingungen
zu verstehen, so daß es möglich wird,
auch solche Isotope – wie bereits die
von H, C, O und S – als Tracer für die
Aufklärung von geochemischen Prozessen zu nutzen. Es bedarf keiner
Phantasie, um bei der bereits weiten
Verbreitung von Multikollektor-ICP–
MS-Geräten in den nächsten Jahren
mit zahlreichen Studien in dieser
Richtung zu rechnen.
«56Fe (relativ zum Standard)
Fe2+ in Lösung. Dies war von den Autoren nicht erwartet worden, weil sich die leichteren
Isotope als die reaktionsfähigeren hätten zeigen sollen. Es wird überlegt, daß die Ursache
darin zu suchen sein mag, daß die schwereren Isotope des Eisens bevorzugt in intermediäre
Komplexe von Fe2+ eintreten, die sich unmittelbar vor der Oxidation bilden. Eine Fraktionierung in derselben Richtung wurde auch in Laborexperimenten beobachtet[326]. Theoretische Berechnungen der Fe-Isotopenfraktionierung auf der Grundlage spektroskopischer
Daten zeigen, daß Fe3+-haltige Halogen- oder H2O-Komplexe tatsächlich das schwerere Isotop 56Fe gegenüber dem 54Fe im Gleichgewicht mit Fe2+-haltigen Komplexen anreichern
sollten[327],[328]. Des weiteren wird vorausgesagt, daß starke Liganden (insbesondere CN–,
aber auch H2O) die schweren Fe-Isotope konzentrieren sollten, wenn sie in Konkurrenz mit
schwachen Liganden (Cl–, Br–) stehen.
1
Fe in Ferrihydrit
Fe in Lösung
0
-10
-20
-30
1
10
% in Lösung verbleibendes Fe
100
ABBILDUNG 201 Fraktionierung der Fe-Isotope bei
Oxidation von Fe2+ und Ausfällung des Fe3+ als Ferrihydrit, 5Fe2O3´9H2O[318] in einem Bach. Gestrichelte
Linien deuten eine Rayleigh-Fraktionierung an.
249
Literaturzitate
24.0
Literaturzitate
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.
23.
24.
25.
26.
27.
28.
29.
30.
31.
32.
33.
250
P. W. Reiners (2002) (U–Th)/He chronometry experiences a renaissance. EOS Trans. AGU 83–3, 21–27
C. Seife (2003) Breakthrough of the year – illuminating the dark Universe. Science 302, 2038–2039
M. J. Rees (2002) How the cosmic dark age ended. Science 295, 51–52
W.J. Kaufmann III & N.F. Comins (1996) Discovering the Universe. W.H. Freeman & Company, New York,
436 Seiten
T. Gehren (2002) Vorlesungsskript im pdf-Format, ca. 300 Seiten, Universitäts-Sternwarte München.
http://www.usm.uni-muenchen.de/, dort über das Stichwort Lehre zu erreichen
R. v. Steiger, P. Hoppe & J. Geis (2002) Vorlesungsskript im pdf-Format, Physikalisches Institut, Universität
Bern, 109 Seiten. http://www.issi.unibe.ch/~vsteiger/nukleosynthese/
Forschungszentrum Karlsruhe, Nukleare Astrophysik (1998) Die Synthese der chemischen Elemente.
http://ik3frodo.fzk.de/synthese.html
M. Jaeger et al. (2001) 22Ne(a,n)25Mg: The key neutron source in massive stars. Physical Review Letters 87,
1–4
P. W. Merrill (1952) Spectroscopic observations of stars of class S. Astrophysical Journal 116, 21–26
E. Anders & N. Grevesse (1989) Abundances of the elements: Meteoritic and solar. Geochim. Cosmochim.
Acta 53, 197–214
D.D. Clayton (1983) Principles of Stellar Evolution and Nucleosynthesis. University of Chicago Press,
Chicago
D.D. Clayton (1997) Moving Stars and Shifting Sands of Presolar History, online-Artikel bei http://
www.psrd.hawaii.edu/July97/Stardust.html
S. Russell & C. Alexander (2000) Stardust. New Scientist 2000, 21–23
Wielen, R., Fuchs, B., & Dettbarn, C. (1996). On the birthplace of the Sun and the places of formation of
other nearby stars. Astronomy and Astrophysics, 314, 438–447.
S. D. Van Dyk (2003) Elusive supernova progenitors. Science 302, 1161–1162
G. Faure (1986) Principles of Isotope Geology, John Wiley & Sons, New York, 589 Seiten
H.-J. Dietze (1975) Massenspektroskopische Spurenanalyse, Akademische Verlagsgesellschaft Geest & Portig,
Leipzig, 224 Seiten
J. Blichert-Toft, C. Chauvel & F. Albarède (1997) Separation of Hf and Lu for high-precision isotope
analysis of rock samples by magnetic sector-multiple collector ICP-MS. Contrib. Mineral. Petrol. 127, 248–
260
W. L. Griffin et al. (2000) The Hf isotope composition of cratonic mantle: LAM-MC-ICPMS analysis of
zircon megacrysts in kimberlites. Geochim. Cosmochim. Acta 64, 133–147
D.-C. Lee & A. N. Halliday (1995) Hafnium–tungsten chronometry and the timing of terrestrial core
formation. Nature 378, 771–774
E. Jäger (1967) in: E. Jäger, E. Niggli & E. Wenk (Herausgeber) Rb–Sr-Altersbestimmungen an Glimmern der
Zentralalpen, Beitr. Geol. Karte Schweiz, NF, 134, 28 – 31
M. H. Dodson (1973) Closure temperature in cooling geochronological and petrological systems. Contrib.
Mineral. Petrol. 40, 259–274
M. Sneeringer, S.R. Hart, N. Shimizu (1984) Geochim. Cosmochim. Acta 48 (1984), 1589 – 1608
I. M. Villa (1998) Isotopic closure. Terra Nova 10, 42–47
A. Steck & J. C. Hunziker (1994) The Tertiary structural and thermal evolution of the Central Alps –
compressional and extensional structures in an orogenic belt. Tectonophysics 238, 229–254
K. Hammerschmidt & E. Frank (1991) Relics of high pressure metamorphism in the Lepontine Alps
(Switzerland) – 40Ar/39Ar and microprobe analyses on white micas. Schweiz. Mineral. Petrogr. Mitt. 71,
261–274
X. K. Zhu, R. K. O’Nions, N. S. Belshaw & A. J. Gibb (1997) Significance of in situ SIMS chronometry of
zoned monazite from the Lewisian granulites, northwest Scotland. Chem. Geol. 135, 35–53
F.S. Spear (2000) Metamorphic Phase Equilibria and Pressure – Temperature – Time Paths, Kapitel 3, Mineral.
Soc. America Monograph, Washington 1993, 25 – 72
J. G. Mitchell (1968) The argon-40/argon-39 method for potassium–argon age determination. Geochim.
Cosmochim. Acta 32, 781–790
A. R. Gillespie, J. C. Huneke & G. J. Wasserburg (1984) Eruption age of a ~100,000-year old basalt from
40
Ar/39Ar analysis of partially degassed xenoliths. J. Geophys. Res. 89, 1033–1048
D. York, C. M. Hall, Y. Yanase, J. A. Hanes & W. J. Kenyon (1981) 40Ar/39Ar dating of terrestrial minerals
with a continuous laser. Geophys. Res. Lett. 8, 1136–1138
P. W. Layer, C. M. Hall & D. York (1987) The derivation of 40Ar/39Ar age spectra of single grains of
hornblende and biotite by laser step-heating. Geophys. Res. Lett. 14, 757–760
S. P. Kelley & J.-A. Wartho (2000) Rapid kimberlite ascent and the significance of Ar–Ar ages in xenolith
phlogopites. Science 289, 609–611
Literaturzitate
34.
35.
36.
37.
38.
39.
40.
41.
42.
43.
44.
45.
46.
47.
48.
49.
50.
51.
52.
53.
54.
55.
56.
57.
58.
59.
60.
61.
62.
63.
64.
W. E. Hames & J. T. Cheney (1997) On the loss of 40Ar* from muscovite during polymetamorphism.
Geochim. Cosmochim. Acta 61, 3863–3872
C. Brooks, I. Wendt & W. Harre (1968) A two-error regression treatment and its application to Rb–Sr and
initial Sr 87 /Sr 86 ratios of younger Variscan granitic rocks from the Schwarzwald massif, southwest
Germany. J. Geophys. Res. 73, 6071–6084
D. York (1969) Least-squares fitting of a straight line with correlated errors. Earth Planet. Sci. Lett. 5, 320–
324
L. Kullerud (1991) On the calculation of isochrons. Chem. Geol. 87, 115–124
R. L. Romer (1994) Rb–Sr data structure – a possible cause for differences in Rb–Sr whole-rock and U–Pb
zircon ages. GFF 116, 93–103
I. Wendt & C. Carl (1991) The statistical distribution of the mean squared weighted deviation. Chem.
Geol. 86, 275–285
Basaltic Volcanism Study Project (1981) Basaltic Volcanism on the Terrestrial Planets, Pergamon Press, New
York, Kapitel 7.2, Seiten 935–947
K.K. Turekian (1985) Die Ozeane, Enke-Verlag, Stuttgart
W. H. Burke, R. E. Denison, E. A. Hetherington, R. B. Koepnick, N. F. Nelson & J. B. Otto (1982) Variation
of seawater 87Sr/86Sr throughout Phanerozoic time. Geology 10, 516–519
G. W. Lugmair, T. Shimamura, R. S. Lewis & E. Anders (1983) Samarium-146 in the early Solar System:
Evidence from neodymium in the Allende meteorite. Science 222, 1015–1018
G. Caro, B. Bourdon, J.-L. Birck & S. Moorbath (2003) 146Sm–142Nd evidence from Isua metamorphosed
sediments for early differentiation of the Earth’s mantle. Nature 423, 428–432
G. W. Lugmair, N. B. Scheinin & K. Marti (1975) Search for extinct 146Sm. I. The isotopic abundance of
142
Nd in the Juvinas meteorite. Earth Planet. Sci. Lett. 27, 79–84
S. B. Jacobsen & G. J. Wasserburg (1980) Sm–Nd isotopic evolution of chondrites. Earth Planet. Sci. Lett.
50, 139–155
R. W. Carlson, D. R. Hunter & F. Barker (1983) Sm-Nd age and isotopic systematics of the bimodal suite,
ancient gneiss complex, Swaziland. Nature 305, 701–704
H.-G. Stosch & G. W. Lugmair (1990) Geochemistry and evolution of MORB-type eclogites from the
Münchberg Massif, southern Germany. Earth Planet. Sci. Lett. 99, 230–249
M. B. Mørk & E. W. Mearns (1986) Sm–Nd isotopic systematics of a gabbro–eclogite transition. Lithos 19,
255–267
E. Jagoutz (1988) Nd and Sr systematics in an eclogite xenolith from Tanzania: Evidence for frozen
mineral equilibria in the continental lithosphere. Geochim. Cosmochim. Acta 52, 1285–1293
F. J. Humphries & R. A. Cliff (1982) Sm–Nd dating and cooling history of Scourian granulites, Sutherland.
Nature 295, 515–517
A. S. Cohen, R. K. O’Nions, R. Siegenthaler & W. L. Griffin (1988) Chronology of the pressure–temperature
history recorded by a granulite terrain. Contrib. Mineral. Petrol. 98, 303–311
K. Mezger, E. J. Essene & A. N. Halliday (1992) Closure temperatures of the Sm–Nd system in metamorphic
garnets. Earth Planet. Sci. Lett. 113, 397–409
N. T. Arndt & S. L. Goldstein (1987) Use and abuse of crust-formation ages. Geology 15, 893–895
D. J. DePaolo (1981) Neodymium isotopes in the Colorado Front Range and crust–mantle evolution in the
Proterozoic. Nature 291, 193–196
T. C. Liew & A. W. Hofmann (1988) Precambrian crustal components, plutonic associations, plate
environment of the Hercynian Fold Belt of central Europe: Indications from a Nd and Sr isotopic study.
Contrib. Mineral. Petrol. 98, 129–138
D. Ben Othman, M. Polvé & C. J. Allègre (1984) Nd-Sr isotopic composition of granulites and constraints
on the evolution of the lower continental crust. Nature 307, 510–515
C. J. Allègre & D. Ben Othman (1980) Nd-Sr isotopic relationship in granitoid rocks and continental crust
development: a chemical approach to orogenesis. Nature 286, 335–342
M. T. McCulloch & B. W. Chappell (1982) Nd isotopic characteristics of S- and I-type granites. Earth
Planet. Sci. Lett. 58, 51–64
D. Ben Othman, S. Fourcade & C. J. Allègre (1984) Recycling processes in granite-granodiorite complex
genesis: the Querigut case studied by Nd-Sr isotope systematics. Earth Planet. Sci. Lett. 69, 290–300
C. Brooks, S. R. Hart, A. Hofmann & D. E. James (1976) Rb–Sr mantle isochrons from oceanic regions.
Earth Planet. Sci. Lett. 32, 51–61
A. Cattell, T. E. Krogh & N. T. Arndt (1984) Conflicting Sm–Nd whole rock and U–Pb zircon ages for
Archaean lavas from Newton Township, Abitibi Belt, Ontario. Earth Planet. Sci. Lett. 70, 280–290
W. A. Russell, D. A. Papanastassiou & T. A. Tombrello (1978) Ca isotope fractionation on the Earth and
other solar system materials. Geochim. Cosmochim. Acta 42, 1075–1090
G. J. Wasserburg, S. B. Jacobsen, D. J. DePaolo, M. T. McCulloch & T. Wen (1981) Precise determination of
Sm/Nd ratios, Sm and Nd isotopic abundances in standard solutions. Geochim. Cosmochim. Acta 45,
2311–2323
251
Literaturzitate
65.
66.
67.
68.
69.
70.
71.
72.
73.
74.
75.
76.
77.
78.
79.
80.
81.
82.
83.
84.
85.
86.
87.
88.
89.
90.
91.
92.
93.
94.
252
M. H. A. Jungck, T. Shimamura & G. W. Lugmair (1984) Ca isotope variations in Allende. Geochim.
Cosmochim. Acta 48, 2651–2658
P. J. Turner et al. (1998) Instrumentation for low- and high-resolution ICPMS. In: Inductively Coupled
Plasma Mass Spectrometry, A. Montaser [Herausgeber], Wiley–VCH, New York, Seite 421–501
T. Hirata (1996) Lead isotopic analyses of NIST standard reference materials using multiple collector
inductively coupled plasma mass spectrometry coupled with a modified external correction method for
mass discrimination effect. Analyst 121, 1407–1411
M. Rehkämper et al. (2002) Thallium isotope variations in seawater and hydrogenetic, diagenetic, and
hydrothermal ferromanganese deposits. Earth Planet. Sci. Lett. 197, 65–81
W. Herr, E. Merz, P. Eberhardt & P. Signer (1958) Zur Bestimmung der Halbwertszeit des Lu-176 durch den
Nachweis von radiogenem Hf-176. Zeitschrift für Naturforschung 13a, 268–273
P. J. Patchett & M. Tatsumoto (1980) Lu–Hf total-rock isochron for the eucrite meteorites. Nature 288,
571–574
E. E. Scherer, C. Münker & K. Mezger (2001) Calibration of the lutetium–hafnium clock. Science 293, 683–
687
Y. Nir-el & N. Lavi (1998) Measurement of the half-life of 176Lu. Applied Radiation and Isotopes 49, 1653–
1655
J. Blichert-Toft, M. Boyet, P. Télouk & F. Albarède (2002) 147Sm–143Nd and 176Lu–176Hf in eucrites and the
differentiation of the HED parent body. Earth Planet. Sci. Lett. 204, 167–181
A. P. Sguigna, A. J. Larabee & J. C. Waddington (1982) The half-life of 176Lu by a g–g coincidence
measurement. Can. J. Phys. 60, 361–364
J. Blichert-Toft & F. Albarède (1997) The Lu-Hf isotope geochemistry of chondrites and the evolution of
the mantle–crust system. Earth Planet. Sci. Lett. 148, 243–258
E. E. Scherer, K. L. Cameron & J. Blichert-Toft (2000) Lu–Hf garnet geochronology: Closure temperature
relative to the Sm–Nd system and the effects of trace mineral inclusions. Geochim. Cosmochim. Acta 64,
3413–3432
T. J. Lapen et al. (2003) Burial rates during prograde metamorphism of an ultra-high-pressure terrane: an
example from Lago di Cignana, western Alps, Italy. Earth Planet. Sci. Lett. 215, 57–72
H. S. Pettingill & P. J. Patchett (1981) Lu-Hf total-rock age for the Amîtsoq gneisses, West Greenland. Earth
Planet. Sci. Lett. 55, 150–156
P. J. Patchett (1983) Importance of the Lu–Hf isotopic system in studies of planetary chronology and
chemical evolution. Geochim. Cosmochim. Acta 47, 81–91
Y. Amelin, D.-C. Lee & A. N. Halliday (2000) Early–middle Archaean crustal evolution deduced from Lu–
Hf and U–Pb isotopic studies of single zircon grains. Geochim. Cosmochim. Acta 64, 4205–4225
S. A. Wilde, J. W. Valley, W. H. Peck & C. M. Graham (2001) Evidence from detrital zircons for the
existence of continental crust and oceans on the Earth 4.4 Gyr ago. Nature 409, 175–178
S. J. Mojzsis, T. M. Harrison & R. T. Pidgeon (2001) Oxygen-isotope evidence from ancient zircons for
liquid water at the Earth’s surface 4,300 Myr ago. Nature 409, 178–181
F. Begemann et al. (2001) Call for an improved set of decay constants for geochronological use. Geochim.
Cosmochim. Acta 65, 111–121
A. E. Ringwood (1982) Phase transformations and differentiation in subducted lithosphere: implications
for mantle dynamics, basalt petrogenesis, and crustal evolution. J. Geol. 90, 611–643
P. J. Patchett, W. M. White, H. Feldmann, S. Kielinczuk & A. W. Hofmann (1984) Hafnium/rare earth
element fractionation in the sedimentary system and crustal recycling into the Earth’s mantle. Earth
Planet. Sci. Lett. 69, 365–378
T. Tanaka & A. Masuda (1982) The La–Ce geochronometer: a new dating method. Nature 300, 515–518
S. Nakai, A. Masuda & B. Lehmann (1988) Am. Mineral. 73, 1111 – 1113
A. P. Dickin, N. W. Jones, M. F. Thirlwall & R. N. Thompson (1987) A Ce/Nd study of crustal
contamination processes affecting Palaeocene magmas in Skye, NW Scotland. Contrib. Mineral. Petrol.
96, 455–464
B. D. Marshall & D. J. DePaolo (1982) Precise age determination and petrogenetic studies using the K–Ca
method. Geochim. Cosmochim. Acta 46, 2537–2545
B. Hirt, G. R. Tilton, W. Herr & W. Hoffmeister (1963) The half life of 187Re. In: Earth Science and
Meteorites, J. Geiss & E. Goldberg [Herausgeber], North Holland, Amsterdam, Seite 273–280
J.-M. Luck & C. J. Allègre (1983) 187Re–187Os systematics in meteorites and cosmochemical consequences.
Nature 302, 130–132
M. Lindner, D. A. Leich, G. P. Russ, J. M. Bazan & R. J. Borg (1989) Direct determination of the half-life of
187
Re. Geochim. Cosmochim. Acta 53, 1597–1606
R. A. Creaser, D. A. Papanastassiou & G. J. Wasserburg (1991) Negative thermal ion mass spectrometry of
osmium, rhenium, and iridium. Geochim. Cosmochim. Acta 55, 397–401
R. M. Ellam, R. W. Carlson & S. B. Shirey (1992) Evidence from Re-Os isotopes for plume-lithosphere
mixing in Karoo flood basalt genesis. Nature 359, 718–721
Literaturzitate
95.
96.
97.
98.
99.
100.
101.
102.
103.
104.
105.
106.
107.
108.
109.
110.
111.
112.
113.
114.
115.
116.
117.
118.
119.
120.
121.
122.
123.
124.
R. J. Walker, J. W. Morgan, E. S. Beary, M. I. Smoliar, G. K. Czamanske & M. F. Horan (1997) Applications
of the 190Pt–186Os isotope system to geochemistry and cosmochemistry. Geochim. Cosmochim. Acta 61,
4799–4807
R. J. Walker, J. W. Morgan, A. J. Naldrett & C. Li (1991) Re–Os isotopic systematics of Ni–Cu sulfide ores,
Sudbury Igneous Complex, Ontario: evidence for a major crustal component. Earth Planet. Sci. Lett. 105,
416–429
K.G. Heumann (1988) In: Inorganic Mass Spectrometry [Herausgeber F. Adams et al.], John Wiley & Sons, S.
301 – 376
R. J. Walker & J. D. Fassett (1986) Isotopic measurement of sub-nanogram quantities of rhenium and
osmium by resonance ionization mass spectrometry. Anal. Chem. 58, 2923–2927
U. Fehn, R. Teng, D. Elmore & P. W. Kubik (1986) Isotopic composition of osmium in terrestrial samples
determined by accelerator mass spectrometry. Nature 323, 707–710
E. H. Hauri & S. R. Hart (1997) Rhenium abundances and systematics in oceanic basalts. Chem. Geol. 139,
185–205
R. J. Walker, R. W. Carlson, S. B. Shirey & F. R. Boyd (1989) Os, Sr, Nd, and Pb isotope systematics of
southern African peridotite xenoliths: Implications for the chemical evolution of subcontinental mantle.
Geochim. Cosmochim. Acta 53, 1583–1595
R. J. Walker, L. M. Echeverría, S. B. Shirey & M. F. Horan (1991) Re–Os isotopic constraints on the origin
of volcanic rocks, Gorgona Island, Colombia: Os isotopic evidence for ancient heterogeneities in the
mantle. Contrib. Mineral. Petrol. 107, 150–162
M. Roy-Barman & C.J. Allègre (1995) Earth Planet. Sci. Lett. 129, 145 – 161
L. Reisberg, C. France-Lanord & A.-C. Pierson-Wickmann (1997) Os isotopic compositions of leachates
and bulk sediments from the Bengal Fan. Earth Planet. Sci. Lett. 150, 117–127
J.-M. Luck, J.-L. Birck & C.-J. Allègre (1980) 187Re–187Os systematics in meteorites: early chronology of the
Solar System and age of the Galaxy. Nature 283, 256–259
J.-M. Luck & C. J. Allègre (1982) The study of molybdenites through the 187Re–187Os chronometer. Earth
Planet. Sci. Lett. 61, 291–296
R. J. Walker & J. W. Morgan (1989) Rhenium–osmium isotope systematics of carbonaceous chondrites.
Science 243, 519–522
L. Reisberg & J.-P. Lorand (1995) Longevity of sub-continental mantle lithosphere from osmium isotope
systematics in orogenic peridotite massifs. Nature 376, 159–162
A. H. Peslier, L. Reisberg, J. Ludden & D. Francis (2000) Os isotopic systematics in mantle xenoliths; age
constraints on the Canadian Cordillera lithosphere. Chem. Geol. 166, 85–101
T. Meisel, R. J. Walker & J. W. Morgan (1996) The osmium isotopic composition of the Earth’s primitive
upper mantle. Nature 383, 517–520
J. E. Snow & G. Schmidt (1998) Constraints on Earth accretion deduced from noble metals in the oceanic
mantle. Nature 391, 166–169
G. Schmidt & J. Snow (2002) Os isotopes in mantle xenoliths from the Eifel volcanic field and the
Vogelsberg (Germany): age constraints on the lithospheric mantle. Contrib. Mineral. Petrol. 143, 694–705
R. J. Walker, J. W. Morgan & M. F. Horan (1995) Osmium-187 enrichment in some plumes: evidence for
core–mantle interaction? Science 269, 819–822
J. M. Luck & K. K. Turekian (1983) Osmium-187/Osmium-186 in manganese nodules and the CretaceousTertiary boundary. Science 222, 613–615
A. Shukolyukov & G. W. Lugmair (1998) Isotopic evidence for the Cretaceous–Tertiary impactor and its
type. Science 282, 927–929
F. T. Kyte, A. Shukolyukov, G. W. Lugmair, D. R. Lowe & G. R. Byerly (2003) Early Archean spherule beds:
Chromium isotopes confirm origin through multiple impacts of projectiles of carbonaceous chondrite
type. Geology 31, 283–286
B. Peucker-Ehrenbrink, G. Ravizza & A. W. Hofmann (1995) The marine 187Os/186Os record of the past 80
million years. Earth Planet. Sci. Lett. 130, 155–167
K.H. Wedepohl [Herausgeber] (1969–1978) Handbook of Geochemistry, Vol. II/5
G. W. Wetherill (1956) Discordant uranium–lead ages. EOS Trans. AGU 37, 320–326
B. Kober (1986) Whole-grain evaporation for 207Pb/206Pb-age-investigations on single zircons using a
double-filament thermal ion source. Contrib. Mineral. Petrol. 93, 482–490
A. Lanzirotti & G. N. Hanson (1995) U–Pb dating of major and accessory minerals formed during
metamorphism and deformation of metapelites. Geochim. Cosmochim. Acta 59, 2513–2526
G. Vavra, D. Gebauer, R. Schmidt & W. Compston (1996) Multiple zircon growth and recrystallization
during polyphase Late Carboniferous to Triassic metamorphism in granulites of the Ivrea Zone (Southern
Alps): an ion microprobe (SHRIMP) study. Contrib. Mineral. Petrol. 122, 337–358
K. Högdahl, P. L. Gromet & C. Broman (2001) Low P–T Caledonian resetting of U-rich Paleoproterozoic
zircons, central Sweden. Am. Mineral. 86, 534–546
P.J. Potts (1992) A Handbook of Silicate Rock Analysis. Blackie, Glasgow, S. 383 – 391
253
Literaturzitate
125.
126.
127.
128.
129.
130.
131.
132.
133.
134.
135.
136.
137.
138.
139.
140.
141.
142.
143.
144.
145.
146.
147.
148.
149.
150.
151.
152.
153.
254
W. Compston, I. S. Williams & C. Meyer (1984) U–Pb geochronology of zircons from lunar breccia 73217
using a sensitive high mass-resolution ion microprobe. Proc. 14th Lunar and Planet. Sci. Conf. [J.
Geophys. Res. 89], B525–B534
D. Günther, S. E. Jackson & H. P. Longerich (1999) Laser ablation and arc/spark solid sample introduction
into inductively coupled plasma mass spectrometers. Spectrochim. Acta 54B, 381–409
K. Suzuki, M. Adachi & T. Tanaka (1991) Middle Precambrian provenance of Jurassic sandstone in the
Mino Terrane, central Japan: Th–U–total Pb evidence from an electron microprobe. Sediment. Geol. 75,
141–147
J. M. Montel, S. Foret, M. Veschambre, C. Nicollet & A. Provost (1996) A fast, reliable, inexpensive in-situ
dating technique: electron microprobe ages on monazite. Chem. Geol. 131, 37–53
A. Cocherie, O. Legendre, J. J. Peucat & A. N. Kouamelan (1998) Geochronology of polygenetic monazites
constrained by in situ microprobe Th–U-total lead determination: implications for lead behaviour in
monazite. Geochim. Cosmochim. Acta 62, 2475–2497
F. Finger, E. Krenn, G. Riegler, S. Romano & G. Zulauf (2002) Resolving Cambrian, Carboniferous, Permian
and Alpine monazite generations in the polymetamorphic basement of eastern Crete (Greece) by means
of the electron microprobe. Terra Nova 14, 233–240
A. O. Nier (1938) Variations in the relative abundances of the isotopes of common lead from various
sources. J. Amer. Chem. Soc. 60, 1571–1576
A. O. Nier, R. W. Thompson & B. F. Murphey (1941) The isotopic constitution of lead and the
measurement of geological time. III. Phys. Rev. 60, 112–117
A. Holmes (1946) An estimate of the age of the Earth. Nature 157, 680–684
F. G. Houtermans (1946) Die Isotopen-Häufigkeiten im natürlichen Blei und das Alter des Urans.
Naturwissenschaften 33, 185–187
M. Tatsumoto, R. J. Knight & C. J. Allègre (1973) Time differences in the formation of meteorites as
determined from the ratio of lead-207 to lead-206. Science 180, 1279–1283
J. H. Chen & G. J. Wasserburg (1983) The least radiogenic Pb in iron meteorites. Lunar and Planetary
Science Conference, Abstracts 14, 103–104
C. Patterson (1956) Age of meteorites and the Earth. Geochim. Cosmochim. Acta 10, 230–237
S.-s. Sun & W.F. McDonough (1989) In: A.D. Saunders & M.J. Norry [Herausgeber] Magmatism in the Ocean
Basins, Geol. Soc. London Special Publ. 42, 313 – 345
A. W. Hofmann (1997) Mantle geochemistry: the message from oceanic volcanism. Nature 385, 219–229
W.M. White (1998) Geol.656: Isotope Geochemistry, Vorlesungsskript Cornell University, ca. 270 Seiten;
zur Zeit der Überarbeitung meines Skriptes war das Skript von Herrn White auch online erhältlich in einer
Serie von mehreren Dutzend pdf-Dateien unter http://www.geo.cornell.edu/geology/classes/Geo656/
656notes00.html; – sehr empfehlenswert! Außerdem und z.T. überarbeitet: Geology 455 Geochemistry,
ca. 700 Seiten, http://www.geo.cornell.edu/geology/classes/geo455/Chapters.HTML
R. L. Rudnick & S. L. Goldstein (1990) The Pb composition of lower crustal xenoliths and the evolution of
lower crustal Pb. Earth Planet. Sci. Lett. 98, 192–207
H. Downes, P. D. Kempton, D. Briot, R. S. Harmon & A. F. Leyreloup (1991) Pb and O isotope systematics
in granulite facies xenoliths, French Massif Central: implications for crustal processes. Earth Planet. Sci.
Lett. 102, 342–357
P. D. Kempton, R. S. Harmon, C. J. Hawkesworth & S. Moorbath (1990) Petrology and geochemistry of
lower crustal granulites from the Geronimo volcanic field, southeastern Arizona. Geochim. Cosmochim.
Acta 54, 3401–3426
R. S. Cohen, R. K. O’Nions & J. B. Dawson (1984) Isotope geochemistry of xenoliths from East Africa:
implications for development of mantle reservoirs and their interaction. Earth Planet. Sci. Lett. 68, 209–
220
G. Loock (1992) Character and distribution of the Indian Ocean mantle domain: A study of the mantle
source compositions of Lau Basin volcanics (SW Pacific) and Indian Ocean mid-ocean ridge basalts.
Dissertation Köln und Mainz, 125 Seiten
S. R. Hart (1984) A large-scale isotope anomaly in the Southern Hemisphere mantle. Nature 309, 753–757
W. M. White & B. Dupré (1986) Sediment subduction and magma genesis in the Lesser Antilles: isotopic
and trace element constraints. J. Geophys. Res. 91, 5927–5941
A. Zindler & S. R. Hart (1986) Chemical Geodynamics. Ann. Rev. Earth Planet. Sci. 14, 493–571
S. R. Hart, E. H. Hauri, L. A. Oschmann & J. A. Whitehead (1992) Mantle plumes and entrainment:
isotopic evidence. Science 256, 517–520
S. E. Church & M. Tatsumoto (1975) Lead isotope relations in oceanic ridge basalts from the Juan de Fuca–
Gorda ridge area, N.E. Pacific Ocean. Contrib. Mineral. Petrol. 53, 253–279
E. C. H. Silk & R. S. Barnes (1959) Examination of fission fragment tracks with an electron microscope.
Phil. Mag. 4, 970–972
P. B. Price & R. M. Walker (1962) Chemical etching of charged particle tracks in solids. J. Appl. Phys. 33,
3407–3412
P. B. Price & R. M. Walker (1962) Observation of fossil particle tracks in natural micas. Nature 196, 732–
734
Literaturzitate
154.
155.
156.
157.
158.
159.
160.
161.
162.
163.
164.
165.
166.
167.
168.
169.
170.
171.
172.
173.
174.
175.
176.
177.
178.
179.
180.
181.
182.
183.
184.
185.
P. B. Price & R. M. Walker (1963) Fossil tracks of charged particles in mica and the age of minerals. J.
Geophys. Res. 68, 4847–4862
G.A. Wagner & P. van den Haute (1992) Fission-Track Dating. Enke, Stuttgart, 285 Seiten.
A. J. Hurford & P. F. Green (1982) A users’ guide to fission-track dating calibration. Earth Planet. Sci. Lett.
59, 343–354
A. J. Hurford & P. F. Green (1983) The z age calibration for fission track dating. Isotope Geoscience 1, 285–
317
J. Carpéna (1992) Fission track dating of zircon: zircons from Mont Blanc granite (French Italian Alps).
J. Geol. 100, 411–421
J. P. Schaer, G. M. Reimer & G. A. Wagner (1975) Actual and ancient uplift rate in the Gotthard region,
Swiss Alps: A comparison between precise leveling and fission-track apatite age. Tectonophysics 29, 293
P. K. Zeitler, N. M. Johnson, C. W. Naeser & R. A. K. Tahirkheli (1982) Fission-track evidence for
Quaternary uplift of the Nanga Parbat region, Pakistan. Nature 298, 255
R. L. Edwards, J. H. Chen & G. J. Wasserburg (1987) 238U–234U–232Th systematics and the precise
measurement of time over the past 500,000 years. Earth Planet. Sci. Lett. 81, 175–192
z.B.: K. R. Ludwig, B. J. Szabo & K. R. Simmons (1991) Crustal subsidence rate off Hawaii determined from
234
U/238U ages of drowned coral reefs. Geology 19, 171–174
K. H. Rubin (2001) Analysis of 232Th/230Th in volcanic rocks: a comparison of thermal ionization mass
spectrometry and other methodologies. Chem. Geol. 175, 723–750
G. J. Hennig (1979) Beiträge zur Th-234/U-234-Altersbestimmung von Höhlensintern sowie ein Vergleich
der erzielten Ergebnisse mit denen anderer Absolutdatierungsmethoden. Dissertation Universität zu Köln,
201 Seiten
Piggott, C. S., & Urry, W. D. (1941). Radioactivity of ocean sediments. American Journal of Science 239,
81–91
N. Isaac & E. Picciotto (1953) Ionium determinations in deep-sea sediments. Nature 171, 742–744
N. Rosholt & Szabo B.J. (1969) Modern Trends in Activation Analysis, Vol. I, J.R. Devoe [Herausgeber], Natl.
Bureau of Standards, Washington, 327
E. D. Goldberg (1963) Geochronology with Pb-210. In: Radioactive Dating, I. A. E. Agency [Herausgeber],
International Atomic Energy Agency, Wien, Seite 121–131
S. Krishnaswami, D. Lal, J. M. Martin & M. Meybeck (1971) Geochronology of lake sediments. Earth
Planet. Sci. Lett. 11, 407–414
H. Shirahata, R.W. Elias, C.C. Patterson & M. Koide (1980) Geochim. Cosmochim. Acta 44, 149 – 162
G. Crozaz, E. Picciotto & W. DeBreuck (1964) Antarctic snow chronology with Pb210. J. Geophys. Res. 69,
2597–2604
S. Newman (1983) 230Th – 238U disequilibrium systematics in young volcanic rocks. Ph.D. thesis Univ. of
California, San Diego, XVII + 283 Seiten
T.-L. Ku (1965) An evaluation of the 234U/238U method as a tool for dating pelagic sediments. J. Geophys.
Res. 70, 3457–3474
E. D. Goldberg & M. Koide (1962) Geochronological studies of deep sea sediments by the ionium/thorium
method. Geochim. Cosmochim. Acta 26, 417–450
E. Piciotto & W. Wilgain (1954) Thorium determination in deep-sea sediments. Nature 173, 632–633
P. I. Chalov & K. I. Merkulova (1966) Comparative rate of oxidation of U-234 and U-238 atoms in certain
minerals. Dokl. Akad. Nauk SSSR 167, 146 [in Russisch]
K. Kigoshi (1971) Alpha-recoil thorium-234: Dissolution into water and the uranium-234/uranium-238
disequilibrium in nature. Science 173, 47–48
R. L. Fleischer & O. G. Raabe (1978) Recoiling a-emitting nuclei. Mechanism for uranium-series
disequilibrium. Geochim. Cosmochim. Acta 42, 973–978
H. H. Veeh (1966) Th230/U238 and U234/U238 ages of Pleistocene high sea level stand. J. Geophys. Res. 71,
3379–3386
A. Kaufman, W. S. Broecker, T.-L. Ku & D. L. Thurber (1971) The status of U-series methods of mollusk
dating. Geochim. Cosmochim. Acta 35, 1155–1183
W. S. Broecker, D. L. Thurber, J. Goddard, T.-L. Ku, R. K. Mathews & K. J. Mesolella (1968) Milankovitch
hypothesis supported by precise dating of coral reefs and deep-sea sediment. Science 159, 297–300
R. L. Edwards, F. W. Taylor & G. J. Wasserburg (1988) Dating earthquakes with high-precision thorium-230
ages of very young corals. Earth Planet. Sci. Lett. 90, 371–381
C. Spötl & A. Mangini (2002) Stalagmite from the Austrian Alps reveals Dansgaard–Oeschger events
during isotope stage 3: Implications for the absolute chronology of Greenland ice cores. Earth Planet. Sci.
Lett. 203, 507–518
B. L. K. Somayalulu, M. Tatsumoto, J. N. Rosholt & R. J. Knight (1966) Disequilibrium of 238-U series in
basalt. Earth Planet. Sci. Lett. 1, 387–391
V. M. Oversby & P. W. Gast (1968) Lead isotope compositions and uranium decay series disequilibrium in
Recent volcanic rocks. Earth Planet. Sci. Lett. 5, 199–206
255
Literaturzitate
186.
187.
188.
189.
190.
191.
192.
193.
194.
195.
196.
197.
198.
199.
200.
201.
202.
203.
204.
205.
206.
207.
208.
209.
210.
211.
212.
213.
214.
215.
216.
217.
218.
219.
256
S. Krishnaswami, K. K. Turekian & J. T. Bennett (1984) The behavior of 232Th and the 238U decay chain
nuclides during magma formation and volcanism. Geochim. Cosmochim. Acta 48, 505–511
C. J. Allègre (1968) 230Th dating of volcanic rocks: A comment. Earth Planet. Sci. Lett. 5, 209–210
C. J. Allègre & M. Condomines (1976) Fine chronology of volcanic processes using 238U–232Th systematics.
Earth Planet. Sci. Lett. 28, 395–406
S. Newman, R. C. Finkel & J. D. Macdougall (1983) 230Th–238U disequilibrium systematics in oceanic
tholeiites from 21°N on the East Pacific Rise. Earth Planet. Sci. Lett. 65, 17–33
D. Landwehr, J. Blundy, E. M. Chamorro-Perez, E. Hill & B. Wood (2001) U-series disequilibria generated
by partial melting of spinel lherzolite. Earth Planet. Sci. Lett. 188, 329–348
B. Bourdon, A. Zindler, T. Elliott & C. H. Langmuir (1996) Constraints on mantle melting at mid-ocean
ridges from global 238U–230Th disequilibrium data. Nature 384, 231–235
P. Englert (1979) Die Bestimmung von Bestrahlungs- und sogenannten terrestrischen Altern von
Steinmeteoriten auf der Grundlage der kosmogen entstandenen Radionuklide 53Mn und 26Al. Dissertation
Universität zu Köln, 182 Seiten
W.F. Libby (1969) Altersbestimmung mit der C14-Methode. BI-Hochschultaschenbuch 403/403a* (Dies ist
die deutsche Übersetzung von Radiocarbon Dating, University of Chicago Press 1955)
H. E. Suess (1954) Natural radiocarbon measurements by acetylene counting. Science 120, 1–3
C. J. Bennett et al. (1977) Radiocarbon dating using electrostatic accelerators: Negative ions provide the
key. Science 198, 508–510
J. R. Arnold & W. F. Libby (1949) Age determinations by radiocarbon content: Checks with samples of
known age. Science 110, 678–680
E. C. Anderson & W. F. Libby (1951) World-wide distribution of natural radiocarbon. Phys. Rev. 81, 64–69
H. E. Suess (1955) Radiocarbon concentration in modern wood. Science 122, 415–417
H. deVries (1958) Variation in concentration of radiocarbon with time and location on Earth. Proc.
Koninkl. Ned. Akad. Wetenschap. B61, 94–102
J.-L. Reyss, Y. Yokoyama & G. Guichard (1981) Production cross sections of 26Al, 22Na, 7Be from argon and
10
Be, 7Be from nitrogen: Implications for production rates of 26Al and 10Be in the atmosphere. Earth
Planet. Sci. Lett. 53, 203–210
F. Tera, L. Brown, J. Morris, I. S. Sacks, J. Klein & R. Middleton (1986) Sediment incorporation in islandarc magmas: inferences from 10Be. Geochim. Cosmochim. Acta 50, 535–550
G. M. Raisbeck et al. (1980) 10Be concentrations and residence time in the deep ocean. Earth Planet. Sci.
Lett. 51, 275–278
B. Peters (1955) Radioactive beryllium in the atmosphere and on the earth. Proc. Indian Acad. Sci. XLI,
67–71
J. R. Arnold (1956) Beryllium-10 produced by cosmic rays. Science 124, 584–585
P. S. Goel, D. P. Kharkar, D. Lal, N. Narasappaya, B. Peters & V. Yatirajam (1957) Beryllium-10
concentrations in deep sea sediment. Deep-Sea Res. 4, 202–210
F. Guichard, J.-L. Reyss & Y. Yokoyama (1978) Growth rate of a manganese nodule measured with 10Be and
26
Al. Nature 272, 155–156
A. E. Litherland (1980) Ultra-sensitive mass spectrometry with accelerators. Ann. Rev. Nucl. Part. Sci. 30,
437–473
L. Brown, I. S. Sacks, F. Tera, J. Klein & R. Middleton (1981) Beryllium-10 in continental sediments. Earth
Planet. Sci. Lett. 55, 370–376
B. Bourdon, S. J. Goldstein, D. Bourlès, M. T. Murrell & C. H. Langmuir (2000) Evidence from 10Be and U
series disequilibria on the possible contamination of mid-ocean ridge basalt glasses by sedimentary
material. G3 Geochemistry Geophysics Geosystems 1, Paper number 2000GC000047
M. C. Monaghan, J. Klein & C. I. Measures (1988) The origin of 10Be in island-arc volcanic rocks. Earth
Planet. Sci. Lett. 89, 288–298
R. W. Kay (1980) Volcanic arc magmas: Implications of a melting–mixing model for element recycling in
the crust–upper mantle system. J. Geol. 88, 497–522
J. G. Ryan & C. H. Langmuir (1988) Beryllium systematics in young volcanic rocks: Implications for 10Be.
Geochim. Cosmochim. Acta 52, 237–244
L. R. McHargue & P. E. Damon (1991) The global beryllium 10 cycle. Rev. Geophys. 29, 141–158
M.R. Ghelman (1988) Kernchemie / Mineralogie Köln, Diplomarbeit, 92 Seiten
S. Vogt (1988) Institut für Kernchemie, Universität zu Köln, Dissertation, 150 Seiten
S. Theis (1986) Institut für Kernchemie, Universität zu Köln, Dissertation, 135 Seiten
D. Elmore & F. M. Phillips (1987) Accelerator mass spectrometry for measurement of long-lived
radioisotopes. Science 236, 543–550
B. G. Polyak & I. N. Tolstikhin (1985) Isotopic composition of the Earth’s helium and the problem of the
motive forces of tectogenesis. Chem. Geol. (Isotope Geoscience Section) 52, 9–33
F. Albarède (1998) Time-dependent models of U–Th–He and K–Ar evolution and the layering of mantle
convection. Chem. Geol. 145, 413–419
Literaturzitate
220.
221.
222.
223.
224.
225.
226.
227.
228.
229.
230.
231.
232.
233.
234.
235.
236.
237.
238.
239.
240.
241.
242.
243.
244.
245.
246.
247.
248.
249.
250.
251.
252.
J. E. Lupton (1983) Terrestrial inert gases: isotope tracer studies and clues to primordial components in the
mantle. Annu. Rev. Earth Planet. Sci. 11, 371–414
E. T. Dixon (2003) Interpretation of helium and neon isotopic heterogeneity in Icelandic basalts. Earth
Planet. Sci. Lett. 206, 83–99
H. Craig & J. E. Lupton (1976) Primordial neon, helium, and hydrogen in oceanic basalts. Earth Planet.
Sci. Lett. 31, 369–385
J. H. Natland (2003) Capture of helium and other volatiles during the growth of olivine phenocrysts in
picritic basalts from the Juan Pernandez Islands. J. Petrol. 44, 421–456
A. Meibom et al. (2003) Are high 3He/4He ratios in oceanic basalts an indicator of deep-mantle plume
components? Earth Planet. Sci. Lett. 208, 197–204
T. Kirsten, H. Richter & D. Storzer (1982) 5th Internatl. Conf. Geochron. Cosmochron. Isotope Geol.,
Nikko/Japan, 183 – 184 [abstract]
M. C. van Soest, D. R. Hilton, C. G. MacPherson & D. P. Mattey (2002) Resolving sediment subduction and
crustal contamination in the Lesser Antilles Island Arc: a combined He–O–Sr isotope approach. J. Petrol.
43, 143–170
R. Hart, L. Hogan & J. Dymond (1985) The closed-system approximation for evolution of argon and
helium in the mantle, crust and atmosphere. Chem. Geol. (Isotope Geoscience Section) 52, 45–73
E. R. Oxburgh & R. K. O’Nions (1987) Helium loss, tectonics, and the terrestrial heat budget. Science 237,
1583–1588
R. K. O’Nions & E. R. Oxburgh (1983) Heat and helium in the Earth. Nature 306, 429–431
F. A. Podosek (1970) Dating of meteorites by the high-temperature release of iodine-correlated Xe129.
Geochim. Cosmochim. Acta 34, 341–365
T. Staudacher & C. J. Allègre (1982) Terrestrial xenology. Earth Planet. Sci. Lett. 60, 389–406
C. J. Allègre, T. Staudacher & P. Sarda (1986–87) Rare gas systematics: Formation of the atmosphere,
evolution and structure of the Earth’s mantle. Earth Planet. Sci. Lett. 81, 127–150
G. W. Lugmair & A. Shukolyukov (1998) Early solar system timescales according to 53Mn–53Cr systematics.
Geochim. Cosmochim. Acta 62, 2863–2886
B. Schwarzschild (2001) X-ray observations of young stars address a puzzle of the solar system’s origin.
Physics Today 54, 19–21
C. M. O. D. Alexander, A. P. Boss & R. W. Carlson (2001) The early evolution of the inner solar system: A
meteoritic perspective. Science 293, 64–68
K. D. McKeegan, M. Chaussidon & F. Robert (2000) Incorporation of short-lived 10Be in a calcium–
aluminum-rich inclusion from the Allende meteorite. Science 289, 1334–1337
E. Zinner (2003) An isotopic view of the early solar system. Science 300, 265–267
D.-C. Lee & A. N. Halliday (1996) Hf–W isotopic evidence for rapid accretion and differentiation in the
early solar system. Science 274, 1876–1879
D.-C. Lee & A. N. Halliday (1997) Core formation on Mars and differentiated asteroids. Nature 388, 854–
857
T. Kleine, C. Münker, K. Mezger & H. Palme (2002) Rapid accretion and early core formation on asteroids
and the terrestrial planets from Hf–W chronometry. Nature 418, 952–955
R. Schoenberg, B. S. Kamber, K. D. Collerson & S. Moorbath (2002) Tungsten isotope evidence from ~3.8Gyr metamorphosed sediments for early meteorite bombardment of the Earth. Nature 418, 403–405
Q. Yin, S. B. Jacobsen, K. Yamashita, J. Blichert-Toft, P. Télouk & F. Albarède (2002) A short timescale for
terrestrial planet formation from Hf–W chronometry of meteorites. Nature 418, 949–952949–952
D.-C. Lee & A. N. Halliday (1995) Hafnium–tungsten chronometry and the timing of terrestrial core
formation. Nature 378, 771–774
C. Göpel, G. Manhès & C. J. Allègre (1994) U–Pb systematics of phosphates from equilibrated ordinary
chondrites. Earth Planet. Sci. Lett. 121, 153–171
C. J. Allègre, G. Manhès & C. Göpel (1995) The age of the Earth. Geochim. Cosmochim. Acta 59, 1445–
1456
A. G. W. Cameron (2002) Birth of a solar system. Nature 418, 924–925
G. Quitté, J.-L. Birck & C. J. Allègre (2000) 182Hf/180W systematics in eucrites: the puzzle of iron
segregation in the early solar system. Earth Planet. Sci. Lett. 184, 83–94
G. W. Lugmair & A. Shukolyukov (1998) Early solar system timescales according to 53Mn–53Cr systematics.
Geochim. Cosmochim. Acta 62, 2863–2886
A. Shukolyukov & G. W. Lugmair (1993) 60Fe in eucrites. Earth Planet. Sci. Lett. 119, 159–166
R. H. James & M. R. Palmer (2000) The lithium isotope composition of international rock standards.
Chem. Geol. 166, 319–326
H.-M. Seitz & A. B. Woodland (2000) The distribution of lithium in peridotitic and pyroxenitic mantle
lithologies — an indicator of magmatic and metasomatic processes. Chem. Geol. 166, 47–64
H. R. Krouse & H. C. Thode (1962) Thermodynamic properties and geochemistry of isotopic compounds
of selenium. Can. J. Chem. 40, 367–375
257
Literaturzitate
253.
254.
255.
256.
257.
258.
259.
260.
261.
262.
263.
264.
265.
266.
267.
268.
269.
270.
271.
272.
273.
274.
275.
276.
277.
278.
279.
280.
281.
282.
258
M. J. Herbel, T. M. Johnson, R. S. Oremland & T. D. Bullen (2000) Fractionation of selenium isotopes
during bacterial respiratory reduction of selenium oxyanions. Geochim. Cosmochim. Acta 64, 3701–3709
B. L. Beard & C. M. Johnson (1999) High precision iron isotope measurements of terrestrial and lunar
materials. Geochim. Cosmochim. Acta 63, 1653–1660
X. K. Zhu, R. K. O’Nions, Y. L. Guo & B. C. Reynolds (2000) Secular variation of iron isotopes in North
Atlantic deep water. Science 287, 2000–2002
X. K. Zhu, R. K. O’Nions, Y. Guo, N. S. Belshaw & D. Rickard (2000) Determination of natural Cu-isotope
variation by plasma-source mass spectrometry: implications for use as geochemical tracers. Chem. Geol.
163, 139–149
C. N. Maréchal, E. Nicholas, C. Douchet & F. Albarède (2000) Abundance of zinc isotopes as a marine
biogeochemical tracer. G3 [Geochemistry Geophysics Geosystems] 1, Paper number 1999GC000029, 17
Seiten
J. Barling, G. L. Arnold & A. D. Anbar (2001) Natural mass-dependent variations in the isotopic
composition of molybdenum. Earth Planet. Sci. Lett. 193, 447–457
J. McManus, T. F. Nägler, C. Siebert, C. G. Wheat & D. E. Hammond (2002) Oceanic molybdenum isotope
fractionation: Diagenesis and hydrothermal ridge-flank alteration. G3 Geochemistry Geophysics
Geosystems 3, 9 Seiten, doi:10.1029/2002GC000356
C. Siebert, T. F. Nägler, F. von Blanckenburg & J. D. Kramers (2003) Molybdenum isotope records as a
potential new proxy for paleoceanography. Earth and Planetary Science Letters 211, 159–171
A. Galy, M. Bar-Matthews, L. Halicz & R. K. O’Nions (2002) Mg isotopic composition of carbonate: insight
from speleothem formation. Earth Planet. Sci. Lett. 201, 105–115
H. Bao et al. (2000) Anomalous 17O compositions in massive sulphate deposits on the Earth. Nature 406,
176–178
J. R. O’Neil (1986) Theoretical and experimental aspects of isotopic fractionation. In: Stable Isotopes in
High Temperature Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J. R.
O’Neil [Herausgeber], Mineralogical Society of America, Washington, Seite 1–40
T. Driesner (1997) The effect of pressure on deuterium–hydrogen fractionation in high-temperature water.
Science 277, 791–794
Y. Bottinga & M. Javoy (1973) Comments on oxygen isotope geothermometry. Earth Planet. Sci. Lett. 20,
251–265
J. Hoefs (1996) Stable Isotope Geochemistry. Springer-Verlag Berlin, 2. Auflage, 241 Seiten
W. Müller, H. Fricke, A. N. Halliday, M. T. McCulloch & J.-A. Wartho (2003) Origin and migration of the
Alpine Iceman. Science 302, 862–866
T. E. McCandless & J. J. Gurney (1997) Diamond eclogites: Comparison with carbonaceous chondrites,
carbonaceous shales, and microbial carbon-enriched MORB. Russ. Geol. Geophys. 38, 394–404
J. R. O’Neil (1986) Appendix: Terminology and Standards. In: Stable Isotopes in High Temperature
Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J. R. O’Neil
[Herausgeber], Mineralogical Society of America, Washington, Seite 561–570
Coplen (1994) Pure and Applied Chemistry 66, 273 – 276
H. Craig & L.I. Gordon (1965) In: Stable Isotopes in Oceanographic studies and Paleotemperatures, Consiglio
Nazionale delle Ricerche, Laboratorio di Geologia Nucleare, Pisa, p. 1 – 22
S. Neshyba (1987) Oceanography – Perspectives on a Fluid Earth, John Wiley & Sons, New York, 506 Seiten
H. C. Urey (1947) The thermodynamic properties of isotopic substances. J. Chem. Soc. 1947, 562–581
Y. Horibe & T. Oba (1972) Temperature scales of aragonite–water and calcite–water systems [japanisch].
Fossils 23/24, 69–79
C. Emiliani (1978) The cause of the ice ages. Earth Planet. Sci. Lett. 37, 349–352
R. T. Gregory & R. E. Criss (1986) Isotopic exchange in open and closed systems. In: Stable Isotopes in
High Temperature Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J. R.
O’Neil [Herausgeber], Mineralogical Society of America, Washington, Seite 91–127
R. T. Gregory & H. P. Taylor Jr. (1986) Non-equilibrium, metasomatic 18O/16O effects in upper mantle
mineral assemblages. Contrib. Mineral. Petrol. 93, 124–135
D. E. Vogel & G. D. Garlick (1970) Oxygen-isotope ratios in metamorphic eclogites. Contrib. Mineral.
Petrol. 28, 183–191183–191
J. Desmons & J. R. O’Neil (1978) Oxygen and hydrogen isotope compositions of eclogites and associated
rocks from the eastern Sesia Zone (Western Alps, Italy). Contrib. Mineral. Petrol. 67, 79–85
H. P. Taylor Jr. & S. M. F. Sheppard (1986) Igneous rocks: I. Processes of isotopic fractionation and isotope
systematics. In: Stable Isotopes in High Temperature Geological Processes, Reviews in Mineralogy Vol. 16,
J. W. Valley, H. P. Taylor Jr. & J. R. O’Neil [Herausgeber], Mineralogical Society of America, Washington,
Seite 227–271
S.R. Taylor (1992) Solar System Evolution, Cambridge University Press, Cambridge, 307 Seiten
D. Mattey, D. Lowry & C. Macpherson (1994) Oxygen isotope composition of mantle peridotite. Earth
Planet. Sci. Lett. 128, 231–241
Literaturzitate
283.
284.
285.
286.
287.
288.
289.
290.
291.
292.
293.
294.
295.
296.
297.
298.
299.
300.
301.
302.
303.
304.
305.
306.
307.
308.
309.
310.
J. Yang & S. Epstein (1983) Interstellar organic matter in meteorites. Geochim. Cosmochim. Acta 47,
2199–2216
L.R. Wager & W.A. Deer (1939) Geological investigations in East Greenland, Part 3. The petrology of the
Skaergaard intrusion, Kangerdlugssuaq region. Meddr. Grønland 105, 1 – 352
H.P. Taylor Jr. & S. Epstein (1963) J. Petrol. 4, 51 – 74
H. P. Taylor Jr. (1968) The oxygen isotope geochemistry of igneous rocks. Contrib. Mineral. Petrol. 19, 1–
71
H. P. Taylor Jr. (1986) Igneous rocks: II. Isotopic case studies of circumpacific magmatism. In: Stable
Isotopes in High Temperature Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P.
Taylor Jr. & J. R. O’Neil [Herausgeber], Mineralogical Society of America, Washington, Seite 273–317
H. P. Taylor Jr. (1980) The effects of assimilation of country rocks by magmas on 18O/16O and 87Sr/86Sr
systematics in igneous rocks. Earth Planet. Sci. Lett. 47, 243–254
H. P. Taylor Jr. (1977) Water/rock interactions and the origin of H2O in granitic batholiths. J. Geol. Soc.
London 133, 509–558
K. Hattori & K. Muehlenbachs (1982) Oxygen isotope ratios of the Icelandic crust. J. Geophys. Res. 87,
6559–6565
W. Hildreth, R. L. Christiansen & J. R. O’Neil (1984) Catastrophic isotopic modification of rhyolitic
magma at times of caldera subsidence, Yellowstone Plateau volcanic field. J. Geophys. Res. 89, 8339–8369
K. Muehlenbachs (1986) Alteration of the oceanic crust and the 18O history of seawater. In: Stable Isotopes
in High Temperature Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J.
R. O’Neil [Herausgeber], Mineralogical Society of America, Washington, Seite 425–444
Y. Bottinga (1969) Calculation of fractionation factors for carbon and oxygen exchange in the system
calcite – carbon dioxide – water. Earth Planet. Sci. Lett. 5, 301–307
T. K. Kyser (1986) Stable isotope variations in the mantle. In: Stable Isotopes in High Temperature
Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J. R. O’Neil
[Herausgeber], Mineralogical Society of America, Washington, Seite 141–164
F. Pineau & M. Javoy (1983) Carbon isotopes and concentration in mid-ocean ridge basalts. Earth Planet.
Sci. Lett. 62, 239–257
M. Javoy, F. Pineau & T. Iiyama (1978) Experimental determination of the isotopic fractionation between
gaseous CO2 and carbon dissolved in tholeiitic magma. Contrib. Mineral. Petrol. 67, 35–39
D. P. Mattey, R. H. Carr, I. P. Wright & C. T. Pillinger (1984) Carbon isotopes in submarine basalts. Earth
Planet. Sci. Lett. 70, 196–206
J. W. Valley (1986) Stable isotope geochemistry of metamorphic rocks. In: Stable Isotopes in High
Temperature Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. J. Taylor & J. R. O’Neil
[Herausgeber], Mineralogical Society of America, Washington, Seite 445–489
P. I. Nabelek, T. C. Labotka, J. R. O’Neil & J. J. Papike (1984) Contrasting fluid/rock interaction between
the Notch Peak granitic intrusion and argillites and limestones in western Utah: evidence from stable
isotopes and phase assemblages. Contrib. Mineral. Petrol. 86, 25–34
R. C. Newton, J. V. Smith & B. F. Windley (1980) Carbonic metamorphism, granulites, and crustal growth.
Nature 288, 45–5045–50333
W. Lamb & J. W. Valley (1984) Metamorphism of reduced granulites in low-CO 2 vapour-free environment.
Nature 312, 56–58
R. H. Becker & R. N. Clayton (1977) Nitrogen isotopes in igneous rocks. EOS Trans. AGU 58, 536]
H. Sakai, D. J. DesMarais, A. Uyeda & J. G. Moore (1984) Concentration and isotope ratios of carbon,
nitrogen and sulfur in ocean-floor basalts. Geochim. Cosmochim. Acta 48, 2433–2441
M. Javoy, F. Pineau & D. Demaiffe (1984) Nitrogen and carbon isotopic composition in the diamonds of
Mbuji Mayi (Zaire). Earth Planet. Sci. Lett. 68, 399–412
E. H. Hauri, J. Wang, D. G. Pearson & G. P. Bulanova (2002) Microanalysis of d13C, d15N, and N
abundances in diamonds by secondary ion mass spectrometry. Chem. Geol. 185, 149–163
W. C. Shanks III (2001) Stable isotopes in seafloor hydrothermal systems: Vent fluids, hydrothermal
deposits, hydrothermal alteration, and microbial processes. In: Reviews in Mineralogy and Geochemistry,
Volume 43: Stable Isotope Geochemistry, J. W. Valley & D. R. Cole [Herausgeber], Mineralogical Society of
America; Geochemical Society, Washington, DC, Seite 470–525
H. Ohmoto (1986) Stable isotope geochemistry in ore deposits. In: Stable Isotopes in High Temperature
Geological Processes, Reviews in Mineralogy Vol. 16, J. W. Valley, H. P. Taylor Jr. & J. R. O’Neil
[Herausgeber], Mineralogical Society of America, Washington, Seite 491–559
K. H. Wedepohl (1964) Untersuchungen am Kupferschiefer in Nordwestdeutschland: Ein Beitrag zur
Deutung der Genese bituminöser Sedimente. Geochim. Cosmochim. Acta 28, 305–364
C. E. Rees (1970) The sulphur isotope balance of the ocean: an improved model. Earth Planet. Sci. Lett. 7,
366–370
Th. Thordarson, S. Self, N. Óskarsson & T. Hulsebosch (1996) Sulfur, chlorine, and fluorine degassing and
atmospheric loading by the 1783–1784 AD Laki (Skaftar Fires) eruption in Iceland. Bull. Volcanol. 58,
205–225
259
Literaturzitate
311.
312.
313.
314.
315.
316.
317.
318.
319.
320.
321.
322.
323.
324.
325.
326.
327.
328.
260
R. M. Garrels & E. A. Perry (1974) Cycling of carbon, sulfur and oxygen through geologic time. In: The
Sea, E. D. Goldberg [Herausgeber], John Wiley and Son, New York, Seite 303
M. R. Rampino (1992) Volcanic hazards. In: Understanding the Earth, G. C. Brown, C. J. Hawkesworth &
R. C. L. Wilson [Herausgeber], Cambridge University Press, Cambridge, Seite 507–552
P. Zhu & J. D. Macdougall (1998) Calcium isotopes in the marine environment and the oceanic calcium
cycle. Geochim. Cosmochim. Acta 62, 1691–1698
J. L. Skulan, D. J. DePaolo & T. L. Owens (1997) Biological control of calcium isotopic abundances in the
global calcium cycle. Geochim. Cosmochim. Acta 61, 2505–2510
N. Gussone et al. (2003) Model for kinetic effects on calcium isotope fractionation (d44Ca) in inorganic
aragonite and cultured planktonic foraminifera. Geochim. Cosmochim. Acta 67, 1375–1382
B. L. Beard & C. M. Johnson (1999) High precision iron isotope measurements of terrestrial and lunar
materials. Geochim. Cosmochim. Acta 63, 1653–1660
M. Sharma, M. Polizzotto & A. D. Anbar (2001) Iron isotopes in hot springs along the Juan de Fuca Ridge.
Earth Planet. Sci. Lett. 194, 39–51
T. D. Bullen, A. F. White, C. W. Childs, D. V. Vivit & M. S. Schulz (2002) Demonstration of significant
abiotic iron isotope fractionation in nature. Geology 29, 699–702
A. S. Ellis, T. M. Johnson & T. D. Bullen (2002) Chromium isotopes and the fate of hexavalent chromium
in the environment. Science 295, 2060–2062
T. Walczyk & F. von Blanckenburg (2002) Natural iron isotope variations in human blood. Science 295,
2065–2066
X. K. Zhu et al. (2002) Mass fractionation processes of transition metal isotopes. Earth Planet. Sci. Lett.
200, 47–62
S. L. Brantley, L. Liermann & T. D. Bullen (2001) Fractionation of Fe isotopes by soil microbes and organic
acids. Geology 29, 535–538
W.L. Griffin, S. Jackson, S. Graham, N. Pearson (2002) Metal isotopes lead the way to riches. In: GEMOC
2001 Annual Report, 26 – 27
C. M. Johnson, B. L. Beard, N. J. Beukes, C. Klein & J. M. O’Leary (2003) Ancient geochemical cycling in
the Earth as inferred from Fe isotope studies of banded iron formations from the Transvaal Craton.
Contrib. Mineral. Petrol. 144, 523–547
(a) J. G. Wiederhold (2002) Fraktionierung von Eisen-Isotopen in einer Stagnogley-Ockererde-Catena auf
Buntsandstein. 83 Seiten, unveröffentlichte Diplomarbeit Universität Karlsruhe und Universität Bern.
(b) J.G. Wiederhold & F. von Blanckenburg (2002) Iron isotope variations in a complete natural soil catena
with lateral iron mobilization and reprecipitation. Goldschmidt Conference Abstracts 2002, S. A834
C. M. Johnson, J. L. Skulan, B. L. Beard, H. Sun, K. H. Nealson & P. S. Braterman (2002) Isotopic
fractionation between Fe(III) and Fe(II) in aqueous solutions. Earth Planet. Sci. Lett. 195, 141–153
E. A. Schauble, G. R. Rossman & H. P. J. Taylor (2001) Theoretical estimates of equilibrium Fe-isotope
fractionations from vibrational spectroscopy. Geochim. Cosmochim. Acta 65, 2487–2497
V. B. Polyakov & S. D. Mineev (2000) The use of Mössbauer spectroscopy in stable isotope geochemistry.
Geochim. Cosmochim. Acta 64, 849–865
@
Isotopengeochemie
Index
Seite
Seite
Symbols
Diffusion . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
e-Wert, Definition . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 57
Diffusionskoeffizient . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
d-Wert, Definition . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 202
Diskordia . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 109–116
DMM . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 128
A
dunkle Energie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10
abgeklungene Radionuklide. . . . . . . . . . . . . . . . . . . 186–192
dunkle Materie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9
Abkühlalter . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 36
Dupal-Anomalie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 127
Achondrite . . . . . . . . . . . . . . . . . . . . . . . . . . 49, 57, 84, 170
Actiniden. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 105
E
AFC-Modell . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 222, 224
Edelgase . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 173–185
AGB-Sterne . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14
Eisen-Isotope . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 245–249
Aktivierungsenergie . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
Elektromagnet. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23
Aktivitäten, von Radionukliden . . . . . . . . . . . . . . . . . . . . 139
Elektronenstrahlmikrosonde, Th–U–Pb-Datierung . . . . . . 118
alpha-Spektrometrie . . . . . . . . . . . . . . . . . . . . . . . . . . . . 140
Alpha-Strahlung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Alpha-Zerfall . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Analysator . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23
Ar-Ar-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 37–41
asymptotischer Riesenast, Sterne . . . . . . . . . . . . . . . . . . . . 14
Ausheilen, von Spaltspuren . . . . . . . . . . . . . . . . . . . . . . . 136
Elemente, Ursprung. . . . . . . . . . . . . . . . . . . . . . . . . . . . 9–22
EM I . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 128
EM II . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 128
epsilon-Wert, Definition. . . . . . . . . . . . . . . . . . . . . . . . . . . 57
equiline . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 154
equipoint . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 154
Erde, Kern–Mantel-Differenzierung . . . . . . . . . . . . . . . . . 191
errorchron. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 43
B
eruptierte Mantelisochronen . . . . . . . . . . . . . . . . . . . . . . . 72
BABI . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 50
Eukrite. . . . . . . . . . . . . . . . . . . . . . . . . . . . . 84, 85, 188, 190
Bateman-Gleichungen. . . . . . . . . . . . . . . . . . . . . . . 144, 148
Kern–Mantel-Differenzierung. . . . . . . . . . . . . . . . . . 191
exponential law, Massenfraktionierung . . . . . . . . . . . . . . . 79
Be10 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 161–166
Bestrahlungsalter, von Meteoriten . . . . . . . . . . . . . . . . . . 167
Beta-Strahlung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Beta-Zerfall . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
F
Faradaybecher. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23, 24
Filament . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
Bethe–Weizsäcker-Zyklus . . . . . . . . . . . . . . . . . . . . . . . . . . 11
Fission-Track-Methode . . . . . . . . . . . . . . . . . . . . . . 133–138
Big Bang . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9
Flugzeitspektrometer. . . . . . . . . . . . . . . . . . . . . . . . . . . . . 26
bulk-earth . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 57
Fluidinfiltration bei Metamorphose . . . . . . . . . . . . . . . . . 232
Bushveld . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 93
Flußmonitor . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 37
C
focal zone . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 129
C14-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 159–161
C3-Pflanzen. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 194
C4-Pflanzen. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 194
FOZO . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 129
Fraktionierung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Fraktionierungsfaktor. . . . . . . . . . . . . . . . . . . . . . . . . . . . 196
CAI . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 190
G
Calcium. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 243–244
Gamma-Strahlung. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
CAM-Pflanzen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 194
Geochrone . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 123
Chandrasekhar-Grenze . . . . . . . . . . . . . . . . . . . . . . . . 14, 22
Gleichgewichtsisotopieeffekte . . . . . . . . . . . . . . . . . . . . . 195
Chondrite . . . . . . 49, 57, 62, 85, 95, 99, 100, 102, 170, 189
Gorgona Island . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 102
Chrom-Isotope . . . . . . . . . . . . . . . . . . . . . . . . . . . . 245–248
Chur . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 57
H
CNO-Zyklus . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 11
Halbwertszeit . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6
common lead . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 120
He3/He4 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 173–182
Cr, Isotopenanomalien . . . . . . . . . . . . . . . . . . . . . . . . . . 192
Helium-Blitz. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13
crossover . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 213
Hertzsprung–Russell-Diagramm. . . . . . . . . . . . . . . . . . . . . 11
crustal residence age . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 62
Hf-Gehalte in der Natur. . . . . . . . . . . . . . . . . . . . . . . . . . . 83
Hf-Sr-Nd-Isotopenkorrelation . . . . . . . . . . . . . . . . . . . . . . 87
D
Hf-W-Chronometer . . . . . . . . . . . . . . . . . . . . . . . . . 187–192
Datierungsmethoden, Übersicht . . . . . . . . . . . . . . . . . . . . . 8
HIMU . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 128
Dekarbonatisierung, C- + O-Isotope . . . . . . . . . . . . . . . . 232
Hochtemperaturalteration, O-Isotope . . . . . . . . . . . . . . . 226
depleted MORB mantle . . . . . . . . . . . . . . . . . . . . . . . . . . 128
Holmes-Houtermans-Modell . . . . . . . . . . . . . . . . . . . . . . 120
A
@
Index
Isotopengeochemie
Seite
Seite
HR-Diagramm siehe Hertzsprung–Russel-Diagramm
Meerwasser, Sr-Isotopenentwicklung . . . . . . . . . . . . . . . . .51
Hypernova . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .16
meteoric water line. . . . . . . . . . . . . . . . . . . . . . . . . . . . . .207
I–J
ICP-MS . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .26
initiales Isotopenverhältnis . . . . . . . . . . . . . . . . . . . . . . . . .42
Mischungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 67–74
Modellalter . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 62–66
Monazit
Ionenquelle . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .24
Th–U–Pb-Alterszonierung . . . . . . . . . . . . . . . . . . . . .119
Th–U–Pb-Mikrosondendatierung . . . . . . . . . . . . . . .118
MORB . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .57, 87, 128
Ionensonde, Funktionsprinzip . . . . . . . . . . . . . . . . . . . . . .117
MSWD, mean standard weighted deviation . . . . . . . . . . . .45
Ionium-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . .143–146
Multikollektor . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .25
Isobare, Definition . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
Mutternuklid . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
Initialwert . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .43
Isochrone . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .43
Isochronengleichung . . . . . . . . . . . . . . . . . . . . . . . . . . . . .43
Isotop, Definition . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
N
Nd in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .55
Nd-Sr-Hf-Isotopenkorrelation . . . . . . . . . . . . . . . . . . . . . . .87
Isotopenaustausch
geschlossenes System . . . . . . . . . . . . . . . . . . . . . . . .217
offenes System . . . . . . . . . . . . . . . . . . . . . . . . . . . . .217
Isotopenentwicklungsdiagramm . . . . . . . . . . . . . . . . . . . . .47
Nicolaysen-Diagramm . . . . . . . . . . . . . . . . . . . . . . . . . . . .43
Isotopenthermometer. . . . . . . . . . . . . . . . . . . . . . . .211, 239
Nuklid, Definition . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
Isotopenverdünnungsanalyse . . . . . . . . . . . . . . . . . . . .27–29
Nuklidkarte. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .4
Isotopieeffekte . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .194
Nova . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .22
Nukleosynthese . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .9
O
K
OIB. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .90, 128
K-Ar-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .31–41
Ordnungszahl. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
K-Ca-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .94–95
Os, Gehalte in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . .98
K-Einfang . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
Ötzi . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .206
kinetische Isotopieeffekte . . . . . . . . . . . . . . . . . . . . . . . . .194
Ozeaninselbasalte, Hf-Isotope . . . . . . . . . . . . . . . . . . . . . . .91
Kohlenstoff . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .228–233
Kollektor . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .23
Konkordia. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .109–116
kosmische Strahlung, Energieverteilung . . . . . . . . . . . . . .158
kosmogene Radionuklide . . . . . . . . . . . . . . . . . . . . .158–172
Kreide/Tertiär-Grenze . . . . . . . . . . . . . . . . . . . . . . . .103, 192
Kupfer-Isotope . . . . . . . . . . . . . . . . . . . . . . . . . . . . .245–248
P–Q
Paläotemperaturbestimmung . . . . . . . . . . . . . . . . . . . . . .209
Parabelspektrograph. . . . . . . . . . . . . . . . . . . . . . . . . . . . . .23
Pb, Gehalte in Natur. . . . . . . . . . . . . . . . . . . . . . . . . . . . .106
Pb210-Methode . . . . . . . . . . . . . . . . . . . . . . . . . . . . 141–143
Pb-Paradox. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .126, 128
PDB . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .201
L
PGE, Platingruppenelemente . . . . . . . . . . . . . . . . . . . . . .102
La-Ce-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .92–93
Photodisintegration . . . . . . . . . . . . . . . . . . . . . . . . . . .14, 18
Laserablation . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .118
Pikes Peak-Komplex . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .94
late veneer-Hypothese . . . . . . . . . . . . . . . . . . . . . . . . . . .103
Planetarische Nebel . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .14
Lu/Hf in der Natur . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .83
Plateaualter . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .39, 117
Lu/Hf in ozeanischen Sedimenten. . . . . . . . . . . . . . . . . . . .90
Potenzfunktion, Fraktionierungskorrektur . . . . . . . . . . . . . .78
Lu-Gehalte in der Natur . . . . . . . . . . . . . . . . . . . . . . . . . . .83
power law, Massenfraktionierung . . . . . . . . . . . . . . . . . . . .78
Lu-Hf-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .83–91
p-Prozeß, Nukleosynthese . . . . . . . . . . . . . . . . . . . . . .18, 20
M
magnetisches Sektorfeld . . . . . . . . . . . . . . . . . . . . . . . .24, 25
mantle array . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .61
Mars, Kern–Mantel-Differenzierung . . . . . . . . . . . . . . . . .191
PREMA . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .128
prevalent mantle . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .128
Proton–Proton-Zyklus . . . . . . . . . . . . . . . . . . . . . . . . . . . . .11
Pulsare . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .16
Quadrupolmassenspektrometer . . . . . . . . . . . . . . . . . . . . .26
massenabhängige Fraktionierung, stabile Isotope . . .193, 205
Massenfraktionierung . . . . . . . . . . . . . . . . . . . . . . . . . .75–82
R
Massenspektrometer. . . . . . . . . . . . . . . . . . . . . . . . . . .23–27
Rayleighsches Destillationsgesetz . . . . . . . . . . . . . . . . . . .206
Massenspektrometrie . . . . . . . . . . . . . . . . . . . . . . . . . .23–27
Rb, Gehalte in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . .42
Massenzahl. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .3
Rb-Sr-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 42–52
mean standard weighted deviation, MSWD . . . . . . . . . . . .45
Re, Gehalte in Gesteinen. . . . . . . . . . . . . . . . . . . . . . . . . . .98
Meerwasser, Os-Isotopenentwicklung. . . . . . . . . . . . . . . .104
reduzierte Masse. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .196
B
@
Isotopengeochemie
Index
Seite
Seite
REE . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 53
Tochternuklid . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Tracer . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4, 43
Trennrohr . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23
Reinelemente . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Re-Os-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 96–104
Riesenstern . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13
Roter Riese . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13
r-Prozeß, Nukleosynthese . . . . . . . . . . . . . . . . . . . . . . 17, 20
Rückstoß . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 133
Rückstoßoxidation. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 146
S
säkulares Gleichgewicht . . . . . . . . . . . . . . . . . . . . . 106, 139
Sauerstoff
Hydro- und Atmosphäre . . . . . . . . . . . . . . . . . 205–210
Lithosphäre . . . . . . . . . . . . . . . . . . . . . . . . . . . 211–227
Sauerstoffisotope. . . . . . . . . . . . . . . . . . . . . . . . . . . 204–227
Schließungstemperatur . . . . . . . . . . . . . . . . . . . . 33, 34, 137
schnelle Neutronen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 37
Schwarzes Loch . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 16
Schwarzschild-Radius . . . . . . . . . . . . . . . . . . . . . . . . . . . . 16
Schwefel . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 236–242
Schwefelisotope, Meerwasser . . . . . . . . . . . . . . . . . . . . . 239
Schwefelisotopie, marine Sulfate und Sulfide . . . . . . . . . . 242
sekundäre Pb-Isochrone . . . . . . . . . . . . . . . . . . . . . . . . . 130
Seltene Erden . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 53
SHRIMP . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 118
Sm in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 55
Sm/Nd in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 55
Sm/Nd in ozeanischen Sedimenten . . . . . . . . . . . . . . . . . . 90
Sm-Nd-System . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 53–66
space–charge effect. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 81
Spallationsreaktionen . . . . . . . . . . . . . . . . . . . . . . . . . . . 158
Spaltspurenmethode . . . . . . . . . . . . . . . . . . . . . . . . 133–138
U–V
U, Gehalte in Natur . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 106
U,Th-Pb-Methoden . . . . . . . . . . . . . . . . . . . . . . . . . 105–132
U234/U238-Methode . . . . . . . . . . . . . . . . . . . . . . . 146–151
U238/Th230-Ungleichgewichte, in Vulkaniten . . . . 152–157
Überriesen. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14
Ungleichgewichtsmethoden . . . . . . . . . . . . . . . . . . 139–157
Uran, im Meerwasser. . . . . . . . . . . . . . . . . . . . . . . . . . . . 143
Urblei . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 121
Urknall . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9
Verteilungsfunktion . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 197
VPDB. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 202
VSMOW . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 201
W–Z
Wärmefluß . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 181
Wärmeproduktion . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 181
Wasserstoff
Hydro- und Atmosphäre . . . . . . . . . . . . . . . . . 205–210
Lithosphäre . . . . . . . . . . . . . . . . . . . . . . . . . . . 211–227
Wasserstoffisotope. . . . . . . . . . . . . . . . . . . . . . . . . . 204–227
Weiße Zwerge. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14, 22
Xenon . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 182–185
Zerfallsgesetz . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Zerfallskonstante . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Zink-Isotope . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 245–246
Zirkone, älteste archaische. . . . . . . . . . . . . . . . . . . . . . . . . 89
Zweikomponentenmischungen . . . . . . . . . . . . . . . . . . 67–74
Zweistufenentwicklung, Pb-Isotope . . . . . . . . . . . . . . . . . 109
Spike . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27
Spontanspaltung . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 133
s-Prozeß, Nukleosynthese . . . . . . . . . . . . . . . . . . . . . . 17, 20
Sr, Gehalte in Gesteinen . . . . . . . . . . . . . . . . . . . . . . . . . . 42
Sr-Nd-Hf-Isotopenkorrelation. . . . . . . . . . . . . . . . . . . . . . . 87
Stabile Isotope, Allgemeines . . . . . . . . . . . . . . . . . . 193–203
Stacey-Kramers-Modell . . . . . . . . . . . . . . . . . . . . . . . . . . 124
Stickstoff . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 234–235
stufenweises Ausheizen . . . . . . . . . . . . . . . . . . . . . . . . . . . 39
Supernova
Typ Ia . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 22
Typ II. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15, 16, 22
T
T Tauri-Sterne . . . . . . . . . . . . . . . . . . . . . . . . . . . 10, 20, 186
Th, Gehalte in Natur . . . . . . . . . . . . . . . . . . . . . . . . . . . . 106
Th, im Meerwasser . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 143
Th230/U234-Methode . . . . . . . . . . . . . . . . . . . . . . 148–151
Thermionenmassenspektrometer. . . . . . . . . . . . . . . . . . . . 24
Thermionenquelle . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
Tieftemperaturalteration, O-Isotope . . . . . . . . . . . . . . . . 226
TIMS . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
C