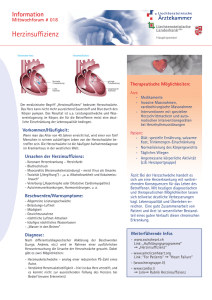
Therapie der chronischen Herzinsuffizienz
Werbung

2000 39. BAYERISCHER INTERNISTEN-KONGRESS © 2001 W. Zuckschwerdt Verlag München 1 Therapie der chronischen Herzinsuffizienz Angiotensin-II-Rezeptorblocker, Aldosteron-Rezeptorantagonisten, Vasopeptidase-Inhibitoren Günter Riegger Klinik und Poliklinik für Innere Medizin II, Universität Regensburg Angiotensinkonversion-Enzymhemmer, Betablocker, Diuretika und Herzglykoside stellen die Standardtherapie der chronischen Herzinsuffizienz dar. Im folgenden möchte ich neuere Therapieprinzipien darstellen und diskutieren, die in das Renin-Angiotensin-Aldosteron-System eingreifen und zusätzlich neue Möglichkeiten eröffnen, in der Herzinsuffizienz protektiv wirksame Systeme wie die natriutischen Peptide in ihrer Wirkung zu verstärken. Angiotensin-II-Rezeptorblocker Die Anwendung von ACE-Hemmern bei Patienten mit Herzinsuffizienz ist bei manchen Patienten problematisch, da Nebenwirkungen wie chronischer Husten auftreten und damit eine Dauertherapie unmöglich wird. Die Blockade des Renin-Angiotensin-Systems ist durch ACE-Hemmer nicht komplett, indem Angiotensin II durch ACE im Gewebe als auch durch Enzyme wie Chymasen generiert werden kann, was möglicherweise eine Wirkungsminderung bedingt. Da Angiotensin-II-Antagonisten direkt den AT1-Rezeptor von Angiotensin II inhibieren, könnten diese Medikamente effizienter in der Blockade des Renin-Systems sein. Durch Blockierung des AT1-Rezeptors an den juxtaglomerulären Zellen der Niere kommt es zu einem Wegfall der hemmenden Wirkung von Angiotensin II auf die Reninsekretion, woraus eine erheblich gesteigerte Produktion von Angiotensin II resultiert. Die erhöhten Angiotensin-II-Spiegel, deren Wirkung auf den AT1-Rezeptor, was Natriumretention,Vasokonstriktion,proliferative Effekte etc. betrifft, medikamentös blockiert ist, können jedoch den AT2-Rezeptor stimulieren, mit den möglicherweise günstigen Effekten einer antiproliferativen und vasodilatatorischen Wirkung. In einer Pilotstudie, der ELITE-Studie (3), fand sich bei 722 Patienten mit mittelschwerer Herzinsuffizienz im Vergleich zwischen dem Angiotensin-II-Rezeptorinhibitor Losartan (50 mg/d) und dem ACE-Hemmer Captopril (3 × 50 mg/d) kein Unterschied in der Nierenfunktion,jedoch eine Reduktion des Risikos eines plötzlichen Herztodes in der Losartan-Gruppe von 46%. Ausgehend von dieser Studie wurde die ELITE-II-Studie durchgeführt (5),deren Ergebnisse im Mai dieses Jahres publiziert wurden. In diese Studie, deren primärer Endpunkt die Gesamtmortalität war, wurden 3152 Patienten im Stadium II–IV der Herzinsuffizienz mit einer Ejektionsfraktion von unter 40% eingeschlossen. Das mittlere Alter der Patienten betrug 71,4 Jahre, die mittlere Ejektionsfraktion 31%. Die Studienmedikation war identisch zur ELITE-Studie, das Follow-up betrug 555 Tage. Im Gegensatz zur Pilotstudie fand sich keine Überlegenheit von Losartan im Vergleich zu Captopril, wobei keine signifikanten Differenzen bei der Gesamtmortalität, der Inzidenz des plötzlichen Herztodes oder der Notwendigkeit einer Reanimation zwischen beiden Gruppen zu verifizieren waren.Auffallend war,wie erwartet, dass in der Losartan-Gruppe signifikant weniger Nebenwirkungen, insbesondere was chronischen Husten betrifft, auftraten. Die Schlüsse,die sich aus dieser Studie,insbesondere im Hinblick auf die hervorragenden Daten der ACE-Hemmertherapie aus Studien wie CONSENSUS (2) und SOLVD (7) ergeben,sind,dass ACE-Hemmer weiterhin als initiale Basistherapie bei chronischer Herzinsuffizienz zu gelten haben, dass jedoch AT1-Rezeptorblocker bei Intoleranz von ACE-Hemmern eine wirksame Alternative darstellen. Aldosteron-Rezeptorantagonisten Aldosteron spielt eine bedeutende Rolle in der Pathophysiologie der Herzinsuffizienz, indem es die Natrium- und Wasserretention begünstigt, es zu vermehrten renalen Verlusten von Magnesium und Kalium führt, die sympathische Aktivität verstärkt, den Parasympathikus inhibiert und wesentlich zur myokardialen vaskulären und interstitiellen Fibrose beiträgt. Aldosteron wirkt sich außerdem ungünstig auf die Baro-Rezeptorfunktion und die Compliance des arteriellen Blutgefäßsystem aus.Aus großen Studien ist bekannt, dass durch die alleinige Gabe von ACE-Inhibitoren nur eine transiente Suppression der Produktion von Aldosteron möglich ist und dass die AldosteronPlasmaspiegel nach einigen Monaten wieder zum Ausgangspunkt zurückkehren (1). Ausgehend von den oben dargelegten pathophysiologischen Überlegungen wurde die RALES-Studie durchgeführt, bei der 1663 Patienten mit chronischer Herzinsuffizienz im Stadium III und IV eingeschlossen wurden. Alle Patienten waren behandelt mit einem ACE-Inhibitor, einem Schleifendiuretikum und in den meisten Fällen mit Herzglykosiden. Ausschlusskriterium war ein Serumkreatinin >2,5 mg/dl und eine Serumkaliumkonzentration über 5,0 mmol/l. 70% der Patienten befanden sich im NYHA-Stadium III, 30% im Stadium IV, die mittlere Ejektionsfraktion betrug 25% (4). Die Hälfte der Patienten erhielt 25 mg Spironolacton/Tag, die andere Hälfte Placebo. Die Studie, die ursprünglich über drei Jahre konzipiert war, wurde nach zwei Jahren abgebrochen, da sich eine hochsignifikante 30%-ige Reduktion des Risikos, was die Gesamtmortalität betrifft nachweisen ließ, wobei sowohl die Mortalität bedingt durch chronisches Pumpversagen als auch bedingt durch plötzli- 2 chen Herztod günstig beeinflusst wurde. Die Häufigkeit einer Hospitalisierung wegen Verschlechterung der Herzinsuffizienz nahm in der Spironolacton-Gruppe um 35% ab, ebenso zeigte sich eine signifikante Verbesserung der Symptome der Patienten im Rahmen der Klassifikation der New York Heart Association. Bedeutsame Fälle von Hyperkaliämie ereigneten sich in zehn Patienten in der Placebo-Gruppe und bei 14 Patienten in der Spironolacton-Gruppe, ein Abbruch der Behandlung hierdurch war bei einem Patienten in der Placebo-Gruppe und bei drei Patienten in der SpironolactonGruppe notwendig. Wie erwartet fand sich eine erhöhte Inzidenz einer Gynäkomastie oder von Brustschmerzen bei Männern in der Spironolacton-Gruppe (10%) im Vergleich zu Männern in der Placebo-Gruppe (1%). Die RALES-Studie zeigt eindeutig, dass Patienten mit relativ schwerer Herzinsuffizienz im Stadium III und IV von einer zusätzlichen niedrig dosierten Therapie mit Spironolacton in Ergänzung zur Standardtherapie profitieren und dass hierdurch eine hochsignifikante und effiziente Reduktion des Risikos, was Mortalität und Morbidität betrifft, möglich ist. Unter Einbeziehung der Ausschlusskriterien und regelmäßiger Kontrolle der Nierenfunktion und der Serumelektrolyte ist diese Therapie sicher und von wenig Nebenwirkungen begleitet. Vasopeptidase-Inhibitoren Bei der chronischen Herzinsuffizienz spielen nicht nur vasokonstriktorisch wirksame neurohurmonale Systeme eine bedeutende Rolle, sondern auch gegenregulatorisch wirksame Mechanismen wie natriuretische Peptide, Stickstoffmonoxyd und Prostaglandine. Natriuretische Peptide werden in den Vorhöfen des Herzens (ANP), im Myokard (BNP) und im Endothel der Blutgefäße (CNP) gebildet. Natriuretische Peptide wirken vasodilatatorisch, natriuretisch und diuretisch, hemmen zentral den Sympaticus, wirken antiproliferativ, reduzieren den venösen Rückfluss zum Herzen und hemmen direkt die Renin- und Aldosteronsekretion.Natriuretische Peptide werden inaktiviert durch neutrale Endopeptidasen (NEP),welche sich vorwiegend in der Niere befinden. Seit neuestem sind Medikamente verfügbar, welche die NEP hemmen und damit die Wirkung naturetischer Peptide verstärken. Vasopeptidase-Inhibitoren sind Medikamente,welche in einem Molekül die Konversion von Angiotensin I zu Angiotensin II blockieren (ACE-Inhibition) und gleichzeitig den Abbau von natriuretischen Peptiden vermindern (NEP-Inhibition). Die erste Substanz dieser neuen Klasse von Medikamenten ist Omapatrilat mit einer gleichstarken hemmenden Wirkung auf NEP- und ACE-Aktivität. Die erste Studie bei Patienten mit chronischer Herzinsuffizienz,die die Wirkung einer Vasopeptidase-Inhibition (Omapatrilat) im Vergleich zur ACE-Hemmung (Lisinopril) untersuchte, ist die ImpressStudie, deren Ergebnisse im August d. J. publiziert wurden (6). In die Studie wurden 573 Patienten mit chronischer Herzinsuffizienz im Schweregrad II–IV eingeschlossen, mit einer Ejektionsfraktion unter 40%. Die eine Hälfte der Patienten erhielt eine Dosis von 40 mg Omapatrilat/Tag, die andere Hälfte 20 mg Lisinopril/Tag über 24 Wochen. Der primäre Endpunkt der Studie war die maximale Belastungstoleranz nach 12 Wochen.Was die maximale Belastbarkeit der Patienten betrifft, so fand sich zwischen beiden Gruppen kein signifikanter Unterschied. Es fand sich zu Gunsten des Omapatrilats ein Trend einer Verminderung des Risikos auf den kombinierten Endpunkt Gesamtmortalität oder der Notwendigkeit einer Klinikeinweisung bei Verschlechterung der Herzinsuffizienz. Ein signifikanter Benefit ließ sich für Omapatrilat im Vergleich zu Lisinopril nachweisen bei Kombinierung von drei Endpunkten wie Gesamtmortalität, Hospitalisierungsrate oder Beendigung der Studienmedikation wegen Verschlechterung der Herzinsuffizienz. Omapatrilat führte zu einer signifikanten Verbesserung der NYHA-Klassifikation im Vergleich zu Lisinopril bei Patienten mit schwerer Herzinsuffizienz (NYHA-Klasse III und IV). Somit liegt mit den jetzt zur Verfügung stehenden Vasopeptidase-Inhibitoren und hier speziell Omapatrilat eine interessante neue Substanz vor, deren Nutzen jedoch mit den bisher vorliegenden Daten nicht eindeutig abzuschätzen ist. Hierzu läuft zur Zeit eine groß angelegte kontrollierte Studie mit dem primären Endpunkt der Gesamtmortalität bei 4420 Patienten mit chronischer Herzinsuffizienz, die im Jahr 2002 beendet sein wird (OVERTURE-Studie). Insgesamt gesehen stehen uns mit den drei hier diskutierten pharmakologischen Interventionsmöglichkeiten bei chronischer Herzinsuffizienz neue Möglichkeiten zur Verfügung.Was die Angiotensin-II-Rezeptorinhibitoren betrifft, so sind diese wirksame Alternativen zu den ACE-Hemmern, falls diese vom Patienten nicht toleriert werden können. Bei Patienten mit schwerer Herzinsuffizienz ist die zusätzliche Therapie mit niedrig dosiertem Spironolacton, bei Berücksichtigung der Nierenfunktion und Elektrolytbilanz von außerordentlichem Nutzen, was Morbidität und Mortalität betrifft. Die neuen Substanzen, die gleichzeitig NEP und ACE inhibieren (Vasopeptidase-Inhibitoren) lassen günstige Effekte bei der Therapie der chronischen Herzinsuffizienz vermuten, ihr Stellenwert wird jedoch erst nach Abschluss der jetzt laufenden OVERTURE-Studie endgültig zu beurteilen sein. Literatur 1. 2. 3. 4. 5. 6. Borghi C,Boschi S,Ambrosioni E,Melandri G, Branzi A, Magnani B. Evidence of a partial escape of renin-angiotensin-aldosterone blockade in patients with acute myocardial infarction treated with ACE inhibitors. J Clin Pharmacol 1993; 33: 40-5 The Consensus Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure. N Engl J Med 1987; 316: 1429-35 Pitt B, Segal R, Martinez FA, et al on behalf of the ELITE Study Investigators. Randomised trial of losartan versus captopril in patients over 65 with heart failure. Lancet 1997; 349: 747-52 Pitt B,Zannad F,Remme W J,Cody R,Castaigne A, Perez A, Palensky J,Wittes J.The effect of Spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J M 1999; 341: 709-17 Pitt B, Poole-Wilson PA, Segal R, Martinez FA, Dickstein K, Camm AJ, Konstam MA, Riegger G, Klinger GH, Neaton J, Sharma D,Thiyagarajan B,on behalf of the ELITE II investigators. Effect of losartan compared with captoril on mortality in patients with symptomatic heart failure: randomised trial - the Losartan Heart Failure Survival Study ELITE II. Lancet 2000; 355: 1582-87 Rouleau J L, Pfeffer M A, Duncan J S, Isaac D, Sestier F, Kerut E K, Porter C B, Proulx G, Qian Ch, Block A J. Compari- 3 7. sion of vasopeptidase inhibitor, omapatrilat,and lisinopril on exercise tolerance and morbidity in patients with heart failure: IMPRESS randomised trial. Lancet 2000; 356: 612-620 The SOLVD Investigators.Effects of enal- april on survival in patients with reduced left ventricular ejection fraction and congestive heart failure. N Engl J Med 1991; 325: 293-302 Anschrift des Verfassers_ Prof. Dr. med. G. Riegger Klinik und Poliklinik für Innere Medizin II Universität Regensburg 93041 Regensburg