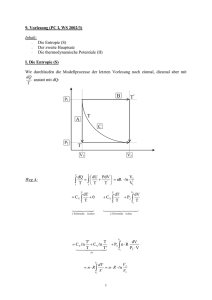
thermodynamik genauer
Werbung

181 9. Wärmelehre 182 9.1 Temperaturskala Temperatur T Wärmeenergie: Temperatur: statistisch verteilte kinetische und potentielle Energie in einem System (relativ zum Grundzustand) Maß für mittlere kinetische Energie eines Systems (im Schwerpunktssystem) Bemerkung: potentielle und kinetische Energie nehmen mit der Temperatur zu; aber nur die kinetische Energie ist streng proportional zur Temperatur Definition: Einheit Kelvin [K] 0K: absoluter Nullpunkt (keinerlei kinetische Energie mehr im System) 273.16 K: Tripelpunkt des Wassers (Eis, Wasser und Dampf sind gleichzeitig vorhanden; der Druck beträgt 612 Pa) Damit ist die gesamte Temperaturskala festgelegt! Es gilt: Genauer: Zwei Systeme in Kontakt tauschen Wärmeenergie aus, bis sie im thermischen Gleichgewicht sind. Ist System A mit System C und System B mit System C im thermischen Gleichgewicht, so sind auch A und B im thermischen Gleichgewicht. „Nullter Hauptsatz der Thermodynamik“ Dient als theoretische Grundlage der Temperaturmessung (System C kann als Thermometer verwendet werden) Bemerkung: Die Kelvin-Skala entspricht der Celsius-Skala, sie ist nur verschoben. Die Celsius-Skala ist definiert über 0° C : Schmelzpunkt des Wassers bei 1.013 bar (273.15 K) 100° C : Siedepunkt des Wassers bei 1.013 bar (373.15 K) 183 9.2 Temperaturmessung: Thermometer 184 In molaren Einheiten: Definition: Ausnutzung thermischer Effekte: Avogadro-Zahl NA (Zahl der Atome pro mol) 1 mol Atome 12C haben eine Masse von 12g • Druck ⇒ NA = 6.022*1023 1/mol • Materialausdehnung • elektrischer Widerstand Damit: pV = Nk BT = N mol N A k BT = N mol RT • thermoelektrische Spannung R = NAkB = 8.31 J/Kmol • Strahlungsleistung • etc. ⇒ der Druck ist (bei festem Volumen) streng proportional zur Temperatur: 9.2.1 Gasdruckthermometer p= Für ein ideales Gas gilt: pV = Nk BT Wird ausgenutzt beim Gasthermometer. Klassischer Aufbau: h p Druck V Volumen N Anzahl Gasteilchen (Atome oder Moleküle) T Temperatur kB : Boltzmann - Konstante kB = 1.38 10-23 J/K T p0 T0 Höhe wird konstant gehalten Hg Gas Druck im Behälter: flexible Verbindung p = pL + h ρ g 185 Bei der Eichtemperatur (z.B. 273.15 K): 186 l = l 0 (1 + α T ) Längenausdehnung: p0 = pL + h0 ρ g α: Ausdehnungskoeffizient Bei einer anderen Temperatur ist dann: p= ⇒ ⇒ ⇒ T p0 = pL + h ρ g T0 p − p0 = ( Werte: T − 1) p0 = (h − h0 ) ρ g T0 ρ gT0 p0 α = 12*10-6 1/K α = 0.51*10-6 1/K V = V0 (1 + γ T ) Volumenausdehnung: γ: Volumenausdehnungskoeffizient T ρg −1 = ( h − h0 ) T0 p0 T= Eisen Quartz Werte: Benzol γ = 10.6*10-4 1/K Quecksilber γ = 1.8*10-4 1/K ( h − h0 ) + T0 Erlaubt präzise absolute Temperaturmessung! 9.2.2 Ausdehnungsthermometer Die thermische Ausdehnung ist bei vielen Materialien in breiten Temperaturbereichen proportional zur Temperatur. Gegenbeispiel: Wasser hat seine maximale Dichte bei 4°C ⇒ γ =0 bei T= 4°C γ <0 bei 0<T< 4°C γ <0 bei T>4°C 187 Kapillare (Radius r) Thermometer ∆x Flüssigkeit (Volumen V0) 188 9.3 Wärmekapazität Gleichverteilungssatz: im thermischen Gleichgewicht ist jeder Freiheitsgrad eines Systems im zeitlichen Mittel mit der Energie 1 k BT 2 angeregt. Eine geringe Veränderung des Volumens erzeugt eine starke Verschiebung in der Kapillare ∆V = γ V0 ∆T = π r 2 ∆x ⇒ ∆x = V0 γ ∆T πr2 (durch Wahl von Volumen und Kapillarradius läßt sich die Verschiebung ∆x für eine gegebene Temperaturveränderung beliebig groß machen!) Freiheitsgrad: jede verallgemeinerte Orts- und Impulsvariable eines Systems, die quadratisch in die Gesamtenergie eingeht (ausgenommen Schwerpunktskoordinaten) Konkret: jede unabhängig wählbare kinetische Energie und (bei Vibrationen) potentielle Energie bildet einen Freiheitsgrad Die Temperatur ist dann also π r2 ∆T = ∆x γ V0 Hier ist zu beachten, dass r und V0 ebenfalls von der Temperatur abhängen, und dass der Ausdehnungskoeffizient nur in einem beschränkten Temperaturbereich gültig ist. Ein solches Thermometer muss daher an möglichst vielen Temperaturfixpunkten geeicht werden. Definition: dQ dT Q: Wärmeenergie 1 dQ M dT M: Systemmasse Wärmekapazität C= Spezifische Wärmekapazität: c= Genauer: Wärmekapazität bei konstantem Volumen CV Wärmekapazität bei konstantem Druck Cp 189 190 Bei „einfachen“ Systemen gilt: ω hier ist die kinetische Energie eines Moleküls: m 1 1 C = f tot k B = N f k B 2 2 ftot : totale Zahl der Freiheitsgrade; 2-atomiges ideales Gas Beispiel: 1 1 Q = f tot k BT = N f k BT 2 2 1 1 m D E kin = M v 2 + Jω 2 + rɺ 2 + r 2 2 2 4 2 m f: Freiheitsgrade pro Atom r Rotation Translation Vibration (kin. und pot. Energie) 1-atomiges ideales Gas Beispiel: m v 1 E kin = m v 2 2 Freiheitsgrade: pro Atom 1 1 1 2 2 2 = mv x + mv y + mv z 2 2 2 Atom 3 unabhängige Energien ⇒ 3 Freiheitsgrade (f=3) f = 3 + 3 Eges = Q = N f 1 3 k BT = Nk BT 2 2 ⇒ f = 3 + 2 CV = 3 Nk B 2 + 0 + (die Rotation um die Molekülachse und die Vibration werden nicht angeregt) 5 Eges = Q = N k BT 2 CV = Wärmekapazität: 1 + 1 = 8 Aber: wegen quantenmechanischer Effekte sind Rotationen mit kleinem Trägheitsmoment und Molekülvibrationen bei Zimmertemperatur meist nicht angeregt Die Gesamtenergie des Gases ist damit: Gesamtenergie des Gases (mit N Atomen): + 5 N k BT 2 0 = 5 191 Beispiel: Festkörper 1 1 E = mv 2 + Dr 2 2 2 Energie pro Atom m ⇒ f= 3 + 3 = 6 Gesamtenergie: Q = 3 N k BT Wärmekapazität CV = 3N k B 192 Bemerkung: auch bei Festkörpern gilt: je tiefer die Temperatur, desto weniger Vibrationsmoden sind angeregt (nur solche mit etwa ℏ ω < k B T ) Damit fällt cV für kleine T auf Null. Wärmekapazität verschiedener fester Stoffe, aufgetragen gegen die normierte Temperatur T/TD Dulong-Petit-Gesetz Feste Stoffe haben also eine Wärmekapzität von 4.14 10-23 J/K pro Atom = 24.84 J/(K mol) Die spezifische Wärmekapazität ist: Die Debye-Temperatur TD hängt vom Material ab: 3N k B 3 N k B 3k B cV = = = M NmAt mAt Stoffe mit großen Atommassen haben geringe spezifische Wärmekapazitäten! Zahlenwerte Material mAt [u] ρ [g/cm3] cp [J/kgK] C [J/K]1cm3 Messing 67.3 8.4 377 3.17 Aluminium 27.0 2.70 897 2.42 Blei 207.2 11.35 129 1.46 Alumunium Kupfer Zinn Blei TD = 426 K TD = 345 K TD = 195 K TD = 96 K 193 9.3 Kinetische Gastheorie: Gasdruck 194 und damit den Druck: p= Fläche A Druck entsteht durch Impulsübertrag bei Stößen der Gasteilchen mit der Wand F 1 2 m = nmv 2 = n v 2 A 3 3 2 2 2 3 N = nE kin = n k BT = nk BT = k BT 3 3 2 V Die Zustandsgleichung des idealen Gases lautet damit: Gasgefülltes Volumen pV = N k BT Abschätzung der Zahl der Stöße mit der Wand Annahme: alle Teilchen haben die gleiche Geschwindigkeit v und bewegen sich nur in x-, y- oder z-Richtung ⇒ im Zeitraum ∆t treffen 1/6 der Teilchen im Volumen v ∆t A auf die Fläche A 9.3.1 Boltzmann-Verteilung Die Zahl der Stöße ist also 1 z = nv∆tA 6 Der Impulsübertrag dabei ist: 1 ∆p = 2 zmv = nmv 2 A∆t 3 Die erzeugt eine Kraft: F= ∆p 1 = nmv 2 A ∆t 3 Eine genauere Behandlung sollte die statistische Verteilung der Geschwindigkeiten berücksichtigen. n: Teilchendichte n= N At V Im thermischen Gleichgewicht ist die Wahrscheinlichkeit, einen Zustand mit Energie E zu besetzen, gegeben durch f ( E ) = a g e − E / kBT BoltzmannVerteilung g: Zahl der Zustände mit Energie E („Entartung“) a: Normierungsfaktor 195 196 Die kinetische Energie für ein Gasteilchen ist: Verteilung der Geschwindigkeiten der Moleküle in Luft für verschiedene Temperaturen 1 E = mv 2 2 Alle Geschwindigkeitsvektoren zu einer gegebenen Energie bilden also eine Kugelschale im dreidimensionalen Geschwindigkeitsraum. Nimmt man an, dass jeder mögliche Vektor eine endliche Fläche auf dieser Kugelschale ausfüllt, gibt es endlich viele mögliche Vektoren, deren Zahl proportional zur Fläche der Kugelschale (d.h. zu v2) ist. Es gilt hier also g (v ) ∝ v 2 Diskussion: Damit folgt für die Geschwindigkeitsverteilung in einem Gas: Wahrscheinlichste Geschwindigkeit (Maximum von f(v) ): 2 m f (v ) = π k BT 3/ 2 v2 e m − v 2 / kBT 2 Maxwell-Verteilung vw = Mittlere Geschwindigkeit: ∞ Die Normierungsfaktoren sind so gewählt, dass 2k BT m v = ∫ v f (v) dv = 8 k BT π m ∞ 0 0 Mittlere quadratische Geschwindigkeit: ∫ f (v)dv = 1 ∞ v 2 = ∫ v f (v)dv = 0 3k BT m 197 ∞ Damit ist die mittlere kinetische Energie: Ekin = 198 ∫ Normierung: f (vx ) dvx = 1 −∞ m 2 m 2 3k T v = v = B 2 2 2 m Die mittlere quadratische Geschwindigkeit ist dann: vx2 = (3 Freiheitsgrade!) ∞ 2 ∫ vx f (vx )dvx = −∞ f(v) vw <v> <v2> (auch negative Werte möglich!) MaxwellBoltzmannVerteilung also Ekin , x = k BT m k T m 2 vx = B 2 2 Zahl der Stöße auf Fläche A in Zeit ∆t : ∞ Z = ∫ nvx ∆tAf (vx )dvx 0 1 2 v/ 0 3 2 kBT (nur positive vx tragen bei!) m Impulsübertrag bei jedem Stoß: ∆ ps = 2mvx 9.3.2 Berechnung des Gasdrucks v v v x v vx Für den Druck auf die Fläche A zählt nur die Geschwindigkeitskomponente senkrecht zu A (hier vx). Gesamter Impulsübertrag in Zeit ∆t : ∞ ∆ p = ∫ 2mvx nvx ∆tAf (vx )dvx 0 1D Geschwindigkeitsverteilung: 1 f (v x ) = 2π m m − 2 vx2 / kBT e k BT ∞ = 2n∆tAm ∫ v 2x f (vx )dvx 0 = n∆tAk BT (1 Freiheitsgrad!) 199 Der Druck ist damit: p= ∆p N = n k BT = k BT ∆ tA V In der Zeit ∆t ist dann die Energieerhöhung des Gases: 1 6 1 3 1 n = n 3k BT ∆V = k BT ∆V = p∆V = ∆W 3 V ∆ E = Z ∆ ET = nv0 A∆t 2mv0 vK = n mv0 2 AvK ∆t pV = N k B T also Auch bei expliziter Berücksichtigung der statistischen Verteilung der Geschwindigkeiten erhält man das ideale Gasgesetz! Gas p 9.5 1. Hauptsatz Geleistete Arbeit: F A (unabhängig von der Kolbengeschwindigkeit vK!) Die Erhöhung der inneren Energie des Gases (der kinetischen Energie aller Gasteilchen) entspricht der geleisteten Arbeit! 9.4 Druckarbeit ∆x 200 ∆W = F ∆ x = pA ∆ x = p ∆V Für ein System, das an seine Umgebung nur durch Wärmübertrag und Arbeit gekoppelt ist, gilt: Führt zur Erwärmung des Gases! ∆U = ∆Q + ∆W Kolben Mikroskopische Beschreibung: betrachten ideales Gas, Geschwindigkeit aller Gasteilchen v0, nur Richtungen x,y, oder z. Während der Kompression bewege sich der Kolben mit Geschwindigkeit vK; die Gasteilchen werden bei der Reflektion beschleunigt: v ' = v0 + 2 v K vK v0 ∆ ET = v‘ Dies führt zu einem Energiegewinn pro auftreffendem Teilchen: m 2 m 2 m 2 v ' − v0 = ( v0 + 4 v0 v K + 4 v K 2 − v0 2 ) 2 2 2 ≈ 2 mv0 v K (für v K ≪ v0 ) 1. Hauptsatz der Thermodynamik (Energieerhaltung) Zugeführte Wärme (Q) oder am System geleistete Arbeit (W) erhöht die innere Energie (U) des Systems. Andere Formulierung: es gibt kein perpetuum mobile, d.h. eine Maschine, die Arbeit leistet, ohne Energie zu verbrauchen (also ohne die innere Energie des Systems zu senken oder Wärme zugeführt zu bekommen). Falls nur Druckarbeit möglich ist: dU = dQ − pdV ⇒ dQ = dU + pdV 201 202 Bemerkung: W bezeichnet die am System geleistete Arbeit dV < 0 ⇒ dW = − pdV > 0 Volumenverkleinerung: Mit CV = N f kB : 2 Es wird Arbeit am System geleistet Cp = N dV > 0 ⇒ dW = − pdV < 0 Volumenvergrößerung: f f +2 k B + Nk B = N kB 2 2 Isobare Wärmekapazität System leistet Arbeit Hieraus ergibt sich das Verhältnis der beiden Wärmekapazitäten: Beispiel: ideales Gas U = CV T = N Innere Energie: Cp f k BT 2 CV = f +2 =γ f Adiabatenkoeffizient dU = CV dT f dQ = dU + pdV = N k B dT + pdV 2 Damit: 9.5.2 Zustandsänderungen Änderungen eines Systems können unter verschiedenen Bedingungen stattfinden: 9.5.1 Isobare Wärmekapazität Gas p F=konst. A dQ Bei Zuführung der Wärmeenergie dQ dehnt sich das Gas aus und leistet Druckarbeit ⇒ geringere Temperaturerhöhung als bei festem Volumen pdV = n k B dT ⇒ dQ = dU + pdV = CV dT + Nk B dT = ( CV + Nk B ) dT Cp = dQ dT = CV + Nk B p = konst . T konstant V konstant p konstant ∆Q=0 (kein Wärmeaustausch) Für ideale Gase folgt: Isothermer Fall Bei konstantem Druck gilt: ⇒ • isotherm : • isochor : • isobar : • adiabatisch : dW T T konstant ⇒ U konstant (dU=0) ⇒ dQ = − dW = pdV Endliche Volumenänderung: dQ T Wärmebad V V N V k BTdV = Nk BT ln V V0 V0 ∆Q = ∫ pdV = ∫ V0 203 Vom System geleistete Arbeit: 204 Adiabatischer Fall V ∆WS = − ∆W = ∆Q = Nk BT ln V0 dW Die auf das System übertragene Wärmeenergie wird vollständig in Arbeit umgesetzt, die innere Energie ändert sich nicht. kein Wärmeübertrag ⇒ dQ=0 dU = CV dT = dW = − pdV Vom System geleistete Arbeit: ∆WS = −CV ∆T Isolation Isochorer Fall Volumen konstant ⇒ dW=0 ∆Q = ∆U = CV ∆T ⇒ V Für die Änderung von der Temperatur in Abhängigkeit vom Volumen folgt: V Übertragene Wärme wird vollständig in innere Energie umgesetzt (die Temperatur erhöht sich) dQ ⇒ V0 Lösung: Isobarer Fall dQ = dU − dW = CV dT + pdV dW = C p dT p ⇒ dQ Damit gilt auch: p ∆V Nk B ∆WS = −∆W = p∆V = Nk B ∆T ∆Q = C p ∆T = C p C 1 ∆U = CV ∆T = V ∆Q = ∆Q Cp γ Nk ∆WS = B ∆Q Cp Umsetzung der übertragenen Wärme in innere Energie und Arbeit ∆U = CV ∆T = − ∫ p (V , T )dV T V = T0 V0 − 2 f Adiabatengleichung pV T = p0V0 T0 Andere Formulierungen durch Einsetzen des idealen Gasgesetzes p V = p0 V0 − f +2 f p T = p0 T0 V = V0 f +2 2 −γ 205 Beispiel: adiabatische Kompression kann zu starker Temperaturerhöhung führen (hier für Luft) V 1 = V0 20 ⇒ V T = T0 V0 Druckerhöhung dabei: − 2 5 = 300K *3.31 = 994K V p = p0 V0 − 7 5 206 9.6 Wärmekraftmaschinen Wärmeenergie kann in mechanische Arbeit umgewndelt werden; bei zyklischen Prozessen allerdings nicht mit 100% Wirkungsgrad! 9.6.1 Carnot-Prozess = 66.3 bar Beschreibt eine idealisierte Wärmekraft-Maschine. Ein Zyklus besteht aus 4 Schritten: 1. T1 vom System geleistete Arbeit: 9.5.2 Adiabatische Kompressibilität Aus p V = V0 p0 − Wärmebad 1 1 γ 1 − −1 Adiabatische Expansion V2 → V3 T1→T2 ⇒ 1 dV 1 1 V = − − V dp V γp vom System geleistete Arbeit: ∆W2 = − ∆U = CV (T1 − T2 ) auf das System übertragene Wärme: Damit ist die adiabatsiche Kompressibilität: κ =− V2 V1 ∆Q1 = ∆W1 2. dV 1 p 1 V = V0 (− ) = (− ) 1 − dp γ γ p p0 γ ∆W1 = Nk BT1 ln auf das System übertragene Wärme: ∆W1 γ folgt Isotherme Expansion V1 → V2 T1 ∆Q2 = 0 ∆W2 3. Isotherme Kompression V3 → V4 T2 vom System geleistete Arbeit: T2 Wärmebad 2 1 κ= γp ∆W3 ∆W3 = Nk BT2 ln V4 V3 (<0!) auf das System übertragene Wärme: ∆Q3 = ∆W3 (<0!) 207 Adiabatische Kompression V4 → V1 4. T2→T1 208 Der Wirkungsgrad (geleistete Arbeit durch zugeführte Wärme) ist damit: vom System geleistete Arbeit: ∆W4 = − ∆U = −CV (T1 − T2 ) η= auf das System übertragene Wärme: ∆Q4 = 0 ∆W4 Der Wirkungsgrad ist immer kleiner als 1 (und umso größer, je größer das Verhältnis der Temperaturen der Wärmebäder T1/T2 ist) Bei den adiabatischen Schritten gilt: V3 T2 = V2 T1 ⇒ − V2 V3 = V1 V4 f 2 ∆WS T1 − T2 T = =1− 2 ∆Q1 T1 T1 und V1 T1 = V4 T2 bzw. ln − f 2 V2 V = − ln 4 V1 V3 Dieser für den Carnot-Prozess gefundene Wirkungsgrad gilt allgemein; es gibt keinen Wärmekraftprozess, der einen besseren Wirkungsgrad hat. Schematisch: Wärmebad 1 Es gilt: Die vom System geleistete Arbeit ist also: ∆WS = ∆W1 + ∆W2 + ∆W3 + ∆W4 V V = Nk BT1 ln 2 + CV (T1 − T2 ) + Nk BT2 ln 4 − CV (T1 − T2 ) V1 V3 V2 = Nk B (T1 − T2 ) ln V1 T1 Q1 Carnot-Prozeß C Q2 Die dem Wärmebad 1 entnommene Wärmeenergie ist: V ∆Q1 = ∆W1 = Nk BT1 ln 2 V1 Q1 = W + Q2 T2 Wärmebad 2 W W = η Q1 Die Wärmebad 1 entnommene Wärme wird teilweise in Arbeit umgewandelt und teilweise Wärmebad 2 zugeführt. 209 Auftragung im pV-Diagramm Der Stirling-Prozeß hat einen etwas schlechteren Wirkungsgrad, weil bei der Verringerung der inneren Energie in Schritt 2 keine Arbeit geleistet wird. p Carnot-Prozeß V1 Adiabaten p = p0V0γ ∆W V2 T2 210 1 Vγ Auftragung im pV-Diagramm p Stirling-Prozeß 1 Isothermen p = Nk BT V T1 T1 V4 V4 T2 V1 ∆W V Isothermen Fläche unter den Kurven: ∫ pdV V2 (vom oder am Systen geleistete Arbeit) ⇒ die im pV-Diagramm umlaufene Fläche ist die pro Zyklus geleistete Arbeit ∆W V 9.6.3 Kältemaschinen 9.6.2 Stirling-Motor Die adiabatischen Schritte des Canot-Prozesses werden hier durch eine einfache isochore Temperaturänderung des Arbeitsmediums ersetzt. Umkehrung des Vorgangs: es wird Arbeit am System geleistet, und dabei Wärme aus dem unteren ins obere Wärmebad „gepumpt“. T1 Damit ergeben sich die folgenden vier Schritte: Q1 = W + Q2 Es gilt: Q2 = Q1 − W = Q1 1. 2. 3. 4. Isotherme Expansion Isochore Temperaturänderung Isotherme Kompression Isochore Temperaturänderung W Q2 ⇒ T2 Q2 = 1 η W −W T2 W T1 − T2 211 Je höher T1 und je niedriger T2, desto mehr Arbeit muß geleistet werden, um eine bestimmte Wärmemenge aus Wärmebad 2 zu entfernen. Bemerkung: Q1 ist immer größer als Q2 ! Ein offener Kühlschrank (mit Wärmetauscher im selben Raum) kühlt daher nicht, sonderen erwärmt den Raum. 212 S nimmt nach dem Zyklus wieder den gleichen Wert an! Es handelt sich um eine Zustandsgröße (beschreibt den Zustand eines Systems unabhängig davon, wie dieser erreicht worden ist). Entropie S Definition: dS = Für diese gilt: 9.7 Entropie Beim Carnot-Prozeß sind die pro Zyklus übertragenen Wärmen: dQrev : bei einem reversiblen V ∆Q1 = Nk BT1 ln 2 V1 Prozeß übertragene Wärme 9.7.1 Entropie ideales Gas V ∆Q2 = − Nk BT2 ln 2 V1 Damit ist aber Für die Größe Bei der isothermen Expansion gilt: ∆Q2 ≠ − ∆Q1 ∆Q2 T2 =− ∆S = ∆Q1 T1 ∆Q T dQrev T ∆W = −∆Q = − Nk BT ln bzw. ∆Q2 T2 + ∆Q1 T1 =0 ⇒ ∆S = ∆Q T = Nk B ln V V0 V V0 Bei der isochoren Temperaturänderung gilt: gilt also: ∆ S zykl = ∆ S1 + ∆ S 2 = 0 dQ = dU + pdV = dU = CV dT ⇒ dS = dQ CV = dT T T (am System geleistete Arbeit) 213 214 T also CV T dT = CV ln T T0 T0 ∆S = ∫ (falls CV konstant ist) Einen beliebigen T,V-Zustand (womit auch p festgelegt ist) kann man z.B. durch Änderung erst von V, dann von T erreichen. Beispiel: isotherme Expansion eines idealen Gases V1 V2 Wahrscheinlichkeit für ein Teilchen in V2, sich in einem Teilvolumen mit Ausdehnung V1 aufzuhalten: Damit ist die Entropie dieses neuen Zustands: p= S = S0 + CV ln T V + Nk B ln T0 V0 Entropie des idealen Gases Wahrscheinlichkeit für N Teilchen, sich alle in V1 aufzuhalten: 9.7.2 Statistische Bedeutung der Entropie Für die Entropie zweier Zustände eines Systems gilt: S1 P = Nk B ln 1 S2 P2 V1 V2 Pi: Wahrscheinlichkeit des Zustands (da ungeordnete Zustände häufig wahrscheinlicher sind als geordnete, ist die Entropie auch ein Maß für die „Unordnung“) Diese Definition erlaubt es, die Entropie durch Abzählung der „Mikrozustände“ zu einem Zustand zu berechnen. V P = 1 V2 N Ordnet man auch dem Zustand „alle Teilchen in V2“ eine Wahrscheinlichkeit zu, erhält man: N V P1 = 1 P2 V2 Die Entropieänderung bei Volumenzunahme ist damit: ∆S = S 2 − S1 = k B ln PV2 − k B ln PV1 PV2 N V V = k B ln = k B ln( 2N ) = Nk B ln 2 PV1 V1 V1 Es ergibt sich das gleiche Ergebnis! 215 9.8 2. Hauptsatz 216 ∆ S1 = − Entropieänderung Wärmebad 1: Bei spontanen Zustandsänderungen eines abgeschlossenen Systems gilt: ∆S ≥ 0 2. Hauptsatz der Thermodynamik T1 ∆Q2 1 Entropieänderung Wärmebad 2: ∆ S 2 = = ( ∆Q1 − ∆W ) T2 T2 In der statistischen Betrachtung: ein System geht nicht von selbst in einen unwahrscheinlicheren Zustand über! (bis auf statistische Schwankungen, die zu geringen negativen ∆S führen können. Im thermodynamischen Limit, d.h. für unendlich große Systeme, geht die relative Amplitude dieser Schwankungen gegen Null). Ein Vorgang ist reversibel, wenn er durch infinitesimale Änderung eines Parameters umgekehrt werden kann. Definition: irreversible Vorgänge ∆S > 0 η < ηCarnot Bei abgeschlossenes System T1 Q1 C Q2 W ∆Q1 = ∆Q2 + ∆W T2 wird ∆W = η∆Q1 Arbeit kann gespeichert werden, z.B. durch adibatische Kompression eines Gases (∆Q=0 ⇒ ∆S=0 ) = 1 ∆Q1 T1 ∆Q2 > ∆Q2Carnot ∆ S 2 > − ∆ S1 fl ∆S > 0 Beispiel: Expansion eines Gases adiabatische (reversible) Expansion dW Beispiel: Carnot-Prozeß 1 1 T (1 − η ) ∆Q1 = 2 ∆Q1 T2 T2 T1 Der Carnot-Prozeß ist reversibel! Für einen Kraftwärmeprozeß mit schlechterem Wirkungsgrad gilt dies nicht: fl ∆S = 0 = ∆ S = ∆ S1 + ∆ S 2 = 0 Zusammen: Für das Gesamtsystem gilt: reversible Vorgänge ∆Q1 Gas ∆Q = 0 Schieber (instantan geöffnet) Gas ⇒ ∆S = 0 irreversible Expansion ideales Gas: ∆ S = Nk B ln V2 >0 V1 217 9.9 Einschub: Wärmetransport Beispiel: Temperaturausgleich System A ∆Q T1 Entropieänderung System A: Entropieänderung System B: Zusammen: 218 System B T1 > T2 T2 ∆ S1 = − ∆S2 = ∆Q Zwei Systeme unterschiedlicher Temperatur tauschen Wärme aus; es wird immer mehr Wärme vom warmen auf das kalte System übertragen als umgekehrt. Bei Temperaturgleichheit ist der resultierende Wärmetransport Null. Es gibt drei Arten von Wärmetransport: T1 • Wärmeleitung • Konvektion (in Gasen und Flüssigkeiten) • Wärmestrahlung ∆Q T2 1 1 − >0 T 2 T1 ∆ S = ∆ S1 + ∆ S 2 = ∆Q 9.9.1 Wärmeleitung In Gasen, Flüssigkeiten und Festkörpern tauschen die Teilchen durch Stöße (im Wesentlichen) kinetische Energie aus. In wärmeren Bereichen haben die Teilchen höhere kinetische Energien ⇒ Energie wird von wärmeren in kältere Bereiche transportiert. Irreversibler Vorgang! Damit legt der zweite Hauptsatz die Richtung des Wärmetransports fest: Wärme wird immer vom heißen zum kalten System übertragen! Beispiel: Gas bei geringem Druck T1 3 Ekin = k BT1 2 T2 3 Ekin = k BT2 2 Annahme: die Gasteilchen stoßen inelastisch mit den Wänden und nehmen deren Temperatur an ⇒ bei jedem Stoß auf die rechte Wand wird die Energie 3 k B (T1 − T2 ) 2 übertragen. 219 220 Jeder Stoß auf die linke Wand übeträgt die Energie 3 2 Zahlenwerte (0º C): k B (T2 − T1 ) Gesamtwärmetransport: 3 Qɺ = Zɺ k ∆T 2 B Material λ [W/mK] Ag 420 Pb 36 Quartz 1,4 Wasser 0,54 Luft 0,024 Zahl der Stöße pro Zeit Gilt nur bei niedrigem Druck; bei höherem Druck finden Stöße auch im Volumen statt; damit wird die pro Stoß auf die Wand übertragene Energie geringer. Bemerkung: dieses Gesetz läßt sich auf eine beliebige Temperaturverteilung erweitern. Der Wärmestrom in einem isotropen Material ist gegeben durch jth = −λ∇T Im Festkörper und in Flüssigkeiten gibt es zwei Formen der Wärmeleitung: bei allen Stoffen: bei leitenden Stoffen: durch Atombewegung durch Elektronenbewegung Allgemein gilt für den Wärmetransport durch ein Volumen: 9.9.2 Konvektion Strömung von Flüssigkeiten oder Gasen zwischen Bereichen unterschiedlicher Temperatur, verursacht durch Wärmeausdehnung und Schwerkraft. Führt häufig zu sehr viel stärkerem Wärmetransport als reine Wärmeleitung. l T1 Gas, Flüssigkeit, Feststoff T2 Querschnittsfläche A A Qɺ = λ ∆T l λ: Wärmeleitkonstante A: Querschnittsfläche l: Länge T1 T2 T1 T2 (hängt ab von Ausdehnungskoeffizienten, Wärmekapazität, Dichte, Viskosität, Geometrie fl nicht einfach zu beschreiben) kaltes Medium wird aufgewärmt und steigt auf 221 9.9.3 Wärmestrahlung 222 9.10 Alternative Formulierung 2. Hauptsatz Jeder Körper strahlt Wärmestrahlung ab; die abgestrahlte Leistung ist etwa: „Es gibt keine periodisch arbeitende Maschine, die Arbeit leistet und dabei nur ein Wärmebad abkühlt“ P = ε Aσ T 4 D.h. es gibt kein sogenanntes perpetuum mobile 2. Art. ε : Emissivität (0 < ε <1) A : Oberfläche σ : Stefan-Boltzmann-Konstante σ = 5.7 10-8 Wm-2K-4 Die Formel gilt exakt für den idealen schwarzen Körper (ε=1); bei anderen Oberflächen wird ein wellenlängenunabhängiger Wert von ε < 1 angenommen - dies ist aber eine Näherung. P1 T2 T1 P2 Flächengröße A (ein perpertuum mobile 1. Art ist eine Maschine, die Arbeit leistet, ohne Energie aufzunehmen) Zusammenhang mit der Aussage, dass die Entropie nur zunehmen kann: gäbe es die oben beschriebene Maschine, ließe sich damit die Entropie eines geschlossenen Systems erniedrigen. Beweis: Von der Fläche 1 abgestrahlte Leistung: 4 P1 = ε1 Aσ T1 Von der Fläche 2 aufgenommene Leistung: 4 P12 = ε 2ε1 Aσ T1 Das perpertuum mobile 2. Art ließe sich mit einem CarnotProzeß koppeln. T1 Q1 Q‘1 P2 C W Q‘2 Analoges gilt für den Energietransport von 2 nach 1. Damit ist die transportierte Leistung: Genauer: berücksichtigt man, dass die nicht absorbierte Leistung reflektiert wird, erhält man: εε 1 2 ε1 + ε 2 − ε1ε 2 Aσ (T14 − T24 ) Q '1 = Q '2 + W = Q '2 + Q1 also T2 P = ε1ε 2 Aσ (T14 − T24 ) P= Carnot Die in das obere Wärmebad eingebrachte Wärme wäre dann: Q '1 > Q1 Das obere Wärmebad würde immer wärmer werden! Entropieänderungen: ∆S2 = − Q '2 1 T2 1 =− W =− Q1 T2 T2 T1 − T2 T1 − T2 223 ∆ S1 = − 1 Q1 Q '1 Q 1 1 + =− 1+ W = − Q1 T1 T1 T1 T1 − T2 T1 − T2 T1 Zusammen: ∆ S = ∆ S1 + ∆ S 2 = − Q1 <0 T1 dU ≤ d (TS ) − SdT − pdV Q1 Q2 1 1 − η Q1 = 0 + = − + T1 T2 T1 T2 Bei einem η >ηCarnot wäre also ∆ S < 0 ∆S = − 9.11 Zustandsfunktionen dU ≤ TdS − pdV d (U − TS ) ≤ − SdT − pdV F = U − TS Für diese gilt offenbar: Freie Energie dF ≤ − SdT − pdV (Gleichheit bei reversiblen Vorgängen!) Die von einem System isotherm geleistete Arbeit ist: Für beliebige Zustandsänderungen eines System gilt: folgt damit: ⇒ Wir definieren eine neue Zustandsfunktion: Bei dem Carnot-Prozeß ist wie schon gezeigt dU = dQ + dW = dQ − pdV d (TS ) = SdT + TdS Eingesetzt in obige Gleichung: „Es gibt keine Wärmekraftmaschine, die einen besseren Wirkungsgrad hat als der Carnot-Prozeß“ Zusammen mit dem 1. Hauptsatz Diese Aussage läßt sich mithilfe eine Koordinatentransformation (Legendre-Transformation) neu formulieren. 1. Es gilt: Alternative Formulierung: dQ dS ≥ T 224 (Gleichheit bei reversiblen Vorgängen!) dWS = pdV ≤ − dF − SdT = − dF =0 Die isotherm geleistete Arbeit ist also maximal die Abnahme der freien Energie! Im isotherm-isochoren Fall gilt: dF ≤ − SdT − pdV = 0 Bei festem T,V kann sich die freie Energie nur verringern; im Gleichgewicht nimmt F den kleinstmöglichen Wert an. 225 d ( pV ) = pdV + Vdp 2. Es gilt: 226 3. Setzt man d (TS ) = SdT + TdS Eingesetzt in obige Gleichung: dU ≤ TdS − d ( pV ) + Vdp ⇒ in obige Gleichung ein, ergibt sich: d (U + pV ) ≤ TdS + Vdp dU ≤ d (TS ) − SdT − d ( pV ) + Vdp ⇒ Wir definieren die Zustandsfunktion: H = U + pV Für diese gilt: d ( pV ) = pdV + Vdp Wir definieren die Zustandsfunktion: Enthalpie dH ≤ TdS + Vdp d (U − TS + pV ) ≤ − SdT + Vdp G = U − TS + pV (Gleichheit bei reversiblen Vorgängen!) Im isentropen-isochoren Fall gilt: dH ≤ TdS + Vdp = 0 Für diese gilt: dG ≤ − SdT + Vdp Freie Enthalpie (Gleichheit bei reversiblen Vorgängen!) Im isotherm-isochoren Fall gilt: Bei festem S,V kann sich die Enthalpie nur verringern und nimmt im Gleichgewicht den kleinstmöglichen Wert an. dG ≤ 0 G wird im Gleichgewicht minimal. Bemerkung: die Enthalpie wird in der Chemie häufig verwendet, da viele Prozesse isobar ablaufen. Z.B. gilt bei dem isobaren, reversiblen Verdampfen einer Substanz: dH = TdS + Vdp = TdS = dQ Die Verdampfungsemthalpie ist also einfach die für das Verdampfen (einer bestimmten Stoffmenge) benötigte Wärme. Bemerkung: Es gilt immer Aber nur im einfachsten Fall ist dU = dQ + dW dW = − pdV Es sind weitere Formen von Arbeit möglich, mit denen das System an die Umgebung koppeln kann. 227 z.B.: Zusammenfassung dW = −σ dA Arbeit gegen die Oberflächenspannung dW = HdM Änderung der Magnetisierung im magnetischen Feld dW = µ dN Änderung der Teilchenzahl (µ: chemisches Potential) etc. Hierbei gilt immer: die Arbeit ist das Produkt einer intensiven und einer extensiven Größe. intensiv: extensiv: unabhängig von der Systemgröße (T, p, µ) proportional zur Systemgröße (S, V, N) Damit gilt bei variabler Teilchenzahl: dU = dQ − pdV + µ dN Und bei reversiblen Vorgängen: dG = − SdT + Vdp + µ dN Isotherm-isochor: 228 dG = µ dN Die freie Enthalpie entspricht also dem chemischen Potential aller Teilchen (für T,p konstant). Bei reversiblen Zustandsänderungen gilt („einfache Systeme“): 1 dQ T dU = TdS − pdV Entropie dF = d (T − US ) = − SdT − pdV Freie Energie dH = d (U + pV ) = TdS + Vdp Enthalpie dG = d (U − TS + pV ) = − SdT + Vdp Freie Enthalpie dS = Damit gilt auch: ∂F ∂G S = − = − ∂T V ∂T p ∂U ∂F p = − = − ∂V S ∂V T ∂H ∂G V = − = − ∂p S ∂p T Innere Energie 229 9.13 Reale Gase 9.12 3. Hauptsatz Bisher wurde Entropie nur relativ definiert. Der dritte Hauptsatz legt den absoluten Wert fest. T →0 Reale Gase zeigen eine Abweichung vom idealen Verhalten wegen der Wechselwirkung der Gasteilchen untereinander. Näherungsweise lassen sie sich beschreiben durch die Van-der-Waals-Gleichung: Für reine, kristalline Stoffe gilt: lim S (T ) = 0 230 3. Hauptsatz der Thermodynamik N2 ( p + a 2 )(V − Nb) = Nk BT V „Binnendruck“ „Kovolumen“ (bei T=0K gibt es keine „Unordnung“ mehr) Daraus folgt direkt: T = 0K ist nicht erreichbar! Abkühlung ist nur möglich durch den Kontakt mit einem Wärmebad oder durch adiabatische Prozesse. In erstem Fall wird die (endliche) Temperatur des Wärmebads angenommen (worraus ein endlicher Wert für die Entropie folgt), in zweitem kann die Entropie nur gleich bleiben, aber nicht verkleinert werden. Damit ist S=0 nicht erreichbar, und folglich auch T=0K nicht. Der Binnendruck ensteht durch die Anziehung der Teilchen untereinander (van-der-Waals-Wechselwirkung) und erhöht die Kompression des Gases. Das Kovolumen beschreibt die endliche Ausdehnung der Teilchen, aufgrund derer das Gas nicht beliebig dicht zusammengepresst werden kann. Aufgelöst nach dem Druck: Nk BT a N 2 p= − V − Nb V 2 Kritischer Punkt Flüssigkeit Phasengemisch Gas 231 Für die innere Energie eines van-der-Waals-Gases gilt: 232 f N2 U = N k BT − a 2 V gilt dann: ∂H dT = − ∂V ∂H dV ∂T Die innere Energie ist volumenabhängig! Dies führt zu Temperaturänderungen bei der Expansion. ⇒ 9.13.1 Joule-Thomson-Effekt „Entspannung“ (Expansion) eines realen Gases. F1 F2 An einem strömenden Gasvolumen V1 wird die Arbeit geleistet: p1V1 p1 p2 Düse oder poröse Wand Es leistet die Arbeit: Für das van-der-Waals-Gas also: f N 2 Nk BT N2 H = N k BT − a + − a 2 V 2 V V − Nb V p2V2 Die Differenz muss die innere Energie verändern: ⇒ U1 + p1V = U 2 + p2V2 V N2 f = Nk BT − − 2a V 2 V − Nb Damit: H1 = H 2 Die Enthalpie bleibt erhalten! Anders ausgedrückt: dH = 0 Temperaturänderung bei isenthalper Volumenänderung H = U + pV Es ist U 2 − U1 = p1V1 − p2V2 Umgeformt: ∂H ∂H dV + dT ∂V ∂T ∂H ∂H dV = − dT ∂V ∂T dH = Mit − Nb N2 ∂H Nk BT + 2a 2 2 dT V Nb V ( ) − = − ∂V = − ∂H V dV f Nk B − ∂T 2 V − Nb 233 Mit Nb ≪ V wird dies: dT NbT − 2aN / k B = dV f 2 − 1V 2 Für große Temperaturen ist der Zähler positiv; die Temperatur nimmt bei Volumenvergrößerung zu. Bei kleinen Temperaturen ist der Zähler negativ; die Temperatur nimmt ab. Die Grenze zwischen beiden Bereichen ist die Temperatur: Ti = 2a kBb Inversionstemperatur