lsg_oc1_12_08
Werbung

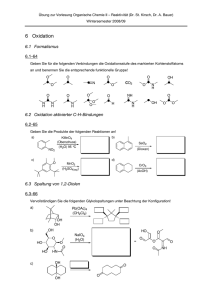
Übungslösungen Organische Chemie 1 (8) 8.1 Der aktivierte Aromat wird para zu einer OH- und meta zur Carboxygruppe bromiert. Letztere wird in einer HCl-katalysierten Fischer-Veresterung mit Methanol umgesetzt (kat. Mengen von SOCl2 sind ein ausgezeichnete Methode zur Hestellung von wasserfreiem HCl in MeOH; erkläre!). Die Brenzcatechin-Einheit wird mit Diphenylmethylendichlorid in ein Acetal überführt, das die nachfolgende basische Verseifung des Esters unbeschadet übersteht. CO2H OH CO2H OH Br2 AcOH OH Br kat. SOCl2 MeOH OH CO2Me Br CO2Me OH Br Ph2CCl2, 160° OH CO2H O Ph LiOH O Ph THF/H2O 1:1 Br O Ph O Ph 8.2 Zur Einführung der Nitrogruppe wird das Anilin zunächst durch Acetylierung gegen Oxidation geschützt. Die Acetamidogruppe wirkt immer noch aktivierend (wenngleich weniger stark als die Aminogruppe) und o,p-dirigierend. Es wird mit Nitriersäure nitriert, und anschliessend wird die Aminogruppe durch Hydrolyse des Acetanilids entschützt. Der resultierende Gewinn an Aktivierung reicht für eine zweifache Bromierung in o-Stellung zur Aminogruppe. Es wird mit in situ hergestellter salpetriger Säure diazotiert, und die Diazoniumgruppe wird mit Cu(I)-Bromid über eine radikalische Zwischenstufe durch ein weiteres Bromatom ersetzt (Sandmeyer-Reaktion), wobei das Redoxpaar Cu+/Cu2+ eine wichtige Rolle spielt. O NH2 O O HN NHAc O HNO3/H2SO4 – AcO– – H2O SEAr Br NaNO2, H2SO4 – 2 H2O N+ H3O+ NO2 Br –H – AcOH 2 Br2 NO2 Na+ Br – 2 HBr SEAr Br NO2 Br N Br CuBr, (HBr) SO42– O2N NH2 NH2 – Na+, – N2, – Cu+, – SO42– O2N Br 8.3 Die Reaktion ist eine E1-Eliminierung, bei der das aus dem intermediär gebildeten Carbeniumion austretende Elektrofug kein Proton, sondern das stabilisierte (Hückelaromatische) Tropyliumion ist. Bei der analogen Umsetzung der sekundären und primären Alkohole 1-Tropylpropan-2-ol und 2-Tropylethanol ist die initiale Bildung des Carbeniumions so sehr erschwert, dass die Reaktion nicht mehr abläuft. Verwendet man in den diesen beiden Fällen HCl statt HClO4 als Säure, so erhält man die entsprechenden Chloride als Produkte einer SN2-Reaktion (ClO4– ist im Gegensatz zu Cl– kaum nukleophil). Siehe K. Conrow, J. Am. Chem. Soc. 1959, 81, 5461–5467. 7.6.2017 Organische Chemie I F. Diederich, B. Bernet 1 OH 70% aq. HClO4, MeCN, 23° 1 C+ + – H2O H H 67% Ein Wort der Vorsicht hinsichtlich praktischer Arbeiten: In der oben gezeigten Reaktion entweicht Isobuten als Gas, und als festes Produkt wird Tropyliumperchlorat erhalten. Organische Perchlorate sind im lösungsmittelfreien Zustand im allgemeinen explosiv (Oxidation des organischen Kations durch das sauerstoffreiche Oxoanion des Chlors mit der Oxidationsstufe VII)! So explodierte isoliertes Tropyliumperchlorat bei der Schmelzpunktbestimmung im Kapillarröhrchen. 8.4 Das (harte) Alkylierungsreagenz Et3O+BF4– (cancerogen!) ethyliert N-Methylacetamid am Sauerstoffatom unter Bildung eines protonierten Imidoesters. In saurer wässriger Lösung wird dieser unter milden Bedingungen zum Ethylester hydrolysiert, während er durch die schwache und wenig nukleophile Base Hydrogencarbonat zum Imidoester deprotoniert wird. OEt H3O+ O Et O – Et2O + Et O+ NHMe Et Et N+ Me O – H3N+Me Et +O NHMe H HCO3– – H2O – CO2 OEt NMe 8.5 Die Reaktionssequenz beinhaltet eine wässrig-saure Acetalspaltung sowie eine Paal-Knorr-artige Pyrrolsynthese der resultierenden 1,4-Dicarbonylverbindung. OHC O 30 mol% PPTS, CO2Me O OHC O CO2Me 20 Äquiv. (NH4)2CO3 CO2Me Aceton/H2O 3:1, 4 h Rückfluss DMF, 120 °C, 30 min N H 8.6 Der erste Schritt ist die zweimalige Bildung von Iminiumsalzen mit Formaldehyd und Essigsäure (formulieren Sie das!) und deren Reduktion mit Natriumcyanoborhydrid. So erhält man tertiäre Dimethylamine, während die Methylierung mit MeI zu Trimethylammoniumsalzen führt (rationalisieren Sie das unterschiedliche Verhalten!). Das tertiäre Amin 2 wird mit mCPBA (meta-Chlorperbenzoesäure) zum N-Oxid 3 oxidiert, welches bei 60 °C eine Cope-Eliminierung eingeht. Siehe M. Suzuki, Y. Kawamoto, T. Sakai, Y. Yamamoto, K. Tomioka, Org. Lett. 2009, 11, 653. NH2 N CH2=O, AcOH, CO2t-Bu NaBH3CN, 1 MeCN, RT, 1 h Ph O– N+ CO2t-Bu mCPBA CH2Cl2, RT, 0.5 h Ph 2 CO2t-Bu 3 CO2t-Bu THF, 60 °C, 0.5 h Ph Ph 4 8.7 Es handelt sich um eine Iodlactonisierung mit Rückseitenangriff des Carboxylats am Epiiodoniumion zum gezeigten Produkt als Enantiomerenpaar. O HO 7.6.2017 I2 + Me I – I– H – H+ H O O H Organische Chemie I rac Me I H H O F. Diederich, B. Bernet O rac 2





![[Cu{C2H4(NH2)2}2][CuI2]2 - chemie.uni](http://s1.studylibde.com/store/data/002538470_1-50622418e8086ee1fd60bf91727579d9-300x300.png)



