61 - Medi
Werbung

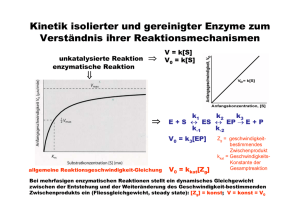
4.7.4 Geschwindigkeit ­enzymatisch katalysierter Reaktionen Beispiel Wenn der Läufer A (Enzym A) über 100 m mit halbmaximaler Geschwindigkeit deutlich schneller (höhere Affinität, KM kleiner) ist als beim 100-m-Hürdenlauf, ist klar, dass er sich eher auf diese Strecke spezialisiert. Substrat A würde also von Enzym A eher umgesetzt werden als Substrat B. Merke! Kann ein Enzym mehrere Substrate umsetzen, wird vorwiegend das Substrat zum Produkt umgewandelt, für das das Enzym den niedrigeren KM-Wert, also die höhere Affinität, besitzt. Michaelis-Menten-Gleichung: Zur MichaelisMenten-Gleichung gibt es eine gute und eine schlechte Nachricht. Die schlechte Nachricht: Ihre Ableitung ist wahnsinnig kompliziert. Sie ergibt sich aus der Reaktionsgleichung k1 k2 k3 E + S ES EP E + P unter Berücksichtigung der einzelnen Geschwindigkeiten k1-3. Jetzt die gute Nachricht: Du musst sie nicht können. Worauf es ankommt, ist ihr Ergebnis: V = Vmax [S] KM + [S] Aus dieser Gleichung lässt sich nämlich die Reaktionsgeschwindigkeit in Abhängigkeit von der Substratkonzentration ableiten. Dabei unterscheidet man drei Fälle: 1. Die Substratkonzentration ist deutlich niedriger als KM (S << KM): V = Vmax [S] KM + [S] wird zu V = Vmax [S] KM Da die Addition von [S] zu KM den Wert im Nenner nicht wesentlich erhöht und somit vernachlässigt werden kann. Da Vmax und KM Konstanten sind, lässt sich die Reaktionsge- www.medi-learn.de schwindigkeit nur durch Erhöhung der Substratkonzentration steigern. Bei niedriger Substratkonzentration ist die Reaktionsgeschwindigkeit V also der Substratkonzentration annähernd proportional. 2. Die Substratkonzentration ist gleich KM (S = KM): In diesem Fall kannst du die Addition im Nenner (KM + [S]) zu 2 ∙ [S] zusammenfassen: [S] V = Vmax wird zu KM + [S] V = Vmax [S] 2[S] oder V = 1 2 Vmax 4 Wie auf S. 59 beschrieben, läuft eine Reaktion, bei der die Substratkonzentration dem KM-Wert entspricht, mit halbmaximaler Geschwindigkeit (V = ½ Vmax) ab. 3. Die Substratkonzentration ist deutlich größer als KM (S >> KM): Jetzt kannst du im Nenner bei der Gleichung (KM + [S]) KM vernachlässigen. V = Vmax V = Vmax [S] KM + [S] [S] [S] wird zu oder V = Vmax Bei hohen Substratkonzentrationen ist die Reaktionsgeschwindigkeit gleich der Maximalgeschwindigkeit. Lineweaver-Burk-Diagramm: Eine andere Möglichkeit, die Reaktionsgeschwindigkeit in Abhängigkeit von der Substratkonzentration aufzutragen, ist das Lineweaver-Burk-Diagramm. Man erhält es durch (wieder sehr komplizierte) Umformung der Michaelis-Menten-Gleichung. Im Wesentlichen werden Kehrwerte gebildet. Es resultiert eine typische Geradengleichung nach dem Muster y = Ax + B: K 1 = M V Vmax 1 1 + [S] Vmax 61