Preparation and Crystal Structure of LiAg30 2 Darstellung und
Werbung

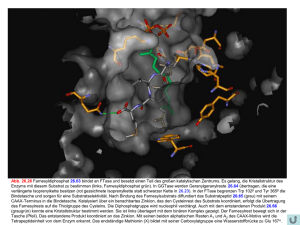
Darstellung und Kristallstruktur von LiAg30 2 Preparation and Crystal Structure of LiAg 30 2 M a r t in J a n s e n Institut für Anorganische und Analytische Chemie der Justus Liebig-Universität Gießen (Z. Naturforsch. 30 b, 854-858 [1975]; eingegangen am 25. August 1975) High Oxygen Pressure Syntheses, Crystal Structure The new oxide LiAg302 was prepared using oxygen pressures of about 300 at. The crystal structure, determined by single crystal X-ray investigations, consists of branched O-Ag-O-Ag chains; Li is coordinated by distorted, edge-sharing oxygen tetrahedra. The space group is Ibam; a — 5.974 Ä, b — 9.945 A, c = 5,694 Ä. Der Born-Haber-Zyklus für binäre und ternäre Silberoxide zeigt, daß die hohe Sublimations­ enthalpie des metallischen Silbers die Bildungs­ wärmen dieser Verbindungen erheblich erniedrigt1. So läßt sich bei der Synthese von Oxiden wie LiAgO 2 oder KAgO 3 die Ausscheidung von metal­ lischem Silber nur durch sehr sorgfältige Tempera­ turführung vermeiden, während Umsetzungen von Ag20 mit den weniger ,basischen' Erdalkalioxiden die Anwendung extrem hoher Sauerstoffdrucke er­ fordern4-5. Auch die bislang beschriebenen Möglich­ keiten zur Synthese von z.B. AgCo02 6-7 beruhen auf der Anwendung hoher 0 2- bzw. 02 /H 2 0 -Drucke. Aufgrund dieser Erfahrungen erscheinen Versuche zur Darstellung der bisher unbekannten alkaliarmen ternären Oxide des Silbers und solcher mit formal höherwertigem Silber nur dann erfolgver­ sprechend, wrenn Sauerstoffdrucke verwendet wer­ den, die den Gleichgewichtsdruck über Ag20 bei der jeweiligen Reaktionstemperatur übersteigen. I. Experimentelle Untersuchungen, Eigenschaften der Proben Unter Ausnutzung der Beobachtung, daß der Sauerstoffdruck über einem Gemenge von KCIO3 und Braunstein (Molverhältnis 10:1) bis zu einer Temperatur von 450 °C ausreicht, um die Zersetzung von Ag20 zu unterbinden, gelang es, AgCo02 auf apparativ einfachem Wege darzustellen8. Bei den Vorversuchen am System Li2 0 /Ag20 mit L i: Ag ^ 1 wurde analog verfahren: In einer zugeschmolzenen Sonderdruckanforderungen an Dr. M a r t i n J a n s e n , Institut für Anorganische und Analytische Chemie der Universität Gießen, D-6300 Gießen, Südanlage 6, BRD. Glasampulle (Supremax) erhitzte man getrennt KC103 /Mn0 2 und das jeweilige Ausgangsgemenge aus Li20 und Ag20 (Ag-Tiegel, 450 °C, 48 h). Es zeigte sich, daß bei einem Li/Ag-Verhältnis von 1:3 eine neue Phase, LiAg3 02 , auftritt. Da die Glasampullen sich nicht immer gefahrlos öffnen ließen und ein definierter Sauerstoffdruck sich auf diese Weise nicht einstellen ließ, verwendete man schließlich Edelstahlautoklaven mit Mano­ meter (Betriebsdaten • Pmax. = 500 atm, V = 38 ml, Tmax. =600 °C). In kristalliner Form erhält man LiAg302 durch dreitägiges Erhitzen von Li20 [aus LiOH (p.a. Merck) dargestellt9] und Ag20 (p.a. Merck) mit Li:Ag = 1,1:3 in einem Korundfingertiegel. Die Temperatur sollte dabei zwischen 450 und 500 °C, der Druck zwischen 250 und 350 atm. liegen. Erhöht man die Reaktionstemperatur auf 550 °C und tempert 14 Tage, lassen sich aus dem Reaktionsprodukt Einkristalle isolieren, die für Röntgenbeugungsuntersuchungen geeignet sind. Rubinrote Kristalle von LiAg302 sind in dünnen Schichten transparent. Besonders in grob kristalli­ ner Form ist es wenig empfindlich gegenüber atmo­ sphärischen Einflüssen. Magnetische Messungen bei Zimmertemperatur zeigen an, daß Diamagnetismus vorliegt. II. Bestimmung der Kristallstruktur Nach Einkristallaufnahmen liegt eine orthorhombische Elementarzelle vor; die Gitterkonstanten wurden durch Ausgleichsrechnung über Guinierdaten bestimmt: a = 5,974 ± 0,004 Ä, b = 9,945 ± 0,005 1, c = 5,694 ± 0,004 Ä, Z = 4, MV = 51,0 cm3 drö = 7,11 g • cm-3 dpyk = 7,04 g • cm- 3 (25 °C). Unauthenticated Download Date | 8/19/17 10:27 PM M. JANSEN • DARSTELLUNG UND KRISTALLSTRUKTUR VON LiAg30 2 Die systematischen Auslöschungen (Reflexe h k l nur mit h - \- k - \- l = 2 n vorhanden, 0 k l nur mit k = 2 n und hOl nur mit h = 2 n ) verweisen auf die Raumgruppen Iba 2 -0 ^ und Ibam-Dj^; die Strukturaufklärung zeigte, daß die zentrosymmetrische Gruppe Ibam vorliegt. Anfangs bestimmte man die c-Achse zu c' =c/2 = 2,847 Ä (Raumgruppe: Cmmm); die Verdoppelung dieser Zelle bewirken 4 sehr schwache Reflexe, die erst nach langer Belichtungszeit (5 Tage) auf Weißenberg- und Drehkristallaufnahmen sichtbar wurden. Bei Versuchen, zunächst die Struktur der Subzelle zu bestimmen, wurden nur die Silberposi­ tionen aufgefunden. Zur Strukturaufklärung wurde ein nach [001] justierter Kristall mit Hilfe eines halbautomati­ schen Zweikreisdiffraktometers (Stadi 2 der Fa. Stoe, MoKa-Strahlung, Graphitmonochromator, scan) vermessen. Für die Schichtlinie mit l = 1 schätzte man die Intensitäten der vier schwachen Reflexe visuell und setzte für die Intensitäten der restlichen, nicht beobachteten Reflexe V3 des m itt­ leren Untergrundes ein. Die Anordnung der Silberteilchen bestimmte man durch Interpretation der Patterson-Synthese; nach Verfeinerung der Silberparameter ließen FourierSynthesen zunächst die Sauerstoff- und schließlich auch die Lithiumlagen erkennen. Die abschließende Verfeinerung aller Teilchen, zu der ausschließlich die gemessenen bzw. beobachteten Reflexe herangezogen wurden, ergab die in Tab. I zusammengestellten Parameter. Der konventionelle i?-Wert beträgt für alle Reflexe mit l = 2 n 0,052. Tab. I. Orts- und Temperaturparameter von LiAg3 0 2, Raumgruppe Ibam, in Klammern: Standardabwei­ chung in Einheiten der letzten angegebenen Stelle. 855 Tab. III gibt die Auswertung einer Guinieraufnahme. Tab. III. LiAg3 0 2, Auswertung einer Guinier-Aufnahme, Eichung mit a_Quarz, CuKa-Strahlung. h k l 1 0 1 2 1 0 2 2 1 0 0 1 2 2 1 3 2 2 1 0 3 3 1 0 3 2 2 1 2 2 0 3 0 2 1 1 4 2 4 3 0 3 1 4 2 5 4 2 3 2 6 1 5 4 2 1 1 5 1 6 3 4 4 0 3 3 1 4 2 6 2 3 0 6 0 0 1 0 0 2 0 1 iS} 2 1 1 2 2 0 0 2 0 2 1 0 3 0 2 1 2 3 2 1 1 0 2 3 0 3 2 sin20O• 103 22,76 24,20 - 66,71 70,81 - 90,79 - 96,08 97,40 - 139,93 144,17 155,70 - 163,88 - 169,41 - 203,93 - 229,19 - 235,98 - 266,30 - 282,78 - 289,53 sin20c * 103 Io Ic 22,66 24,03 59,01 66,60 70,72 73,32 90,63 90,94 95,98) 96,13J 97,36 131,11 139,00 139,92 144,05 155,86 162,73 163,96 166,85 169,45 192,21 203,92 205,66 216,29 229,18 235,13 236,05 237,59 240,18 251,27 264,31 266,40 277,24 277,76 282,89 285,65 289,62 5 3 4,2 2,0 0,4 1,1 1,4 0,4 9,6 - 1 1 - 10 •K - 0,1 6 8 3,9 1,7 9,1 0,1 - 0,1 4 2 1 4,3 1,3 0,7 0,2 1,0 0,5 0,8 0,0 0,5 0,0 0,2 0,8 0,0 4,6 0,0 0,6 1 1 1 1 - 4 - 1 - 0,0 0,0 0,9 0,3 0,0 2 1,8 - 0,0 2 1,3 III. Beschreibung und Diskussion der Kristallstruktur a) Nachbarschaftsverhältnisse Li Ag(l) Ag(2) O 4(b) 4(c) 8(e) 8(j) X y z B [Ä2] 0,5 0 0,25 0,3268 (11) 0 0 0,25 0,0945 (8) 0,25 0 0,25 0 2,3 1,41 1,30 1,44 (6) (2) (2) (15) Tab. II zeigt, daß der Gang der beobachteten und berechneten Strukturfaktoren bei den 4 visuell ge­ schätzten Reflexen der Ebene h k l gut überein­ stimmt, was naturgemäß für die restlichen, nicht beobachteten Reflexe, deren Intensitäten willkür­ lich festgesetzt worden waren, nicht zutrifft. Zu bemerken bleibt, daß die berechneten Struktur­ faktoren dieser Reflexe alle deutlich kleiner sind, als diejenigen der beobachteten Reflexe. Koordinationszahl (C.N.) und Koordinations­ polyeder des einwertigen Silbers in ternären Oxiden hängen entscheidend vom jeweiligen Partnermetall bzw. -nichtmetall a b : liegen diese in sehr viel höhe­ ren Oxydationsstufen als + 1 vor, so werden deren spezifische Koordinationsbedürfnisse - in der Regel unter Ausbildung komplexer Anionen - struk­ turbestimmend (vgl. z.B. Ag2S0 4 ), während in Oxiden mit niedrig geladenen Gegenpartnern die von Ag+ bevorzugte C.N. 2 mit < (O-Ag-O) «180° zum Tragen kommt. Mit zwei nächsten Sauerstoff­ nachbarn (dAg(i)_o = 2 ,1 7 Ä (2 x ); dAg(2>-o = 2 ,1 5 Ä (2 x ); alle Winkel O-Ag-O = 180°; (vgl. Tab. IV) Unauthenticated Download Date | 8/19/17 10:27 PM M. JANSEN • DARSTELLUNG UND KRISTALLSTRUKTUR VON LiAg30 2 Tab. II. Beobachtete (FO) und berechnete (FC) Strukturfaktoren. k 1 0 0 0 0 0 — 339,3 — 359,5 618,4 0 574,0 0 ; — 106,4 — 110,4 0 234,9 252,5 0 287,6 276,9 0 224,2 301,9 141,1 0 138,6 0 104,9 98,6 0 74,1 73,0 0 — 271,3 — 278,6 836,9 0 874,9 0 — 195,8 — 202,3 0 408,1 407,2 0 — 88,2 — 93,5 305,9 0 304,0 0 226,4 209,5 0 153,8 152,6 116,7 0 98,8 0 57,0 59,9 0 777,3 818,6 0 — 218,1 — 216,0 0 557,8 558,4 0 — 143,2 — 139,4 0 253,7 250,2 0 277,3 270,1 0 140,3 144,5 0 175,2 150,3 0 87,7 93,7 0 51,7 48,4 0 — 273,7 — 274,6 0 633,3 645,4 0 — 159,9 — 143,3 336,2 0 312,6 0 — 64,7 — 69,3 0 196,2 191,8 154,4 0 136,2 0 114,9 121,9 0 101,2 81,1 0 510,8 535,3 0 — 176,0 — 160,0 0 408,6 388,1 0 — 100,1 — 96,8 0 197,7 191,8 136,2 0 135,0 0 137,1 137,7 0 103,6 88,5 0 54,0 66,0 0 — 115,0 — 111,7 0 378,5 370,2 0 — 121,6 — 113,3 0 259,6 248,0 0 97,6 101,4 132,2 0 115,4 0 30,7 68,8 0 330,8 329,5 0 — 119,5 — 108,5 0 266,7 247,8 0 — 77,9 — 61,5 0 84,5 84,6 0 63,1 78,1 0 77,7 60,1 1 1 1 1 1 2 2 2 2 2 3 3 3 3 3 4 4 4 4 4 5 5 5 5 5 6 6 6 6 6 7 7 7 7 8 8 8 8 8 9 9 9 9 10 10 10 10 11 11 11 12 12 12 12 13 FO FC FO FC h k l 2 4 6 8 1 3 5 7 0 2 4 6 8 1 3 5 7 0 2 4 6 8 1 3 5 7 0 2 4 6 1 3 5 7 0 2 4 6 1 3 5 0 2 4 6 1 3 5 0 2 4 1 3 0 2 0 2 4 1 3 4 0 0 0 0 1 1 1 1 2 2 2 2 2 3 3 3 3 4 4 4 4 4 5 5 5 5 6 6 6 6 7 7 7 7 8 8 8 8 9 9 9 10 10 10 10 11 11 11 12 12 12 13 13 14 14 14 14 14 15 15 1 2 734,3 737,0 2 — 196,6 — 211,9 2 372,3 392,7 2 — 99,0 — 99,6 2 263,8 266,3 2 272,6 275,3 2 137,7 137,9 2 83,1 97,4 2 903,3 889,6 2 — 267,2 — 279,8 2 509,7 527,2 2 — 127,5 — 122,7 2 221,9 235,5 2 283,5 279,4 2 204,6 202,3 2 167,8 149,6 2 94,5 97,2 2 — 295,6 — 311,3 2 673,2 627,7 2 — 175,3 — 165,4 2 323,2 319,8 2 — 81,7 — 76,4 2 258,3 250,7 2 162,3 145,6 2 150,7 146,6 2 107,3 91,8 2 504,4 554,6 2 — 182,5 — 173,3 2 428,8 428,5 2 — 126,8 — 125,9 2 195,4 189,2 2 133,5 135,6 2 138,4 119,7 2 75,5 79,4 2 — 174,6 — 168,7 2 432,7 435,1 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 0 0 0 0 0 1 — 146,7 276,4 125,0 150,4 76,0 371,1 — 154,4 291,3 — 75,5 102,7 124,6 98,0 — 106,6 270,7 — 102,3 78,6 91,6 208,2 — 55,9 — 105,1 246,5 — 78,4 68,6 50,6 — 13,6 — 128,2 262,7 133,7 134,7 87,6 393,9 — 137,7 284,9 — 70,0 100,8 112,4 67,7 — 95,0 269,4 — 88,5 83,0 76,3 219,3 — 75,7 — 90,2 232,2 — 67,6 68,9 49,3 — 24,0 h k l 2 0 4 4 1 3 5 0 2 4 1 3 5 0 2 4 1 3 0 2 1 3 0 2 2 1 2 1 3 3 1 1 1 2 2 2 3 3 3 4 4 4 5 5 5 5 5 6 6 6 6 6 7 7 7 7 7 8 8 8 8 8 0 1 1 1 2 2 2 3 3 3 4 4 4 5 5 6 6 7 7 8 8 1 2 3 4 2 4 6 8 10 5 7 9 6 8 10 5 7 9 2 4 6 8 10 1 3 5 7 9 2 4 6 8 10 1 3 5 7 9 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 4 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 FO FC — 191,0 405,0 177,0 189,1 108,0 — 159,1 495,5 — 136,3 185,2 154,8 119,5 449,4 — 142,1 384.0 176,3 103,8 — 172,4 447,4 143,6 122,4 371,0 — 122,8 37,3 — 74,9 57,6 — 44,1 9,8 7,5 10,5 15,3 10,2 7,5 — 11,9 — 9,8 — 8,5 — 9,5 — 10,9 — 8,8 13,9 10,9 9,2 9,5 — 10,2 — 11,2 — 12,2 12,2 12,5 10,9 — 11,5 — 12,2 — 11,2 — 11,5 12,2 12,9 9,5 12,2 12,5 12,9 — 13,2 — 13,9 — 199,2 416,0 166,1 178,3 100,9 — 172,1 521,9 — 140,5 173,8 136,8 110,7 500,0 — 144,2 390,2 164,4 103,1 — 175,3 432,7 133,3 99,7 377,7 — 118,9 43,8 — 92,2 61,5 — 48,7 7,0 4,2 18,5 30,7 7,4 7,7 — 26,3 — 17,9 — 1,9 — 3,4 — 0,9 — 5,5 21,1 15,5 22,2 14,8 — 7,3 — 14,4 — 3,8 3,4 5,o 0,9 — 3,6 — 2,8 — 16,5 — 11,4 5,9 12,1 3,4 5,2 8,7 1,4 — 6,0 — 4,9 Unauthenticated Download Date | 8/19/17 10:27 PM 857 M. JANSEN • DARSTELLUNG UND KRISTALLSTRUKTUR VON LiAg30 2 Tab. IV. Abstände [A] und Winkel für LiAg302Li - O -L i - Ag(2) Ag(l) - O -A g (l) - Ag(2) Ag(2) - O - Ag(2) -L i -A g(2) -A g (l) O - Li - Ag(2) -A g (l) -O O - Ag(l) - O O - Ag(2) - O Ag(l) - O - Ag(2) Ag(2) - O - Ag(2) 1,99 2,85 2,90 2,17 2,84 3,23 2,15 2,84 2,90 2,99 3,23 1,99 2,15 2,17 2,80 180° 180° 96,8° 82,8° (4 x ) (2 x ) (4 X ) (2 x ) (2 x ) (8 X ) (2 x ) (2 x ) (2 x ) (2 X ) (4 x ) (2 x ) (2 x ) (110) und zu (110) ausgerichtete Ag604 -Schichtpakete entstehen. Die kristallographisch identischen AgöO-i-Pakete durchdringen sich gegenseitig: Die Kanten der Sechsecke parallel (110) bzw. (llo) durchstoßen die Schichten parallel (110) bzw. (110) jeweils in den Mittelpunkten der Sechsecke bei 0 , 0 , 0 und 1/2, 7 2 , xh bzw. 0 , 0 , V2, und x/2, V2, 0 , vgl. Abbn. 1 und 2. • Li O Ag O 0 (2 x ) entspricht die Umgebung der Silberteilchen in LiAg302 also den Erwartungen, auch wenn die Ab­ stände Ag-0 größer sind als diejenigen in der kubi­ schen Modifikation von Ag20 (dAg_o =2,05 Ä). Lithium ist in Form eines bisphenoidisch verzerrten Tetraeders (zwei kurze Kanten mit 2,80 Ä und vier lange mit 3,41 Ä) von vier Sauerstoffteilchen um­ geben; die Li-O-Abstände wurden zu 1,99 Ä be­ stimmt; sie stimmen mit denen in Li20 überein. O2ist jeweils von 2 Li+ + 3 Ag+ so umgeben, daß die Basis des quadratisch-pyramidalen Koordinations­ polyeders aus zwei cis-ständigen Li- und Ag-Teilchen besteht; an der Spitze befindet sich stets Ag+. In Anbetracht der Tatsache, daß chemisch und kristallchemisch so verschieden geartete Teilchen wie Li+ und Ag+ dieses Polyeder aufbauen, ist die geringe Abweichung der OLi2Ag3-Gruppe von der idealen quadratischen Pyramide erstaunlich. b) Verknüpfungsprinzipien Aus der Formel LiAg3C>2 ergibt sich, daß die AgC>2Gruppen nicht wie in Na 3AgÜ2 10 ,isoliert“ vorliegen können, sondern daß jedes O (wenigstens im Mittel) drei Ag verknüpfen muß. In LiAg302 wird dies durch die Ausbildung eines dreidimensionalen, in sich geschlossenen Netzes von -Ag-O-Ag-OKetten realisiert, die an jedem O eine Verzweigung erfahren. Auf diese Weise entstehen gewellte Sechs­ ringe (,Sesselform‘, Diederwinkel = 98,5°), deren Eckpunkte jeweils durch O und die Kantenmitten durch Ag markiert sind. Diese Sechsringe sind über alle sechs Kanten derart verknüpft, daß parallel zu Abb. 1. Perspektivische Darstellung der Kristallstruk­ tur von LiAg302. Ag f k l • L 0 . '/2 o *= \ \ 0: © z =0 k 11 - Li: A *= Abb. 2. Oben: Projektion der Kristallstruktur von LiAg30 2 längs [001], unten: (llO)-Ebene mit den unmittelbar benachbarten Sauerstoffteilchen. Für den [Li0 2 ]-Teil der Kristallstruktur ergeben sich (tetraedrische Koordination von Li+ voraus­ gesetzt) zwei einfache Verknüpfungsmöglichkeiten: Aufbau eines Raumnetzes durch eckenverknüpfte Tetraeder (etwa analog a-Quarz) oder Ausbildung kanten verknüpft er Tetraederketten (wie z. B. [FeS2]_ in KFeS2). In LiAg30 2 ist die zweite der beiden Möglichkeiten realisiert, die ^ L i02-Ketten erstreckten sich längs [001] (vgl. Abb. 1). Unauthenticated Download Date | 8/19/17 10:27 PM 858 M. JANSEN • DARSTELLUNG UND KRISTALLSTRUKTUR VON LiAg30 2 c) Anordnung der Kationen In LiAg302 treten mehrere ungewöhnlich kurze Metall-Metall-Abstände auf. Wie die Abb. 2 zeigt, sind die Ag+ in zweidimensional dicht gepackten Schichten angeordnet, wobei innerhalb dieser Schichten die Ag-Ag-Abstände 2,84 Ä (2 x ) und 3,23 (4 X ) betragen. Die gesamte Umgebung von Ag (1) innerhalb einer Kugel mit r — 3,23 Ä besteht aus den beiden erwähnten 0 und zehn Ag, diejenige von Ag (2) aus zwei 0 und ebenfalls zehn Metall­ ionen (2 L i-f 8 Ag). Für die teilweise recht kurzen Metall-Metall-Abstände könnte man folgende Er­ klärungen diskutieren: 1 ) Gewöhnlich beobachtet man in ternären Oxi­ den Anionenkontakte, was auf deren Größe und damit auf ihren großen Anteil am Raumbedarf der jeweiligen Verbindung zurückgeführt werden kann. In LiAg302 geht mehr als die Hälfte des Molvolu­ mens auf den Raumbedarf der Kationen (56,5%) zurück, so daß Kationenkontakt nur durch Aufbau einer sperrigen Kristallstruktur vermeidbar wäre. 2) Da jedes Ag von zwei weiteren Silberteil­ chen im Abstand von 2,84 Ä (im metallischen Ag: dAg-Ag = 2,89 Ä) umgeben ist, könnte man Ag-Ag-Bindungen, also Ausbildung eines 1-dimen­ sionalen Ag-Clusters längs [001] diskutieren. Metal­ lische Wechselwirkungen erscheinen wegen der transparent roten Einkristalle unwahrscheinlich, doch sollen zur Sicherheit Leitfähigkeitsmessungen durchgeführt werden. d ) Beziehungen zwischen LiAgzOz und dem antiF lußspattyp LiAg30 2 , ein Oxid vom Typ M2O, läßt eine ge­ wisse strukturelle Verwandtschaft zum Li20 er­ kennen: 1/a der ,Tetraederlücken' der beträchtlich verzerrten kubisch-flächenzentrierten Sauerstoff­ anordnung in LiAg302 ist geordnet mit Lithium be­ setzt; die Silberteilchen (3/4 der Kationen) sind aus den Tetraedermittelpunkten jeweils auf die Tetra­ ederkanten verschoben, so daß die oben beschrie­ 1 Vgl. R. H o p p e , Z. Anorg. Allg. Chem. 296,104 [1958]. 2 R. 3 S c h o l d e r , Angew. Chem. H . S a b ro w sk y u . R . H opp e, 70, 583 [1958]. Z. Anorg. Allg. Chem. 358, 241 [1968]. H.-L. K e l l e r u . Hk. M ü l l e r - B u s c h b a u m , Z. Naturforsch. 28b, 263 [1973]. 5 H.-L. Keller u. Hk. M ü l l e r - B u s c h b a u m , Z. Anorg. Allg. Chem. 393, 266 [1972]. 6 W . S t ä h l i n u . H . R. O s w a l d , Z. Anorg. Allg. Chem. 367, 206 [1969]. 4 bene Zweierkoordination des Silbers zustande­ kommt. Ähnliche Beziehungen bestehen auch zwischen den Strukturen von Na3Ag0210 und Na20; hier sind 3/4 der Tetraederlücken einer kubisch-dichten Sauerstoffanordnung mit Na besetzt, während sich Ag, wiederum aus den Schwerpunkten der restlichen Tetraederlücken herausgerückt, auf den Tetraeder­ kanten befindet11. e) Vergleich m it SrAg^Oi 5 und K A gO 3 Der den Verbindungen LiAg302 = L i 2Agß04 und SrAg604 formal gemeinsame Ag604 -Teil legt nahe, nach strukturellen Beziehungen zwischen beiden zu suchen. Diese sind jedoch nur andeutungsweise vor­ handen : im Gegensatz zu LiAg30 2 sind in SrAgß04 zwei kristallchemisch verschiedene Arten von Ag1+ vorhanden, eine in der -O-Ag-O-Gruppierung ( < O -A g-0: 162, 176 und 180°, dAg-o= 2,08Ä ) eine andere gegenüber O mit C. N. 2 + 2 (dAg_o: 2,34 Ä (2 X) und 2,84 Ä (2 x)). Es liegen folglich unterschiedliche Verknüpfungen in den Ag604-Teilchen der beiden Strukturen vor. Be­ merkenswert ist jedoch, daß für beide Kristall­ strukturen innerhalb der Fehlergrenzen gleiche Ag-Ag-Abstände (SrAgß0 4 : 2,81 und 2,84 Ä; LiAg30 2: 2,84 Ä) bestimmt wurden. Obwohl in KAgO die Verknüpfung der -O-Ag-Onaturgemäß grundlegend von derjenigen in LiAg30 2 verschieden ist, stimmen Abstände und Winkel in den Ag404 -Gruppen und im Ag302-Gerüst von LiAg302 gut überein (vgl. Tab. IV, KAgO: dAg_o = 2,16 Ä, -s(Ag-O-Ag) «90°): es gelingt, aus einem beliebigen 4 X(Ag02/2) Teilstück des Ag60 4 -Gerüstes unter Beibehaltung sämtlicher Winkel und Abstände das [Ag40 4 ]4~-Anion des KAgO zu falten. Die Sauerstoffautoklaven wurden dankenswerter­ weise in der Mechanischen W erkstatt des Institutes unter Leitung von Herrn W. S c h n e i d e r gebaut. Herrn Prof. R u d o l f H o p p e danke ich sehr herz­ lich für anregende Diskussionen und Unterstützung mit Sachmitteln. R . D. S h a n n o n , D. B . R o g e r s u . C. T. P r e w i t t , Inorg. Chem. 10, No. 4, 716 [1971]. 8 M. J a n s e n u . R . H o p p e , Diss. M. Jansen, Gießen 1973. 9 W . K l e m m u . H.-J. S c h a r f , Z. Anorg. Allg. Chem. 303- 263 [I960]; in Anlehnung an D e F o r c r a n d , C. R , Acad. Sei. 146, 802 [1908]. 10 F. S c h e n k u . R . H o p p e , Naturwissenschaften 56, 414 [1969]. 11 R . H o p p e , unveröffentlicht. 7 Unauthenticated Download Date | 8/19/17 10:27 PM