Vorlesung 30.04.09 Immunologie für Biologen, Biochemiker und
Werbung

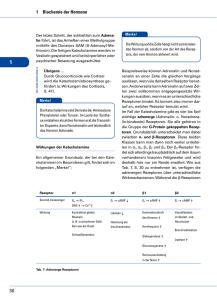
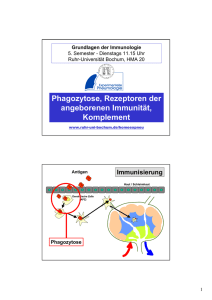
Vorlesung 30.04.09 Immunologie für Biologen, Biochemiker und Molekulare Biotechnologen Sommersemester 2009 Angeborene Immunität Institut für Medizinische Mikrobiologie, Immunologie und Hygiene Direktor: Prof. Dr. Dirk Busch PD Dr. Carsten Kirschning <[email protected]> T.: 4140 4132 Themen I •Barrieren: Mukosale Oberflächen, Epithelien •Zellen: Granulozyten, Monozyten, dendritische Zellen, NK Zellen •Infektion: Adhäsion, Opsonisierung, Phagozytose, antimikrobielle Peptide, reaktive Sauerstoffverbindungen •Pathogen assoziierte molekulare Muster (PAMPs), Mustererkennungsrezeptoren (PRRs), Themen II •PRRs: lösliche / zellgebundene /zytoplasmatische Rezeptoren: LPS bindendes Protein (LBP); Scavenger-, toll-like-Rezeptoren (TLRs); Leuzin reiche Wiederholungsmotiv (LRR)- / Helikasedomäne- tragende Rezeptoren •Botenstoffe: Zytokine, Chemokine, NO •Zellaktivierung, NF-kappaB, mitogen-aktivierte Proteinkinasen; •Komplement: klassischer-, MB-Lektin- und alternativer Signalweg, C3, Mediatoren, Immunkomplexe, Lysis. Erregererkennung durch Immunzellen Mikrobielle und virale Verursacher von Infektionen Bakterien Pilze Viren Protozoa und Würmer Das Immunsystem angeboren (nicht spezifisch) Komponenten: Tage: Zelluläre 0 adaptiv (spezifisch) Humorale 2 Zelluläre 4 INFEKTION Humorale 6 Systeme der Wirtsabwehr Barriere Invasion & Infektion Innate Immunität + + Haut und Schleimhäute Schneller Umbau, Peristaltik, Selbstreinigung durch Sekrete und mukoziliären Transport, etc Zelluläre und humorale Abwehr Makrophagen, Granulozyten, Lysozym, Komplement, Phagozytose, oxidativer Burst, NK Zellen etc Inflammation Adaptive Immunität Zelluläre und humorale Abwehr Antikörper, Zytokine, T Helfer- und zytotoxische T-Zellen, B-Zellen Resistenz durch angeborene und erworbene Immunität Das spezifische Immunsystem ist besonders wichtig für: Kontrolle intrazellulärer Erreger (Tuberkulose, Leishmanien etc.) durch Makrophagen (IFN) Opsonisierung von Bakterien durch Antikörper Lyse virus-infizierter Zellen durch T-Zellen Zeitliche Staffelung von Immunantworten Figure 2-1 Bacteria / pathogen associated molecuar patterns (PAMPs) Erregererneutralisierung durch Phagozytose Phagozytose: Rezeptoren und Signalwege Phagozytose © New Science Press Ltd. 2004 Phagosomenreifung + bakterielle Evasion •Injektion bakterieller Proteine Aufnahme (Salmonella) oder Blockade (Yersinia) ph 7 Transferrinrezeptor Rab5 •Lyse der Phagosomenmembran + •Flucht ins Zytosol (Listeria, Shigella, etc.) Rab7 LAMP1 ph 4.5 •Autophagosom (Legionella, Brucella) •Blockade der Azidifizierung (Mycobacteria) •Blockade lysosomaler Enzyme (Salmonella) Phagozyten NADPH-Oxidase Lekstrom-Himes and Gallin, N Engl J Med, 343:1703, 2000 Sauerstoff-unabhängiges Killing im Phagolysosom Effektor Molekül Funktion Kationische Proteine (Kathepsin) Zerstörung mikrobieller Membranen Lysozym Hydrolyse von Mukopeptiden in der Zellwand Lactoferrin Eisendeprivation des Pathogens Hydrolytische Enzyme (Proteasen) Verdau von killed Organismen Zellanlockung entlang des Gradienten eines chemotaktischen Faktors Leukozytenrekrutierung zum Entzündungsort © New Science Press Ltd. 2004 Lipopolysaccharid (LPS / Endotoxin) Saccharide / Struktur O-spezifische Kette n HO P Äußerer Kern Innerer Kern Always 2-Keto-3-desoxyoctonic-acid (KDO), as well as phosphorylated Heptoses in the L-Glycero-D-mannoconfiguration. Highly constant Lipid A O O O O O O O O NH O O O O NH O O O O O n1 n2 O R2 n1 n2 n3 E. Coli T H 14 14 12 H. influenzae T H 14 14 14 N. meningitides H D 12 14 12 C. violaceum H D 10 12 12 R2 n2 P DiglucosamineDisaccharide with esterand amide-bound betahydroxylipidic acids. Constant R1 O R1 n1 Up to 50 repetitive units of oligosaccharides, mostly not homo-polymeres. Heterogenous, may be lacking Hexoses such as D-Glucose (Glc), D-Galactose (Gal), 2Amino-des-oxy-D-Glucose (GlcN), N-Acetyl-glucosamine (GlcNAc) and N-Acetylgalactosamine (GalNAc). Variable O O Domänen OH n3 ©Schumann LPS Erkennung durch Immunzellen LBP LPS LPS TNF CD14 IL-1 IL-6 Schumann, Wright Science 1990 Embryonale Polarisation und Musterbildung der Fruchtfliege (Drosophila melanogaster) Embryonalentwicklung von Drosophila Moussian and Roth Current Biology 2005 Modell der Aktivierung von Toll Moussian and Roth Current Biology 2005 Vergleich CD14 - Toll - IL-1 Rezeptor I Spätzle LPS Leuzin-reich. Wdh.-motiv LxxLxLxxN/CxL Immunglobulinfamilie Zellmembran TIR (Toll-IL1Rezeptor domäne) TLR vermittelte Signaltransduktion Pattern recognition in Drosophila and vertebrates Hoffmann 2003, Nature Vergleich der Eigenschaften vererbter und erworbener Rezeptoren Systemische Ausweitung einer lokalen Immunrekation Infektion induziert Freisetzung von Mediatoren aus MOs Einwanderung von Leukozyten und Gerinnung Zytokine aktivierter Makrophagen Epitheliale Barrieren des Organismus für Infektionen Hautinfektion Mustererkennung: Bindung und Signaltransduktion cytokine Myd88 vermittelt nicht alle LPS Signale Myd88-/- Maus ist LPS resistent Kawai et al.1998, Immunity Akira and Takeda 2004, Nature Reviews Immunol. Myd88 und TIR enthaltende Adaptorproteine DD TIR Myd88 Weitere TIR enthaltende Proteine: TIRAP (TIR cont. adapter prot.) / MAL (Myd88 adapter like) TRIF (TIR containing adapter inducing IFN beta) / TICAM (TIR containing molecule) 1 TRAM (TRIF related adapter molecule) / TICAM2 Aktiv. TLR spezifische zytoplasmatische Moleküle Kawai and Akira 2005, Curr. Op. in Imm. Toll like rezeptor (TLR) Signal Akira Nature Rev 2004 Picard Science 2003 TNF Freisetzung aus Blutzellen nach Konfrontation mit TLR-Liganden oder Bakterien C gesunde Person (Kontrolle) P1, P2 IRAK4-negative Patienten Picard Science 2003 Vergleich der Eigenschaften vererbter und erworbener Rezeptoren Adaptive Immunität unterstützt angeborene Immunität Figure 1-26 Komponenten des Immunsystems: Zelluläre Faktoren Entwicklung des hämatopoetischen Systems T-Lymphozyt B-Lymphozyt Natural Killer Cell Lymphoide Reihe Omnipotente Stammzelle Pluripotente Stammzelle Myeloide Reihe Erythrozyt Monozyt Granulozyt Thrombozyt Makrophage Figure 1-4 part 1 of 3 Neutrophiler Granulozyt (Neutrophile Zelle) Figure 1-4 part 2 of 3 Natürliche Killerzelle Figure 1-6 Natürliche Killer (NK) Zellen große granuläre Lymphozyten (LGL) kill virus-infizierte oder maligne Zellen Exprimieren spezifisch CD56 & CD16 doch kein CD3 Aktivierbar mit IL2 Integration aktivierender und inhibitorischer Signale von verschiedenen Rezeptoren (missing self hypothesis) Bolitho et al., Curr Opin Immunol 2007 Aktivierung und Wanderung von DC in der Haut in afferente LymphOrgane Aufregulation kostimulatorischer Moleküle und Antigenpräsentation im regionalen Lymphknoten Mustererkennung im Zytoplasma Meylan Nature 2006 Das Komplementsystem Jules Bordet 1890: Vibrio cholerae wird getötet durch Serum, Alexin, Paul Ehrlich: Substanz, die Funktionen von Antikörpern komplettiert. Das Komplementsystem wird von mehr als 30 löslichen und zellgebundenen Proteinen konstituiert, die über regulative Kaskaden zur -Lysis von Zellen, Bakterien und Viruspartikeln, -Opsonisierung zur Erhöhung der Phagozytoserate bestimmter Antigene, -Aktivierung von Immunantworten, z. B. Entzündungsreaktionen und Freisetzung immunregulatorischer Mediatoren, durch Bindung an spezifische Rezeptoren auf Immunzellen, Anlockung von Fresszellen -sowie zur Beseitigung von Immunkomplexen aus dem Kreislauf system und weiteren Aktivierung in der Milz und Metabolisierung in der Leber beitragen. Initiatoren der alternativen Aktivierung des Komplementsystems Mikrobielle Evasion Komponenten und Wirkungen des Kompl.-Systems C1 Adhäsion an Fc von Antikörper auf opsonisierten Oberflächen Schritte des klassischen Signalwegs Aufbau des Menbranangriff-Komplex Aufgaben des Komplementsystems •Zerstörung von Pathogenen •Opsonisierung von Pathogenen •Anlocken von Fresszellen Mechanismus: Enzymkaskade, in deren Verlauf inaktive Komponenten (Zymogene) nacheinander gespalten werden und aktivierte Serinproteasen entstehen Natürliche Immunität Zeitverlauf: Erworbene Immunität sofort-96h ab 4 Tage Zelltypen: Natürliche Killerzellen, Makrophagen, Neutrophile T-, B-Zellen Spezifität: konservierte Strukturen (molekulare Pattern) Gedächtnis: NEIN Rezeptoren: keine somatische Rekombination ~100 Rezeptoren 1014-1018 Antigene JA somatische Rekombination hohe Vielfalt Komponenten der Natürlichen Immunität Barrieren: Epithelien, Schleimhäute, Defensine, Lymphozyten Zellen: Granulozyten, Makrophagen, Natürliche Killerzellen (NK) Proteine: Komplement, Mannose-bindendes Lektin, C-reaktives Protein PRRs Zytokine: Tumor Nekrose Factor , Interleukin-1, Chemokine, Interferon-, - intraepitheliale 3 Klassen von Mustererkennungsrezeptoren / pattern recognition receptors (PRR): A) Sezernierte Proteine B) endozytierende Rezeptoren C) signalgebende Rezeptoren