Protokoll
Werbung

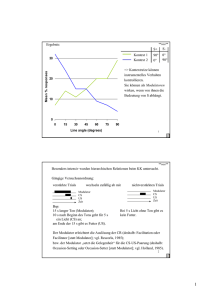
Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Reinigung und Charakterisierung der Aspartat-Aminotransferase aus Schweineherz 1. Einführung Vorraussetzung für die Charakterisierung, die Aufklärung der Struktur und die Untersuchung molekularer Mechanismen eines Enzyms ist die Gewinnung des Enzyms aus einem geeigneten Organismus/Gewebe in möglichst reiner Form durch Enzymreinigung. Im Praktikum sollten am Beispiel der Aspartat-Aminotransferase(Asp-AT) die gebräuchlichen Methoden der Enzymreinigung kennengelernt werden. Die Asp-AT ist ein Homodimer aus 2 identischen Untereinheiten(je 45kDa) und spielt eine zentrale Rolle im N-Metabolismus. Das Enzym katalysiert folgende Reaktion: Asp-AT L-Aspartat + 2-Ketoglutarat Oxalacetat + L-Glutamat Die Asp-AT gehört zur Enzymklasse der Transaminasen, die alle als Cofaktor Pyridoxalphosphat(ein Derivat des Pyridoxins, Vitamin B6) besitzen. Dieses bildet mit einem Lysinrest der großen Dömäne jeder Untereinheit eine Schiff-Base(internes Aldimin). Die Asp-AT kommt in allen Geweben vor und zwar in jeweils unterschiedlichen Isoformen sowohl in den Mitochonrien als auch im Cytoplasma. Im Cytoplasma hat das Enzym die Aufgabe Aspartat für den Harnstoffzyklus bereitzustellen, während es in den Mitochondrien die Desaminierung von Aspartat für den Aminosäureabbau katalysiert. Besonders hohe Konzentrationen an Asp-AT finden sich im Herzen und in der Leber, weshalb zur Aufreinigung ein frisches Schweineherz verwendet wurde. In der klinische Diagnostik deute eine erhöhte Asp-AT- und Ala-AT-Aktivität im Serum auf eine Schädigung der Leben hin, wohingegen eine erhöhte Aktivität der Asp-AT für sich allein Kennzeichen eines Herzinfarktes ist. Zur quantitativen Bestimmung des Enzyms, um den Verlauf der Reinigung verfolgen zu können benötigt man einen spezifischen Test. Neben der Möglichkeit die Bildung von Oxalacetat bei pH 7(Enolation!) durch Messung der Extinktionszunahme bei 259nm bietet sich ein messtechnisch leichter auszuführender gekoppelter enzymatischer Test an. Asp-AT L-Aspartat + 2-Ketoglutarat Oxalacetat + NADH + H+ Oxalacetat + L-Glutamat MDH NAD+ + Malat Durch die Kopplung der Reaktion der Asp-AT mit der Reaktion der Malat-Dehydogenase kann der Verbrauch an NADH bei 366nm gemessen werden. Vorraussetzung für ist, dass sich gebildetes Oxalacetat niemals anreichert, was durch eine 100x höhere Konzentration der MDH gewährleistet wird. Zu einer Störung des Test kann es bei Anwesenheit der Glutamat-Dehydrogenase kommen welche folgende Reaktion katalysiert: l-Gluatamat + NAD+ H2O 2-Ketoglutarat+ NH4+ + NADH + H+ 1 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Die Gluatamat-Dehydrogenase sollte jeoch im ersten Reinigungsschritt entfernt werden, da es sich um ein mitochondriales Enzym handelt, welches somit nicht in Lösung geht(frisches Schweineherz!) 2. Isolierung und Reinigung der Asp-AT 2.1. Präparation eines Schweinherzhomogenats(Rohextrakt, RE) Frisches Schweineherz von Aurikeln, Fett- und Bindegewebe befreien und in kleinen Portionen im Fleischwolf zerkleinern Je 200g Hackfleisch mit 300ml gekühltem Maleatpuffer(4°C) im Mixer(Warring blender) homogenisieren(30sec,Stufe:high, mehrmals wiederholen) 5ml Rohextrakt 10 min in der Tischzentrifuge zentrifugieren; Überstand abdekantieren ; Volumen bestimmen; 0,5ml für nachfolgende Tests auf Eis aufbewahren → RE(F I); Farbe: bräunlich rot Tests mit F 1 o Volumenbestimmung: 2,2ml → 2,3ml des Überstandes entsprechen 44% der eingesetzten 5ml Rohextrakt, da bei der Reinigung 140ml RE eingesetzt wurden, würden dem Überstand hier analog 61,6ml entsprechen(wichtig für Auswertung) o Aktivitätstest: Einsatz: 50µl einer 1:100 Verdünnung → ∆E/min= 0,0491; Volumenakt.= 29 U/ml Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden) o Proteinbestimmung nach Lowry: Einsatz: 5µl und 10µl RE → c(Protein)= 35,51mg/ml Messwerte und Eichgerade siehe Teil3(Material und Methoden 2.2 Hitzedenaturierung Bei diesem Reinigungsschritt, soll der Großteil der löslichen Proteine denaturiert (→Aggregation) und damit zusammen mit unlöslichen Bestandteilen(Zellkern, Mitos(GDH!) , ….) durch Zentrifugation abgetrennt werden. Die Asp-AT geht bei diesen hohen Temperaturen nicht kaputt, da sie durch Zusatz von Maleatpuffer und 2-Ketoglutarat überwiegend in der stabilen PLP-Form vorliegt. Durch einen Überschuss an 2-Ketoglutarat, wird das Gleichgewicht der Reaktion zur PLP-Form verschoben. Beim Maleat handelt es sich um ein Analogon, des Aspartats, welches mit dem Aspartat um die Bindestelle am PLPEnzym konkurriert. Es stabilisiert dessen 3-dimensionale Form wird aber nicht umgesetzt. 140 ml RE in 500 ml Erlenmeyerkolben in Topf mit Wasser unter permanentem Drehen auf 60°C erhitzen(Thermometer in Kolben, permanent drehen!); Dauer bis Erreichen der 60°C: 4min Bei Erreichen der 60°C, 30ml 40mM 2-Ketoglutarat-Lösung, pH 6 zugeben und bis auf 75°C weiter erhitzen; Dauer bis Erreichen der 75°C: 3min 20 min bei 75°C inkubieren(gesamte Heizdauer>60°C nicht länger als 40min) Gesamtdauer der Hitzedenaturierung: 27min Extrakt auf Eis unter Drehen bis auf 5°C Abkühlen lassen Zentrifugieren(10min, 10000Upm, GSA-Rotor) 2 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Überstand abdekantieren, Volumen bestimmen; 0,5ml für nachfolgende Tests auf Eis aufbewahren → Hitzeüberstand=F II; Farbe: bräunlich rosa, klar Tests mit F II(Hitzeüberstand) o Volumenbestimmung: 110ml o Aktivitätstest: Einsatz: 50µl einer 1:100 Verdünnung → ∆E/min= 0,0245; Volumenakt.= 14 U/ml Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden) o Proteinbestimmung nach Lowry: Einsatz: 20µl und 50µl FII → c(Protein)= 3,14mg/ml Messwerte und Eichgerade siehe Teil3(Material und Methoden 2.3 Fraktionierung durch Ammoniumsulfat Proteine können bei bestimmten Konzentrationen sogenannter chaotroper Salze reversibel denaturiert und damit ausgefällt(ausgesalzt) werden. Triebkraft der Proteinfaltung ist der hydrophobe Effekt, bzw. der entropische Effekt die Wechselwirkung hydrophober Bereiche mit dem Wasser zu minimieren um dessen Entropie zu steigern. Gibt man nun chaotrope Reagenzien, wie(NH4)2SO4 in hoher Konzentration, zu,welche dem Wasser von Anfang an eine stark geordnete Struktur aufzwingen so ist der Entropiegewinn durch die Proteinfaltung zu gering und die Proteine entfalten sich. Aus Tabellen kann entnommen werden wie viel (NH4)2SO4 zu einer Lösung dazugegeben werden muss um eine bestimmte Sättigung(in%) zu erreichen. Um andere, “nicht gewünschte“ Proteine auszusalzen, wobei die Asp-AT in Lösung bleibt, wird die Lösung(F I+ Maleatpuffer) zunächst auf 55%-Sättigung gebracht. Aus Tabelle: 55%gesättigte (NH4)2SO4-Lösung ≡ 326mg/ml → 72 g (NH4)2SO4 auf 220ml Danach wird die Sättigung mit (NH4)2SO4 75% erhöht um die Asp-AT auszusalzen. Aus Tabelle: 75%gesättigte (NH4)2SO4-Lösung ≡ 127mg/ml → 31,75g (NH4)2SO4 auf 250 ml F I (110ml) mit gleichem Volumen gekühltem(4°C) Maleatpuffer verdünnen Im Eisbad unter Rühren portionsweise 72g Ammoniumsulfat zugeben Nachdem alles aufgelöst ist 20min weiterrühren lassen Zentrifugieren(15 min, 10000Upm=10000g, GSA-Rotor, 4°C) Überstand abdekantieren,; Volumen bestimmen und auf Eis stellen Niederschlag in 5ml 30mM Natriumacetatpuffer, pH 5,4 lösen; Volumen bestimmen, 0,5ml davon für nachfolgende Tests auf Eis aufbewahren → Niederschlag=AS I Farbe: hellbräunlich, klar Im Eisbad unter Rühren portionsweise 31,75 g Ammoniumsulfat zum Überstand(250ml) zugeben Nachdem alles aufgelöst ist 20min weiterrühren lassen Zentrifugieren(15 min, 10000Upm, GSA-Rotor, 4°C) Überstand abdekantieren; Niederschlag in 5ml 30mM Natriumacetatpuffer, pH 5,0 lösen; Volumen bestimmen, 0,5ml davon für nachfolgende Tests auf Eis aufbewahren → Niederschlag=AS II, Farbe: gelb 3 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Überstand abdekantieren,; Volumen bestimmen und auf Eis stellen; 0,5ml für nachfolgende Tests auf Eis aufbewahren → Überstand=AS III, Farbe: bräunlich gelb Tests mit AS I, II und III o Volumenbestimmung: AS I: 8ml AS II: 5ml AS III: 251ml o Aktivitätstest: Einsatz: AS I: 50µl einer 1:10 Verdünnung AS II: 50µl einer 1:200 Verdünnung AS III: 50µl einer 1:10 Verdünnung → ∆E/min: AS I: 0,2374 Volumenakt.: AS I: 14 U/ml AS II: 0,2346 AS II: 277 U/ml AS III: 0,0089 AS III: 0,526 U/ml Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden) o Proteinbestimmung nach Lowry: Einsatz: AS I: 5µl und 10µl AS II: 5µl und 10µl AS III: enthält zuviel (NH4)2SO4, welches die Proteinbestimmung stören würde → c(Protein) : AS I 16,61mg/ml AS II: 6,77mg/ml AS III: ----Messwerte und Eichgerade siehe Teil3(Material und Methoden 2.3. Dialyse Mittels Dialyse kann zum einen das (NH4)2SO4 wieder entfernt werden (Renaturierung), zum anderen dient die Dialyse allgemein dem Umstellen auf einen geeigneten Puffer. Dialyseschlauch(ca. 20cm) in dest. H2O einweichen(ca. 5min) AS II über Nacht gegen 5l 30mM Natriumacetatpuffer pH 5,0 dialysieren( Kühlraum, 4°C) Abzentrifugieren von ausgefallenem Protein(10min, 8000g=9000Upm, SA-Rotor, 4°C) Überstand abdekantieren, Volumen bestimmen; 0,5ml für nachfolgende Tests auf Eis aufbewahren → Überstand = Dialysat Tests mit Dialysat o Volumenbestimmung: 7,6 ml o Aktivitätstest: Einsatz: 50µl einer 1:200 Verdünnung → ∆E/min= 0,1039; Volumenakt.= 14 U/ml Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden) o Proteinbestimmung nach Lowry: Einsatz: 10µl Dialysat → c(Protein)= 2,98 mg/ml Messwerte und Eichgerade siehe Teil3(Material und Methoden) 4 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 2.4. Chromatographie an CM-Sephadex C-50 Bei dem Reinigungsschritt mittels Ionenaustauschchromatographie handelt es sich um den spezifischsten Schritt der Reinigung. Als Tragermaterial wird Sephadex verwendet, an das Carboxymethyl(+Na) eine schwache Säure gebunden is(schwacher Kationenaustauscher). Die Asp-AT liegt ist bei pH 5 postiv geladen und bindet an die Säule, wohingegen neutrale und negativ geladene Teilchen durchgewaschen werden. Durch schrittweise Erhöhung der Na-Konzentration(Gegenion) des Elutionspuffers(Na+-Gradient) wird die Asp-AT durch Säule(1,5 x 10 cm) mit 10ml H2O befüllen→ Markierung für Füllmenge an Säulenmaterial In Säule 0,5 ml Äquilibrierungspuffer(30mM Natriumacetat, pH 5,0) vorlegen → verhindert Bildung von Luftblasen beim Befüllen mit Säulenmaterial Säule portionsweise mit 10ml CM-Sephadex-Säulenmaterial befüllen Überstehenden Säulenmaterialspuffer bis einige mm über Säulenbett ablaufen lassen CM-Sephadex 3x mit je 10ml Äquilibrierungspuffer waschen und pH des Eluats testen(5,0!), Flussrate 1ml/min(alle 3sec1 Tropfen) Dialysat(bei pH 5 positiv geladen) auf Säule auftragen(aufwirbeln vermeiden!) Elution in 3 Schritten: 1. Elution: Nachwaschen der Säule mit 20ml Aquilibirierungspuffer und 10 Fraktionen a 2ml in Sarstedt-Röhrchen sammeln(auf Eis stellen!) → negativ geladene und neutrale Teilchen(Verunreinigungen) werden heruntergewaschen 2. Elution: Waschen mit 20ml 80mM Natriumcetatpuffer pH 5,0 und 10 Fraktionen a 2ml sammeln → Erhöhung der Ionenstärke des Elutionspuffers, schwach gebundene (z.B positiv polarisierte Teilchen werden heruntergewaschen 3. Elution: Elution mit 20ml 200mM Natriumacetatpuffer pH 5,0 und 10 Fraktionen a 2ml sammeln → Elution der Asp-AT mit den „gelbsten(PLP!!)“ Fraktionen #25-29 Aktivitätstest durchführen Aktivitätstest: Einsatz: jeweils 50µl einer 1:100 Verdünnung → ∆E/min: # 25= 0,0187 # 26= 0,3615 #27= 0,1922 #28= 0,0941 #29= 0,0204 Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden Die Fraktionen 26 und 27 wurden anschließend zu einer CM-Sephadex-Poolfraktion vereint. Auch in den anderen Fraktionen(#25, 28, 29) ist eine deutliche Aktivität messbar. Da diese Fraktionen nicht in den „Pool“ mit aufgenommen wurden, geht natürlich eine beträchtliche Menge Asp-AT verloren. Diesem quantitativen Verlust wurde aber das Kriterium der Reinheit, welche dadurch erhöht wird, übergeordnet. 5 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Tests mit „Poolfraktion“(#26, 27) o Volumenbestimmung: 4,6 ml o Aktivitätstest: Einsatz: 50µl einer 1:100 Verdünnung → ∆E/min= 0,2528; Volumenakt.= 149U/ml Messwerte und Extinktions-Zeit-Diagramm siehe Teil3(Material und Methoden) o Proteinbestimmung nach Lowry: Einsatz: 100µl „Poolfraktion“ → c(Protein)= 1,01 mg/ml Messwerte und Eichgerade siehe Teil3(Material und Methoden 2.4. SDS-Polyacrylamidgelelektrophorese Zum Abschluss der Reinigung werden alle relevanten Proben auf eine SDS-Page aufgetragen um die Reinigung qualitativ verfolgen zu können und die Reinheit zu überprüfen. Gießen von Trenn- und Sammelgel(siehe 3.4) Probenzubereitung: je 50µl der einzelnen Reinigungsstufen(RE/F I, F II, AS I, AS II, Dialysat, CM-Sephadex-Fraktion) mit gleichem Volumen SDS-Probenpuffer versetzen und 3min bei 95°C inkubieren Auftragung folgender Volumina der einzelnen Fraktionen aufs Gel(→ entspricht ca. 10µg) zusammen mit Proteinstandard Fraktion Auftragsvolumen[µl] RE/F I F II AS I AS II Dialysat CMSephadex Standard 5 10 5 10 10 15 5 Elektrophorese bei 25mA ca 1h 10min Fixieren mit Fixierer=Entfärberlösung → überschüssiges SDS und Puffer werden ausgewaschen → schärfere Banden, Färbelsg. mehrmals verwendbar 20min Färben mit Färbelösung(Coomassie Brilliant Blue) → Sichtbarmachung der Proteinbanden Mehrmals Entfärben mit Entfärberlösung + Schaumstoff Ergebnis siehe Auswertung(2.5.) 6 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 2.5. Auswertung Reinigungstabelle: Fraktion Rohextrakt (F I) Hitzeüberstand (F II) AS I AS II AS III Dialysat CMSepharoseFraktion Volumen [ml] ∆E/min Proteinmenge Volumenakt. Spezifische Gesamtakt. Ausbeute[%] [mg/ml] [U/ml] Akt.[U/mg] [U] 61,6 0,0491 35,51 29 0,817 1786,4 ----- 110 0,0245 3,14 14 4,61 1593,2 100% 8 5 251 7,6 0,2374 0,2346 0,0089 0,1039 16,61 6,77 0,845 40,97 2,98 14 277 0,53 123 41,31 112,3 1456,3 132,1 933,6 7,05 91,4 8,29 58,6 4,6 0,2528 1,01 149 147,9 687,5 43,2 Wie zu erwarten nimmt die spezifische Aktivität innerhalb der Reinigung zu, wohingegen die Gesamtaktivität und die Proteinmenge abnimmt. Als Bezugsgröße(100%-Wert) wird die F-II Fraktion verwendet, da aufgrund der Konsistenz des RE die Gesamtaktivität nicht sehr gut mit den nachfolgenden Fraktionen vergleichbar ist. Bei der Ammoniumsulfatfällung geht nur relativ wenig Enzym verloren, während bei der Dialyse die Ausbeute stark absinkt, was schwer zu erklären ist, das es sich bei der Dialyse eigentlich nicht um einen Reinigungsschritt handelt(spezif. Akt. bleibt gleich). Möglicherweise ist Enzym bei der Dialyse ausgefallen. Beim der Ionenaustauschchromatographie, als spezifischstem Reinigungsschritt, nimmt die spezifische Aktivität und damit die Reinheit am stärksten zu, wobei der Verlust auch ein starker Verlust zu verzeichnen ist, welcher. wie schon erwähnt, auf die Vereinigung nur der am stärksten konzentrierten Eluatfraktionen zurückzuführen ist. Insgesamt ist mit einer Ausbeute von 43,2% und einer spezifischen Aktivität von 147,9 mg/ml ein sehr gutes Ergebnis erzielt worden. Ergebnis SDS-Page Asp-AT 7 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Während der RE ein Gemisch aus unterschiedlichsten Proteinen enthält, kann man am Gel erkennen, dass nach der Hitzedenaturierung eine Vielzahl dieser Proteine(Verunreinigungen) abgetrennt wurde. Nach der Ammoniumssulfatfällung(AS II) bzw. der Dialyse kommt es zur Anreicherung einer Bande welche in der AS I Fraktion nicht sehr prominet ist, so dass hauptsächlich Verunreinigungen in diesem Schritt entfernt wurden. Die restlichen Verunreinigungen werden an der Säule vollständig entfernt, so dass danach nur noch eine Asp-AT-Bande vorhanden ist. Auch anhand des Gels zeigt sich, dass die Reinigung sehr gut geklappt hat und dass das Enzym in reiner Form erhalten wurde. Bestimmung des Molekulargewichts der Asp-AT Da das Molekulargewicht der Standardproteine bekannt ist, kann durch halblogarithmische Auftragung des Molekulargewichts gegen die Laufstrecke in % eine Eichgerade erstellt werden. Aus der Eichgerade kann dann der lnMW abgelesen werden, der zur Laufstrecke der Asp-AT gehört und daraus das MW bestimmt werden. Myosin Β-Galactosidase Phosphoylase b BSA Ovalbumin Carboanhydrase MW[kDa] lnMW Wanderung in % 205 116 97,4 66 45 29 5,32 4,75 4,58 4,19 3,81 3,37 32 42,4 47,2 56 70,4 88 Laufstrecke der Asp-AT: 74% Dies entspricht: lnMW= 3,8 → MW= 44,7kDa Da die Asp-AT ein Homodimer aus 2 identischen Untereinheiten ist, welche als eine Bande im Gel laufen: MWAsp-AT= 2x 44,7=89,4 kDa Der ermittelte Wert stimmt nicht ganz mit dem Literaturwert von 93,15kDa überein. 8 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 2.6. Trypsinverdau im Gel zur MALDI-Analyse In diesem Versuchsteil soll das Enzym eindeutig mittels Massenspektrometrie identifiziert werden. Dazu wird die „vermeintliche“ Asp-AT Bande der CM-Sephadex-Spur ausgeschnitten und im Gel mit Trypsin verdaut. Die kleineren Peptidfragmente können dann massenspektrometrisch untersucht werden. Asp-AT Bande ausschneiden und würfeln; Volumen: ca. 8µl unter sanftem Schütteln in einem 2ml Eppendorfcup jeweils 30 min nacheinander extrahieren mit: 50mM NH4HCO3 50mM NH4HCO3/Acetonitril(3:1) 25% Acetonitril 50% Acetonitril 1h lyophylisieren Trypsinverdau über Nacht bei 37°C(Endkonzentration Trypsin ca. 2µg/100µl Gelvolumen), 1,5 fache des Gelvolumens an 50mM NH4HCO3 mit Trypsin zugeben → Trypsin mit 50mM NH4HCO3 auf geeingete Konzentration bringen (hier: 2µg/100µll) → 12µl zugeben Gelstücke 2x mit 100mM NH4HCO3 jeweils 1h extrahiern Gelstücke 1x mit 100mM NH4HCO3/Acetonitril(1:1) 1h lang extrahieren jeweils das 2-3-fache des Gelvolumens einsetzten→20µl Lyophylisieren der vereinigten Extrakte für 4h Trockenen Rückstand in 50µl H2O aufnehmen Lyophylisieren ca. 1h Identifizierung der Peptidfragmente mittels MALDI 9 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 2.7. Bestimmung des KM der Asp-AT für Aspartat CM-Sephadex-Fraktion mit 0,1M Kaliumpuffer auf Aktivität 5-8 U/ml einstellen → erneute Aktivitatsmessung: 95,41 U/ml → Verdünnung 1:15 auf 6,4 U/ml aus 1M Aspartat-Lösung je 1ml einer 1:4, 1:20, 1:100-Verdünnung herstellen 6 Ansätze wurden in je einer Küvette nach folgendem Schema zusammenpipettiert: Küvette 1 2 3 4 5 6 0,2 - 0,1 0,1 0,1 - [ml] Aspartalsg 1:100 1:25 1:4 H2O 0,1 M K-Phosphat;pH 7,5 NADH MDH Asp-AT(6,4U/ml) 0,1 0,1 0,2 - 0,1 0,1 je 0,74 je 0,02 je 0,01 je 0,02 Leerwert der Extinktion bei 366nm beobachten Bei Konstanter Extinktion Start der Reaktion mit je 10µl 2-Ketoglutara Extinktion 3min lang alle 30sec ablesen Extinktions-Zeit-Diagramme siehe 3.3 Auswertung Michaelis-Menten-Kinetik: Die Umsatzgeschwindigkeiten(∆E/min), die sich graphisch aus den Extinktionszeitdiagrammen(siehe 3.3.) ergeben, werden gegen die Aspartatkonzentration aufgetragen. deltaE/min= Umsatzgeschwindigkeit Michaelis-Menten-Kinetik 0,6 0,5 0,4 0,3 0,2 0,1 0 0 0,02 0,04 c(Aspartat) in [M] vmax= 0,5[1/min] KM = 0,01 M=10 mM(bei 0,5 vmax) 10 0,06 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Lineweaver-Burk-Diagramm: Zur besseren Auswertung wird die Kehrwerte der Umsatzgeschwindigkeiten gegen den Kehrwerte der Substratkonzentrationen aufgetragen. Lineweaver-Burk-Diagramm 25 1/deltaE/min 20 15 10 5 y = 0,0216x + 1,7504 0 -500 -5 0 500 1000 1500 1/c(Substrat) in [1/M] vmax: Schnittpunkt der Geraden mit y-Achse= 1/vmax= 1,7504 [min] → vmax= 0,571[1/min] KM: Schnittpunkt der Geraden mit x-Achse= -1/KM= -81,03 [1/M] → KM= 0,0123 M=12,3mM Das Michaelis-Diagramm und das Lineweaver-Burk-Diagramm liefern sehr ähnliche Ergebnisse, wobei die Ergebnisse aus der Lineweaver-Burk-Auftragung viel genauer sind, da sie genauer abgelesen werden können. Volumenaktivität aus vmax(mit Wert aus Lineweaver-Burk-Auftragung) VolumenaktivitätAv v max VKüvette VeinpipettierteEnzymlsg d Verdünnungsfaktor[U / ml ] = (0,571x 1/0,02x 3,4x1)U/ml= 8,3U/ml Die tatsächliche Volumenaktivität bei Substratsättigung ist etwas größer, als die theoretisch durch die Verdünnung ermittelte Aktivität von 6,4 U/ml. Möglicherweise wurde beim Verdünnen nicht exakt pipettiert. Trotzdem liegt diese Aktivität noch im gut messbaren Bereich. 11 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 3.Material und Methoden Um den Erfolg bzw. Misserfolg der Anreicherung während der Reinigung verfolgen zu können, wurden nach jedem Reinigungsschritt Proben entnommen. Diese wurden zum Einen, einem für das Enzym charakteristischen Aktivitätstest unterzogen, zum Anderen dienten sie der Proteinbestimmung. 3.1. Proteinbestimmung nach Lowry Die Eichgerade für die Proteinbestimmung muss jedes Mal, wenn die Proteinmenge unbekannter Proben bestimmt werden soll, neu erstellt werden. 1 Substanzen Eichgerade Lowry-Test 2 3 4 5 Mengen in ml/Probe SerumalbuminLösung [mg/ml] H20 Cu-Reagens (A+B+C) 0 0,2 0,05 0,15 0,1 0,1 0,15 0,05 0,2 0 2,5 2,5 2,5 2,5 2,5 Nach 10 min bei RT werden jeweils 0,2 ml Folin-Ciocalteu-Lösung zugegeben(sofort whirlmixen!) Nach mindestens 30 höchstens 60 min wird die Extinktion bei 578nm im Photometer gemessen(hohe Konz. NH4+- und Phosphationen stören!) An zwei Tagen wurde ein Lowry-Test und damit eine Eichgerade erstellt: Tage Tag 1.(Dienstag) Tag 2.(Mittwoch) 1 0,064 0,074 Extinktion bei 578nm 2 3 0,23 0,36 0,247 0,381 4 0,512 0,506 Eichgerade(1.Tag) Extinktion bei 578nm 0,7 y = 2,836x + 0,076 0,6 0,5 0,4 0,3 0,2 0,1 0 0 0,05 0,1 0,15 Proteinmenge [mg] 12 0,2 0,25 5 0,632 0,717 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Extinktion bei 578nm Eichgerade (2. Tag) 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 y = 3,09x + 0,076 0 0,05 0,1 0,15 0,2 0,25 Proteinmenge[mg] Von den Proben der verschiedenen Reinigungsschritte wurden die im Teil 2 angegeben Mengen für den Lowry-Test eingesetzt und mit Wasser auf insgesamt 200µl ergänzt. Reinigungsschritte RE bzw. F I Probe 1 Probe 2 FII Probe 1 Probe 2 AS I Probe 1 Probe 2 ASII Probe 1 Probe 2 Dialysat Probe CMSepharose Poolfraktion eingesetztes Volumen[µl] E [mg] aus Eichgerade Verdünnungsfaktor/ml c(Protein)[mg/ml] 5 10 0,621 1 0,192(EG1) 0,326(EG1) 200 100 38,4 32,6 35,51 20 50 0,264 0,497 0,066(EG1) 0,148(EG1) 50 20 3,31 2,97 3,14 5 10 0,36 0,535 0,092(EG2) 0,149(EG2) 200 100 18,38 14,85 16,61 5 10 0,182 0,28 0,034(EG2) 0,066(EG2) 200 100 6,86 6,6 6,77 10 0,168 0,03(EG2) 100 2,98 100 0,387 0,101(EG2) 10 1,01 3.2. Asp-AT-Test(Aktivitätstest) Der Reihenfolge nach werden in eine Plastikküvette(d=1cm) folgende Substanzen pipettiert: Substanzen 1M K-Phosphatpuffer,pH 7,5 H 1M Aspartat NADH(15mg/ml) MDH(1mg/ml) Asp-AT Volumen[ml] 0,100 0,710 0,100 0,020 0,005 0,500 durchmischen 3 min bei 366nm Extinktion im Photometer verfolgen(Konstanz!) Start: Zugabe von 20µl 1M α-Ketogluarat + Mischen Extinktion 3min lange alle 30s notieren 13 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Mit allen entnommenen Proben(siehe Teil2) sowie den Fraktionen 25-29 des Eluats der CMSephadex-Säule wurde der Aktivitätstest durchgeführt. Die Anfangssteigung im ExtinktionsZeit-Diagramm entspricht ∆E/min. Mittels ∆E/min lässt sich über das Lambert-BeerscheGesetz direkt die Volumenaktiviät[U/ml] nach folgender Formel berechnen: VolumenaktivitätAv E VKüvette t VeinpipettierteEnzymlsg d Verdünnungsfaktor[U / ml] Extinktion bei 578nm Nach Start mit α-Ketoglutarat ohne αKG Zeit [min] FI F II 3 1,251 1,387 AS I 1,402 0 1,251 0,5 1,242 1,37 1 1,222 1,358 1,5 1,199 2 1,173 2,5 1,142 3 1,105 Verdünnungsfaktor ∆E/min Volumenaktivität[U/ml] 100 0,0491 29 AS II AS III Dialysat CMSepharose „Pool“ 1,132 0,942 1,42 1,198 1,144 0,971 1,431 1,211 1,341 1,033 0,97 1,444 1,116 1,248 0,909 0,965 1,403 1,005 1,345 1,134 0,77 0,96 1,355 0,876 1,333 1,008 0,616 0,956 1,302 0,75 0,452 0,95 1,243 0,608 0,28 0,946 1,187 0,455 200 0,2346 277 10 0,0089 0,526 1,381 1,322 1,307 100 0,0245 14 1,416 0,86 0,709 10 0,2374 14 200 0,1039 123 Aktivitätstest der # der CM-Sephadexsäule Extinktion bei 366nm Zeit[min] Nach Start mit Ketoglutarat ohne KG 3 #25 #26 #27 #28 #29 1,262 1,208 1,15 1,456 1,548 1,283 1,622 1,439 0 1,298 1,159 0,5 1,293 1,019 1,21 1,586 1,486 1 1,284 0,856 1,123 1,545 1,476 1,5 1,273 0,679 1,028 1,5 1,467 2 1,265 0,474 0,927 1,452 1,456 2,5 1,254 0,256 0,822 1,397 1,443 3 1,243 - 0,71 1,34 1,433 100 0,0187 100 0,3615 100 0,1922 100 0,0941 100 0,0204 Verdünnungsfaktor ∆E/min 14 100 0,2528 149 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Extinktions-Zeit-Diagramme: FI F II 1,28 1,26 1,24 Extinktion Extinktion 1,22 1,2 1,18 1,16 1,14 1,12 y = -0,0491x + 1,2642 1,1 1,08 0 1 2 3 1,39 1,38 1,37 1,36 1,35 1,34 1,33 1,32 1,31 1,3 y = -0,0245x + 1,3819 0 4 0,5 1 1,5 t/min AS I 3,5 1,2 Extinktion 1,2 Extinktion 3 1,4 1,4 1 0,8 0,6 y = -0,2374x + 1,4583 0,4 1 0,8 0,6 0,4 y = -0,2891x + 1,177 0,2 0,2 0 0 0 0,5 1 1,5 2 2,5 3 0 3,5 0,5 1 1,5 Extinktion 0,975 0,97 0,965 0,96 y = -0,0089x + 0,973 0 0,5 1 1,5 2 2,5 3 1,6 1,4 1,2 1 0,8 0,6 0,4 0,2 0 0 3,5 0,5 1 1,5 Extinktion y = -0,2528x + 1,2393 0,2 0 1 1,5 2 2,5 3 3,5 # 25 1,4 1,2 0,5 3,5 Zeit[min] CM-Sephadex-Poolfraktion 0 3 y = -0,1039x + 1,4522 t/min 1 0,8 0,6 0,4 2,5 Dialysat AS III 0,955 0,95 0,945 0,94 2 Zeit [min] Zeit[min] Extinktion 2,5 AS II 1,6 Extinktion 2 Zeit[min] 2 2,5 3 3,5 1,31 1,3 1,29 1,28 y = -0,0187x + 1,3009 1,27 1,26 1,25 1,24 0 1 2 Zeit[min] Zeit[min] 15 3 4 Biochemisches Großpraktikum I Böhm Maria #27 1,4 1,2 1 0,8 Extinktion Extinktion #26 0,6 0,4 0,2 0 y = -0,3615x + 1,1924 0 0,5 1 1,5 2 2,5 1,4 1,2 1 0,8 0,6 0,4 0,2 0 0 3 2 3 #28 #29 Extinktion Extinktion 1 Zeit[min] 1,5 1 y = -0,0941x + 1,6328 0 0 y = -0,1922x + 1,303 Zeit[min] 2 0,5 23.11.2007 1 2 3 1,5 1,49 1,48 1,47 1,46 1,45 1,44 1,43 1,42 y = -0,0204x + 1,4955 0 4 4 1 2 3 4 Zeit[min] Zeit[min] 3.3. KM-Bestimmung Ergebnisse der Messungen: Zeit[min] 3 ohne KG Nach Start mit Ketoglutarat 0 0,5 1 1,5 2 2,5 3 ∆E/min Extinktion bei 366nm 1 2 3 1,259 1,195 1,195 4 1,207 5 1,191 6 1,198 1,215 1,199 1,179 1,158 1,136 1,112 1,086 0,0431 1,187 1,097 0,991 0,867 0,74 0,599 0,433 0,2506 1,161 1,009 0,85 0,666 0,462 0,241 0,136 0,3571 1,237 1,028 0,793 0,514 0,231 1,232 1,202 1,168 1,133 1,092 1,048 1,003 0,0766 16 1,238 1,17 1,094 1,01 0,917 0,818 0,715 0,175 0,5052 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Extinktions-Zeit-Diagramme: 2 1,4 1 1,2 Extinktion Extinktion 1,25 1,2 1,15 1,1 1 0,8 0,6 y = -0,0765x + 1,2402 0,4 0,2 y = -0,0431x + 1,2197 0 1,05 0 0,5 1 1,5 2 2,5 3 0 3,5 1 Zeit[min] 1,4 1,4 1,2 1,2 1 0,8 0,6 y = -0,175x + 1,2571 0,2 4 1 0,8 0,6 y = -0,2506x + 1,2208 0,4 0,2 0 0 0 1 2 3 4 0 1 2 3 Zeit[min] Zeit[min] 5 6 1,4 4 1,4 1,2 1,2 y = -0,3571x + 1,182 1 Extinktion Extinktion 3 4 Extinktion Extinktion 3 0,4 2 Zeit[min] 0,8 0,6 0,4 0,2 1 0,8 0,6 0,4 y = -0,5052x + 1,2658 0,2 0 0 0 1 2 3 4 0 Zeit[min] 0,5 1 1,5 Zeit[min] 17 2 2,5 Biochemisches Großpraktikum I Böhm Maria 23.11.2007 3.4. Lösungen: Zum Titrien: 2N NaOH: 8g auf 100ml H2O 2N KOH: 11,2 g auf 100ml H2O 0,5N HCl: 50ml 1N HCl +50ml H2O Hitzedenaturierung: 50mM Maleatpuffer, pH 6,0; 5mM EDTA x Na2 enthaltend: 25mmol Maleinsäure(2,9g) und 2,5mmol(0,9306g) EDTA x Na2 mit 2N KOH auf pH 6 einstellen, mit H2O auf 0,5l auffüllen 40mM 2-Ketoglutarat, pH 6,0: 4mmol(0,904g) 2-Ketoglutarat, mit 0,5N HCl auf pH 6 einstellen mit H2O auf 100ml auffüllen Fraktionierung durch Ammoniumsulfat: 30mM Na-Acetat-Puffer, pH 5, 4: 3mmol(171µl) Essigsäure, pH mit 2N NaOH auf 5,4, mit H2O auf 100ml 30mM Na-Acetat-Puffer, pH 5, 0: 6mmol(343µl) Essigsäure, pH mit 2N NaOH auf 5,0, mit H2O auf 100ml Für die Dialyse wurden 5l dieses Puffers(5) hergestellt. Dieser Puffer ist gleichzeitig der Äquilibrierungspuffer für die CM-Sephadexsäule. Ionenaustauschchromatographie an CM-Sephadex-Säule: 80mM Na-Acetat-Puffer, pH 5, 4: 3mmol(171µl) Essigsäure, pH mit 2N NaOH auf 5,4, mit H2O auf 100ml 30mM Na-Acetat-Puffer, pH 5, 4: 3mmol(171µl) Essigsäure, pH mit 2N NaOH auf 5,4, mit H2O auf 100ml SDS-Page: Trenngel: für ein Gel Sammelgel: Tris (1M, pH 8,8) H2O SDS (10%) TEMED (5%) Acrylamid (30%) Per (15 mg/mL) 3,05mL 1,34mL 0,08mL 0,165mL 2,44mL 0,22mL Tris (1M, pH 6,8) H2O SDS (10%) TEMED (5%) Acrylamid (30%) Per (15 mg/mL) Elektrodenpuffer: Tris Glycin SDS H2O 3,03g 14,41g 1g ad 1L 18 0,33mL 1,54mL 0,0028mL 0,055mL 0,43mL 0,11mL Biochemisches Großpraktikum I Böhm Maria 23.11.2007 Fixierer / Entfärber: Essigsäure (techn.) Methanol H2O 70mL 300mL ad 1L Aktivitätstest/KM-Bestimmung 1 M Kaliumphosphatpuffer, pH 7,5: 50ml 1 M(11,4g) K2HPO4 vorlegen und mit 1 M(2,738g) KH2PO4(20ml herstellen) auf pH 7,5 titrieren 1M 2-Ketoglutarat, pH 7-8 3mmol(0,6783) 2-Ketoglutarat mit H2O auf 3ml(pH mit pH-Papier prüfen!) 1M Na-Aspartat, pH 7-8: 20mmol(3,46g) Na-Aspartat mit H2O auf 10ml(pH mit pH-Papier prüfen!) 1mg/ml Malat-Dehydrogenase(MDH) in 50% Glycerin/50% H2O: wurde gestellt 15mg/ml NADH in 0,1 M Kaliumphosphatpuffer, pH 7,5: wurde gestellt Proteinbestimmung nach Lowry: Folin-Ciocalteu-Lösung(2N): wurde gestellt A: 3%(w,v =weight per volume) Na2CO3 in 0,1 N NaOH, 100ml → 3g Na2CO3 auf 100ml mit NaOH B: 4%(w,v) Na, K-Tatrat in H2O; 10 ml C: 2%(w,v) CuSO4 x 5 H2O in H2O; 10 ml Zur Proteinbestimmung wurden 1ml B und 1ml C gemischt und mit A auf 100ml aufgefüllt(Reihenfolge wichtig!) Zum Verdünnen des Enzyms: 0,1M Kaliumphosphatpuffer, pH 7,5 10ml 1M Kaliumphosphatpuffer, pH 7,5 + 90 ml H2O 19