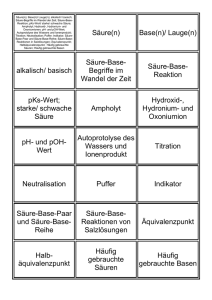
Theorie - Universität Tübingen
Werbung

Kurstag 2 Maßanalyse 2. Teil Titration von starken und schwachen Säuren Stichworte zur Vorbereitung Massenwirkungsgesetz, Prinzip von Le Chatelier, Broenstedt, korrespondierendes Säure-Base-Paar, pH-Wert-Berechnung und Titration. Ziel des Versuchstags Das Hauptziel des Versuchtags ist es, mit Hilfe der Titration qualitative Analysen von Säuren durchzuführen. Zudem sollen die Grundlagen der Säure-Base-Theorie vermittelt und das Berechnen von pH-Werten erlernt werden. Kurstag 2: Maßanalyse 2.Teil Theorie Massenwirkungsgesetz Man informiere sich anhand von chemischen Lehrbüchern über das Massenwirkungsgesetz (Hinreaktion, Rückreaktion, dynamisches Gleichgewicht, Gleichgewichtszustand, reversible Reaktion, Gleichgewichtskonstante). Säuren und Basen: Definition nach Broenstedt Nach Broenstedt sind Säuren Verbindungen, die Protonen abgeben können, diese werden auch als Protonendonatoren bezeichnet. Basen sind Verbindungen, die Protonen aufnehmen können, sie werden auch als Protonenakzeptoren bezeichnet. Korrespondierendes Säure-Basenpaar Nach obiger Definition wäre eine Verbindung HA, die in wässriger Lösung (dem wichtigsten Lösemittel) nach der Gleichung: HA → H+ + Areagiert, eine Säure. Zwar kann man bei manchen Reaktionen praktisch davon ausgehen, dass sie nur in einer Richtung verlaufen, real besteht aber jede chemische Reaktion aus einer Hinund einer Rückreaktion. Folglich stellt sich bei jeder chemischen Reaktion ein Gleichgewicht zwischen den Edukten und den Produkten der Reaktion ein. Das Verhältnis Gleichgewichtslage der der Edukte und Reaktion Produkte wird durch zueinander das und damit die Massenwirkungsgesetz beschrieben. Auf obige Reaktion angewandt bedeutet dies, dass auch die Rückreaktion der Reaktion betrachtet werden muss: H+ + A- → HA Wie man erkennen kann, nimmt das A--Teilchen in diesem Fall ein Proton auf und ist damit nach der Definition von Broenstedt eine Base, also ein Protonenakzeptor. Kombiniert man beide Reaktionsgleichungen, ergibt sich: H+ + AHA Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 1 Kurstag 2: Maßanalyse 2.Teil Je nachdem auf welcher Seite der Reaktion das Gleichgewicht liegt (d.h. ob die Reaktion eher nach links oder rechts verläuft), fungiert das Teilchen A als Säure HA oder als Base A-. Es existiert zu jedem Teilchen HA ein Teilchen A-, das das gleiche Grundgerüst wie das HA-Teilchen besitz und bei Aufnahme eines Protons zu diesem wird. Ebenso existiert zu jedem Teilchen A- ein Teilchen HA, das das gleiche Grundgerüst wie das A--Teilchen besitz und bei Abgabe eines Protons zu diesem wird. Die beiden Teilchen HA und A- bilden miteinander ein korrespondierendes SäureBase-Paar. H+ + AHA Obige Gleichung ist insofern nicht ganz korrekt, als in wässriger Lösung (dem wichtigsten Lösemittel) freie H+-Ionen (Protonen) nicht stabil sind: sie lagern sich sofort an ein Molekül H2O zum H3O+-Ion an. Korrekt müsste obige Gleichung lauten: H3O+ + AHA + H2O Jede Säure liefert durch Protonenabgabe ihre korrespondierende Base, umgekehrt wird bei der Protonenaufnahme aus einer Base ihre korrespondierende Säure gebildet. Beispiele für Säure-Basen-Paare: Proton + korrespondierende Base Säure H+ + ClHCl H+ + H2O H3O+ H+ + NH3 NH4+ korrespondierende Säure Base + Proton NH4 NH3 + H+ H3O+ H2O + H+ H2O OH- + H+ Ac- + H3O+ HAc + H2O Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 2 Kurstag 2: Maßanalyse 2.Teil Eine wässrige Lösung wird als sauer bezeichnet, wenn sich in ihr viele H +- bzw. H3O+-Ionen befinden. Als basisch werden wässrige Lösungen bezeichnet, die viele OH--Ionen enthalten. Die Eigenschaft als Säuren oder Basen zu fungieren ist keine absolute Eigenschaft: Säuren geben bei der Reaktion ihr Proton immer an eine Base ab, die dieses aufnimmt und damit in ihre korrespondierende Säure übergeht. Basen nehmen bei einer Reaktion immer das Proton einer Säure auf und überführen die Säure so in ihre korrespondierende Base. An einer Säure-Base-Reaktion müssen immer zwei korrespondierende SäureBase-Paare beteiligt sein. H3O+ + ClHCl + H2O In dieser Reaktion fungiert von links nach rechts HCl als Säure und H 2O als Base, von rechts nach links H3O+ als Säure und Cl- als Base. Einige Teilchen wie z.B. Wasser haben die Fähigkeit entweder als Säure oder als Base reagieren zu können. D.h. sie können je nach Reaktionspartner entweder ein Proton aufnehmen oder ein Proton abgeben. Solche Verbindungen bezeichnet man als amphoter (Ampholyte). So reagiert Wasser mit HCl nach folgender Gleichung: H3O+ + ClHCl + H2O Wasser fungiert in diesem Fall als Base, weil es von der Salzsäure ein Proton aufnimmt. Mit NH3-Gas reagiert Wasser jedoch wie folgt: NH4+ + OHNH3 + H2O In diesem Fall gibt Wasser an NH3 ein Proton ab, reagiert also als Säure. Ein weiteres Beispiel hierfür wäre die stufenweise Dissoziation einer mehrprotonigen Säure, etwa der Schwefelsäure: H3O+ + HSO4H2SO4 + H2O H3O+ + SO42HSO4- + H2O Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 3 Kurstag 2: Maßanalyse 2.Teil Das HSO4--Ion reagiert in der ersten Rückreaktion als Base, in der zweiten Hinreaktion als Säure. Ionogen abspaltbarer Wasserstoff Nicht alle Wasserstoff enthaltenden Verbindungen können diesen als Proton abspalten. Im wesentlichen besitzen diese Eigenschaft nur solche Verbindungen, bei denen das Wasserstoffatom an stark elektronegative Elemente der 6. und 7. Hauptgruppe gebunden ist, z.B. an F, Cl, J, O, S. Dies lässt sich am Beispiel der Essigsäure anschaulich zeigen. Essigsäure mit der Formel O H3C O H enthält 2 Arten von H-Atomen: 3 H-Atome am Kohlenstoff gebunden, 1 H-Atom am Sauerstoff gebunden. Die C-H-Bindung ist sehr fest und wegen dem geringen Elektronegativitätsunterschied kaum polarisiert, während die OH-Bindung durch die elektronenziehende Wirkung des Sauerstoffs sehr stark polarisiert ist. Essigsäure kann daher in wässriger Lösung nur das am Sauerstoff gebundene H als H+-Ion nach folgender Gleichung abdissoziieren: O H3C + H2O O H O H3C + H3O+ O Starke und schwache Säuren bzw. Basen In einem korrespondierenden Säure-Base-Paar gilt immer folgende Regel: Je stärker eine Säure ist, desto schwächer ist die aus ihr entstehende korrespondierende Base und umgekehrt. Starke Säuren Verbindungen, die in wässriger Lösung (d.h. Wasser reagiert als Base) praktisch zu 100% dissoziiert vorliegen. Bsp.: In der Salzsäure ist z.B. die elektronenziehende Wirkung des Chloratoms so stark, dass nahezu 100% Dissoziation erfolgt: HCl + H2O → H3O+ + Cl- Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 4 Kurstag 2: Maßanalyse 2.Teil Entsprechend ist das Cl- als korrespondierende Base der HCl äußerst schwach basisch. Starke Basen Salze, die in wässriger Lösung ebenfalls zu 100% dissoziiert vorliegen. Bsp.: wie etwa NaOH oder KOH die in Na+ bzw. K+ und OH- dissoziieren. Bei ihrer Lösung in Wasser zerfallen diese Salze also direkt in OH--Ionen und ihr Kation. Die OH--Ionen, die die Lösung basisch machen, müssen also nicht erst durch eine Reaktion mit Wasser gebildet werden. Mittelstarke Säuren Verbindungen, die in wässriger Lösung nur teilweise dissoziieren. Bsp.: Phosphorsäure (siehe auch mehrprotonige Säure) Schwache Säuren Verbindungen, die in wässriger Lösung nur zu einem geringen Prozentsatz dissoziieren. Hier stellt sich ein Dissoziationsgleichgewicht ein. Bsp.: Essigsäure Da die Essigsäure eine schwache Säure ist, ist die korrespondierende Base Acetat relativ stark basisch. Sie nimmt also zu einem nicht geringen Teil Protonen aus der Lösung auf und reagiert zurück zu Essigsäure. Dies hat zur Folge, dass Essigsäure nur sehr schwach dissoziiert ist (abhängig von der Konzentration zu ca. 1%). Mehrprotonige Säuren Verbindungen, bei denen die Abspaltung der H+-Ionen in der Regel stufenweise erfolgt. Bsp.: Schwefelsäure H2SO4 + H2O H3O+ + HSO4HSO4- + H2O H3O+ + SO42- Bei der Schwefelsäure dissoziiert das erste H+ praktisch quantitativ ab, während das zweite H+ nur noch teilweise dissoziiert. Das HSO4--Ion ist daher im Gegensatz zu H2SO4 als eher mittelstarke Säure aufzufassen. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 5 Kurstag 2: Maßanalyse 2.Teil Bsp.: Phosphorsäure (3-protonige Säure) H3PO4 + H2O H3O+ + H2PO4- H2PO4- + H2O H3O+ + HPO42- HPO42- + H2O H3O+ + PO43- Hier stellt sich schon beim ersten Dissoziationsgrad ein Gleichgewicht ein, die Phosphorsäure ist daher nur eine mittelstarke Säure. Quantitative Erfassung der Dissoziation von schwachen Säuren mit Hilfe des Massenwirkungsgesetzes Massenwirkungsgesetz, Dissoziationskonstante Mit Hilfe des Massenwirkungsgesetzes (MWG) lässt sich die Lage des Gleichgewichts einer Reaktion in Form einer Gleichgewichtskonstanten berechnen. Handelt es sich um eine Säure-Base-Reaktion und damit um eine Dissoziation, so wird die Gleichgewichtskonstante auch Dissoziationskonstante genannt. Für die allgemeine Reaktion aA+bB AaBb ergibt sich nach dem Massenwirkungsgesetz die Gleichgewichtskonstante K: [A a Bb ] [A]a [B]b K= Wie aus der Formel ersichtlich wird, ist K groß, wenn das Gleichgewicht weit auf Produktseite liegt bzw. ist K klein, wenn das Gleichgewicht weit auf der Eduktseite liegt. Bezüglich der Dissoziation von Säuren in wässriger Lösung nach der allgemeinen Gleichung: HA + H2O A- + H3O+ ergibt sich nach dem MWG: K= [A - ] [H3O+ ] [HA] [H 2O] Da sich jedoch die Konzentration von Wasser während der Reaktion im Gegensatz zu denen der anderen Reaktionspartner nur minimal ändert, kann man diese Konzentration als konstant ansehen und in die Dissoziationskonstante mit einbeziehen. Damit ergibt sich die neue Dissoziationskonstante KS: Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 6 Kurstag 2: Maßanalyse 2.Teil [A- ] [H3O+ ] KS = K [H 2O] = [HA] Analog lässt sich eine Dissoziationskonstante KB für die Reaktion von Basen mit Wasser ableiten: K B = K [H 2O] = [HA] [OH- ] [A- ] Für starke Säuren bzw. Basen, die praktisch vollständig dissoziiert sind, ist demnach der Wert von KS bzw. KB sehr groß. Für schwache Säuren bzw. Basen, die nur zu geringen Teilen dissoziiert sind, ist der Wert von KS bzw. KB sehr klein. Hier einige Beispiele: Säure KS starke/schwache Säure HCl → H+ + Cl- vollständig dissoziiert stark H2SO4 → H+ + HSO4- vollständig dissoziiert stark HSO4- H+ + SO42- 1,3 ∙10-2 mittelstark H3PO4 H+ + H2PO4- 1,1 ∙10-2 mittelstark 1,8 ∙10-5 schwach H+ + CH3OO- CH3COOH H2PO4 H+ + HPO42- 1,2 ∙10-7 schwach HPO42- H+ + PO43- 1,8 ∙10-12 sehr schwach 1,8 ∙10-16 sehr schwach H2O H+ + OH- Wie man sieht, sind die Werte der Dissoziationskonstanten KS und auch KB in vielen Fällen sehr klein und deshalb ungünstig zu handhaben. Um die Säure- bzw. Basenstärken besser vergleichen zu können, werden der pK S- und der pKB-Wert eingeführt. Diese sind wie folgt definiert: pK B = - logK B pK S = - logKS Durch diese mathematische Umformung werden die Zahlenwerte vereinfacht. Säure KS HCl → H+ + Cl- vollständig dissoziiert H2SO4 → H+ + HSO4- vollständig dissoziiert HSO4- 1,3 ∙10-2 H+ + SO42- Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen pKS 1,89 7 Kurstag 2: Maßanalyse 2.Teil H+ + H2PO4- H3PO4 H+ + CH3OO- CH3COOH 1,1 ∙10-2 1,96 1,8 ∙10-5 4,74 H2PO4- H+ + HPO42- 1,2 ∙10-7 6,92 HPO42- H+ + PO43- 1,8 ∙10-12 11,74 1,8 ∙10-16 15,75 H2O H+ + OH- In diesem Fall bedeutet ein großer pKS- bzw. pKB-Wert, dass es sich um eine schwache Säure bzw. Base handelt, ein kleiner pKS- bzw. pKB-Wert, dass es sich um eine starke Säure bzw. Base handelt. Ionenprodukt des Wassers Wasser ist nur zu einem sehr geringen Prozentsatz nach folgender Gleichung in Ionen gespalten: H2O H+ + OH- Für die Dissoziationskonstante des Wassers gilt also: H + OH - K= = 1,8 10-16 H O 2 Wegen der sehr geringen Dissoziation des Wassers kann man die Größe [H 2O] in obiger Gleichung als konstant betrachten und in K mit einbeziehen. Man erhält dann eine neue Konstante KW, das so genannte Ionenprodukt des Wassers: K W = K H 2O = H + OH - Setzt man für K den Wert 1,8 10-16 ein und überlegt sich, dass in einem Liter Wasser 55,5Mol Wasser enthalten sind, so ergibt sich für KW = 99,9 10-16 ≈ 10-14. Und damit: KW = [H+] [OH-] = 10-14 Bei der Dissoziation von reinem Wasser entstehen H+ und OH- in gleichen Mengen, also im Verhältnis 1:1. Um die H+-Ionen-Konzentration berechnen zu können, stellt man folgende Überlegung an: Die Konzentrationen an H+- und OH--Ionen sind gleich groß: [H+] = [OH-]. 2 Eingesetzt in obige Formel ergibt sich: K W = H + = 10-14 . Nach der Konzentration der H+-Ionen aufgelöst: H + = 10-14 = 10-7 Wegen [H+] = [OH-] ist auch die Konzentration der OH--Ionen: OH - = 10-7 . Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 8 Kurstag 2: Maßanalyse 2.Teil pH-Wert Wie schon erwähnt, sind in sauren Lösungen die H+-Ionen, in basischen Lösungen die OH--Ionen für deren chemischen Charakter verantwortlich. Um den Charakter dieser Lösungen quantifizieren und vergleichen zu können, ist es notwendig, die Konzentration einer der beiden Ionenarten zu bestimmen. Konventionsgemäß hat man sich darauf verständigt, die H+-Konzentration zu bestimmen und anzugeben. Da diese Werte jedoch wie die KS- und KB-Werte unhandlich sind, wurde der pH-Wert wie folgt definiert: pH = - log H + Eine Lösung ist neutral, wenn sie den pH = 7 hat. Als sauer bezeichnet man Lösungen mit pH < 7, als basisch Lösungen mit pH > 7. Analog dazu gibt es auch einen pOH-Wert, der folgendermaßen definiert ist: pOH = - log OH - Der Zusammenhang zwischen pH und pOH ergibt sich durch Logarithmieren folgender Formel: K W = H + OH - = 10-14 + -lg OH -lg10-14 = - lg H + OH - 14 = -lg H + - 14 = pH + pOH pH-Wert-Berechnung für starke Säuren Da bei starken Säuren HA angenommen werden kann, dass sie zu 100% dissoziieren, gilt für die H+-Ionen-Konzentration in wässrigen Lösungen, die starke Säuren enthalten: [HA] = [H+] Somit lässt sich der pH durch Einsetzen in pH = - log H + direkt aus der Konzentration der Säure berechnen. Für mehrprotonige starke Säuren wie Schwefelsäure ist zu beachten, dass pro Säuremolekül mehrere - in diesem Fall 2 Protonen – abgegeben werden können und damit die H+-Ionen-Konzentration entsprechend größer ist als die Konzentration der starken Säure – in diesem Fall doppelt so groß. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 9 Kurstag 2: Maßanalyse 2.Teil Bsp.: pH-Wert einer 1M HCl Für die H+-Konzentration gilt: [H+] = [HCl]=1mol/l Also ergibt sich für den pH-Wert: pH = - lg 1 = 0 Da der pH-Wert nichts anderes als eine mathematische Umformung der H+Konzentration ist, kann aus diesem ebenso die Konzentration einer Säure berechnet werden. Bsp.: Konzentration einer HCl-Lösung mit pH = 2 Für die H+-Konzentration gilt: - lg H + = pH = 2 lg H + = - 2 10 lg H + = 10-2 [H + ] = 10-2 = 0,01 Also ergibt sich für die HCl-Konzentration: [H+] = [HCl] = 0,01mol/l pH-Wert-Berechnung für schwache Säuren Im Gegensatz zu starken Säuren sind schwache Säuren nur zu einem sehr geringen Prozentsatz dissoziiert. Diese Eigenschaft macht es schwieriger als bei starken Säuren die Konzentration an H+-Ionen zu bestimmen. Dies soll am Beispiel der Essigsäure im Folgenden erläutert werden. Essigsäure dissoziiert in Wasser nach folgender Gleichung: CH3COOH CH3COO- + H+ Wendet man auf diese Gleichung das Massenwirkungsgesetz an, ergibt sich: CH 3COO - H + KS = CH3COOH Da bei der Dissoziation von Essigsäure CH3COO- und H+ in gleichen Konzentrationen auftreten, gilt: CH3COO- = H + Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 10 Kurstag 2: Maßanalyse 2.Teil Eingesetzt folgt: 2 H + KS = CH3COOH Da Essigsäure nur zu einem sehr geringen Prozentsatz dissoziiert ist, kann man zur Vereinfachung annehmen, dass sich die Konzentration an nicht dissoziierter Essigsäure nicht merklich von der Anfangs-Essigsäurekonzentration unterscheidet und diese Konzentrationen gleichsetzen. 2 H + KS = CH3COOH Anfang Löst man nach der Konzentration der H+-Ionen auf, ergibt sich: H + = K S CH 3COOH Anfang Logarithmiert man diese Formel, erhält man auch für schwache Säuren den pH-Wert: pH = -lg H + = -lg K S CH 3COOH Anfang = 1 pK S - lg CH 3COOH Anfang 2 Bsp.: pH-Wert der 1M Essigsäure (pKS = 4,74) Also ergibt sich für den pH-Wert: pH = 1 1 pK S - lg CH 3COOH Anfang = 4,74-lg1 = 2,37 2 2 pH-Berechnung für Basen Da in basischen Lösungen die OH--Ionen und nicht die H+-Ionen den chemischen Charakter der Lösung bestimmen, ist es bei diesen notwendig, zunächst die Konzentration der OH--Ionen und daraus den pOH zu bestimmen. Aus diesem Wert kann mit Hilfe des Ionenprodukts des Wassers der pH-Wert folgendermaßen bestimmt werden: 14 = pH + pOH pH = 14 - pOH pH-Berechnung für starke Basen Analog den vorhin erwähnten Überlegungen bezüglich des chemischen Verhaltens starker Säuren, kann auch bei starken Basen davon ausgegangen werden, dass sie zu 100% dissoziieren. Man kann also ebenfalls Folgendes annehmen: Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 11 Kurstag 2: Maßanalyse 2.Teil [A-] = [OH-] Daraus ergibt sich der pOH- und somit der pH-Wert. Bsp.: pH-Wert einer 1M NaOH-Lösung Für die OH--Konzentration gilt: [OH-] = [NaOH] = 1 mol/l Also ergibt sich für den pOH-Wert: pOH = - lg 1 = 0 Mit dem Ionenprodukt des Wasser ergibt sich der pH: pH = 14 – pOH = 14 – 0 = 14 pH-Berechnung für schwache Basen Schwache Basen verhalten sich ebenfalls analog zu schwachen Säuren. Man kann also alle Annahmen und daraus abgeleiteten Formeln übernehmen, wenn man folgende Parameter ersetzt: KS → KB pKS → pKB [H+] → [OH-] pH → pOH Man muss ebenfalls beachten, dass die oben abgeleiteten Gleichungen für die Dissoziation einer Säure in Wasser gelten und dem entsprechend das MWG aufgestellt wurde. Jetzt wird die Dissoziation einer Base in Wasser behandelt, also folgende Reaktion: A- + H2O HA + OH- Das MWG für diese Reaktionsgleichung lautet: KB = HA OH - A - Der pOH-Wert ergibt sich folglich aus: pOH = -lg OH - = -lg K B A - = 12 pK - lg A - Anfang B Anfang Dann kann der pH-Wert wie bereits gezeigt aus dem Ionenprodukt des Wassers berechnet werden. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 12 Kurstag 2: Maßanalyse 2.Teil Bsp.: pH-Wert für 1M Acetat-Lösung Zur Berechnung des pOH = -lg OH - = -lg pOH verwendet man 1 K B A - = pK B - lg A - Anfang Anfang 2 folgende Formel: Wie man sieht, benötigt man analog zur pH-Berechnung bei schwachen Säuren den KB- bzw. den pKB-Wert. Diese sind in der Literatur nur selten angegeben, da sie sich leicht aus dem KS- bzw. pKS-Wert der korrespondierenden schwachen Säure ableiten lassen. Ähnlich dem pH- und pOH-Wert besteht auch hier eine Beziehung über das Ionenprodukt des Wassers: K B KS = 10-14 pK B + pKS = 14 Im Fall der Essigsäure ergibt sich der pKB des Acetat zu: pK B (Acetat) = 14 - pKS (Essigsäure) = 14 - 4,74 = 9,26 Nun kann der pOH berechnet werden: pOH = 1 1 pK B - lg A - = 9,26 - lg1 = 4,63 Anfang 2 2 Damit ergibt sich für den pH-Wert: pH = 14 - pOH = 14 - 4,63 = 9,37 Titrationskurven Bisher wurden nur Lösungen beschrieben, in denen entweder eine Säure oder eine Base vorlag. Wie schon in Kurstag 1 beschrieben, reagieren Säuren und Basen in einer Neutralisationsreaktion miteinander. Dieses Prinzip macht man sich in der Maßanalyse – bei der Titration – zu Nutze. Ebenso kann die Titration genutzt werden, um eine unbekannte Säure oder Base bezüglich ihrer Stärke, Wertigkeit und auf einen geeigneten Indikator (für die quantitative Analyse) hin zu überprüfen. Zu diesem Zweck ist es notwendig, den gesamten Verlauf der Titration in Form einer Titrationskurve zu visualisieren. Dies kann entweder im Labor mit Hilfe eines pH-Meters (s.u.) oder – wenn der AnfangspH bekannt ist – durch theoretische Berechnung geschehen. Titrationskurven erhält man, indem man den pH-Wert der zu untersuchenden Lösung während des gesamten Titrationsvorganges bestimmt und ihn in einem Diagramm gegen das zugegebene Volumen (in ml) der Maßlösung aufträgt: Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 13 Kurstag 2: Maßanalyse 2.Teil In den Diagrammen lassen sich 4 bzw. 3 wichtige Punkte erkennen: 1) Anfangs-pH-Wert der Analyse: hier wurde noch keine Maßlösung zugegeben 2) Nur bei schwachen Säuren! Halbäquivalenzpunkt: es wurde genau soviel Maßlösung hinzugegeben, dass der pH-Wert der Lösung dem pKS-Wert bzw. pKB-Wert der Analysensubstanz entspricht. 3) Äquivalenzpunkt: hier wurde gerade so viel Maßlösung zugegeben, dass sich gleich viele Maßlösung-Teilchen wie Analyse-Teilchen (gleiche Stoffmengen) in der Lösung befinden. Der Äquivalenzpunkt entspricht dem Endpunkt bei quantitativer Titration. 4) End-pH: wenn der Äquivalenzpunkt überschritten wurde, trägt nur noch die Maßlösung zu einer pH-Änderung bei. Gibt man weitere Maßlösung hinzu, so nähert sich der pH-Wert der Lösung dem pH-Wert der reinen Maßlösung an. pH-Wert-Berechnung bei Titrationen Bezüglich der pH-Wert-Berechnung bei Titrationen sind zwei Fälle zu unterscheiden: 1) Man titriert eine starke Säure mit einer starken Base oder umgekehrt. 2) Man titriert eine schwache Säure mit einer starken Base oder umgekehrt. Im Weiteren werden die Berechnungen am Beispiel der Titration von Säuren mit Basen erläutert. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 14 Kurstag 2: Maßanalyse 2.Teil Im ersten Fall liegt die starke Säure in der zu analysierenden Lösung vollständig dissoziiert vor. In der Lösung ist also eine der Stoffmenge der Säure entsprechende Stoffmenge H+-Ionen vorhanden. Die pH-Änderung im Laufe der Titration wird verursacht durch das Verschwinden von H+-Ionen nach folgender Reaktion: H+ + OH- H2O Um den pH-Wert zu einem beliebigen Zeitpunkt zu berechnen, ist es notwendig, die H+-Ionen-Konzentration an diesem zu bestimmen. Da die zugegebenen OH --Teilchen im Verhältnis 1:1 (s.o.) mit den H+-Teilchen reagieren, kann man aus der Stoffmenge der zugegebenen OH--Teilchen auf die Anzahl der neutralisierten H+-Teilchen rückschließen. Da die Konzentration und das Volumen der zugegebenen Maßlösung bekannt sind, kann man diese Stoffmenge leicht mit Hilfe der Formel 1.2 [n=cV] ausrechnen. Nun weiß man, wie viele H+-Teilchen neutralisiert wurden. Aus dem Anfangs-pH lässt sich wie oben beschrieben, die Anfangskonzentration und damit nach Formel 1.2 die anfängliche Stoffmenge an H +-Ionen in der Analyselösung bestimmen. Von dieser Stoffmenge (also der anfänglichen Anzahl an H +-Ionen) wird die Anzahl der neutralisierten H+-Teilchen abgezogen und man erhält die Anzahl an sich noch in der Analyse befindlichen H+-Teilchen. Diese Stoffmenge der H+-Teilchen kann mit Hilfe der Formel 1.2 und dem aktuellen Gesamtvolumen der Analyse in eine H+- Konzentration umgerechnet werden. Aus der Konzentration ergibt sich dann der pH-Wert (s.o.). Nach diesem Schema kann zu jedem beliebigen Zeitpunkt der Titration der pH-Wert berechnet werden. Im zweiten Fall liegt die schwache Säure nur zu einem geringen Teil dissoziiert vor. Die H+-Ionen-Konzentration entspricht also nicht der Anfangskonzentration der Säure. Bei Titration mit OH--Ionen werden von diesen ebenfalls H+-Ionen der Essigsäure neutralisiert: HAc + OH- H2O + Ac- Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 15 Kurstag 2: Maßanalyse 2.Teil Aber das dabei entstehende Acetat-Ion reagiert wie oben erwähnt basisch, d.h. es ist in der Lage, Protonen vom Wasser aufzunehmen und dadurch wieder OH --Ionen zu erzeugen. Das Gleichgewicht der Gesamtreaktion liegt nicht – wie bei starken Säuren – ganz auf der rechten Seite, wir müssen also die Rückreaktion berücksichtigen. Die Schwierigkeit ist es nun, die Konzentration der den pH-Wert bestimmenden H+Ionen in der zu analysierenden Lösung zu berechnen. Hierzu betrachten wir zunächst das Dissoziationsgleichgewicht der Essigsäure: H3O+ + Ac- HAc + H2O Wie bereits erwähnt, kann die Gleichgewichtslage durch das MWG beschrieben werden: CH3COO- H3O+ KS = CH3COOHnicht dissoziiert Um das unbequeme Rechen mit negativen Zehnerpotenzen zu vermeiden, ist man übereingekommen, die Gleichung zu logarithmieren. Man erhält dann: CH3COO- lgKS = lg H3O + lg CH3COOHnicht dissoziiert + Mit folgenden Definitionen: -lgKS = pKS und -lg H + = pH Die Gleichung vereinfacht sich dann zu: pKS = pH - lg CH3COO- CH3COOHnicht dissoziiert oder CH3COO- pH = pKS + lg CH3COOHnicht dissoziiert Die Gleichung heißt Henderson-Hasselbalch-Gleichung und wird zur Berechung von pH-Werten und pK-Werten schwacher Säuren bei Mischung mit Basen und bei Puffern (siehe Kurstag 3) verwendet. Der pH wird ausschließlich vom Verhältnis Acetat zu Essigsäure bestimmt. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 16 Kurstag 2: Maßanalyse 2.Teil Wendet man die Henderson-Hasselbalch-Formel bei Titrationen an, kann man mit ihr jeden beliebigen pH-Wert nach dem Anfangswert (nur reine Säure) und vor dem Äquivalenzpunkt (wenn nur noch die korrespondierende Base vorliegt) berechnen. Verwendet man in beiden Fällen der Titration relativ zur Analyse hoch konzentrierte Maßlösungen, so kann die Volumenzunahme durch Zugabe der Maßlösung vernachlässigt werden. Bsp.: Mischung 50ml einer 0,2M Essigsäure mit 50ml einer 0,02M NaOH-Lösung Um den pH-Wert zu berechnen, benötigt man die Konzentration an entstandenen Acetat-Ionen. Diese lässt sich aus der Anfangskonzentration der Essigsäure und der zugegebenen NaOH-Lösung berechnen. Die Anfangskonzentrationen vor der Reaktion (!) sind – da das Volumen durch die Mischung der Lösungen verdoppelt wurde – nur noch halb so groß wie die Konzentrationen der Ausgangslösungen: c(EssigsäureAnfang) = 0,1M c(NaOHAnfang) = 0,01M Jedes zugegebene NaOH-Teilchen erzeugt ein Acetat-Ion, folglich muss die Konzentration an Acetat nach der Reaktion gleich der Anfangskonzentration der NaOH-Teilchen sein: c(Acetat) = c(NaOHAnfang) = 0,01M Da die Acetat-Teilchen aus den Essigsäure-Molekülen entstehen, muss deren Konzentration nach der Reaktion um die Konzentration der Acetat-Teilchen abgenommen haben: C(Essigsäurenicht dissoziiert) = c(EssigsäureAnfang) - c(Acetat) = 0,09M Mit dem bekannten pKS-Wert kann man den pH-Wert berechnen: CH3COO- 0,01M pH = pKS + lg = 4,74 + lg = 4,74 - lg9 3,4 0,09M CH3COOHnicht dissoziiert Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 17 Kurstag 2: Maßanalyse 2.Teil Beispiele für Titrationskurven starker und schwacher Säuren 1.) Titration von 100 ml 0,1M HCl mit 1M NaOH: zugegebene noch vorhandene pH ml 1M NaOH Konzentration an HCl [M] 0 0,1 1 5 0,05 1,3 9 0,01 2 9,9 0,001 3 9,99 0,0001 4 0,1M HCl hat nach der Definition des pH-Wertes einen pH = 1. Bei der Titration findet folgende Reaktion statt: HCl + NaOH NaCl + H2O Versetzt man die 100 ml 0,1M HCl mit 5 ml 1M NaOH, so wird nach dieser Reaktionsgleichung die Hälfte der HCl umgesetzt, die Lösung ist jetzt nur noch 0,05M an HCl bzw. H+-Ionen, entsprechend einem pH von 1,3. Gibt man insgesamt 9 ml 1M NaOH zu, so ist die Lösung nur noch 0,01M an HCl bzw. an H+-Ionen entsprechend einem pH von 2. Für die Zugabe von 9,9 ml ergibt sich entsprechend ein pH von 3, für die Zugabe von 9,99 ml ein pH von 4. Man erkennt, dass in der Nähe des Äquivalenzpunktes eine kleine Laugenmenge eine große pH-Änderung hervorruft. Trägt man die Werte in ein Diagramm ein, so erhält man die Titrationskurve einer starken einprotonigen Säure. Der Äquivalenzpunkt liegt für starke Säuren exakt bei pH 7. Gibt man über den Äquivalenzpunkt hinaus weiter 1M NaOH zu, so wird der pH ausschließlich durch die Zunahme der OH--Ionen bestimmt Charakteristisch für diese Titrationskurven ist der sehr flache Anstieg am Anfang und der steile Anstieg in der Nähe des Äquivalenzpunktes. Der Äquivalenzpunkt für starke Säuren liegt immer im Neutralen also bei pH=7. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 18 Kurstag 2: Maßanalyse 2.Teil 2.) Titrationskurve von 100 ml 0,1M Essigsäure mit 1M NaOH Als Indikatoren für diese Titration sind alle Verbindungen geeignet, die ihren Farbumschlag im pH-Bereich von 4-10 haben. In das Diagramm (bei Titration von mehrprotonigen Säuren) eingezeichnet ist der Umschlagsbereich von Methylorange. Die Änderung des pH-Wertes während der Titration muss hier mit Hilfe der Henderson-Hasselbalch-Gleichung berechnet werden: [CH3COO- ] pH = pK S + lg [CH3COOH]nicht dissoziiert Zugegebene ml noch vorhandene pH 1M NaOH Konzentration an HAc [M] 0 0,1 2,87 1 0,09 3,79 2 0,08 4,15 5 0,05 4,74 9 0,01 5,69 9,9 0,001 6,74 9,99 0,0001 7,74 Charakteristisch ist ein kurzer steiler Anstieg zu Beginn der Titration, da noch keine Acetat-Ionen vorhanden sind. Darauf folgt um den pKs-Wert ein Bereich, in dem die Kurve nahezu horizontal verläuft. Dieser Bereich beruht auf der hier auftretenden Pufferwirkung (siehe Kurstag 3). Nahe dem Äquivalenzpunkt folgt der, schon von starken Säuren bekannte, sprunghafte Anstieg. Der Äquivalenzpunkt schwacher Säuren liegt im Alkalischen. Aus einer experimentell aufgenommenen Titrationskurve einer unbekannten schwachen Säure lässt sich sehr einfach der pK-Wert bestimmen, indem man den pH-Wert bei Halbneutralisation bestimmt. An diesem Punkt ist pH = pK (siehe oben). Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 19 Kurstag 2: Maßanalyse 2.Teil 3.) Titration von mehrprotonigen schwachen Säuren Bei der Titration einer mehrprotonigen schwachen Säure mit Natronlauge werden die H+-Ionen in der Regel schrittweise abgegeben. Bei der Titration z.B. der Phosphorsäure H3PO4 erhält man etwa folgende Titrationskurve: H3PO4 hat dann entsprechend 3 Äquivalenzpunkte, 3 pK-Werte und auch 3 Pufferbereiche (siehe Kurstag 3). Wirkungsweise der Farbindikatoren Die bei der maßanalytischen Bestimmung von Säuren und Basen verwendeten Indikatoren sind organische, teilweise sehr kompliziert aufgebaute, schwache Säuren bzw. Basen, deren undissoziierte Form eine andere Farbe besitzt als die dissoziierte Form. rot HA gelb H+ + A- Methylorange Ihre Wirkungsweise, d.h. die Ursache des Farbumschlags soll am Beispiel des pNitrophenols erläutert werden: p-Nitrophenol ist wie alle Phenole eine schwache Säure mit einer Dissoziationskonstante von ungefähr 10-7. Die undissoziierte Form ist praktisch farblos, die dissoziierte Form tiefgelb. Der Umschlag erfolgt um den Neutralpunkt: Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 20 Kurstag 2: Maßanalyse 2.Teil Mit Hilfe eines einzelnen Indikators lässt sich lediglich feststellen, ob der pH-Wert einer Lösung unterhalb oder oberhalb seines Umschlagsbereichs liegt. Verwendet man Indikatoren, um bei Titrationen den Äquivalenzpunkt zu ermitteln, ist darauf zu achten, dass der Umschlagspunkt des Indikators mit dem pH-Wert des Äquivalenzpunktes übereinstimmt. Verwendet man dagegen ein Gemisch verschiedener Indikatoren mit abgestuften Umschlagsbereichen, so erhält man für jeden pH-Wert eine charakteristische Mischfarbe (Indikatorpapier). Säure-Base-Wirkung von Salzen Säure und Basen gibt es nicht nur in Lösungen, sondern es existieren auch saure bzw. basische Salze (Kristalle). Diese enthalten dann mindestens ein Ion, das beim Lösen des Salzes in Wasser mit diesem sauer oder basisch reagiert und damit in der Lösung OH-- bzw. H+-Ionen erzeugt. Allgemein gilt: Salze aus schwacher Säure und starker Base reagieren alkalisch (CH 3COO-Na+), Salze aus starker Säure und schwacher Base reagieren sauer (NH 4Cl). Salze aus starker Säure und starker Base reagieren neutral (NaCl). Salze aus schwacher Säure und schwacher Base reagieren in etwa neutral (NH 4+CH3COO-). Da das NH4+Ion fast genauso stark sauer wirkt wie das CH3COO--Ion basisch, gleichen sich beide in ihrer Wirkung in etwa aus. Beispiele: 1.) Natriumacetat in Wasser gelöst. 2.) Ammoniumchlorid in Wasser gelöst: Eine wässrige Lösung von NH4Cl reagiert schwach sauer. Das NH4+-Ion gibt als schwache Säure H+-Ionen an das Wasser ab: NH4+ + H2O H3O+ + NH3 Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 21 Kurstag 2: Maßanalyse 2.Teil 1. Aktuelle und potentielle Acidität In einer 0,1M Essigsäure beträgt die H+ -Ionen Konzentration nur 1,34 ∙ 10-3 M, es sind also nur 1,34 % der gelösten Essigsäuremoleküle in H+ und CH3COOdissoziiert. Wenn man diese 0,1M Essigsäure mit NaOH titriert, könnte man zunächst annehmen, dass nur diese 1,34% H+-Ionen bei der Titration erfasst werden. Tatsächlich wird jedoch die gesamte Menge an Essigsäure erfasst, weil die aus dem Dissoziationsgleichgewicht entfernten H+-Ionen sofort durch Dissoziation neuer Essigsäuremoleküle nachgeliefert werden. 1 mol Essigsäure liefert bei der Titration mit NaOH auch 1 mol H +-Ionen. Diese sich aus der Konzentration der Säure ergebende Menge an H +-Ionen bezeichnet man als potentielle Acidität. Diejenige Menge an H+-Ionen, die sich in einer wässrigen Essigsäurelösung befindet, bezeichnet man als aktuelle Acidität. Für starke Säuren sind aktuelle und potentielle Acidität identisch. Beispiel: 0,1M HCl potentielle Acidität → 0,1 mol/l aktuelle Acidität 0,1 N Essigsäure → 0,1 mol/l potentielle Acidität → 0,1 mol/l aktuelle Acidität → 1,34 ∙ 10-3 mol/l Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 22 Kurstag 2: Maßanalyse 2.Teil Neue Geräte und Arbeitsweisen pH-Messung mit der Glaselektrode am pH-Meter Exakte pH-Wert-Messungen werden heute am einfachsten mit einer Glaselektrode und einem pH-Meter durchgeführt. Das Prinzip dieser Messung ist relativ kompliziert und kann hier nur angedeutet werden. Die Glaselektrode besteht aus einem Glasrohr, an dessen unterem Ende einen sehr dünnwandige Glaskugel angeschmolzen ist. Die Elektrode ist gefüllt mit einer Lösung eines Salzes (KCl). In diese Lösung taucht eine Pt-Elektrode zur Messung der Potenzialdifferenz ein. Taucht man diese Elektrode in eine Lösung ein, dann bildet sich an der sehr dünnwandigen Glasmembran ein Membranpotenzial aus. Dieses Membranpotenzial ist abhängig von der H+-Ionenkonzentration der Lösung, in die sie eintaucht. Durch Messung dieses Potenzials und entsprechender Eichung lässt sich so der pH-Wert einer Lösung sehr gut und einfach messen. Beim Arbeiten mit der Glaselektrode müssen einige Dinge beachtet werden: 1. Die Glaskugel der Elektrode darf nie austrocknen, sondern muss zwischen den Messungen immer in der mit KCl-Lösung gefüllten Schutzkappe aufbewahrt werden. 2. Vor und nach jeder Messung muss die Glaskugel der Elektrode immer gut mit destilliertem Wasser gespült werden. 3. Während den Messungen ist darauf zu achten, dass die Glaskugel ohne Kontakt zur Gefäßwand ständig von der Analysenlösung bedeckt ist. Des Weiteren ist darauf zu achten, dass der Rührfisch während der Messung nicht gegen die Elektrode schlägt. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 23 Kurstag 2: Maßanalyse 2.Teil Vorfragen 1. Wann entspricht bei der Titration einer schwachen Säure der pH-Wert dem pKS-Wert? 2. Warum liegt der Äquivalenzpunkt bei der Titration einer starken Säure bei 7? Wo liegt er bei einer schwachen Säure und warum? 3. Wie lautet das Prinzip von Le Chatelier? Wie kann man es auf Säure-BaseReaktionen übertragen, wie auf Titrationen? Übungsaufgaben 1. Berechnen Sie den pH-Wert von 0.2M HCl und 0.1M H2SO4 und vergleichen Sie die Ergebnisse. 2. Im Gastrointestinal-Trakt herrschen in den unterschiedlichen Abschnitten unterschiedliche pH-Werte. Warum? Berechnen Sie zu den angegebenen Konzentrationen die zugehörigen pHWerte: OH--Konzentration [M] Mundregion Speiseröhre Magen Duodenum 1,59 ∙ 10-7 10-7 Nahrung Darm H+-Konzentration [M] 0,01 2,51 ∙ 10-6 10-6 3. Warum ist bei folgender Tabelle der pKS2-Wert jeweils höher als der pKS1Wert? Name pKS1 pKS2 pKS3 Fumarsäure 3,02 4,39 - Oxalsäure 1,42 4,29 - Zitronensäure 3,06 4,74 5,39 4. Sie geben 10ml einer 2M H2SO4 zu 290ml Wasser. Wie groß ist der pH-Wert? 5. Was für einen pH-Wert hat eine Mischung aus 2M Essigsäure und 5M Natriumacetat-Lösung? Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 24 Kurstag 2: Maßanalyse 2.Teil Durchführung 1. Aufgabe Aufnahme der Titrationskurve einer 0,2M Essigsäure im Vergleich zu einer 0,2M HCl (Versuch wird 2x pro Tisch durchgeführt) In einem 150ml Becherglas stellt man ca. 60 ml 0,2M Essigsäure (hergestellt aus 2M Essigsäure aus dem Regal) her und titriert diese Lösung unter Rühren auf dem Magnetrührer mit der ausstehenden 0,4M Natronlauge. Dabei wird der pH-Wert im Anfangs- und Endbereich (hier ändert sich der pH-Wert relativ stark) nach der Zugabe von jeweils 1 ml 0,4M NaOH, im Mittelbereich nach der Zugabe von jeweils 2 ml NaOH mit Hilfe einer Glaselektrode gemessen und notiert. Die Messung wird beendet, wenn der pH-Wert ca. 13 erreicht hat. (Warum?) Die gemessenen pH-Werte werden nun in ein Koordinatensystem eingetragen (Ordinate: pH-Wert; Abszisse: zugegebenes Volumen (ml) 0,4M NaOH). Die erhaltenen Punkte werden durch eine Kurve verbunden: Man erhält so die Titrationskurve der Essigsäure, die für schwache Säuren charakteristisch ist. Aus der Kurve liest man den Äquivalenzpunkt ab. Anschließend nimmt man analog die Tirationskurve einer 0,2M HCl (hergestellt aus 2M HCl vom Regal) mit 0,4M NaOH auf und trägt die gemessenen pH-Werte in das gleiche Diagramm ein. Der Versuch wird pro Tisch nur 2x durchgeführt. Geben Sie an, wo der Pufferbereich abgelesen werden kann. Welchen Indikator würde man für eine Titration mit Natronlauge nehmen? 2. Aufgabe: Neuer Versuch. Falls Sie damit Probleme haben, bitte an Assistenten wenden. In diesem Versuch werden die Salze Formel Natriumacetat, ____________ Natriumhydrogenphosphat ____________ Natriumdihydrogenphosphat, ____________ Natriumcarbonat ____________ Ammoniumsulfat ____________ Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 25 Kurstag 2: Maßanalyse 2.Teil in Wasser gelöst und der pH-Wert mit Hilfe eines pH-Papiers geprüft. Falls das pHMeter frei ist, können die Werte mit Hilfe der Glaselektrode bestimmt werden. Na-Acetat pKs 4.8 Na-hydrogen- Na-dihydrogen- phosphat phosphat pK1:2.0 pK1:2.0 pk2: 7.2 pk2: 7.2 pK3: 12.0 pK3: 12.0 Na-carbonat Ammoniumsulfat 10.4 9.2 pKB pHgem pHber. Formeln für die Berechnung (Lösungen werden als 1 M angenommen. für basisches Salz: pH = 14-1/2(pKB-log [Base]) für saures Salz: pH = ½(pKs)-log [Säure]). Vorgehensweise: Eine Spatelspitze des Salzes wird in ca. 1ml Wasser (fast vollständig) gelöst (evt. schütteln) und danach der pH-Wert gemessen. Entsorgung Die verwendeten Lösungen sind in den verwendeten Mengen nicht umweltbelastend und können dem Abwasser beigegeben werden. Chemisches Praktikum für Mediziner Interfakultäres Institut für Biochemie, Universität Tübingen 26