Antwort
Werbung

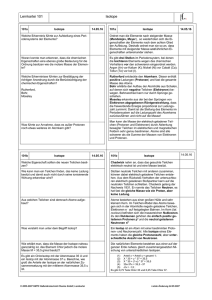
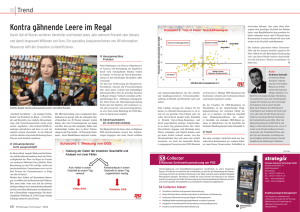
Ein geochemisches Quiz als Vorbereitung zur Prüfung Bernard Bourdon Andreas Stracke 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 1 (Wert: 10 CHF) Woher wissen wir, wann der Erdkern entstand? (1) Wir haben keine Ahnung! (2) Wir können Sm-Nd Isotope verwenden (3) Wir können Hf-W Isotope verwenden 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Man kann das Alter des Erdkerns mit Hf-W Isotopen bestimmen. 10 Series1 Series2 Series3 Series4 Series5 8 10 6 182W mantle 4 20 2 Erdmantle 30 50 0 0 20 40 60 80 100 120 140 Chondrite -2 -4 Zeit in Ma 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 2 (Wert 100 CHF) Warum ist Eisen das häufigste Element in der Erde? (1) Eisen ist seit dem Urknall anwesend (2) Eisen hat die höchste Bindungsenergie (3) Eisen ist sehr nützlich für die Menschheit 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Eisen hat die höchste Bindungsenergie pro Nukleon. Im Sonnensystem ist Fe häufig als Folge der stellaren Nukleosynthese. 56Fe A 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Eisen ist refraktär während der Akkretion: es entweicht nicht. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 3 (Wert: 1000 CHF) Warum ist Wasserstoff das häufigste Element in Jupiter? (1) Weil Wasserstoff refraktär ist. (2) Weil Jupiter im kalten Gebiet liegt (3) Weil Jupiter gross ist (4) Weil Wasserstoff ein häufiges Element in der Sonne ist 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Jupiter ist H-reich, weil seine Dichte niedrig ist. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Jupiter liegt in einem Gebiet, wo die Temperatur während der Akkretion kalt war. Mercury Venus Earth Mars Aufgrund der EisKondensation enstehen die Gasplaneten 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Jupiter Saturn Frage 4 (Wert 100 CHF) Was ist das 'Tal der Stabilität? (1) Eines ruhiges Tal im Wallis (2) Eine Zone auf der Nuklidkarte (3) Eine Nuklidgruppe, die eine kleine Bindungsenergie hat. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Die Nuklidkarte Protonenanzahl + or EC - Neutronenanzahl 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 5 (1000 CHF) Welche Hauptprozesse steuern die Zusammensetzung des Meerwassers? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Globale Quellen und Senken für Hauptelemente im Meerwasser (in 1012 mol/yr) Ion Fluss Atm Evap Cl 5.8 1.1 4.7 Na 8.3 0.9 4.7 Mg 5.0 SO4 3.2 1.2 Ca 11.9 1.2 HCO3 30.6 Si 5.8 Ton Karb Opal Sulfide MOR 0.8 0.1 0.6 4.9 1.2 -0.5 17 -4.8 (input) 34 -2.4 7.0 -1.1 (input) Rot=Senke, Ton: Kationenaustausch in Estuaren, Evap: Evaporite, MOR: Mittelozeansiche Rücken (hydrothermale Aktivität), Atm: Luft-Wasser Austausch, Karb: Karbonate. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 7 (CHF 10) Warum sind die Ozeane salzig? (1) Weil die Ozeane sehr alt sind. (2) Weil Salz löslich ist. (3) Weil Salz in den Ozeanen akkumuliert wird. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort: Die Ozeane sind salzig, weil die gelösten Bestandteile aus der Verwitterung mit Flüssen ins Meer transportiert werden. Die Salinität nimmt mit zunehmender Verdunstung zu und mit Regen und Schmelze des Eis nimmt ab. Die Hauptquellen der Elemente sind die ozeanische (hydrothermale Zirkulation) und kontinentale Kruste (Flüsse). 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 6 (10'000 CHF) Was erklärt die Veränderung des 13C/12C Verhaltnis, während des Karbons? (1) Eine grössere Einlagerung von organischem Kohlenstoff (2) Der grössere O2 Partialdruck der Atmosphäre (3) Die schnellere Verwitterung der Kruste 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort Es gab eine grössere Einlagerung von organischem Kohlenstoff, wodurch auch weniger O2 durch Photosynthese verbraucht wird. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 8 (Wert 100 CHF) Warum ist die Häufigkeit des Eisens so niedrig im Flusswasser? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Die Solubilität des Eisens in Lösungen ist tief. Im pH-Bereich von Flusswasser ist die FeSolubilität sehr tief. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 9 (CHF 10'000 CHF) Welche Argumente sprechen für die sog. Late Veneer Hypothese? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Die Hypothese des Late Veneers basiert auf der Häufigkeit der siderophilen Elementen Die Häufigkeit des HSE kann nicht mit SilikatMetall Gleichgewicht erklären werden. Die HSE sind nach der Kerntrennung angekommen! Drake, 2000 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 10 (Wert 1000 CHF) Warum enden die Fusionreaktionen in RiesenSternen? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Während der stellaren Nukleosynthese werden schwere Elemente in grossen Sternen produziert. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Für schwere Elemente ist die Coulombbarriere zu hoch! Die Energie W, die benötigt wird um zwei Ladungen, die anfangs undendlich weit auseinander sind zusammenzu- bringen beträgt: Die elektrostatische Abstossung zwischen positiven Ladungen im Kern (Coulombbarriere) muss überwunden werden, um Kerne zu fusionieren. Die elektrische Abstossungskraft dominiert bei grossen Entfernungen zwischen den Nukleonen, während die starke Kernkraft bei kurzen Abständen überwiegt. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 11 (Wert 10'000 CHF) Wie kann man zeigen, dass U und Th nicht durch den s-prozess gebildet werden? (1) Es gibt keinen stabilen Nuklide bis U und Th im Tal der Stabilität. (2) U und Th sind radioaktiv (3) Die Bindungsenergie von U und Th ist nicht ausreichend. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Es gibt keine stabile Nuklide nach 209Bi. s-process findet nur statt wenn stabile Nuklide vorhanden sind, deshalb ist der r-process die einzige Möglichkeit um U und Th zu produzieren. Die Nuklidkarte 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 12 Warum ist der obere Mantel an inkompatiblen Elementen verarmt? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort Durch partielles Schmelzen verarmt der obere Erdmantel an inkompatiblen Elementen, welche letztendlich in der kontinentalen Kruste eingelagert werden. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 13 Warum sind Ca2+ und HCO3- die Hauptbestandteile in Flusswasser? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort Die Häufigkeit von Ca2+ und HCO3- in Flusswasser ist eine Folge des grossen Einflusses der Karbonatverwitterung, die durch die Häufigkeit von Karbonatgesteinen an der Oberfläche und deren Verwitterungsanfälligkeit bedingt ist. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 14 Warum hat die Verbrennung von fossilen Brennstoffen zu einem Ungleichgewicht im Kohlenstoffkreislauf geführt? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort Die Verbrennung von fossilen Brennstoffen führt zu einer schnellen Freisetzung von organischem Kohlenstoff C der in einem langzeitigen Kohlenstoffreservoir gespeichert ist. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 15 Die Verteilung von Elementen zwischen der Kruste und dem Mantle ist abhängig von der Zusammensetzung und dem Druck und der Temperatur . Warum ist das der Fall? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort: Die Verteilung von Elementen ist ein thermodynamischer Prozess, der durch die Elementverteilungskoeffizienten gesteuert wird, welche abhängig sind von der Zusammensetzung des Systems und dem Druck und der Temperatur. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 16 Aufgrund seines Ionenradiuses und seiner Ladung sollte W in Wasser schwer löslich sein. Warum ist W trotzdem ein sehr häufiges Element in Flusswasser? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort W hat eine hohe Polarisierbarkeit (log Z2/r >1.3), was dazu führt das es eine leicht löslichen WO4 2-Komplex bildet. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 17: Wie sind kompatible und inkompatible Elemente definiert? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort 17: D m-n i solid i melt i x x G exp( RT mn 0 ) Xsolid und Xmelt = Konzentration von Element I in Schmelze und Mineral. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 18: Warum enthält die kontinentale Kruste etwa 40% der gesamten Alkali Element der Erde obwohl sie nur etwa 0.4% der Erdmasse ausmacht? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort : Die kontinentale Kruste ist an inkompatiblen Elementen angereichert, da sie durch Schmelzen des Erdmantels entstand. Dabei gelangen die inkompatibelsten Elemente, wie z.B. die Alkalimetalle bevorzugt in die Schmelze. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 19: Welche Aussage lässt sich anhand der Spurenelementzusammensetzung über den Aufschmelzgrad und die Aufschmelztiefe der beiden Basalte machen? Tipp: Man kann die vereinfachte Annahme machen, dass beide Gesteine aus derselben Quelle stammen 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort 19: Der Ozeaninselbasalt (ocean island basalt) hat einen niedrigeren Aufschmelzgrad, da er stärker an inkompatiblen Elementen angereichert ist und hat eine grössere Aufschmelztiefe (Fraktionierung der schweren seltenen Erd Elemente deutet auf Bildung im Granatstabilitätsfeld hin). 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 20: Welches Mineral verwittert am leichtesten bzw. schnellsten, Olivin (Mg2SiO4), Pyroxen (MgSiO3) oder Quartz (SiO2)? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort 20: Das Verhältnis von Si zu O ist ein Mass für den Grad der Polymerisierung, d.h. die Vernetzung der SiO4 Tretraeder der Schmelze. Olivin verwittert am leichtesten (Si:O = 1:4), Quartz am schwersten (Si:O = 1:2). 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 21: Wie kommen die wichtigsten Unterschiede in der chemischen Zusammensetzung der gasreichen Planeten wie Jupiter und den terrestrischen Planeten zustande? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort 21: Die gasreiche Planeten bilden sich jenseits der sog. „snowline“ wo Gase und volatile Bestandteile kondensieren können. Für die terrestrischen Planeten ist das nicht der Fall (höhere T näher am Zentrum des solaren Urnebels). 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 22 Kennzeichnen Sie in der folgenden Tabelle die Nuklide die nur durch den r- bzw. s-Prozess gebildet werden und solche die durch beide Prozesse gebildet werden. 76 184Os 186Os 187Os 188Os 189Os 0.018% 1.6% 1.6% 13.3% 26.4% 75 74 73 Z/N 28. Mai 2008 185Re 187Re 37.4% 62.6% 182W 183W 184W 186W 26.3% 14.3% 30.7% 28.6% 119 120 180Ta 181Ta 0.012% 99.98% 117 118 121 122 123 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort: s-Prozess Nuklide 76 184Os 186Os 187Os 188Os 189Os 0.018% 1.6% 1.6% 13.3% 26.4% 75 74 73 Z/N 28. Mai 2008 185Re 187Re 37.4% 62.6% 182W 183W 184W 186W 26.3% 14.3% 30.7% 28.6% 119 120 180Ta 181Ta 0.012% 99.98% 117 118 121 122 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources 123 Antwort: r-Prozess Nuklide 76 184Os 186Os 187Os 188Os 189Os 0.018% 1.6% 1.6% 13.3% 26.4% 75 74 73 Z/N 28. Mai 2008 185Re 187Re 37.4% 62.6% 182W 183W 184W 186W 26.3% 14.3% 30.7% 28.6% 119 120 180Ta 181Ta 0.012% 99.98% 117 118 121 122 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources 123 Frage 23 (100'000 CHF) Wie kann man Vanadium als ein Mass für die O2Fugazität des Erdmantels verwenden? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort: die Begründung eines 'Vanadium-Oxybarometers': Man kann das V/Sc Verhältnis in der Schmelze beobachten. Die Verteilungskoeffizienten von V und Sc sind fast gleich aber V hängt von den Redox Bedingungen ab. V ist inkompatibler bei hohem fO2 , weil V4+ häufiger ist, d.h. V/Sc ist bei niedrigen F (Mengenanteil der Schmelze) am höchsten. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Frage 24 (Wert 1'000'000 CHF) Warum hat Venus viel CO2 und wenig H2O in seiner Atmosphäre? 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Antwort Venus hat wahrscheinlich genauso viel Wasser wie die Erde am Anfang. Die Temperatur an der Venusoberfläche war nie kalt genug, um Wasser zu kondensieren. Weil die Temperatur hoch war, blieb das Wasser in der Atmosphäre und konnte nicht entweichen. 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Tut mir leid... 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Gewonnen! 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Auf ein Neues! 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources Sorry! 28. Mai 2008 B. Bourdon, A. Stracke / Institute of Isotope Geochemistry and Mineral Resources