Meningitis
Werbung

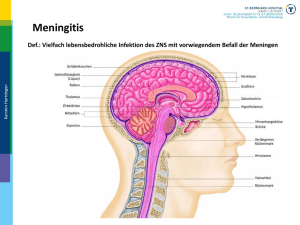
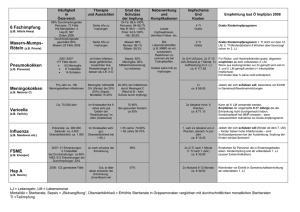
Meningitis Internistische Klinik I. Station für Infektiologie Kovács Beáta 2016 Meningitis - Definition Eine Entzündung des Zentralnervensystems kann potenziell durch alle menschlichen Erreger ausgelöst werden, aber manche Erreger weisen eine spezifische Affinität zum Nervengewebe auf. Die Meningitis ist eine Entzündung der Hirn- und Rückenmarkshäute. Meningitis kann als „eitrig” und „serös” oder „bakteriell” und „viral” kategorisiert werden. Enzephalomyelitis Rückenmarks. ist eine Entzündung des Gehirns und des Akute bakterielle Meningitis Die akute bakterielle Meningitis wird in die primäre Form und in die sekundäre Form unterteilt. Die sekundäre Form kann durch eine Infektion benachbarter Organe (Sinusitis, Mastoiditis, Otitis, Hirnabszess, subdurales Empyem) oder entfernter Organe (Endokarditis, Pneumonie, Sepsis), aber auch iatrogen (Ventrikeldrainage, paravertebrale Infektion, epidurale Anästhesie, Lumbalpunktion) oder posttraumatisch auftreten. Abhängig von dem Erreger kann die Letalität sogar 20% betragen. Akute bakterielle Meningitis Die ambulant erworbene, primäre Meningitis wird am häufigsten von Streptococcus pneumoniae, Neisseria meningitidis, Haemophilus influenzae und, insbesondere im höheren Lebensalter, von Listeria monocytogenes verursacht. Höheres Alter, Alkoholismus, Zustand nach Splenektomie und Infektionen im HNO-Bereich sind Risikofaktoren für eine Pneumokokken-, Meningokokken- und Haemophilus-Meningitis. Die seltenen Defekte des Komplement-Systems können wiederholten Erkrankungen durch N. meningitidis führen. zu Bei Patienten mit einer Grundkrankheit oder mit einer Immundefizienz gehören L. monocytogenes, Enterobakterien und Enterokokken zu den häufigsten Erregern. Im Säuglingsalter wird die bakterielle Meningitis von Streptococcus agalactiae, Escherichia coli und L. monocytogenes verursacht. Nach neurologischen Eingriffen und bei posttraumatischen Infektionen können überwiegend koagulasenegative Staphylokokken, Staphylococcus aureus und Streptokokken nachgewiesen werden. Infektionsweg Meningokokken, H. influenzae und S. pneumoniae werden aerogen übertragen. Eine L. monocytogenes-Infektion entsteht nach oraler Aufnahme der Bakterien (durch frische Milch, ungewaschenes Gemüse, weichen Käse und ungekochtes Fleisch). Die Neugeborenen-Meningitis wird durch Infektion mit Bakterien aus der mütterlichen Vaginalflora verursacht. Pathogenese Die Bakterien kolonisieren den Oro-/Nasopharynx, dann verursachen sie eine Bakteriämie. Möglicherweise aufgrund spezifischer Bindung an Gefäßendothelien und die den Plexus choroideus und die Ventrikel auskleidenden Epithelien entsteht die Meningitis. Bakterielle Bestandteile schädigen die Blut-Hirn-Schranke und induzieren einen massiven Entzündungsreiz, der den Einstrom von Leukozyten in den Liquor nach sich zieht und zu einem Hirnödem führt. Symptome Leitsymptome sind Kopfschmerzen, Fieber, Nackensteife, Photophobie und Übelkeit. Opisthotonus, Verwirrtheit und epileptische Anfälle können auftreten. Neben der Nackensteife sind auch die Dehnungszeichen nach Kernig und Brudzinski häufig positiv. Typisch, aber nicht spezifisch für die Meningokokken-Meningitis und Meningokokken-Sepsis sind hämorrhagische Exantheme (Petechien, flächige Einblutungen, insbesondere an den unteren Körperpartien wie z.B. an dem Gesäß und an den Beinen). In 10-15% aller Meningokokken-Meningitiden (aber auch bei Infektionen mit S. pneumoniae und anderen Bakterienspezies) entsteht als besonders schwere Form des septischen Schocks das Waterhouse-Friderichsen-Syndrom (auch als Purpura fulminans bezeichnet), das mit einer akuten hämorrhagischen Nekrose der Nebennieren einhergeht. (Infolge der Verbrauchskoagulopathie führt es zu Hautblutungen.) Waterhouse-Friderichsen-Syndrom Listeriose Eine Meningitis bzw. Enzephalitis durch L. monocytogenes sollte bei Neugeborenen bzw. im Alter von >50 Jahren, bei gleichzeitiger Infektion der Meningen und des ZNS-Parenchyms, bei subkortikalem Hirnabszess und bei neurologischen Herdsymptomen in Betracht gezogen werden. In 5-10% der Fälle präsentiert sich die Listeriose des ZNS als isolierte Hirnstammenzephalitis. In typischen Fällen zeigt die Erkrankung einen biphasischen Verlauf. Im Prodromalstadium fehlen meningitische Zeichen. In der zweiten Phase treten rasch Meningitis sowie Herdsymptome und Hirnnervenausfälle (III, V, VI, VII, IX) auf. Diagnostik Beim Verdacht einer ZNS-Entzündung soll eine Liquorprobe zur Bestimmung des Liquorsediments (Zellzahl, Zellverteilung), des Liquorprotein- und Glukosespiegels, zusätzlich zur mikrobiologischen Untersuchung (zur Kultur und Gram- und Ziehl-Neelsen-Färbung) entnommen werden. Wenn der Patient Bewusstseinsstörung oder fokale neurologische Symptome hat, sollte nach Beginn der Antibiotikatherapie eine KopfCT durchgeführt werden. Bei klinischen Zeichen der Einklemmung (einseitig erweiterte und auf Licht nicht reagierende Pupille, Streckkrämpfe) oder einer deutlichen Raumforderung bei der Kopf-CT ist die Lumbalpunktion kontraindiziert. Zugrunde liegende Erkrankungen (Sinusitis, Otitis, Hirnabszess) können mittels Kopf-CT demonstriert werden. Liquordiagnostik Die Gesamtzellzahl und die Zellverteilung werden durch die mikroskopische Untersuchung des Liquors bestimmt. Bei allen akut entzündlichen Prozessen im ZNS kann mit einer Pleozytose im Liquor gerechnet werden. Eine bakterielle Meningitis führt rasch zu einer granulozytären Reaktion mit mehr als 1000 Zellen/ul, die makroskopisch als Trübung erkennbar ist. Ausnahmen hiervon sind Patienten mit Immundefekten und Patienten mit einer Meningitis durch Listeria monocytogenes, Borrelia burgdorferi oder Mycobacterium tuberculosis, bei denen eine adäquate granulozytäre Reaktion fehlt. Die lymphozytäre Reaktion ist typisch für eine Virusinfektion der Meningen und des Gehirns, aber in der Frühphase der viralen Meningitis können jedoch auch Granulozyten überwiegen. Bei einer Virusmeningitis liegt die Gesamtzellzahl unter 1000 Zellen/ul. Der normale Wert von Liquor/Serum-Glukosequotient liegt bei 0,6. Liquoreiweißkonzentration Zur orientierenden Beurteilung der Blut-Liquor-Schrankenfunktion eignet sich die Bestimmung der Liquoreiweißkonzentration. (Der Normalwert des Liquoreiweißspiegels liegt unter 500 mg/l.) Ein erhöhter Liquor/Serum-Albuminquotient weist auf eine erhöhte Blut-Liquor-Schrankenpermeabilität hin, wodurch eine Entzündung des Zentralnervensystems gekennzeichnet wird. Liquor/Serum-Albuminquotient (Normalbereich <0,008) mögliche Erkrankung bis 0,01 (leichter Anstieg) Zoster-Ganglionitis multiple Sklerose chronische HIV-Enzephalitis blande virale Meningitis bis 0,02 (mittelgradiger Anstieg) virale Meningitis opportunistische Meningoenzephalitiden über 0,02 (hochgradiger Anstieg) eitrige Meningitis tuberkulöse Meningitis HSV-Enzephalitis Guillain-Barré-Polyradikulitis Typische Liquorbefundkonstellation bei verschiedenen Formen der Meningitis „eitrige” Meningitis „seröse” Meningitis Neuroborreliose Viren B. burgdorferi L. monocytogenes trüb klar klar klar klar >1000 <1000 <1000 <1000 <1000 granulozytär lymphozytär lymphozytär lymphozytär gemischt Gesamtprotein (mg/l) >1000 <1000 >1000 <1000 >1000 Liquor/SerumAlbuminquotient >0,02 <0,02 >0,02 keine gesicherten Daten >0,02 Liquor/SerumGlukosequotient <0,5 >0,5 >0,5 >0,5 <0,5 N. meningitidis S. pneumoniae H. influenzae makroskopische Beurteilung Zellzahl (Zellen/ul) Differenzialzellbild Listeriose tuberkulöse Meningitis M. tuberculosis Spezifische Diagnostik Zur Identifikation des Erregers und Erstellung eines Antibiogramms sollte eine Liquorprobe möglichst vor Therapiebeginn zur direkten mikroskopischen Untersuchung und zur Kultur geschickt werden. Nach Gram und Ziehl-Neelsen gefärbte Liquor-Präparate können auf den Infektionserreger hinweisen. (Pneumokokken sind grampositive Diplokokken, Meningokokken sind gramnegative intrazelluläre Diplokokken, Haemophilus influenzae ist ein gramnegatives Stäbchen, Mykobakterien sind säurefeste Bakterien.) Latex-Agglutinationstests erfassen erregerspezifische Antigene von Neisseria meningitidis / Escherichia coli K1 Streptococcus pneumoniae Haemophilus influenzae Typ b Streptococcus agalactiae. Ein Latex-Agglutinationstest kann auch nach dem Beginn der Antibiotika-Behandlung eine spezifische Diagnose liefern. Nukleinsäure-Amplifikationsverfahren (PCR) werden für Nachweis von Viren und Mykobakterien im Liquor eingesetzt. den Therapie der bakteriellen Meningitis Die wichtigste Behandlungsmaßnahme bei einer schweren lebensbedrohlichen Meningitis ist die rasche Gabe von Antibiotika unmittelbar nach der neurologischen Untersuchung und Entnahme der Untersuchungsmaterialien für den Erregernachweis. Bei der empirischen Wahl des Antibiotikums soll das mögliche Erregerspektrum der bakteriellen Meningitis berücksichtigt werden. Ein ausreichend liquorgängiges Antibiotikum soll verwendet werden. Im Neugeborenenalter (unter sechs Wochen) kommen gehäuft gramnegative Enterobakterien (E. coli K1), Gruppe-B-Streptokokken (S. agalactiae) und L. monocytogenes vor, sodass eine empirische Initialtherapie mit Ampicillin in Kombination mit Cephalosporinen der dritten Generation (z.B. Cefotaxim oder Ceftriaxon) oder mit einem Aminoglykosid empfohlen wird. L. monocytogenes hat eine natürliche Resistenz gegen Cephalosporine, aber Ampicillin ist wirksam gegen den Erreger! Therapie der bakteriellen Meningitis Bei Kindern bis zum zwölften Lebensjahr sind N. meningitidis, S. pneumoniae und H. influenzae die häufigsten Erreger, deshalb wird ihnen eine Monotherapie mit Cephalosporinen der dritten Generation (z.B. Cefotaxim oder Ceftriaxon) empfohlen. Bei Kindern ab dem zwölften Lebensjahr und bei Erwachsenen ohne Grundkrankheiten wird zur initialen Antibiotikatherapie einer ambulant erworbenen Meningitis (N. meningitides, S. pneumoniae) ein Cephalosporin der dritten Generation verwendet, wenn Kokken im Liquor (Grampräparat) nachweisbar sind. Lassen sich im Grampräparat keine Bakterien nachweisen, so kann initial ein Cephalosporin mit Ampicillin (und eventuell auch mit Gentamicin) kombiniert werden, um eine Wirksamkeit gegen L. monocytogenes zu erhalten. Diese Kombination ist besonders bei älteren Patienten mit Abwehrschwäche empfehlenswert, da die Listeriose in dieser Gruppe häufig auftritt. Therapie der bakteriellen Meningitis Geht der Meningitis ein Schädel-Hirn-Trauma oder ein neurochirurgischer Eingriff voraus, wird bei der empirischen Therapie ein Cephalosporin der dritten (Ceftazidim) oder vierten (Cefepim) Generation, oder Meropenem, plus Vancomycin (ein AntiStaphylokokken-Antibiotikum, das auch gegen MRSA wirksam ist) verabreicht. Bei einer Shunt-Infektion sollte der Shunt entfernt und vorübergehend eine externe Liquordrainage angelegt werden. Die Antibiotikatherapie muss gezielt entsprechend dem nachgewiesenen Isolat hoch dosiert und für einen Zeitraum von ca. drei Wochen vorgenommen werden. Bei der empirischen Therapie werden Vancomycin+Cefepim oder Vancomycin+Ceftazidim oder Vancomycin+Meropenem verwendet. Eine zusätzliche intrathekale Antibiotikaapplikation von Vancomycin (10-20 mg täglich), Teicoplanin (5-10 mg täglich) bei Staphylokokkenund Enterokokken-Infektionen oder Tobramycin (2x5-10 mg täglich) bei Infektion von Pseudomonas aeruginosa kann sinnvoll sein. Therapie der bakteriellen Meningitis Die Therapiedauer beträgt bei ambulant erworbenen Meningitiden nicht weniger als sieben Tage. Bei S. pneumoniae ist die Therapiedauer 10-14 Tage. Eine Meningitis von S. agalactiae sollte 14-21 Tage behandelt werden. Eine Meningitis bzw. Meningoenzephalitis durch L. monocytogenes oder Enterobakterien sollte 3-4 Wochen behandelt werden. Eine Kontroll-Liquoruntersuchung am Ende der Behandlung ist bei komplikationslosem Verlauf nicht erforderlich. Lediglich bei der neonatalen Meningitis durch Enterobakterien und P. aeruginosa ist eine Kontrollpunktion relevant, denn die Therapiedauer hängt von dem Ergebnis ab. Die gramnegative Meningitis des Neugeborenen soll noch zwei Wochen nach der ersten negativen Liquorkultur weiterbehandelt werden. Die minimale Behandlungsdauer beträgt in diesem Fall drei Wochen. Therapie der bakteriellen Meningitis Bei der Pneumokokken-Meningitis ist der routinemäßige Einsatz von Kortikosteroiden empfohlen, weil ein besserer Verlauf erreicht werden kann und signifikant weniger Hörschäden und neurologischen Spätschäden auftreten werden. Empfohlen wird die Gabe von 4x0,15 mg/kg Dexamethason über vier Tage jeweils 15 Minuten vor Verabreichung des Antibiotikums. Bei Patienten mit einer Meningitis als Folge einer bakteriellen Endokarditis wird der Einsatz von Kortikosteroiden nicht empfohlen. Ein Waterhouse-Friderichsen-Syndrom intensivmedizinische Therapie. erfordert eine Bei Hirnödem und Hirndruckzeichen kommen eine Osmotherapie mit Mannit, Oberkörperhochlagerung von 30 Grad und gegebenenfalls Hyperventilation in Frage. Bei einer Liquorabflussstörung bzw. bei Hydrozephalus ist die Anlage einer externen intraventrikulären Liquordrainage oder eines ventrikuloperitonealen Shunts wichtig. Beim Auftreten eines epileptischen Anfalls ist eine antikonvulsive Medikation erforderlich. Alter typische Erreger empirische Therapie Neugeborene < 6 Wochen Escherichia coli Streptocossus agalactiae Listeria monocytogenes Cephalosporin der 3. Generation (Ceftriaxon 2x50 mg/kg/Tag) plus Ampicillin (4x50-100 mg/kg/Tag) Kinder bis zum 12. Lebensjahr Neisseria meningitidis Streptococcus pneumoniae Haemophilus influenzae Cephalosporin der 3. Generation (Ceftriaxon 2x50 mg/kg/Tag) Kinder ab dem 12. Lebensjahr und Erwachsene Neisseria meningitidis Streptococcus pneumoniae Listeria monocytogenes Cephalosporin der 3. Generation (Ceftriaxon 2x2 g/Tag) evtl. in Kombination mit Ampicillin (6x2g/Tag) nosokomial erworben, postoperativ bzw. posttraumatisch Staphylokokken Enterobakterien Pseudomonas aeruginosa Vancomycin (30-45 mg/kg/Tag in 23 Dosen geteilt) plus Cefepim (3x2 g/Tag) oder plus Ceftazidim (3x2 g/Tag) oder plus Meropenem (3x2 g/Tag) abwehrgeschwächte und ältere Patienten Streptococcus pneumoniae Listeria monocytogenes Cephalosporin der 3. Generation (Ceftriaxon 2x2 g/Tag) plus Ampicillin (6x2g/Tag) Shunt-Infektion Staphylococcus aureus Staphylococcus epidermidis Pseudomonas aeruginosa Propionibacterium acnes Vancomycin (30-45 mg/kg/Tag in 23 Dosen geteilt) plus Cefepim (3x2 g/Tag) oder plus Ceftazidim (3x2 g/Tag) oder plus Meropenem (3x2 g/Tag) Prävention Ein Patient mit einer Meningokokken-Meningitis muss bis zu 24 Stunden nach Beginn einer wirksamen Therapie isoliert werden. Das mit der Pflege des Patienten betraute Personal sollte für diesen Zeitraum Schutzkittel, Handschuhe und Nasen- und Mundschutz tragen sowie die grundlegenden Hygienemaßnahmen einhalten. Das Erkrankungsrisiko für enge Kontaktpersonen von Patienten mit einer Meningitis durch H. influenzae Typ b oder Meningokokken ist 200- bis 1000fach höher als das Risiko der Allgemeinbevölkerung. Bei Meningokokken-Meningitis ist eine Chemoprophylaxe zur Eradikation von Erregern aus dem Nasopharynx für Mitglieder desselben Haushaltes, für Personen mit engem Kontakt zum Erkrankten und fürs Krankenhauspersonal indiziert, das wahrscheinlich vor Therapiebeginn Kontakt mit respiratorischen Sekreten des Patienten hatte. Chemoprophylaxe bei Meningokokken-Meningitis Antibiotikum Erwachsene Kinder Rifampicin 2x600 mg täglich p.o. für 2 Tage 2x10 mg/kg täglich p.o. für 2 Tage Ciprifloxacin 1x500 mg nicht empfohlen Ceftriaxon 1x250 mg i.m. oder i.v. (für Schwangere) 1x125 mg i.m. oder i.v. Prävention Der Impfstoff gegen H. influenzae Typ b bildet einen Teil der Grundimmunisierung im Kindesalter. Die Impfung gegen Pneumokokken bildet schon einen Teil der Grundimmunisierung im Kindesalter. Diese Impfung wird aber auch bei Personen mit einem hohen Risiko für eine PneumokokkenInfektion empfohlen (Asplenie, Sichelzellanämie, nephrotisches Syndrom). Verschiedene konjugierte Immunstoffe gegen Meningokokken (gegen Serogruppe A,C,Y,W135) stehen zur Verfügung. Diese Impfung wird Personen, die sich in Meningokokken-Endemiegebieten aufhalten (z.B. Pilgerfahrt nach Mekka), gefährdetem Laborpersonal und Patienten mit Asplenie empfohlen. Eine rekombinante Vakzine gegen N. menengitidis der Serogruppe B, (häufigster Erreger der Meningokokken-Infektionen) steht seit einigen Monaten auch zur Verfügung. Chronische Meningitis Von einer chronischen Meningitis kann gesprochen werden, wenn die klinischen Symptome einer Meningitis zusammen mit entzündlichen Liquorveränderungen länger als vier Wochen andauern. Die Infektion kann die Meningen betreffen oder im Hirnparenchym lokalisiert sein. Häufige Erreger einer chronischen Meningitis sind Borrelia burgdorferi, Mycobacterium tuberculosis, Treponema pallidum und Toxoplasma gondii. Als weitere Erreger kommen Brucellen, Aspergillen, Aktinomyzeten, Nokardien, Histoplasma capsulatum, Coccidioides immitis oder auch Helminthen (Zystizerkose, Echinokokkose) in Frage. Zu den seltenen Erregern gehören Rickettsien, Ehrlichien, Bartonellen, Tropheryma whippelii und Cryptococcus neoformans (bei HIV-infizierten Patienten). Nichtinfektiöse Ursachen sind Vaskulitis und Morbus Wegener. Meningiosis, Sarkoidose, ZNS- Chronische Meningitis Kopfschmerzen, Fieber und Nackensteife sind die führenden Symptome, die Infektion kann aber auch sehr bland verlaufen. In manchen Fällen liegen weitere Befunde vor, die auf eine spezifische Ätiologie hinweisen. Diese sind das Erythema chronicum migrans bei Neuroborreliose, Hirnnervenausfälle bei Tuberkulose, bihiläre Adenopathie bei Neurosarkoidose oder extrazerebrale Neoplasie bei Meningiosis. Im Blut sind meist unspezifische Entzündungsparameter vorhanden. Erregerspezifische Antikörper sind im Serum nachweisbar. Im Liquor sind Hinweise für eine Entzündung im ZNS zu finden (Pleozytose, Proteinerhöhung, Immunglobulinsynthese im ZNS). Bei der MRT können die chronische Kontrastmittelgabe sichtbar gemacht Hirnparenchymbeteiligung beurteilt werden. Meningitis und nach eine Chronische Meningitis Wegen des breiten Erregerspektrums soll eine ätiologische Therapie anwenden. Bei Neuroborreliose soll man ein Cephalosporin der dritten Generation (Ceftriaxon) verwenden. Wenn eine Antibiotika-Monotherapie keine Besserung bringt, soll mit einer tuberkulostatischen Therapie begonnen werden, auch wenn die Ergebnisse der Erregernachweise noch nicht vorliegen. Diese sollte so lange fortgeführt werden, bis eine tuberkulöse Meningitis mit Sicherheit ausgeschlossen werden kann. Die Therapiedauer beträgt bei entsprechendem Verdacht auf eine tuberkulöse Meningitis zwölf Monate. Eine negative PCR auf M. tuberculosis aus dem Liquor, ein negative Liquorbefund und ein negativer Tuberkulintest schließen eine Tuberkulose nicht aus. Die BCG-Impfung verhindert die TB-Infektion nicht, vermindert aber die Progression zu einer klinischen Erkrankung und ist hochwirksam zur Verhinderung einer disseminierten Erkrankung mit Meningitis im Kleinkindalter (60-80 % Risikoreduktion). Bei älteren Kindern ist die Wirksamkeit deutlich schlechter und im Erwachsenenalter konnte in den meisten Studien keine Schutzwirkung nachgewiesen werden. Virusmeningitis, aseptische Meningitis, seröse Meningitis Im Gegensatz zu den bakteriellen Infektionen sind der klinische Befund und Liquorveränderungen geringer ausgeprägt. Je nach auslösendem Erreger können zusätzlich Symptome von Seiten anderer Organsysteme (z.B. Hautexanthem oder Transaminasenanstieg) vorhanden sein. Aseptische Meningitiden bleiben in der Mehrzahl der Fälle ätiologisch ungeklärt, da sie spontan und ohne Residuen abheilen oder aus anderen Gründen keine eingehende virologische Diagnostik erfolgt. Die am häufigsten nachgewiesenen Erreger sind Enteroviren, wobei ECHO-und Coxsackie-B-Viren dominieren Mumpsvirus (relativ selten infolge der Impfmaßnahmen) FSME-Virus Herpesviren (HSV 1, 2, EBV, CMV, VZV) Adenoviren Masernvirus Rötelnvirus Influenza- und Parainfluenzaviren lymphozytäre Choriomeningitisvirus (LCMV) Rotavirus Infektionsweg Wegen des breiten Spektrums der in Frage kommenden Erreger sind die Infektionswege sehr unterschiedlich: Tröpfcheninfektion (meistens) sexuelle Übertragung (HSV 2) Zeckenstich, rohe Milch (FSME-Virus) Inhalation von Staub, der den eingetrockneten Urin von Mäusen enthält (LCMV) Klinik Typische Symptome der Virusmeningitis sind Kopfschmerzen, Nackensteife, Photophobie, Übelkeit und Fieber. Meist bestehen auch Allgemeinsymptome wie Müdigkeit, Abgeschlagenheit, Appetitmangel, Myalgien, Brechreiz, Bauchschmerzen, Durchfall und Hautausschläge. Fokale neurologische Ausfälle und Bewusstseinsstörung gehören aber nicht zum klinischen Bild der aseptischen Meningitis. Diagnostik Im Blut sind die Entzündungsparameter und die Leukozyten meist leicht erhöht, das Differenzialblutbild ist lymphomonozytär verändert. Im Liquor kann initial ein granulozytäres Zellbild vorhanden sein, das aber schon sehr früh in eine mononukleäre Pleozytose (<1000 Zellen/ul) übergeht. Der Gesamtproteinspiegel ist normal oder nur leicht erhöht, auch der Liquorglukosespiegel ist normal oder nur leicht gesunken. Eine intrathekale Antikörperproduktion tritt erst im weiteren Krankheitsverlauf auf (frühestens zwei Wochen nach der Infektion) und kann retrospektiv zur Diagnosesicherung beitragen. Die Viren können im Liquor durch Amplifikationsverfahren (PCR) nachgewiesen werden. Zur Nukleinsäure- Abklärung einer Infektion ist der erregerspezifische IgMAntikörpernachweis im Serum meist ausreichend. Ein viermaliger Anstieg der IgG-Serumantikörper kann zwischen Akutserum und Zweitserum (10-12 Tage später) bestimmt werden und die Verdachtsdiagnose retrospektiv erhärten. Therapie der viralen Meningitis Die virale Meningitis verläuft fast immer gutartig, selbstlimitierend und heilt ohne Residuen ab. Dementsprechend ist die Behandlung symptomatisch und besteht aus Bettruhe, gegebenenfalls aus Analgetika und Antipyretika. Eine Therapie mit Aciclovir (3x5-10 mg/kg/Tag i.v. für sieben Tage) ist bei Verdacht auf eine Meningitis durch Herpesviren erforderlich. Die Herpes-simplex-Enzephalitis ist eine lebensbedrohliche Krankheit, kann die hämorrhagische Nekrose des Temporallappens verursachen. Die Diagnose kann mithilfe einer MRT gestellt werden und durch Serologie bestätigt werden. Prophylaxe Die Impfung gegen Mumps-, Masern- und Rötelnvirus bildet einen Teil der Grundimmunisierung. Unter den zahlreichen Enterovirus-Serotypen ist eine Impfprophylaxe nur gegen die drei Polioviren möglich, diese ist allerdings sehr effektiv und hat in Amerika, Australien und Europa bereits zum vollständigen Verschwinden dieser Viren geführt. Differenzialdiagnostisch müssen die viralen Meningitiden von einigen bakteriellen Meningitiden, die ebenfalls mit dem Liquorbefund einer lymphozytären Meningitis einhergehen, abgegrenzt werden. Hinzu zählen Meningitiden durch Borrelia burgdorferi Treponema pallidum Mycobacterium tuberculosis Leptospira spp. Mycoplasma pneumoniae Chlamydophila pneumoniae Coxiella burnetii Auch Protozoen und Pilze können eine seröse Meningitis auslösen. Plasmodium falciparum Toxoplasma gondii Candida albicans Cryptococcus neoformans Histoplasma capsulatum Blastomyces dermatitidis Auch parameningeale Infektionen, neoplastische Meningitiden sowie nichtinfektiöse Entzündungen bei Vaskulitiden kommen als Differentialdiagnosen in Frage. FSME-Virus Frühsommer-Meningoenzephalitis-Virus Tick-borne encephalitis virus Das FSME-Virus ist ein kleines, umhülltes Plusstrang-RNA-Virus aus der Familie Flaviviridae, Genus Flavivirus. Das Erregerreservoir sind kleine Nager und andere wild lebende Säugetiere. Die Hauptvektoren des Virus stellen Zecken (Ixodes ricinus, Ixodes persulcatus) dar. Die Übertragung auf den Menschen erfolgt fast immer durch Zeckenstich, aber auch durch Verzehr roher Milch, da auch Haustiere (insbesondere Ziegen) infiziert werden können. Die überwiegende Zahl der FSME-Infektionen verläuft inapparent. Manifeste Erkrankungen zeigen meist einen biphasischen Verlauf. Zunächst kommt es zu einem unspezifischen fieberhaften Infekt mit Kopf- und Gliederschmerzen von einigen Tagen bis zu einer Woche. Nach einem symptomfreien Intervall von einigen Tagen kommt es dann bei 10-30% der Erkrankten in der zweiten Phase zur Beteiligung des Zentralnervensystems (als aseptische Meningitits, Meningoenzephalitis, Meningomyeloradikulitis). FSME-Virus Frühsommer-Meningoenzephalitis-Virus Tick-borne encephalitis virus Wirksame Virustatika zur Behandlung der FSME sind nicht vorhanden. Als bleibende Residuen können postenzephalitische Syndrome und persistierende schlaffe Lähmungen auftreten. Die Letalität liegt unter 2%. Routinemäßig wird für die Diagnostik der Nachweis von IgM- und IgGAntikörpern im Serum und auch im Liquor durchgeführt. Für die aktive Immunisierung stehen Totimpfstoffe aus Formalininaktiviertem Virus zur Verfügung. Die Grundimmunisierung besteht aus drei Impfungen, Auffrischimpfungen werden alle 3-5 Jahre empfohlen.