Elektrophorese - TCI @ Uni
Werbung

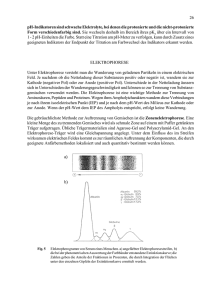
Vorlesungs-Skript zu „Instrumentelle Methoden“ PD Dr. Cornelia Kasper (Stand SoSe 2009) Elektrophoretische Methoden Teil 1: Gelelektrophorese Theoretische Grundlagen Allgemein versteht man unter Elektrophorese die Wanderung geladener Teilchen in einem elektrischen Feld einer Lösung oder einer Trägermatrix. Die Wanderungsgeschwindigkeit einzelner Teilchen hängt von ihrer spezifischen elektrophoretischen Beweglichkeit (Mobilität) ab. Diese wird durch die unterschiedlichen oberflächlichen Ladungen und der Molekülgröße bestimmt. Ein Substanzgemisch wird dabei in einzelne Zonen aufgetrennt. Elektrophoretische Beweglichkeit Die beschleunigende Kraft Fe =q*E und die bremsend wirkende Reibungskraft Ffr = fc*v liegen im Gleichgewicht, sodass sich Teilchen mit einer konstanten Geschwindigkeit v im v= Feld bewegen. q⋅E = u⋅E fc Der Proportionalitätsfaktor u ist die substanzspezifische Größe, genannt Mobilität. q: Ladung fc: Reibungskoeffizient E: elektrische Feldstärke Elektroosmotischer Fluß (EOF) Bei vielen Materialien bildet sich (z.B. an den Wänden einer Silica-Kapillare) eine Doppelschicht aus, wodurch der Fluß des Lösungsmittels bei Anlegen einer elektrischen Spannung in Richtung der Kathode gebracht wird. Dies bezeichnet man als Elektroosmotischen Fluß (EOF). Die Geschwindigkeit des EOF ist abhängig vom ζ-Potential (Potential in der Scherebene, Grenzfläche zwischen starrer und diffuser Doppelschicht). Elektrophorese und Elektroosmose überlagern sich, wobei der EOF häufig der elektrophoretischen Migration übergeordnet ist. Kationen haben erhöhte Geschwindigkeit in Richtung der Kathode. Neutrale Moleküle werden durch den EOF überhaupt in Bewegung gesetzt. Bei basischem pH Æ EOF höher als Wanderungsgeschwindigkeit der Ionen Æ Auch Anionen werden durch den EOF zur Kathode transportiert Elektroendosmose In der Gelelektrophorese tritt die Elektroendosmose auf. Aufgrund fixierter Ladungen an der Matrixoberfläche entsteht im elektrischen Feld ein, der Elektrophoreserichtung entgegen gesetzter osmotischer Fluß. Verzerrungen und Verdünnungen der Zonen sind die Folge. Elektrophorese kann in Lösung und in stabilisierenden Matrices durchgeführt werden. Es werden hauptsächlich drei Methoden angewandt: • Zonenelektrophorese • diskontinuierliche Elektrophorese (Disk-Elektr.) • isoelektrische Focussierung Zonenelektrophorese Bei meist basischem Puffer wandern die geladenen Teilchen (meist negativ geladen) mit unterschiedlichen Wanderungsgeschwindigkeiten in Richtung Anode. Die Auftrennung ist abhängig von Ladung, Größe und Form der Teilchen. Die Ladung wird durch den pH-Wert des Puffers beeinflusst. Je nach Größe und Masse verbleiben die Moleküle in bestimmten Zonen im Gel. Durch einen ebenfalls im Gel wandernden Molekülmarker kann die Molmasse der Proteine bestimmt werden. Molekülgrößen können durch Porengradientengele bestimmt werden. Durch eine kontinuierliche Veränderung der Monomerkonzentration der Polymerisationslösung erhält man nach dem Gießen der Gele eine Matrix mit steigendem Vernetzungsgrad. Die Proteine bleiben im stets enger werdenden Netz je nach Größe stecken. DISK-Elektrophorese Durch Kombination verschiedener Puffer miteinander verhindert man die Aggregation der Proteine und erhält schärfere Banden. Die Gelmatrix wird in ein weitmaschiges Sammelgel und ein engporiges Trenngel unterteilt. Bei dem Tris-Chlorid/ Tris-Glycin System hat das Sammelgel einen pH-Wert von 6,8 und das Trenngel einen pH von 8,8. Glycin hat auf Grund des pH-Wertes eine niedrige elektrophoretische Mobilität und fungiert als Folge-Ion, Chlorid hat eine hohe Mobilität und dient als Leit-Ion. Die Mobilitäten der aufzutrennenden Proteine liegen zwischen denen der Leit- und Folge-Ionen. Nach Anlegen eines elektrischen Feldes setzt die Isotachophorese ein. Dabei wandern alle Ionen mit der gleichen Geschwindigkeit und bilden einen Proteinstapel in Reihenfolge ihrer Mobilitäten. Vorteil des Stapeleffekts ist eine Vermeidung des Aggregierens der Proteine durch langsame Wanderung. Eine Aufkonzentrierung erfolgt vor Eintritt in das Trenngel. Nach Eintritt in das Trenngel lösen sich die Stapel auf und es erfolgt nach dem Zonenprinzip eine Auftrennung. SDS-Polyacrylamid-Elektrophorese SDS (Sodiumdodecylsulfate) ist ein anionisches Detergenz, das die Eigenladung von Proteinen überdecken kann. Die Folge ist eine hohe Auflösung die mit der diskontinuierlichen Elektrophorese erreicht werden kann. Durch den Einsatz von SDS entstehen Micellen mit einheitlicher negativer Ladung. Bei der Probenvorbereitung werden die Proteine im Überschuß mit SDS, sowie mit Mercaptoethanol oder DTT versetzt und auf 95 °C erhitzt. Die Tertiär und Sekundärstrukturen sowie die Schwefelbrücken werden aufgebrochen und das Molekül gestreckt. Die diskontinuierliche SDS-haltige Elektrophorese nach Lämmli ist die standardmäßig durchgeführte Elektrophorese. Isoelektrische Focussierung Um die Ladung eines Proteins zu bestimmen wird eine isoelektrische Focussierung durchgeführt. Dabei wandert ein Protein durch einen pH-Gradienten bis es an den pH-Wert gelangt an dem seine Nettoladung gleich Null ist. Dies ist der isoelektrische Punkt, der die Summe aller positiven und negativen Ladungen des Proteins ist. Da die Proteine an dieser Stelle keine Ladung mehr besitzen können sie auch nicht mehr wandern. Die Focussierung ist eine so genannte Endpunktmethode. Bei einer normalen Elektrophorese würden alle Proteine bei ausreichend langer Laufzeit das Gel passieren und „auslaufen“. Die Elektrophorese ist zeitlich begrenzt. Zweidimensionale Elektrophorese Leistungsstärkste analytische Methode zur Trennung von Proteingemischen mit tausenden von Einzelproteinen und Peptiden ist die 2D-PAGE. Der Unterschied zur eindimensionalen Elektrophorese besteht in der Auftrennung einer Probe nach zwei unterschiedlichen Parametern, der Ladung (pI) und der Masse. Dazu werden im ersten Schritt die Proteine auf schmalen Gradienten-Gelstreifen einer isoelektrischen Focussierung unterzogen und somit nach den pI-Werten getrennt. Im zweiten schritt erfolgt eine Trennung nach Masse über eine SDS-PAGE. Dazu wird das focussierte Streifengel im rechten Winkel auf ein PAGE-Gel gelegt und die Elektrophorese somit in einer zweiten Dimension durchgeführt. Als Ergebnis erhält man nach der Färbung ein Gel mit Punkten und nicht wie sonst üblich mit Banden. Teil 2: Kapillarelektrophorese Schematischer Aufbau einer Kapillarelektrophorese Puffergefäße Kapillare (Länge: 5-100 cm; Innendurchmesser: 20 – 200 µm) Detektor (z. B. Absorptionsdetektor, Laserinduzierte Fluoreszenz (LIF), Massenspektrometer) Spannungsquelle (Anlegen konstanter Spannung (in kV) oder Stromstärke (in µA)) Zwei Elektroden (Anode (der positive Pol) und Kathode (der negative Pol); Stromfluss im normalen Modus: In Richtung der Kathode) Trennmechanismen der Kapillarelektrophorese Injektion der Probe an der Anode Æ Wanderung zur Kathode Injektionsmethoden: Hydrodynamische Injektion (Vakuum, Druck, Gravitationskraft); Elektrokinetische Injektion Detektion der Probe am Kapillarfenster Trennung der Ionen aufgrund verschiedener elektrophoretischen Mobilitäten (unterschiedlichen Verhältnissen von Masse zu Ladung der jeweiligen Moleküle). Positiv geladene Ionen wandern am schnellsten, neutrale wandern mit dem elektroosmotischen Fluss (EOF) und trennen sich kaum, anionische wandern am langsamsten. Negative Ionen werden durch den EOF zu Kathode transportiert. Begriffserklärung „Elektroosmotischer Fluss“ Silanol-Gruppen an der der Oberfläche der Kapillarinnenseite sind aufgrund ihrer Dissoziation negativ geladen. Puffermoleküle fungieren als Gegenionen und erzeugen diffuse Doppelschicht. Diffuse Doppelschicht Siehe auch Teil 1. Kapillarzonenelektrophorese (CZE) Trennung nach Unterschied in Größe und Ladung Zunächst wird die Probe (AB) in die Kapillare injiziert Unter Einfluss des elektrischen Feldes wird die Probe in diskrete Zonen (A und B) unterteilt, die ihrerseits Analyten mit der gleichen elektrophoretische Mobilität enthalten Puffer, pH-Wert, elektrische Feldstärke bleiben konstant Kapillaraffinitätelektrophorese (CAE) Untersuchung von Wechselwirkungen zwischen einem Rezeptor und Liganden Bestimmung von Bindungskonstanten und - stöchiometrie Unterschied in der Mobilität zwischen Protein und dem gebildeten Komplex Ligand trägt eine Ladung Molekulargewicht des Komplexes unterscheidet sich wesentlich von der des Proteins Micellarelektrokinetische Chromatographie Hybridtechnik aus Elektrophorese und Chromatographie Zusatz von Micellenbildnern (Detergenzien) zum Puffersystem Æ pseudostationäre Phase aus geladenen Micellen Trennung basierend auf Verteilung der Analyte zwischen Lösung und Micelleninneren Kapillargelelektrophorese Trennung nach unterschiedlichen Masse/Ladungsverhältnissen DNA-Moleküe und SDS-denaturierte Proteine besitzen bei unterschiedlichen Massen sehr ähnliche Masse/ Ladungsverhältnissen. Gelmedium bewirkt einen Siebeffekt und behindert die elektrophoretische Wanderung der größeren Moleküle stärker als die der kleineren. Quervernetzte Gele: Acrylamid, Bisacrylamid Æ definierte Porengröße, starre physikalische Eigenschaften, begrenzte Lebensdauer Lineare Gele: Meist Dextrane, Polyethylenglykole, loses Geflecht linearer Polymerketten Vergleich mit klassischen Gelelektrophorese: Vorteile Nachteile Kürzere Trennzeiten Keine präparative Probensammlung Online-Detektion Keine parallele Trennung mehrerer Proben Geringer Arbeits- und Geräteaufwand Nicht zweidimensional durchführbar Isoelektrische Fokussierung (CIEF) Trennung der Analyten nach ihrem isoelektrischen Punkt Injektion der Probe in einem Ampholytgemisch in die Kapillare Eine starke Säure wird an der Anode platziert (Anolyt), eine starke Base dient als Kathodenpuffer (Katholyt). Anlegen der Spannung Æ pH-Gradient Æ Ampholyt-Ionen wandern entsprechend ihrem pI. Bei pI = pH endet die elektrophoretische Wanderung. Diffusion E-Feld Anode + + Ladung des Analytmoleküls - Verd. H3PO4 i en d a r G pH - Kathode t Verd. NaOH pH = pI Isotachophorese (ITP) Trennung nach Größe und Ladung Zwei Elektrolyte: Leitelektrolyt (LE) und Endelektrolyt (TE) Mobilität Leitelektrolyt > Mobilität aller Analyt-Ionen Mobilität Endelektrolyt < Mobilität aller Analyt-Ionen Anlegen konstanten Stroms Æ Bildung eines Feldstärkengradients Probenaufgabe der Proben-Ionen (A, B) an der Grenzfläche der beiden Elektrolyte Feldstärkengradient verhindert Diffusion scharfer Zonengrenzen Literatur: • F. Lottspeich/H. Zorbas, Bioanalytik • H.Engelhardt, W.Beck, T. Schmitt, Kapillarelektrophorese