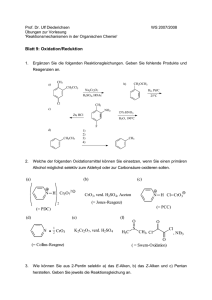
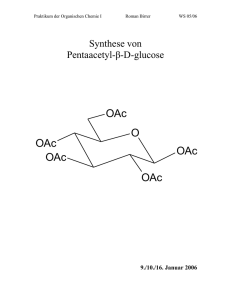
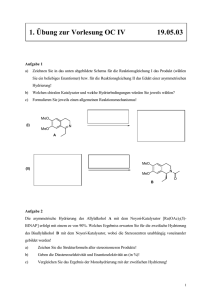
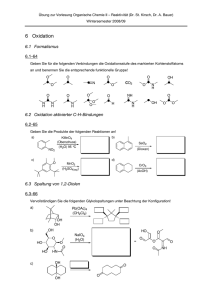
Wichtige Oxidationen von Alkoholen:
Werbung
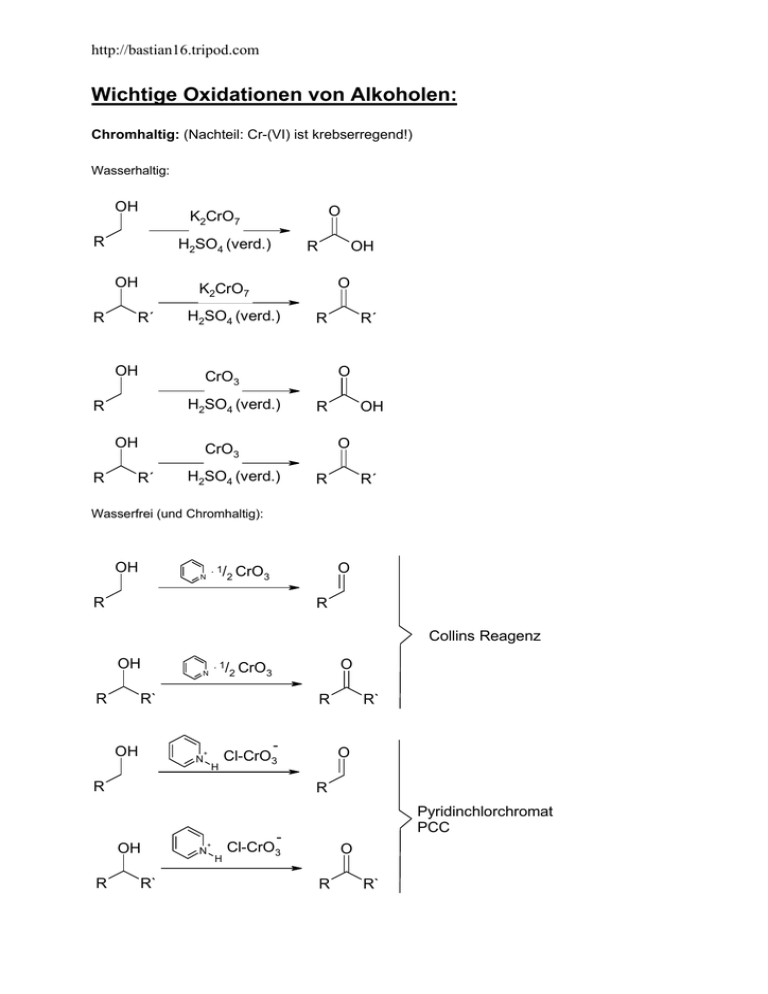
http://bastian16.tripod.com Wichtige Oxidationen von Alkoholen: Chromhaltig: (Nachteil: Cr-(VI) ist krebserregend!) Wasserhaltig: OH R H2SO4 (verd.) OH R R OH O K2CrO7 R´ H2SO4 (verd.) OH R H2SO4 (verd.) OH R H2SO4 (verd.) OH O CrO3 R´ R´ O CrO3 R R O K2CrO7 R R´ Wasserfrei (und Chromhaltig): OH . 1/ N O 2 CrO3 R R Collins Reagenz OH R N . 1/ R` OH R N + H Cl-CrO3 R R` O R OH R O 2 CrO3 R` N + H Pyridinchlorchromat PCC Cl-CrO3 O R R` http://bastian16.tripod.com 2- OH N Cr2O7 + O H 2 R R Pyridindichromat PDC 2- OH R N Cr2O7 + O H 2 R` R R` Chromfrei: (werden bevorzugt verwendet, da nicht krebserregend) O OH H3C S CH3 O + Cl Cl O O NEt3 R OH R O H3C S CH3 R` + Swern-Oxidation R O O Cl Cl Nachteil: Basenlabile Substanzen werden durch NEt3 angegriffen. (Bsp.: Eliminierung) O R NEt3 R` O O OH OAc R I O OAc OAc O R O + R R` OAc 2HOAc OAc O OH + O I O I O OAc OAc R + R` O I OAc + 2HOAc Dess-MartinReagenz Keine Eliminierung als Nebenreaktion möglich. http://bastian16.tripod.com - OH O R N + O Me OH R O Pr4N+ RuO4 NMO R O N + O Me NMO NMO überführt das entstehende RuO3- wieder in RuO4- . Somit wird RuO4nur katalytisch eingesetzt. O - Pr4N+ RuO4 R` TPAP: Tetrapropylammoniumperruthenat (modernes Oxidationsmittel) R R` “Sonderfälle“: OH R Durch Hypochloride lassen sich selektiv nur sekundäre Alkohole oxidieren, da Ketone ca. 20kJ/mol stabiler sind als Aldehyde. (Development produkt controlled) R OH R O Ca(OCl)2 O Ca(OCl)2 R` R R` (Reaktion läuft bei Anwesenheit von Wasser und Phasentransferkatalyse ab) OH MnO2 (aktiviert) O -Mn2+ R OH Eine Oxidation von allylischen OH-Gruppen ist selektiv durch aktivierten Braunstein möglich R MnO2 (aktiviert) ==> alpha-beta ungesättigte Aldehyde und Ketone O -Mn2+ R R OH R MnO2 (aktiviert) O -Mn2+ R http://bastian16.tripod.com OH OH O +NaIO4 -H2O oder Pb(OAc)4 -2HOAc O Ein Glycol lässt sich sowohl durch NaIO4 als auch durch Pb(OAc)4 in zwei Aldehyde spalten. Bei NaIO4 ist ein 5-gliedriger ÜZ essentiell. Bei Pb(OAc)4 ist jener zwar bevorzugt aber nicht essentiell.